Екзокринна недостатність підшлункової залози: сучасні можливості замісної терапії
 Хронічні захворювання органів травлення є найчастішою патологією, що трапляється як у дорослих, так і в дітей. Серед гастроентерологічних захворювань перше місце посідає патологія верхніх відділів шлунково-кишкового тракту, що становить майже половину всіх захворювань, передусім за рахунок патології гастродуоденальної зони [2]. Хронічні запальні захворювання верхніх відділів органів травлення досить часто супроводжуються ураженням підшлункової залози (ПЗ).
Хронічні захворювання органів травлення є найчастішою патологією, що трапляється як у дорослих, так і в дітей. Серед гастроентерологічних захворювань перше місце посідає патологія верхніх відділів шлунково-кишкового тракту, що становить майже половину всіх захворювань, передусім за рахунок патології гастродуоденальної зони [2]. Хронічні запальні захворювання верхніх відділів органів травлення досить часто супроводжуються ураженням підшлункової залози (ПЗ).
Екзокринна функція ПЗ відіграє ключову роль у травленні завдяки секреції панкреатичного соку, що складається з численних ферментів і водного розчину, багатого на бікарбонат натрію. Постпрандіальна секреція може збільшуватися до 1-2 л на добу. Для перетравлення введених в організм макроелементів виділяються три основні типи ферментів: білки (трипсиноген‑1, -2 та -3, хімотрипсиноген, проеластаза‑1 і -2, протеаза Е, калікреїноген, прокарбоксипептидаза А1, А2, В1 і В2), вуглеводи (α-амілаза) та ліпіди (ліпази). Якщо ліпази й амілаза секретуються в активній формі, то протеази – як проферменти. Трипсиноген перетворюється на активну форму трипсин у дванадцятипалій кишці за допомогою ентерокінази (протеази, що виділяються ентероцитами), а трипсин, своєю чергою, активує інші протеази ПЗ [10].
Від 5 до 40% дієтичних ацильних ланцюгів тригліцеридів вивільняються в шлунку ліпазою шлунка, яка продовжує свою дію у дванадцятипалій кишці разом із ліпазою ПЗ доти, доки ці ферменти не зруйнуються протеазами ПЗ. Ліпаза ПЗ людини специфічно розщеплює зовнішні ефіри sn‑1 і sn‑3 на молекулах тригліцеридів і генерує дві вільні жирні кислоти та 2-моногліцерид. Ця ліпаза потребує специфічного кофактора – коліпази, щоб закріпитися на поверхні крапель ліпідів, які містять фосфоліпіди, й оточена ліпідами жовчі (жовчними солями та фосфоліпідами). Хоча in vitro оптимальним для активності цієї ліпази є рН від 8 до 9, жовчні солі in vivo дають ферменту змогу ефективно працювати при рН від 6 до 6,5 [10].
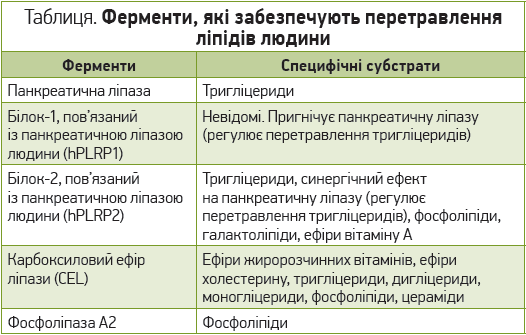
Панкреатична ліпаза (табл.) відповідає за гідроліз від 40 до 70% тригліцеридів. Білок‑1, пов’язаний із панкреатичною ліпазою людини (hPLRP1), не виявляє ліполітичної активності, але певною мірою пригнічує ліполіз тригліцеридів молока за допомогою панкреатичної ліпази. Білок‑2, пов’язаний із панкреатичною ліпазою людини (hPLRP2), виявляє широку субстратну специфічність, гідролізуючи тригліцериди молока (має синергічний ефект із панкреатичною ліпазою), фосфоліпіди, галактоліпіди й ефіри жиророзчинних вітамінів. Карбоксиловий ефір ліпази (CEL), також відомий як ліпаза, активована солями жовчі (також виділяється молочною залозою – BSSL) гідролізує тригліцериди, дигліцериди, фосфоліпіди й ефіри жиророзчинних вітамінів і холестерину. Варто зазначити, що hPLRP2, який високо експресується в молодому віці, відіграє важливу роль у перетравленні ліпідів у немовлят, яких годують жіночим молоком, разом із BSSL. Фосфоліпаза А2 гідролізує фосфоліпіди до лізофосфоліпідів, що має важливе значення для оптимального поглинання ліпідних поживних речовин [10].
Продукти, що утворюються під час ліполізу, розчиняються в жовчних солях – змішаних міцелах і ліпосомах (везикулах), які дають змогу всмоктуватися через ворсинки кишечнику. Після всмоктування перетравлені ліпіди перетворюються назад на тригліцериди, фосфоліпіди й ефіри холестерину та жиророзчинні вітаміни, потім упаковуються як хіломікрони та транспортуються через грудну протоку в системну циркуляцію для доставки до різних ділянок тіла [10].
ПЗ досягає зрілої функції до 2-річного віку. Секреція ПЗ у літніх людей знижується та становить 56% від функції молодих людей. У чоловіків рівень секреції може бути вищим, аніж у жінок. На склад секрету ПЗ істотно впливають кількість і тип ліпідів, що споживаються. Встановлено, що 2-тижнева дієта в здорових людей із високим вмістом жирів / низьким вмістом вуглеводів асоціюється з 4-разовим збільшенням вивільнення ферментів ПЗ порівняно з дієтою, багатою на вуглеводи або білки. Рівень панкреатичної ліпази у дванадцятипалій кишці залежить від типу та кількості спожитих ліпідів [10].
Екзокринна недостатність ПЗ (ЕНПЗ) – це стан, що характеризується дефіцитом екзокринних ферментів ПЗ і призводить до нездатності нормально перетравлювати їжу [4]. Серед причин ЕНПЗ – захворювання ПЗ та непанкреатичні захворювання [4, 15, 21].
У більшості випадків (50-70%) хронічний панкреатит виникає внаслідок зловживання алкоголем. Спадкове (автосомно-домінантне) захворювання реєструється в родинах з обтяженим анамнезом хронічного панкреатиту й уражає переважно молодих осіб до 20 років. Більшість випадків спадкового хронічного панкреатиту спричинена мутацією гена катіонного трипсиногена (PRSS1), деякі – спонтанними мутаціями, які пошкоджують інактивацію трипсину. Інші мутації стосуються генів інгібітора Казаля 1 типу серинової протеази (SPINK1); карбоксипептидази А1 (СРА1); трансмембранного регулятора кістозного фіброзу (CFTR); хімотрипсиногена С (CTRC) та карбоксиестроліпази (CEL). Окреме місце як етіопатогенетичний фактор виникнення хронічного панкреатиту посідає дефіцит α1-антитрипсину [1].
Важлива роль в етіології хронічного панкреатиту належить обструктивним чинникам – стриктурам, пухлинам протоків ПЗ, дисфункції сфінктера Одді та вродженим вадам розвитку ПЗ (кільцеподібна, розділена ПЗ); жовчнокам’яній хворобі з холецистолітіазом та/або холедохолітіазом, особливо в жінок [1].
Іншими етіологічними чинниками ризику хронічного панкреатиту є дієта з недостатнім вмістом білка, низьким або високим вмістом жирів; прийом лікарських засобів (інгібіторів ангіотензинперетворювального ферменту, статинів, диданозину, ламівудину, гідрохлортіазиду, вальпроєвої кислоти, пероральних контрацептивів, інтерферонів) [1].
Прогресування хронічного панкреатиту пов’язане з фіброзом паренхіми ПЗ на тлі хронічного запалення з подальшою структурною перебудовою органа та формуванням його функціональної зовнішньо- та внутрішньосекреторної недостатності [1].
Крім панкреатиту, ЕНПЗ є основним наслідком захворювань, що призводять до втрати паренхіми ПЗ (муковісцидозу, обструкції головної протоки ПЗ, целіакії) та/або кислотно-опосередкованої інактивації її ферментів (у разі синдрому Золлінгера – Еллісона). Частими причинами ЕНПЗ також є хірургічні резекції шлунково-кишкового тракту та ПЗ (наприклад, гастректомія, дуоденопанкреатектомія, операція шунтування шлунка). Утім, ЕНПЗ спостерігають і при інших, менш поширених станах, до яких належать рак ПЗ, метаболічні хвороби (цукровий діабет), порушена гормональна стимуляція екзокринної панкреатичної секреції, запальні захворювання кишечнику, порушення координації між моторною та секреторною функціями (асинхронія), порушення ентеропанкреатичного зворотного зв’язку, гемохроматоз ПЗ тощо [20].
Клінічні прояви
Зміни секреції ферментів ПЗ призводять до порушення всмоктування поживних речовин, причому зміна всмоктування жирів і жиророзчинних вітамінів зазвичай спричиняє початкові симптоми. Оскільки екзокринна ПЗ зберігає велику резервну здатність для секреції ферментів, перетравлення жиру особливо не порушується, поки вихід ліпази не знизиться до 10% від нормального рівня [4].
До основних симптомів ЕНПЗ належать стеаторея, втрата маси тіла, втомлюваність, метеоризм, здуття живота, набряки та подеколи анемія [16].
Діагностика
Оскільки у 20% пацієнтів із хронічним панкреатитом, що призводить до ЕНПЗ, не відзначається характерного болю, стеаторея може бути єдиною скаргою. Стеаторея класично визначається як щонайменше 7 г фекального жиру протягом 24 год у контексті 72-годинного тесту на випорожнення при споживанні 100 г жиру щодня. Проте кількісне визначення калового жиру є незручним і складним. Тест на фекальну еластазу може бути використаний для демонстрації нестачі ендогенного ферменту. Встановлено, що його чутливість до тяжкої недостатності ПЗ становить 72%, а специфічність – 90%. Фекальна еластаза має меншу чутливість у разі легкої стеатореї та не настільки корисна в пацієнтів із діабетом, оскільки її активність зменшується зі збільшенням його тривалості. Золотим стандартом оцінки екзокринної функції ПЗ є секретин-церулеїновий або секретин-панкреозиміновий тести, проте вони зазвичай проводяться лише в спеціалізованих центрах і займають багато часу [10]. Пацієнти здебільшого звертаються для обстеження, коли залишається 10% екзокринної функції ПЗ, що призводить до мальабсорбції ліпідів [4]. Стеаторея (пінисті, з неприємним запахом випорожнення), втрата маси тіла, дискомфорт у животі є типовими симптомами та пов’язані з неадекватним перетравленням ліпідів. Навіть за значної недостатності ПЗ переварювання білка та крохмалю зазвичай підтримується на нормальному фізіологічному рівні. Проте, щойно прогресує недостатність ПЗ, мальабсорбція ліпідів стає головною проблемою та причиною багатьох клінічних симптомів і дефіциту харчування.
Ускладнення
Пацієнти з ЕНПЗ часто змінюють свій раціон, щоби зменшити споживання важко засвоюваних продуктів. Кореляція між зовнішньосекреторною недостатністю ПЗ, вторинною причиною захворювання або станом і хронічним недоїданням, що виникає внаслідок дефіциту поживних речовин і мальабсорбції жиру, є причиною тривалих ускладнень. Наслідки аномального перетравлення ліпідів призводять до розладів харчування з порушенням всмоктування жиророзчинних вітамінів (A, D, E, K), збідненням мікроелементів і зниженням циркулювальних ліпопротеїнів. Сама ЕНПЗ може спричинити або посилити порушення моторики, що здатне призвести до швидкого спорожнення шлунка та змінити рухливість дуоденального каналу й жовчного міхура. У пацієнтів відзначається швидший транзит тонкою кишкою. Недоїдання при цьому асоціюється з підвищеним ризиком інфікування, серцево-судинних захворювань, саркопенії й остеопорозу та може призвести до збільшення захворюваності та смертності, зниження якості життя пацієнтів [7].
Замісна терапія
Ферментні препарати призначають перорально, вживають під час основних прийомів їжі або перекусів у дозах, які з терапевтичною метою можуть бути скореговані. Застосування пероральної терапії передує створенню Управління з контролю якості продуктів харчування та лікарських засобів США (FDA) в 1938 році, й нині заміна ферментів є основою терапії в пацієнтів, у яких діагностовано порушення всмоктування через ЕНПЗ [10]. Головною метою замісної терапії панкреатичними ферментами є забезпечення достатньої активності ліпази у дванадцятипалій кишці [17]. При цьому необхідно мінімізувати мальабсорбцію поживних речовин, особливо ліпідів, для чого важливо досягти адекватної концентрації активних ферментів ПЗ у дванадцятипалій кишці одночасно з доставкою їжі.
Відомо, що вплив соляної кислоти на панкреатичні ферменти призводить до руйнування 90% їх кількості. Препарати з кишковорозчинним покриттям були розроблені, щоб уникнути інактивації в шлунку, оскільки фермент захищений покриттям від кислого середовища, а потім розчиняється у дванадцятипалій кишці, коли рН перевищує 5,3-5,5. Однак ефективної доставки та вивільнення важко досягти, оскільки рН у шлунку може коливатися від 6 унаслідок буферної здатності їжі до 2 під час їди, а рН дванадцятипалої кишки коливається від 4 до 6 з високою індивідуальною мінливістю. Фактично характеристики розчинення допоміжних речовин сильно відрізняються з погляду оптимального рН (наприклад, 5 або 5,8) та часу (від 49 до 71 хв для періоду напіввивільнення), не біоеквівалентні in vitro та, ймовірно, in vivo, а також залежать від рН вмісту дванадцятипалої кишки. Перші препарати, покриті оболонкою, яка розчиняється в тонкому кишечнику, не потрапляли до дванадцятипалої кишки так швидко, як дрібні частинки їжі, що погіршувало їхню здатність сприяти травленню. Пізніше почали використовувати технологію мікросфер із покриттям, стійким до дії шлункового соку та розчинним у pH тонкого кишечнику, що дає змогу стабілізувати систему доставки. Дослідження продемонстрували, що розмір частинок або мікросфер впливає на доставку до дванадцятипалої кишки, а частинки меншого розміру спорожнюються швидше й оптимальний розмір становить 1,4 мм [10].
Ефективність схеми лікування оцінюють за досягненням задовільних нутритивних результатів і нівелюванням симптомів [3]. Замісна ферментотерапія відіграє важливу роль у разі муковісцидозу [13], ефективна й у разі целіакії [12].
Останнім часом активно вивчають ефективність і безпечність застосування поліферментних препаратів бактеріального походження. Мікробні ферменти є потужнішими й ефективнішими, ніж панкреатин тваринного походження, внаслідок чого менша кількість одиниць мікробних ферментів дає еквівалентні результати порівняно з ферментом ПЗ тваринного походження [11, 19]. Було доведено, що збільшення абсорбції жирів і білків цими мікроорганізмами суттєво впливає на ліпідний профіль і фізичний розвиток [16]. Доведено, що ферментна замісна терапія з використанням ферментів мікробного походження суттєво покращує травлення в людей [18]. За результатами рандомізованого подвійного сліпого плацебо-контрольованого дослідження з паралельними групами оцінювали безпечність та ефективність у пацієнтів із функціональною диспепсією багатоферментного комплексу бактеріального походження. Сорок пацієнтів були рандомізовані у співвідношенні 1:1 на дві групи: 20 пацієнтів отримували протягом 60 днів багатоферментний комплекс, інші 20 пацієнтів – плацебо. Вживання багатоферментного комплексу мало значно більший ефект (p<0,001) порівняно з плацебо. Не повідомлялося про несподівані реакції, пов’язані з продуктами дослідження. Не було виявлено клінічно значущих відхилень у фізичних даних і статистично значущих змін біохімічних і гематологічних показників [14].
Ці мікробні ферменти було оцінено в клінічних випробуваннях фази II та III у пацієнтів з ЕНПЗ і муковісцидозом. У міжнародному контрольованому рандомізованому подвійному сліпому плацебо-контрольованому дослідженні за участю 138 осіб ліпаза, протеаза й амілаза мікробного походження призначалися в різних дозах 117 пацієнтам із муковісцидозом протягом 28 днів. Найефективнішим виявилося лікування хворих, які отримували по 25 000 од. ліпази та протеази, а також 3750 од. амілази [6]. Встановлено, що ліпротамаза (містить високоочищені біотехнологічного походження ліпазу, протеазу й амілазу) добре переноситься, істотно підвищує всмоктування ліпідів і білків, зменшує вагу випорожнень [5].
При перетравленні вуглеводів гліколіз, індукований сумішшю мікробних ферментів, розпочався через 20 хв від початку процесу травлення, амілаза та глюкоамілаза продемонстрували активність у кислих умовах шлунку, а через 2 год у шлунку дія мікробних ферментів була ефективнішою в 7 разів, аніж у разі застосування панкреатину тваринного походження. Тваринний панкреатин неактивний у шлунку, оскільки його доставка відбувається в кишковорозчинних гранулах, щоб уникнути інактивації кислотою. Ефективність протеолізу під впливом суміші мікробних ферментів була очевидною після 2 год травлення в шлунку, хоча існувала можливість насичення ферменту під час перебування в кишечнику, при цьому ферменти зберігали протеолітичну активність у кишечнику протягом 2 год. Ці результати вказують на ефективність суміші мікробних ферментів, яку слід використовувати як добавку для перетравлення їжі в людей із порушеннями травлення та/або ЕНПЗ. Окрім того, переважне перетравлення їжі в шлунку забезпечить добре перетравлений хімус дванадцятипалої кишки, що запобігає розладу травлення та відчуттю переповнення шлунку [8].
В Україні суміш мікробних ферментів представлена засобом Панжест (Pangest) із системою доставки «капсула в капсулі», яка використовується для захисту ферментів і дає змогу доставляти ферменти в певні відділи шлунково-кишкового тракту. Зовнішня капсула розпадається після потрапляння в шлунок, де травні ферменти, обрані для вивільнення в шлунку, розщеплюють їжу на менш складні та легше засвоювані поживні речовини. Ці ферменти активні та стабільні в умовах кислого рН шлунку. Внутрішня капсула виготовлена з рослинного полімеру, розпадається в кишечнику. Унікальні полімерні властивості розроблені для протистояння кислим умовам шлунку та захищають внутрішню капсулу від розпаду та вивільнення її вмісту до потрапляння в тонкий кишечник. Отже, весь вміст ферментів внутрішньої капсули потрапляє в тонкий кишечник, де вони стимулюють перетравлення їжі замість ферментів ПЗ. Ферменти відібрані таким чином, щоб забезпечувати їхню активність у діапазоні рН тонкого кишечнику. Панжест містить ліпазу (3200 од. у зовнішній, 4500 од. Міжнародної федерації фармацевтики – у внутрішній капсулі), амілазу (1720 і 2250 од. декстринізації відповідно), глюкоамілазу (11,2 та 6 од. вимірювання амілоглюкозидази), мальтодекстрин, α-галактозидазу (62,5 од. вимірювання активності галактозидази у внутрішній капсулі), протеазу 3,0 (62,5 од. вимірювання спектрофотометричної кислої протеази), протеазу 4,5 (2496 од. вимірювання гемоглобіну на основі тирозину в зовнішній капсулі та 500 – у внутрішній), протеазу 6,0 (1500 од. вимірювання гемоглобіну на основі тирозину), нейтральну протеазу (по 1500 од. мікробної протеази).
Попереднє перетравлення їжі в шлунку запобігає розвитку розладів шлунку та відчуття переповнення, оскільки належний добре засвоюваний хімус буде доставлений до тонкого кишечнику. Застосування травних ферментів збільшує засвоєння жиру та запобігає порушенню засвоєння поживних речовин у пацієнтів із розладами ПЗ, як-от муковісцидоз.
У ході дослідження ліполітичної ефективності було доведено, що ферменти Панжест є ефективнішими в перетравленні жиру, ніж тваринний панкреатин. Відзначено посилення ліполізу на вході у дванадцятипалу кишку в 19 разів. Що стосується перетравлення вуглеводів, то амілаза та глюкоамілаза продемонстрували активність у кислих умовах шлунку. Як і очікувалося, тваринний панкреатин був неактивний за цих умов рН, оскільки його доставка відбувалася в кишковорозчинних гранулах, щоб уникнути інактивації кислотою. Гліколіз, індукований ферментами Панжест, розпочинався через 20 хв після прийому їжі, а через 2 год у шлунку він був у 7 разів ефективнішим, аніж у разі використання тваринного панкреатину. Ефективність протеолізу під впливом ферментів Панжест відзначалася протягом 2 год травлення в шлунку. У кишечнику ферменти зберігали протеолітичну активність протягом іще 2 год.
Отже, клінічна ЕНПЗ виникає, коли секрет ПЗ не підтримує нормальну функцію травлення, що призводить до порушення всмоктування поживних речовин та інших симптомів, як-от діарея, що впливає на якість життя й у підсумку зумовлює недоїдання. Корекція вищевказаних порушень подеколи може не лише сприяти зменшенню проявів зовнішньосекреторної панкреатичної недостатності, а й запобігати її загостренню.
Результати останніх досліджень доводять, що ферменти мікробного походження є ефективнішими, зберігають свою стабільність в умовах нагрівання й інактивації шлунковою кислотою й активні за ширшого діапазону рН порівняно з травними ферментами тваринного походження. При цьому завдяки ферменту α-галактозидазі зменшується утворення кишкових газів після прийому їжі з високим вмістом клітковини. Дослідження in vivo на тваринах і результати клінічних досліджень показали ефективність і безпечність використання ферментів мікробного травлення для усунення ЕНПЗ. Варто враховувати, що пацієнту з ЕНПЗ важливо також змінити спосіб життя (наприклад, припинити вживати алкоголь і курити) [9].
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 23-24 (516-517), 2021 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...