Чому рак легені діагностують на пізніх стадіях розвитку
 Рак легені (РЛ) є найчастішим онкологічним захворюванням у світі (H. Sung et al., 2021). У 2020 р. на РЛ захворіло понад 19 млн осіб, а померло близько 10 млн, що у структурі онкологічної захворюваності і смертності склало 11,4 та 18,0% відповідно. В Україні у 2019 р. захворіло 12 720 осіб, серед них 10 126 чоловіків і 2594 жінки. Необхідно підкреслити, що серед захворілих не прожили й одного року після установлення діагнозу 60,0% чоловіків і 49,5% жінок (З.П. Федоренко та ін., 2021).
Рак легені (РЛ) є найчастішим онкологічним захворюванням у світі (H. Sung et al., 2021). У 2020 р. на РЛ захворіло понад 19 млн осіб, а померло близько 10 млн, що у структурі онкологічної захворюваності і смертності склало 11,4 та 18,0% відповідно. В Україні у 2019 р. захворіло 12 720 осіб, серед них 10 126 чоловіків і 2594 жінки. Необхідно підкреслити, що серед захворілих не прожили й одного року після установлення діагнозу 60,0% чоловіків і 49,5% жінок (З.П. Федоренко та ін., 2021).
У чоловіків РЛ посідає перше місце серед усіх онкологічних захворювань. За даними різних авторів, в Україні й інших країнах РЛ у 60-70% випадків діагностують у III-IV клінічній стадії, коли використати повний обсяг спеціального лікування уже неможливо (Л.С. Болгова и др., 2020; W.D. Travis et al., 2015).
Описана критична ситуація обґрунтовує необхідність наукових розробок у напрямі ранньої діагностики, гістогенезу, характеру росту, швидкого прогресування РЛ, які могли б сприяти підвищенню ефективності лікування та визначенню профілактичних засобів. Виконані до цього часу численні наукові дослідження стосовно зазначених питань поки що не дали бажаних результатів. Досі залишається багато невирішених питань, які могли б прояснити підходи до адекватної рентгенологічної та морфологічної діагностики на більш ранніх стадіях розвитку РЛ, від чого залежить успіх лікування.
Оприлюднені результати численних експериментальних досліджень, присвячених гістогенезу РЛ, свідчать про різні погляди науковців на клітини, з яких бере свій початок це захворювання (G. Ferone et al., 2020). Патологоанатомічні дослідження A. Have-Opbroek та співавт. (1997) дозволили стверджувати, що РЛ формується як з альвеолярного, так і з циліндричного епітелію бронхів. Однак у відомих фундаментальних дослідженнях (Э.Р. Вейбель, 1970; В.В. Ерохин и др., 2000; А.К. Загорулько, Т.А. Аскарі, 2002), виконаних на всіх рівнях ієрархічних ступенів розвитку епітеліальних клітин легені, доведено, що стовбуровими клітинами цього органа є пневмоцити 2 типу (альвеолярний епітелій – АЕ – 2 типу).
Виконуючи науково-дослідну роботу, присвячену РЛ, ми визначили, що з поверхні пухлин, розгалужених у великих бронхах, не завжди можна отримати пухлинні клітини. При дослідженні взятих під час виконання фібробронхоскопії мазків з екзофітного пухлинного вузла в цитологічних препаратах ми лише в 25% випадків виявили ракові клітини. Виконане дослідження аналогічних зіскрібків з поверхні екзофітних пухлин бронха на операційному матеріалі 31 хворого дозволило отримати пухлинні клітини у 9 (28%), у решти 22 (72%) визначено тільки клітини циліндричного епітелію, яким вкрита слизова оболонка бронха в нормі. Цей факт дозволив зробити висновок про те, що злоякісна пухлина росте під епітелієм бронха.
Невизначеність багатьох питань розвитку і росту РЛ зумовило необхідність звернутися до літератури, щоб отримати найбільш повну морфологічну та функціональну характеристики епітеліальних клітин легені.
Ми вивчили фундаментальні праці Э.Р. Вейбель (1970), И.К. Есиповой (1975), В.В. Ерохина и соавт. (2000), присвячені морфології ієрархічних епітеліальних структур легені в нормі і в патології. При цьому визначено, що респіраторний відділ легені складається з 20 тисяч респіраторних бронхіол. Кожна з них підрозділяється на альвеолярні ходи, а кожен альвеолярний хід закінчується двома альвеолярними мішечками. На стінках респіраторних бронхіол є окремі альвеоли, які відкриваються в просвіт бронхіол, а на стінках альвеолярних ходів розміщується декілька десятків альвеол. В організмі людини нараховується 300-400 млн альвеол. Їх загальна площа становить 90-120 м2, а в окремих випадках збільшується до 194 м2. При видиху вона зменшується в 2,0-2,5 раза (В.В. Ерохин и др., 2000).
И.К. Есипова (1975) доповнила структурні дані щодо бронхіального дерева. Вона обґрунтувала, що будова легеневих структур під плеврою подібна до структур у воротах легені, а Ф. Неттер, незалежно від И.К. Есиповой, продемонстрував цей факт на схемі (рис. 1; Ф. Неттер, 2019). Це означає, що у воротах легені також є бронхіоло-альвеолярні структури, які відходять від великих бронхів. Цей факт підтверджують інші автори (A. Giangreco et al., 2002; J.B. Sneddon et al., 2007).
 Рис. 1. Подібність будови легені в периферичному відділі й анатомічних воротах: безпосередній ріст бронхіол з ацинусами від великих бронхів (Ф. Неттер, 2019)
Рис. 1. Подібність будови легені в периферичному відділі й анатомічних воротах: безпосередній ріст бронхіол з ацинусами від великих бронхів (Ф. Неттер, 2019)
Вчені визначили, що морфологічні і відповідно функціональні відділи легені складаються з анатомічного мертвого простору, під яким розуміють кондуктивну, тобто повітропровідну, частину дихального дерева – бронхи, а під альвеолярним мертвим простором – сукупність альвеол, у яких збережена тільки вентиляція. У цих місцях, як стверджують дослідники (Э.Р. Вейбель, 1970; В.В. Ерохин и др., 2000), розвивається альвеолярний шунт. Саме в цьому місці складаються умови для постійної шкідливої дії хімічних і біологічних реагентів на клітини альвеолярного епітелію. На перших етапах відбувається стимуляція захисної реактивної проліферації, а в згодом це може сприяти розвитку численних захворювань, у тому числі ракових. У разі постійної дії на велику площу (100-194 м2) альвеолярного епітелію не завжди чистого повітря, а забрудненого і з цигарковим димом, виникають реактивні зміни альвеолярного епітелію різного ступеня. Саме клітини АЕ 2 типу, які, за даними багатьох авторів, належать до стовбурових клітин (СК), починають проявляти свою здатність до проліферації й активного надмірного росту, що може призвести до розвитку РЛ (T.J. Desai et al., 2014; W.S. Heng et al., 2019; S.D. Reynolds et al., 2000).
Вчені стверджують, що РЛ починає свій розвиток з АЕ – з плюрипотентних СК. Крім того, у клітинах АЕ 2 типу знайдено пухлинний антиген – цитокератин-19 (A. Gazdar et al., 2004).
Респіраторні альвеолярні клітини мають неправильну витягнуту форму. На вільній поверхні цитоплазми цих клітин є мікроворсинки, спрямовані в порожнину альвеол, що значно збільшує загальну площу контакту повітря з поверхнею епітелію.
Великі альвеолярні клітини сьогодні належать до пневмоцитів 2 типу. Вони ще називаються секреторними, тому що секретують ліпопротеїдні речовини (сурфактант), які створюють плівку на поверхні епітелію (И.К. Есипова, 1975). Установлено також, що клітинам АЕ 2 типу характерні 4 види функціональної активності: секреторна, реутилізація молекул деградованого сурфактанту, всмоктування рідини з альвеол і репродуктивна.
Значний об’єм секреції, велика сумарна площа апікальної поверхні альвеол, обернутої в порожнину альвеол, та наявність клітин, що є джерелом поверхнево активних речовин і білка, дозволили вченим прийти до висновку, що респіраторний відділ легені людини є активно синтезуючою залозою (Л.К. Романова, 1984; В.В. Ерохин и др., 2000).
Найважливішими показниками проліферативної активності клітин є мітотична активність і час їх оновлення. Виконані дослідження дозволили установити високу мітотичну активність в АЕ 2 типу. На експериментальних моделях вивчена мітотична активність епітелію трахеї, що склала 3,4 на 1000 клітин, у бронхах середнього калібру – 1,0-1,5, у дрібних бронхах – 0,5-1,5 і в 5-6 разів більше у клітинах міжальвеолярних перегородок, у яких діляться клітини АЕ 2 типу, – 8,25. Найбільш активно проліферуючою клітинною структурою є АЕ 2 типу, на яку припадає 50% мітозів серед всіх епітеліальних клітин легені (Э.Р. Вейбель, 1970; И.К. Есипова, 1975; В.В. Ерохин и др., 2000). Саме цим клітинам належить також дуже важлива роль у відновних процесах у разі гострих і хронічних запальних захворювань, які супроводжуються збільшенням їх кількості й ознаками гіперплазії.
Другим важливим аргументом проліферативної активності АЕ 2 типу є час оновлення епітеліальних клітин легені. Проведені дослідження дозволили встановити час оновлення клітин епітеліальної вистилки трахеї – 47,6 доби, великих бронхів – 18,1, середніх – 7-10, дрібних – 167-200, а в клітинах міжальвеолярних перегородок, де міститься АЕ 2 типу, цей час найкоротший – 3-7 діб (Э.Р. Вейбель, 1970).
Відомо, що ступінь кровопостачання тканин є передумовою для росту і поділу клітинних структур. Так, альвеоли мають максимальне кровопостачання у вигляді вузькопетлистої капілярної сітки, яка щільно обплітає кожну альвеолу (рис. 2; Р.А. Синельников, 2010).
 Рис. 2. Часточка легені, максимальне кровопостачання альвеол (за Р.А. Синельниковим, 2010)
Рис. 2. Часточка легені, максимальне кровопостачання альвеол (за Р.А. Синельниковим, 2010)
За даними Э.Р. Вейбель (1970), альвеолярні кровоносні капіляри формують густу сітку, як тонке безперервне судинне полотно площею 35-40 м2. Ця капілярна сітка поширюється в межах легеневих часточок, а в деяких ділянках легені – на сегменти і навіть на частки легені. Суміжні стінки альвеол, альвеолярних ходів, респіраторних бронхіол формують загальну для прилеглих до них респіраторних структур стінку.
Установлене максимальне кровопостачання забезпечує ріст і можливість реактивної проліферації, а у разі хронічної дії біологічних і хімічних реагентів може виникнути нестримний ріст клітин, порушення їх диференціації, що спостерігається при злоякісному рості (Э.Р. Вейбель, 1970; В.В. Ерохин и др., 2000).
Сьогодні широко вивчаються питання СК легені в нормі і при патологічних процесах, які характеризуються швидким оновленням і найбільше вираженим потенційним ростом (А.К. Загорулько та ін., 2002; A. Giangreco et al., 2002; C.F. Kim et al., 2005; J.B. Sneddon et al., 2007). Досліджується також структурно-морфологічний комплекс епітеліальних клітин легені, так званої ніші. До них належать клітини переходу бронхіолярного епітелію в альвеолярний, підслизові залози трахеї і нейроендокринна тканина бронхів (A. Giangreco et al., 2002; L. Xiaoming et al., 2008). Ніші з епітеліальними клітинами звертають на себе особливу увагу при вивченні пухлинних процесів у легені насамперед тому, що існує модель, згідно з якою в результаті деяких порушень клітинних ніш спостерігається гіперекспресія проліферативних процесів, які стимулюють СК до проліферації і швидкого росту. Автори вивчили більш глибокі відношення СК в одній ніші і їх вплив на сусідні (J.B. Sneddon et al., 2007). Продемонстрована здатність самих трансформованих СК активувати інші клітини ніші. Таким чином реалізується зворотний зв’язок, що зумовлює подальшу проліферацію СК. Дослідники також стверджують про можливість трансформованих СК активувати не тільки клітини своєї ніші, а й сусідніх, що призводить до початку і поширення проліферації, а потім – до розвитку конкретних патологічних процесів.
Результати багаторічних досліджень структури легені в нормі і патології дозволили И.К. Есиповой (1975) дійти принципово нового висновку про те, що першою і головною морфофункціональною структурою, яка цілісно реагує на шкідливий агент, є термінальна бронхіола. Це важливе положення було схвалене і затверджене групою міжнародних експертів з морфологічної номенклатури. Іншими словами, авторка довела, що всі патологічні процеси в легені починаються з бронхіоло-альвеолярних структур.
Дещо пізніше В.В. Ерохин и соавт. (2000) підтвердили концепцію И.К. Есиповой. Вони також дійшли висновку, що найбільш простим і логічним визначенням захворювання пневмонія є запальний процес, який розвивається в респіраторному відділі легені. Отже, терміном «пневмонія» може бути позначений патологічний процес, що супроводжується появою в альвеолах і термінальних бронхіолах виражених ознак альтерації, ексудації та проліферації, пов’язаних з дією певного етіологічного фактора хімічної чи біологічної природи.
Результати експериментальних робіт дозволяють уточнити факт початку росту і розвитку РЛ з епітеліальних клітин, так званої ніші. Цими клітинами є АЕ 2 типу.
Детальне вивчення результатів експериментальних робіт стосовно гістогенезу РЛ (Л.А. Грицюте, 1975; Г.М. Веснушкин и др., 2006) дозволило визначити, що незалежно від того, яким шляхом тварині введено канцероген – ендотрахеально, внутрішньосудинно чи перитонеально, – пухлина розвивалася здебільшого в периферичному відділі легені, під плеврою, де немає великих бронхів. Результати фундаментальних досліджень згаданих авторів підтверджуються медичною практикою. Так, Н.О. Максимович (1980) на підставі вивчення патологоанатомічних препаратів при вірусній пневмонії, показала можливість первинного потрапляння повітря з дрібнодисперсним вмістом із вірусом грипу безпосередньо в порожнину альвеол з її первинним ураженням.
Вивчення патологоанатомічних особливостей росту і розвитку РЛ на операційному матеріалі з використанням сучасних морфологічних методів дослідження (Л.С. Болгова и др., 2013) дозволило підтвердити важливе наукове положення И.К. Есиповой про те, що патологічні процеси в легенях розвиваються з бронхіоло-альвеолярної частини респіраторного відділу. При гістологічному дослідженні матеріалів 120 хворих із різними гістологічними типами РЛ показано ріст пухлини з клітин АЕ. Для наочності продемонстровано в одній альвеолі клітини без атипії і поруч – ріст клітин з усіма ознаками ракової пухлини (рис. 3).
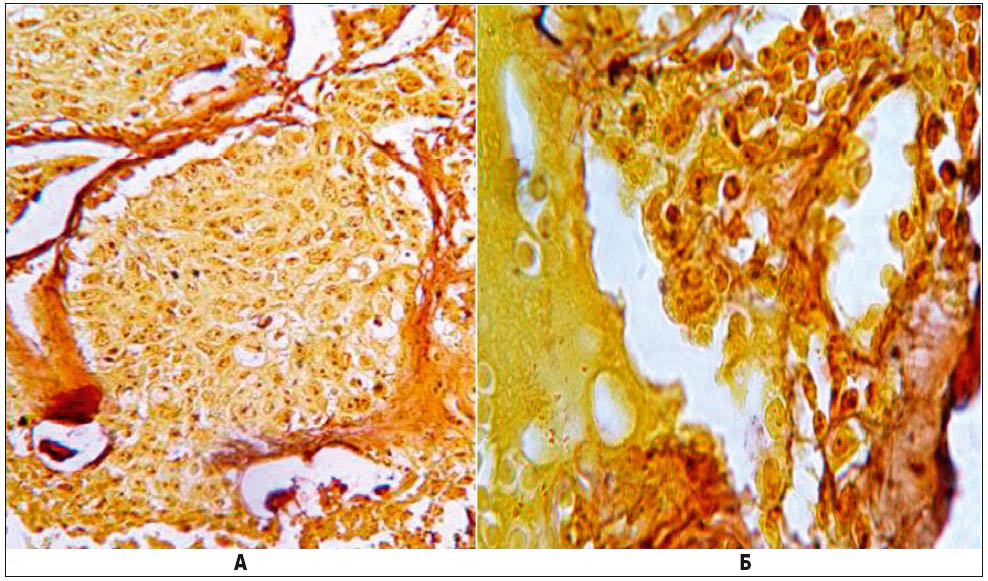 Рис. 3. Ріст пухлини в альвеолах. Гістологічний препарат, фарбування за W. Howell, D. Black: А – ×400; Б – фрагмент, ×1000 (Л.С. Болгова и др., 2013)
Рис. 3. Ріст пухлини в альвеолах. Гістологічний препарат, фарбування за W. Howell, D. Black: А – ×400; Б – фрагмент, ×1000 (Л.С. Болгова и др., 2013)
Спостерігається ріст пухлинних клітин від базальної мембрани в порожнину альвеоли. Результати підтверджені комплексом сучасних гістологічних, імуногістохімічних, цитологічних, імуноцитохімічних, цитогенетичних та електронно-мікроскопічних методів дослідження (Л.С. Болгова и др., 2013; Т.Н. Туганова и др., 2011).
Отримані наукові дані є обґрунтуванням того, що наявність на рентгенограмі затемнення будь-якого розміру є підставою для подальшого обстеження з метою виключення чи підтвердження ракового ураження. Поодинокі невеликі тіні до 3-5 мм можуть свідчити про початок захворювання, що потребує профілактичних засобів для запобігання подальшому прогресуванню, якщо немає можливості морфологічно верифікувати патологічний процес чи уникнути його прогресування. Це може бути новим базовим аргументом для розроблення програми профілактики легеневих захворювань і в першу чергу – РЛ.
Таким чином, виявлені об’єктивні морфологічні дані, отримані в експерименті і підтверджені патологоанатомічними і цитологічними дослідженнями з використанням сучасних морфологічних методів, є цілком переконливими щодо того факту, що АЕ 2 типу є СК легені в нормі і при розвитку патологічного процесу будь-якої етіології, у тому числі РЛ.
Іншими словами, розвиток РЛ починається з клітин АЕ 2 типу, яких у легені нараховуються мільйони, що довго забезпечує основну дихальну функцію органа. Ріст пухлини також відбувається безсимптомно і, коли пацієнти звертаються за медичною допомогою, лікарі в 60-70% випадків констатують ІІІ-ІV клінічну стадію РЛ.
Підсумовуючи викладені дані, можна стверджувати: пізня діагностика РЛ відбувається через початок розвитку захворювання з клітин альвеолярного епітелію, що не викликає клінічних проявів, і тільки велика маса пухлини може зумовлювати клінічні симптоми – слабкість, кашель тощо, які змушують пацієнта звертатися за медичною допомогою.
Література
- Болгова Л.С., Туганова Т.Н. Рак легкого: вопросы гистогенеза и цитологической диагностики. – К.: КИМ, 2013. – 168 с.
- Вейбель Э.Р. Морфометрия легких человека / Пер. с англ. Н.П. Вольберг; предисл. проф. Л.Л. Шика. – М.: Медицина, 1970. – 174 c.
- Веснушкин Г.М., Плотникова Н.А., Семенченко А.В., Анисимов В.Н. Мелатонин угнетает канцерогенез легких, индуцированный уретаном у мышей // Вопр. онкологии. – 2006. – Т. 52, № 2. – С. 164-168.
- Грицюте Л.А. Экспериментальные опухоли легких. – М.: Медицина, 1975. – 166 с.
- Ерохин В.В., Романова Л.К. Клеточная биология легких в норме и при патологии. – М.: Медицина, 2000. – 496 c.
- Есипова И.К. Легкое в норме. Ч. I. – Новосибирск: Наука, 1975. – 285 с.
- Есипова И.К. Легкое в патологии. – Ч. II. Новосибирск: Наука, 1975. – 248 с.
…
23. Xiaoming L., Engelhardt J.F. The Glandular Stem. Progenitor Cell Niche in Airway Development and Repair. ProcamThorac Soc. 2008: 5(6): 682-688.
Повний список літератури знаходиться в редакції.
Пропонуємо нашим читачам ознайомитися з новими роботами Лідії Севастянівни Болгової, орієнтованими на фахівців галузі та студентів медичних і біологічних факультетів.
 Цитологія органів і тканин людини / За ред. Л.С. Болгової. – К.: Книга-плюс, 2018.
Цитологія органів і тканин людини / За ред. Л.С. Болгової. – К.: Книга-плюс, 2018.
У навчальному посібнику подана структура клітин всіх органів і тканин людини, знання яких необхідні при освоєнні предмета цитологічної і гістологічної діагностики різних захворювань, насамперед онкологічних. Демонструються детальні цитоморфологічні ознаки клітин у нормі на мікрофотографіях хорошої якості, що допомагає морфологам вивчити особливості структури епітеліальних і мезенхімальних клітин різних органів і систем людського організму. Знання структури клітин необхідні для цитологів, котрі працюють у судовій медицині, для розпізнавання змінених органів, з яких отримують діагностичний матеріал. Посібник може стати доповненням до нових видань підручника «Гістологія».
Навчальний посібник орієнтований на лікарів, які займаються морфологічною діагностикою патологічних процесів: цитопатологів, патологоанатомів, цитологів судової медицини, курсантів медичних післядипломних навчальних закладів, студентів медичних університетів, біологічних факультетів і наукових співробітників.
 Цитоморфологічна діагностика пухлин людини / Л.С. Болгова. – К.: Книга-плюс, 2021. – 408 с.
Цитоморфологічна діагностика пухлин людини / Л.С. Болгова. – К.: Книга-плюс, 2021. – 408 с.
У навчальному посібнику вміщена коротка історична довідка про розвиток методу цитологічної діагностики в світі, на території СНД і в Україні. Цитологічна діагностика використовується не тільки для морфологічної верифікації доброякісних і злоякісних пухлин, локалізованих у різних органах і тканинах на будь-якій глибині, а й для скринінгу, що не потребує коштовної апаратури, лише підготовленого фахівця. У посібнику викладені основні принципи, методи і можливості цитологічної діагностики пухлин людини різних локалізацій. Наведені основні гістологічні та детальні цитоморфологічні ознаки доброякісних і злоякісних пухлин епітеліального і мезенхімального генезу. Нозологічні форми пухлин подані згідно з сучасними міжнародними гістологічними класифікаціями. Посібник ілюстрований кольоровими мікрофотографіями хорошої якості.
Навчальний посібник укладений за зразком підручника для морфологічної діагностики пухлин людини і рекомендований для цитопатологів, патологоанатомів, лікарів лабораторної діагностики, цитологів у судовій медичній експертизі, лікарів-онкологів, наукових співробітників, лікарів різних спеціальностей, які цікавляться онкоморфологією, та студентів медичних і біологічних факультетів університетів.
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (73) 2021 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




