Ефективність і безпека системних глюкокортикоїдів для знеболення при ревматоїдному артриті: систематичний огляд і метааналіз
Біль є симптомом, що найбільше турбує пацієнтів із ревматоїдним артритом (РА). Для швидкого полегшення болю в людей з активним РА у складі комбінованої хворобомодифікувальної терапії часто призначають глюкокортикоїди (ГК) [2, 3]. Короткочасне призначення низьких доз пероральних ГК вважається ефективною стратегією зменшення болю, але сила аналгетичного ефекту та його тривалість є недостатньо вивченими для діапазону доз ГК, що застосовуються в сучасній клінічній практиці [4, 5]. Для визначення ефективності та доцільності призначення ГК пацієнтам із РА з метою знеболення було проведено систематичний огляд і метааналіз. Огляд результатів представлено в цій статті.
Вступ
Хворобомодифікувальна терапія біологічними препаратами здатна зменшувати передусім інтенсивний біль, пов’язаний із високою активністю захворювання. Проте повне усунення болю спостерігається нечасто. Багато пацієнтів продовжують скаржитися на постійний біль, незважаючи на ефективне пригнічення запального процесу [8]. Вони продовжують відчувати біль у спокої та під час повсякденної активності, непокоїть підвищена чутливість суглобів за звичної рухової активності або незначного тиску на суглоби. Така больова чутливість може свідчити про сенситизацію периферичних або центральних ноцицептивних шляхів [9].
Хронічний біль у суглобах також може виникати при тривалому, недостатньо контрольованому захворюванні внаслідок розвитку поширеного вторинного остеоартрозу [13]. Отже, протиревматичних хворобомодифікувальних засобів може бути недостатньо для адекватного знеболення в пацієнтів із РА.
Представлене дослідження було спрямоване на визначення кількісної оцінки специфічних ефектів системних ГК на біль у разі РА протягом періоду їх призначення залежно від шляхів уведення та доз.
Методи
Пошук досліджень проводили в базах даних OVID Medline, OVID Embase та Cochrane Central до 22 жовтня 2020 р. Також пошук здійснювали в списках посилань публікацій. Рецензенти незалежно оцінювали заголовки, реферати та повні тексти у двох примірниках.
Дослідження шукали за такими характеристиками. Опис: перший автор, рік видання, назва дослідження та його реєстраційний номер. Учасники та клінічні дані на початковому етапі: кількість, вік, стать, шкала DAS, 28-суглобовий DAS (DAS28), HAQ й інші показники активності/тяжкості РА. Втручання: назви ГК та їхні дози, назви препаратів для хворобомодифікувальної терапії, шлях і тривалість уведення ГК, тривалість подальших оцінок. Результати: всі результати, пов’язані з болем, включаючи результати втоми в усі моменти часу.
Типи досліджень та учасники
В огляд було включено рандомізовані контрольовані дослідження, опубліковані в рецензованій літературі. Дослідження проводили за участю дорослих пацієнтів (віком понад 18 років), яким було встановлено діагноз РА відповідно до встановлених критеріїв [15].
Види втручань
Були включені ті дослідження, що порівнювали системні ГК з неактивним лікуванням (з іншими хворобомодифікувальними препаратами, які були однаковими в усіх досліджуваних групах) або лікування різними ГК чи різні схеми їх застосування (наприклад, дозування або шляхи введення). Один синтетичний агоніст глюкокортикоїдних рецепторів, ідентифікований під час пошуку, також було включено в огляд.
Кінцеві точки
Больові відчуття були розподілені на спонтанні та спричинені. Спонтанний біль передбачав біль у тілі, суглобах або біль уранці/ввечері. До спричиненого болю відносили біль, індукований дослідником із подальшою оцінкою за суглобовим індексом Річі (RAI), кількістю чутливих суглобів (TJC), кількісним сенсорним тестуванням больової чутливості, а також біль, що виникає під час руху. Додатково до опублікованого протоколу визначили втому як показник, пов’язаний із болем.
Статистичний аналіз і метааналіз
Проводили метааналіз болю, спричиненого болю та втоми. Стандартизовану середню різницю (SMD) розраховували для оцінки змін показників від вихідного рівня. Було також розраховано середні значення (MD), що давало змогу оцінити абсолютні показники, а не стандартизовані показники відносних ефектів. Ступінь неоднорідності визначали за допомогою статистики I2 і tau-статистики [19]. Аналіз у підгрупах було проведено для дослідження потенційних джерел варіацій: шлях уведення, тривалість лікування та ризик упередженості.
Результати
Усього було ідентифіковано 880 тез та оцінено 226 повних текстів. Надалі відібрали 33 повні тексти, в яких повідомлялося про ефективність ГК щодо спонтанного болю, 38 – щодо спричиненого болю, 26 – інші пов’язані з болем результати.
Жодне з досліджень не повідомляло про посилення болю у відповідь на лікування системними ГК, при цьому в більшості досліджень відзначалося істотне покращення стану під час подальшого спостереження.
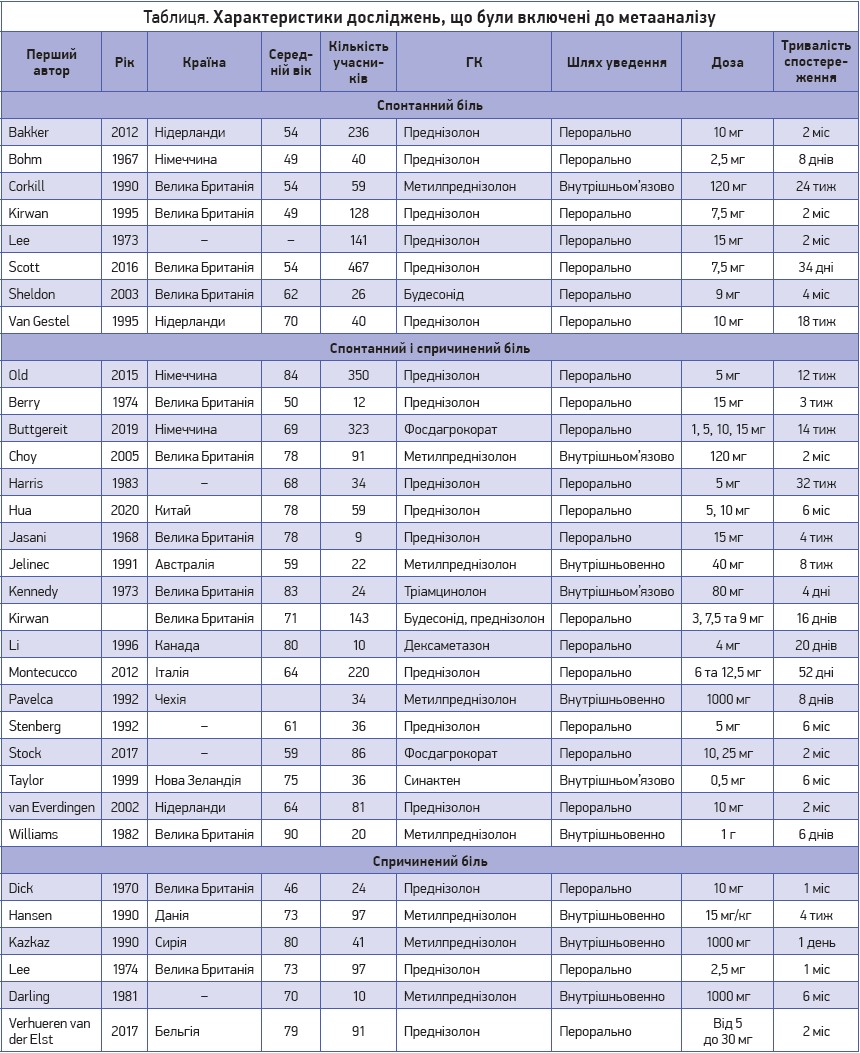
Загалом до метааналізу було включено 33 дослідження (у 26 оцінювали спонтанний біль, у 25 – спричинений біль). У більшості досліджень використовували ГК перорально, в чотирьох – внутрішньом’язово, в шести – внутрішньовенно, в одному – введення ГК за допомогою іонофорезу. У згаданих дослідженнях як ГК найчастіше застосовували преднізолон і метилпреднізолон (табл.).
Найчастіше для оцінки болю використовували 100-міліметрову візуально-аналогову шкалу (ВАШ), показники RAI та TJC. Усього в 33 дослідженнях було залучено 3123 учасники (70% жінок). Середній вік учасників становив 55 років. Базові характеристики активності захворювання вказували на активний РА.
Спонтанний біль
Метааналіз найбільш ранніх результатів досліджень щодо впливу ГК на спонтанний біль продемонстрував зниження спонтанного болю на тлі прийому цих препаратів: SMD -0,67 (від -0,84 до -0,50; 95% довірчий інтервал (ДІ) зі значною гетерогенністю (I2=62%, tau=0,28, p<0,01).
Пероральні ГК, які вивчали окремо (15 досліджень), продемонстрували статистично значуще зниження спонтанного болю з показником SMD -0,65 (від -0,82 до -0,49) із вираженою гетерогенністю (I2=56%, tau=0,21, p=0,0045). Середнє зниження показника за ВАШ становило 11 мм (від 15 до 7 мм).
У подальшому підгруповому аналізі досліджували вплив тривалості курсу пероральних ГК на динаміку спонтанного болю. Виявилося, що ефективність знеболення є найвищою в перші місяці терапії ГК, після чого починає знижуватися. Зокрема, середнє зменшення показника за ВАШ було найвираженішим (-15 мм) серед пацієнтів, які приймали ГК протягом 0-3 міс. Для більшої тривалості лікування (>3-6 міс і >6 міс) зниження становило 8 і 7 мм відповідно.
У дослідженнях, що були оцінені як дослідження високої якості, також було отримано подібні результати лікування ГК. Найбільш ранні результати випробувань високої якості (n=14) продемонстрували досягнення показника SMD -0,57 (95% ДІ від -0,73 до -0,42). Не було виявлено зв’язку між шляхом уведення та знеболювальним ефектом.
Спричинений біль
Метааналіз усіх досліджень щодо оцінки спричиненого болю продемонстрував у найбільш ранні часові проміжки SMD -0,57 (95% ДІ від -0,75 до -0,41) зі значною гетерогенністю (I2=72%, tau=0,42, p (Q) <0,001 (р Еггера = 0,0041). При цьому найвираженіше та статистично значуще зниження спричиненого болю спостерігалося саме на тлі прийому пероральних ГК (15 досліджень): SMD -0,71 (95% ДІ від -0,97 до -0,45; із гетерогенністю I2=78%, tau=0,43, p (Q) <0,001).
Окрім того, на тлі прийому пероральних ГК відзначалося покращення показників RAI (9,7 бала) та TJC (2,5 чутливих суглобів). Із метою вивчення впливу тривалості застосування пероральних ГК на спричинений біль було проведено підгруповий аналіз. Найпомітніше покращення за показниками RAI (10 балів) і TJC (3,6 чутливого суглоба) досягалося протягом перших 3 міс лікування. У підгрупі пацієнтів, що отримували ГК понад 6 міс, спостерігалося закономірне зниження ефективності терапії (покращення за TJC становило 0,8, а за RAI – 2,3 бала).
У дослідженнях високої якості (n=16) було отримано подібні результати: SMD -0,52 (від -0,73 до -0,31). Шляхи введення ГК по-різному впливали на спричинений біль. Найбільша ефективність знеболення спостерігалася в разі перорального введення ГК: SMD -0,71 (95% ДІ від -0,97 до -0,45; 15 досліджень). У разі внутрішньом’язового введення SMD становив -0,08 (95% ДІ від -0,53 до 0,35; 3 дослідження), внутрішньовенного – -0,33 (95% ДІ від -0,76 до 0,10; 6 досліджень).
Дослідження скасування ГК та пряме порівняння між ГК або схемами лікування
Як спонтанний, так і спричинений біль посилювалися при скасуванні ГК у більшості досліджень. Прямі порівняння різних пероральних ГК показали, що бетаметазон у дозі 1 мг на добу та преднізолон у дозі 8 мг на добу мали подібну ефективність порівно з будесонідом у дозуванні 9 і 3 мг на добу [44]. Одне випробування, в якому застосовували частковий агоніст глюкокортикоїдних рецепторів фосдагрокорат у дозі 15 мг на добу дало подібні результати до 10 мг преднізолону, але сильніший вплив на спонтанний біль, аніж 5 мг преднізолону через 8 тиж [37]. Інше дослідження фосдагрокорату виявило подібну його ефективність у дозі 25 і 10 мг на добу порівняно з преднізолоном у дозі 7,5 і 5 мг на добу [49]. У дослідженні CAPRA‑1 преднізолон пролонгованого вивільнення забезпечив подібне полегшення болю порівняно з преднізолоном стандартного вивільнення після 12-тижневого прийому [75].
Втома
У п’яти дослідженнях вивчали вплив прийому системних ГК на втому [28, 32, 34, 35, 89, 92]. У трьох випробуваннях повідомлялося про зменшення втоми на тлі застосування системних ГК порівняно з плацебо (два високоякісні подвійні сліпі дослідження [28, 35] та одне відкрите [32]) при оцінюванні за такими шкалами, як FACIT-F (функціональна оцінка терапії хронічного захворювання), ВАШ, Short Form 36-Vitality. У цих дослідженнях брали участь 907 осіб, які застосовували пероральні ГК тривалістю від 12 до 28 тиж. Метааналіз дав можливість припустити, що ГК асоціюється зі зменшенням утоми в пацієнтів із РА порівняно з плацебо: SMD -0,24 (95% ДІ від -0,47 до 0,001) [28, 32, 35]. Повідомлялося, що скасування пероральних ГК (або заміна на плацебо) підвищувало втому у двох дослідженнях [89, 92].
Обговорення
Отримані дані свідчать, що системні ГК зменшують біль і його наслідки в людей з активним РА. Системні ГК також можуть зменшувати втому в людей з активним РА. Поліпшення болю при застосуванні системних ГК було найвираженішим протягом перших 3 міс від початку лікування, однак ефект ставав менш вираженим після 6 міс терапії. Системні ГК часто застосовують для полегшення симптомів у пацієнтів з активним РА. Чинні британські настанови рекомендують використовувати ГК на ранніх стадіях РА з метою стримування запалення [2], і подібні дослідження було включено в цей метааналіз. Тривале використання ГК рекомендується, якщо хворобомодифікувальна терапія іншими біологічними препаратами виявилася неефективною [2]. На індивідуальному рівні поліпшення болю на 10-20 мм за 100-міліметровою ВАШ можна вважати клінічно важливим досягненням [93]. Середньостатистичні ефекти після перших 6 міс лікування можуть не мати клінічного значення та свідчать про те, що менш ніж половина учасників, які отримують довготривале лікування ГК, мають клінічно значуще покращення порівняно з плацебо.
Системні ГК також знижували втому, але покращення було незначним порівняно з плацебо. Відсутність аналгетичної реакції доза-відповідь для пероральних ГК або між пероральними та парентеральними ГК може свідчити про те, що максимальний аналгетичний ефект досягається при застосуванні низьких доз (можливо, ≤15 мг перорального преднізолону на добу). Тривале застосування ГК, особливо у високих дозах, пов’язане з ризиком небажаних явищ, включаючи повну заміну суглоба, ризик переломів, цукровий діабет і серцево-судинні захворювання [7, 94]. Системні ГК є ефективною стратегією зменшення болю в людей з активним РА, але користь може не перевищувати ризики, пов’язані з тривалим лікуванням.
В описаному метааналізі больові відчуття були розподілені на спонтанні та спричинені. Автори виявили подібну ефективність зниження як спонтанного, так і спричиненого болю при застосуванні системних ГК.
Втома відображає механізми в центральній нервовій системі, тісно пов’язані з центральною сенсибілізацією та болем, тому зменшення втоми також є важливим результатом терапії осіб із РА [12, 95]. Системні ГК проникають крізь гематоенцефалічний бар’єр і можуть чинити психоактивні ефекти (деякі з яких можуть бути небажаними) [96]. Однак аналгетична відповідь на ГК, найімовірніше, пояснюється їхньою протизапальною дією в суглобах, а не дією на рівні центральної нервової системи. Відносно незначне зменшення втоми у відповідь на лікування ГК також може свідчити про відсутність значущого впливу ГК на центральні механізми.
Представлений метааналіз має деякі обмеження. Не всі дослідження повідомляли про вплив лікування на біль і не всі отримані дані підлягали метааналізу. Проте результати метааналізу було підтверджено іншими дослідженнями, включеними в систематичний огляд. У дослідженнях використовували різні схеми лікування, як-от переключення та комбінована терапія, хоча всі випробування давали змогу визначати специфічні ефекти ГК.
Системні ГК можуть використовуватися також як агенти, що модифікують перебіг захворювання [3, 4]. Однак інші аспекти якості життя, крім болю та втоми, які є важливими для пацієнтів, не були розглянуті в цьому метааналізі. Вплив на біль може відрізнятися залежно від того, чи був біль основним показанням для застосування ГК. Результати досліджень було отримано на основі самозвітів пацієнтів, що є певним обмеженням у дослідженнях болю, який за визначенням є суб’єктивним досвідом. Багато випробувань були невеликими й зосереджені на короткому курсі лікування. Додаткові дослідження тривалістю понад 6 міс могли б дати точніші оцінки аналгетичної ефективності ГК.
Нинішнє використання ГК для лікування болю при РА значною мірою керується клінічним досвідом, а не надійними доказами рандомізованих контрольованих досліджень. Чимало пацієнтів із РА, які погано контролюють біль за допомогою хворобомодифікувальної терапії часто отримують ГК у високих дозах. За оцінками експертів, у США близько третини пацієнтів із РА використовують системні ГК [6]. Утім, користь від них із часом зменшується, тоді як ризик побічних явищ може зростати.
Результати, отримані при прямих порівняннях ГК, не дали змогу досягти консенсусу щодо ефектів різних схем цих препаратів [99], оскільки відібрані дослідження були неоднорідними й могли не відображати поточну клінічну практику. Щоб визначити, які пацієнти зможуть отримати найбільшу користь від системних ГК для персоналізованого лікування, треба подальші дослідження. Також потрібні додаткові дослідження, щоб визначити потенційні переваги та ризики скасування системних ГК у людей, які вже тривалий час застосовують ці препарати.
Висновки
Системні ГК здатні забезпечити досить швидкий і виражений аналгетичний ефект у осіб із РА, що мають недостатній контроль болю. Аналгетична дія триває зазвичай упродовж 3 міс із подальшим поступовим зниженням. Слід зазначити, що системні ГК також можуть зменшувати втому, яка чинить різко негативний вплив на якість життя пацієнтів із РА.
Довідка «ЗУ»
Метилпреднізолон (Медрол, Солу-Медрол, Pfizer) є одним із найвивченіших представників групи ГК та вважається одним із найбезпечніших препаратів для проведення ГК-терапії ревматичних захворювань. При застосуванні метилпреднізолону спостерігається нижча частота характерних для терапії ГК побічних ефектів навіть порівняно з преднізолоном, який широко використовується в клінічній практиці. Метилпреднізолон може успішно застосовуватися в різних режимах – від низькодозових до пульс-терапії. Зокрема, в дослідженні BARFOT тривале (протягом 2 років) використання низьких доз метилпреднізолону в поєднанні з базисною терапією раннього РА сприяло швидшому настанню ремісії, яка асоціювалася зі зменшенням деструкції кістки протягом 4 років спостереження. У дослідженні STIVEA метилпреднізолон у високих дозах (80 мг на добу) використовували в пацієнтів із раннім запальним поліартритом протягом 3 тиж, що сприяло віддаленню термінів призначення препаратів базисної терапії та запобіганню переходу гострого поліартриту в РА у 20% випадків.
McWilliams D.F., Thankaraj D., Jones-Diette1 J. et al. The efficacy of systemic glucocorticosteroids for pain in rheumatoid arthritis: a systematic literature review and meta-analysis. Rheumatology. 2022; 61: 76-89. doi: 10.1093/rheumatology/keab503.
Адаптований переклад з англ. В’ячеслава Килимчука
Медична газета «Здоров’я України 21 сторіччя» № 4 (521), 2022 р.
СТАТТІ ЗА ТЕМОЮ Ревматологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....
Зв’язок між рівнем сироваткової сечової кислоти (ССК) і ризиком серцево-судинних захворювань (ССЗ) упродовж багатьох років є предметом вивчення дослідників. Установлено, що рівень ССК – незалежний предиктор смерті від усіх причин і серцево-судинної смерті, зокрема від гострого коронарного синдрому, інсульту та серцевої недостатності (СН). Також опубліковано багато робіт про зв’язок між ССК і функцією нирок. Попри значну кількість публікацій, деякі моменти, а саме: яким є оптимальний поріг ССК для визначення ризику ССЗ, чи необхідна корекція значень ССК для функції нирок, чи є ССК ключовим патологічним елементом метаболічної дисрегуляції, потребують прояснення....