Альфа-ліпоєва кислота – потенціал застосування при діабетичній полінейропатії та інших станах: ефективність, особливості застосування, можливості лікування
Діабетична полінейропатія (ДП) – одне з найпоширеніших хронічних ускладнень цукрового діабету (ЦД), яке значуще погіршує якість життя пацієнтів із ЦД 1 і 2 типу. Епідеміологічні дані свідчать, що вже на момент встановлення діагнозу ЦД у 10-20% пацієнтів також виявляють периферичну нейропатію. За недостатнього контролю захворювання частота ДП зростає зі збільшенням стажу діабету. Так, через 5 років ЦД поширеність нейропатії становить 26%, а через 10 років це ускладнення розвивається у 41% пацієнтів із діабетом. Загалом, на певному етапі ДП виникає у від 50 до 66% хворих на ЦД [1].
Діабетична полінейропатія супроводжується збільшенням частоти госпіталізацій, погіршує якість і зменшує тривалість життя пацієнтів із ЦД. Такі ускладнення ДП, як виразки стопи та ампутації нижніх кінцівок, є найпоширенішими причинами госпіталізації осіб із ЦД у країнах Західної Європи. Показники смертності, особливо за наявності діабетичної автономної нейропатії серця (ДАНС), у пацієнтів із ДП також вищі, ніж у загальній популяції пацієнтів із ЦД. Так, середній рівень 10-річної летальності в пацієнтів із ЦД і ДАНС становить 27% проти 5% у пацієнтів без ознак ДАНС. Значуще погіршується й якість життя пацієнтів із ДП – через виражений біль, запаморочення, діарею та еректильну дисфункцію [2].
Доведено, що контроль глікемії є наріжним каменем у профілактиці розвитку та прогресування ДП, однак результати досліджень свідчать, що не менш важливо впливати і на інші ланцюги патогенезу ДП, зокрема оксидативний стрес [3]. Одним із найперспективніших у цьому аспекті засобів є альфа-ліпоєва кислота (АЛК), потенціал застосування якої не обмежується ДП. Щодо терапевтичної дії АЛК, варто зосередитися на доклінічних і клінічних дослідженнях, що оцінюють фармакологічні ефекти АЛК, також ураховуючи аспекти, пов’язані з її біодоступністю.
Огляд фармакологічних ефектів АЛК
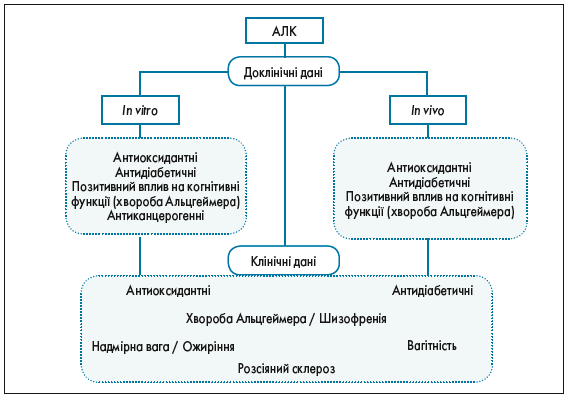
Перше клінічне застосування АЛК датується 1959 роком. Відтоді АЛК викликає зацікавленість як у дослідників, так і у клініцистів, а сфери її застосування безперервно розширюються. Фармакологічні ефекти АЛК в лікуванні ДП передусім пов’язані з її антиоксидантною активністю, однак крім того результати експериментальних і клінічних досліджень підтверджують її детоксикаційні, протизапальні, протиракові та нейропротекторні властивості, а також демонструють позитивний вплив АЛК на стан серцево-судинної системи та когнітивні функції, що відображено на рисунку [4].
Антиоксидантний потенціал АЛК
Є безліч літературних даних щодо антиоксидантних властивостей АЛК, зокрема утворення хелатних комплексів із металами, поглинання вільних радикалів, відновлення ендогенних антиоксидантів, таких як глутатіон, вітаміни C і E, і прискорення репарації після пошкоджень, спричинених оксидативним стресом. Здатність АЛК хелатувати метали пояснюється наявністю тіолових груп. Крім того, АЛК підвищує внутрішньоклітинний рівень глутатіону, який зв’язує та виводить з організму широкий спектр токсинів, особливо токсичних металів.
Дослідження Goralska та співавт. показало, що введення АЛК сприяло зменшенню концентрації іонів заліза в епітеліальних клітинах. Це супроводжувалося підвищеною резистентністю клітин до дії перекису водню, що означає, що АЛК безпосередньо зменшує оксидативний стрес. Таким чином, АЛК – це універсальний біологічний антиоксидант, як водо-, так і жиророзчинний, і здатний нейтралізувати активні форми кисню (АФК) всередині клітин і поза ними [5].
Антидіабетичний потенціал АЛК
Останні дані свідчать про вагому роль у розвитку ЦД надмірного утворення АФК і зниження антиоксидантного потенціалу. Кілька досліджень підкреслюють можливість використання АЛК при ЦД завдяки її здатності збільшувати поглинання цукру в інсуліночутливих та інсулінорезистентних м’язових тканинах, а також стимулювати поглинання глюкози шляхом перерозподілу транспортерів глюкози до плазматичної мембрани та фосфорилювання тирозину субстрату рецептора інсуліну‑1 [6].
АЛК і хвороба Альцгеймера
Достатньо вагомі дані наголошують на залученні оксидативного стресу в патогенез хвороби Альцгеймера (ХА). Дослідження in vitro підтвердили нейропротекторний вплив АЛК, який полягає в захисті кортикальних нейронів від цитотоксичного впливу, індукованого пептидом Aβ або H2O2, що частково пояснюється активацією сигнального шляху PKB/Akt [7]. Інше дослідження показало, що АЛК здатна ефективно захищати культивовані нейрони гіпокампа від токсичного впливу пептиду Aβ і Fe/H2O2 [8].
Ще один механізм, який забезпечує позитивні ефекти АЛК в разі деменції або ХА, полягає в активації холінацетилтрансферази, що збільшує всмоктування глюкози і, відповідно, забезпечує більшу кількість ацетил-КoA для виробництва ацетилхоліну [9].
Запалення є ще однією ланкою патогенезу ХА, на яку здатна впливати АЛК. Запальний процес при ХА локалізований навколо амілоїдних бляшок, оточених активованими астроцитами та мікроглією, і характеризується підвищеним рівнем вільних радикалів і прозапальних цитокінів [10, 11]. Dinicola та співавт. виявили, що AЛК знижує рівень прозапальних цитокінів інтерлейкіну (ІЛ)-1β та ІЛ‑6 у клітинах нейробластоми людини SK-N-BE через модуляцію, залежну від метилювання ДНК, створюючи шлях для впливу епігенетичних механізмів на контроль/профілактику ХА [12].
АЛК і рак
Зростаюча кількість літературних даних свідчить на користь потенціалу застосування АЛК при лікуванні раку [13, 14]. Ракові клітини перетворюють більшу частину глюкози на лактат для подальшого вироблення АТФ. Це явище відоме під назвами «ефект Варбурга» або «аеробний гліколіз». Постійна активація аеробного гліколізу в ракових клітинах призводить до активації онкогенів або втрати пухлинних супресорів, тим самим призводячи до прогресування раку. При цьому інгібування аеробного циклу може сприяти протираковому ефекту [15, 16]. Піруватдегідрогеназа каталізує перетворення пірувату на ацетил-КоА, тим самим запобігаючи утворенню лактату. Feuerecker та співавт. досліджували, чи здатна AЛК активувати піруватдегідрогеназу в пухлинних клітинах. Результати показують, що AЛК пригнічує проліферацію клітин, поглинання [18F]-ФДГ і утворення лактату, а також посилює апоптоз у клітинних лініях нейробластоми Kelly, SK-N-SH, Neuro‑2a та в клітинній лінії раку молочної залози SkBr3 [17].
У ще одному досліджені було показано, що АЛК пригнічує проліферацію та ріст клітин раку щитоподібної залози шляхом активації AMPK і подальшого пригнічення сигнального шляху mTOR-S6 у клітинних лініях BCPAP, HTH‑83, CAL‑62 і FTC‑133. У тому ж дослідженні було також виявлено, що АЛК достовірно пригнічує ріст пухлини на мишачій моделі ксенотрансплантата з використанням клітин BCPAP і FTC‑133 [18]. У клітинах раку легень AЛК пригнічує проліферацію клітин за допомогою Grb2-опосередкованої регуляції рецептора епідермального фактора росту [19].
Дослідження також показали, що АЛК здатна генерувати АФК, які сприяють АЛК-залежній загибелі клітин при раку легень [20], раку молочної залози і раку товстої кишки, що свідчить про те, що вона запускає мітохондріальний шлях апоптозу в ракових клітинах. Нещодавно також було показано, що AЛК пригнічує міграцію та інвазію метастатичних клітин раку молочної залози. Таким чином, наукові дані свідчать, що АЛК можна застосовувати для лікування та профілактики раку [5].
Ефективність і безпека АЛК: огляд клінічних досліджень
Клінічну ефективність і безпеку АЛК активно вивчають із 1950-х років, коли вперше були виявлені її антиоксидантні властивості. Встановлено, що АЛК ефективно полегшує деякі симптоми, пов’язані з діабетом, віковими серцево-судинними та нервово-м’язовими порушеннями, збільшенням ваги, унаслідок прийому антипсихотичних препаратів і метаболічним ожирінням. Крім того, останнім часом зросла кількість клінічних досліджень, метою яких є вивчення інших потенційних терапевтичних властивостей АЛК [5].
Діабетична полінейропатія
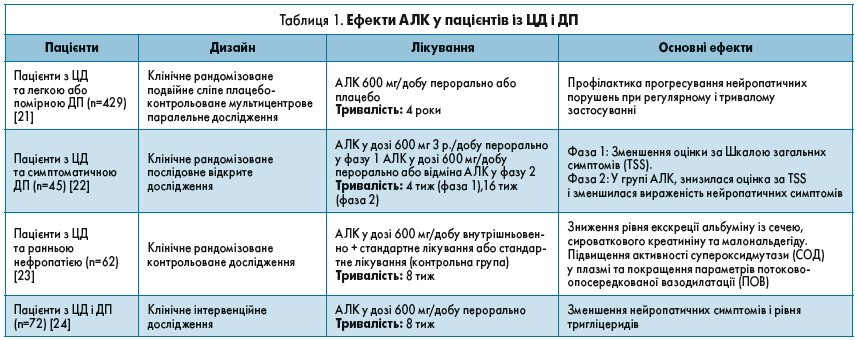
Численні дослідження продемонстрували ефективність АЛК в лікуванні ДП, що відображено в таблиці 1.
Так, у рандомізованому подвійному сліпому плацебо-контрольованому багатоцентровому порівняльному дослідженні, проведеному Ziegler та співавт., було показано, що AЛК ефективна при діабетичній сенсомоторній полінейропатії (ДСПН) легкого і середнього ступеня тяжкості [21]. Прийом АЛК в дозі 600 мг/добу протягом 4 років супроводжувався підвищенням оцінки за шкалою нейропатичних порушень нижніх кінцівок (NIS-LL) у пацієнтів із легкою і помірною ДСПН. Збільшення оцінки за шкалою NISS-LL під час дослідження більш як удвічі було визначене як значуще. Статистичний аналіз охоплював різні підгрупи груп лікування. Серед усіх підгруп через 4 роки середнє покращення за шкалою NIS-LL (більш як 1 бал) спостерігалося у групі, що приймала АЛК, у підкатегоріях, в яких на початку дослідження індекс маси тіла (ІМТ) був нижче ніж 30 кг/м2, у пацієнтів із діабетом 1 типу, у курців і в підгрупі, де учасники отримували інгібітор ангіотензинперетворювального ферменту (іАПФ). Підгрупи, в яких були чоловіки старше 55 років із серцево-судинними захворюваннями в анамнезі і нейропатією впродовж понад 3 років із ДСПН стадії 2a, продемонстрували значне збільшення оцінки за NIS-LL у групі AЛК проти групи плацебо.
У цьому дослідженні було показано, що тривалий і регулярний прийом AЛК має значний потенціал для запобігання прогресуванню нейропатичних порушень при легкій і помірній ДСПН.
У рандомізованому відкритому дослідженні ефекти АЛК досліджували під час двох послідовних фаз [22]. Сорок п’ять пацієнтів із діабетом і симптоматичною полінейропатією були залучені до фази 1 дослідження. Усі учасники отримували 600 мг АЛК тричі на добу перорально протягом 4 тижнів. Прийом будь-яких інших препаратів, що зменшують нейропатичний біль, був заборонений. Не всі із 45 пацієнтів завершили фазу 1 через відмову з особистих причин і використання заборонених препаратів. Через 4 тиж показники пацієнтів, в яких оцінка за шкалою загальної оцінки симптомів (TSS) зменшувалася на більш як 3 бали, порівнювали з вихідним значенням і переходили у фазу 2, де учасників випадковим чином розділили на 2 групи: одна група продовжувала прийом АЛК, інша – ні (контроль) упродовж 16 тижнів. Кінцевою точкою фази 2 була зміна оцінки за TSS, параметри якої охоплювали пекучий і ріжучий біль, парестезії та оніміння. Наприкінці фази 2 оцінка за TSS у групі AЛК знизилася, тоді як у контрольній групі змін виявлено не було. Потрібно зазначити, що вираженість пекучого болю і парестезій зменшилася з моменту рандомізації до кінця дослідження; однак вираженість ріжучого болю й оніміння не змінилася в групі, яка отримувала AЛК у фазі 2. Крім того, використання знеболювальних засобів у групі АЛК було нижчим, ніж у групі контролю.
Таким чином, це дослідження показало, що АЛК покращує нейропатичні симптоми, одночасно зменшуючи потребу у використанні ліків для невідкладної допомоги в пацієнтів із ЦД 2 типу і симптоматичною полінейропатією.
Sun та співавт. вивчали ефективність АЛК у двоетапному рандомізованому контрольованому дослідженні [23]. На першому етапі 62 пацієнти з ранньою стадією діабетичної нефропатії були розділені на контрольну і дослідну групу, яка отримувала АЛК. Обидві групи продовжували отримувати постійну цукрознижувальну терапію (стандартне лікування) і дотримувалися суворої дієти, однак їм не давали іАПФ. У дослідній групі пацієнти отримували АЛК в дозі 600 мг/добу внутрішньовенно протягом 2 тижнів. На другому етапі в дослідження було залучено 21 пацієнта, які були розділені на 2 групи: групу нормоальбумінурії (рівень екскреції альбуміну із сечею (РЕАС) менш ніж 30 мг/24 год) і групу мікроальбумінурії (РЕАС 30-300 мг/24 год). Під час дослідження лише в одного пацієнта спостерігали побічні ефекти (легка нудота). Якість екзосом у зразках сечі оцінювали за допомогою електронної мікроскопії. У результаті було встановлено, що в групі АЛК знижувалися рівні сироваткового креатиніну і малонового діальдегіду, а також РЕАС. Аналіз потоково-опосередкованої вазодилатації (ПОВ) з кількома параметрами показав позитивну кореляцію лише за активністю супероксиддисмутази (СОД). Крім цього було встановлено, що рівні експресії CD63-позитивної екзосоми були вищими в групі AЛК.
Це дослідження показало, що на ранніх стадіях ДП короткотривале застосування AЛК може захистити нирки від оксидативного стресу.
Нещодавно Agathos та співавт. вивчали вплив АЛК (600 мг/добу, перорально) на 72 хворих на ЦД із нейропатією, які одночасно приймали протидіабетичні ліки у 40-денному проспективному інтервенційному дослідженні [24]. Було заплановано два контрольних огляди протягом 40 днів: одне – на початку дослідження (вихідний рівень), друге – на 40-й день (кінцевий рівень). Крім того, під час візитів були отримані зразки крові. Згідно з результатами анкет симптоми нейропатії зменшилися між двома візитами. У результатах лабораторних досліджень під час другого візиту середній рівень тригліцеридів натщесерце значно знизився, тоді як інші параметри не змінилися.
Дослідження показало, що прийом AЛК покращує якість життя пацієнтів із ДП, зменшуючи вираженість основних симптомів і рівень тригліцеридів.
Dimitrios Karalis та співавт. у своєму дослідженні оцінювали вплив АЛК на частоту розвитку в пацієнтів із ЦД 2 типу периферичної нейропатії і депресивного розладу, який може виникати через відчуття пригніченості, зумовлене зміною способу життя, необхідною для уникнення ускладнень діабету [25].
АЛК підвищує чутливість до інсуліну, що може збільшити синтез серотоніну і тим самим зменшити прояви депресивного розладу.
У дослідження було включено 148 пацієнтів із Греції, хворих на ЦД 2 типу (68 чоловіків і 80 жінок, вік – 50-75 років). Усі вони не курили та не вживали алкоголь. Учасники отримували комбінацію гліклазиду, інгібітора натрій-глюкозного котранспортера 2-го типу (іНГКТ‑2), метформіну та аналогів глюкагоноподібного пептиду 1 (ГПП‑1). Жоден із них не отримував інсулін. Будь-яке інше лікування, яке постійно отримували пацієнти з приводу інших супутніх захворювань, не було змінено чи призупинено. В усіх пацієнтів проводили регулярний моніторинг функції нирок, печінки та очей – усі показники були в межах нормальних значень. Також слідкували, щоб пацієнти отримували збалансовану дієту, аби підтримувати майже постійний ІМТ. Усім давали 1 таблетку 600 мг АЛК за 2 год до їди протягом 8 місяців. Частоту розвитку периферичної нейропатії і депресивного розладу оцінювали за допомогою Опитувальника суб’єктивної оцінки периферичної нейропатії (SPNSQ) і Шкали депресії Бека (BDI).
Застосування AЛК як через 4, так і через 8 міс сприяло статистично значущим результатам, зокрема середній бал розвитку периферичної нейропатії знизився на 4,79 через 4 і на 6,22 – через 8 міс прийому. Щодо частоти розвитку депресивного розладу, то середнє зниження оцінки за опитувальником SPNSQ дорівнювало 4,43 через 4 і 7,56 – через 8 міс лікування, обидва значення були статистично значущими.
Отже, дослідження підтвердило, що АЛК – це потужний антиоксидант, доповнення яким традиційної терапії достовірно знижує частоту депресії і периферичної нейропатії в пацієнтів із ЦД 2 типу.
Evangelos Agathos та співавт. у своєму проспективному інтервенційному дослідженні також вивчали вплив АЛК на нейропатичні симптоми в пацієнтів із ДП [26]. Учасники дослідження з больовою формою ДП отримували АЛК в дозі 600 мг/добу перорально протягом 40 днів. Оцінку симптомів нейропатії проводили за шкалами NSS, SPNSQ і DN‑4 на початку та на 40-й день дослідження. Вплив лікування на якість життя оцінювали за Коротким опитувальником вираженості больового синдрому (BPI), Опитувальником вираженості симптомів нейропатичного болю (NPSI) та Шкалою обмеження фізичних можливостей Шихана (SDS). Також оцінювали зміну маси тіла, артеріального тиску, рівня глюкози в сироватці крові і ліпідів натще.
На 40-й день дослідження в усіх 72 учасників спостерігали достовірне зменшення вираженості нейропатичних симптомів за шкалами NSS, SPNSQ і DN4 проти вихідного рівня. Оцінка за шкалами BPI, NPSI та SDS, яка стосувалася непрацездатності, обмежень у соціальному та сімейному житті, також була достовірно нижчою. Крім того, 50% пацієнтів оцінили свій стан здоров’я як «кращий» або «набагато кращий» після застосування АЛК. На 40-й день дослідження рівні тригліцеридів натще знизилися, але не було виявлено різниці в масі тіла, артеріальному тиску, рівні глюкози або концентрації інших ліпідів.
Таким чином, результати дослідження підтверджують, що застосування АЛК в пацієнтів із ЦД 2 типу пов’язане зі зменшенням вираженості нейропатичних симптомів, рівня тригліцеридів і покращенням якості життя.
АЛК і надмірна вага / ожиріння
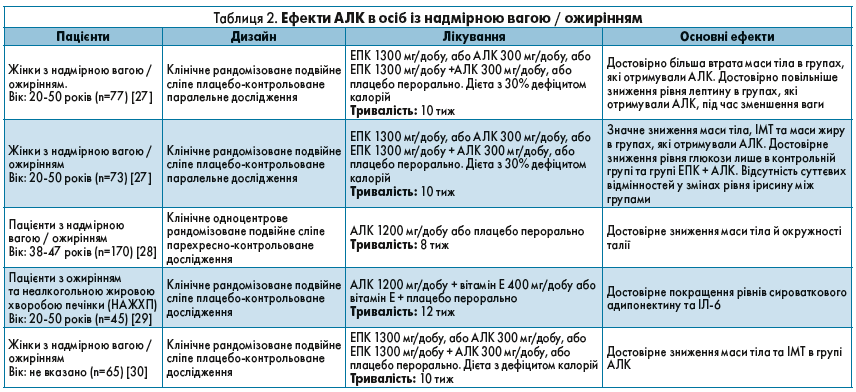
Вплив АЛК на контроль ваги оцінювали в кількох клінічних дослідженнях, результати яких виявилися багатообіцяючими (табл. 2).
У дослідженні Huerta та співавт. взяли участь 77 здорових жінок із надмірною вагою / ожирінням зі значеннями ІМТ від 27,5 до 40 кг/м2 [27]. Усі учасники були випадковим чином розділені на 4 групи, які щоденно отримували 1300 мг ейкозапентаєнової кислоти (EПК), або 300 мг АЛК, або 1300 мг EПК плюс 300 мг AЛК, або плацебо протягом 10 тижнів. Під час дослідження всі учасники дотримувалися дієти, добовий калораж якої був знижений на 30%. У результаті група АЛК продемонструвала значно більшу втрату маси тіла і значуще зниження рівня лептину з 1-го тиж лікування, незважаючи на відсутність суттєвого зниження швидкості метаболізму в стані спокою. Помітне зниження рівня тригліцеридів і діастолічного артеріального тиску спостерігали в групі ЕПК+АЛК. Загалом в усіх групах, за винятком групи тільки ЕПК, спостерігали достовірне зниження рівня лептину і помітне покращення рівня інсуліну під час перорального тесту на толерантність до глюкози. Протягом усього періоду дослідження побічних ефектів виявлено не було.
Huerta та співавт. також досліджували потенційний зв’язок між рівнем циркулюючого ірисину, метаболізмом глюкози і впливом на них AЛК або EПК [27]. Ірисин є міокіном; однак його роль в ожирінні поки що не до кінця з’ясована. У рандомізоване плацебо-контрольоване подвійне сліпе паралельне клінічне дослідження було залучено 73 здорові жінки з надмірною вагою або ожирінням. Дизайн груп лікування, дози ЕПК, АЛК та комбінації ЕПК/АЛК були ідентичними таким у вищезгаданому дослідженні. Рівень глюкози в крові достовірно знизився лише в контрольній групі та в групі комбінації ЕПК/АЛК. Повідомлялося про статистично значуще зменшення маси тіла, окружності стегон і жирової маси в групах, які отримували АЛК, порівняно з контрольною групою та групами, які отримували лише ЕПК. Після зменшення ваги в усіх групах спостерігали зниження рівня ірисину, однак його концентрація незначуще відрізнялася між групами.
У дослідженні Li та співавт. (n=170) вивчали вплив терапії AЛК на масу тіла, окружність талії та ліпідний обмін у пацієнтів із надмірною вагою або ожирінням (ІМТ ≥25 кг/м2) [28]. Група AЛК отримувала препарат у дозі 1200 мг/добу перорально протягом 8 тиж, потім, після 4-тижневого втручання, ця група продовжувала отримувати плацебо протягом 8 тиж. Прямо протилежна послідовність введення АЛК і плацебо була використана для групи плацебо. Відповідно до статистичного аналізу змішаної моделі, введення AЛК супроводжувалося достовірним зменшенням маси тіла й окружності талії.
Hosseinpour-Arjmand та співавт. оцінили вплив АЛК на рівні ферментів печінки і маркерів запалення в разі НАЖХП у пацієнтів з ожирінням [29]. У дослідження було включено 45 пацієнтів з ожирінням і НАЖХП, які щоденно отримували 1200 мг АЛК + 400 мг вітаміну Е або плацебо + 400 мг вітаміну Е протягом 12 тижнів. Застосування AЛК сприяло помітному підвищенню рівня адипонектину в сироватці крові і зниженню рівня IЛ‑6, а також рівнів інсуліну порівняно з плацебо.
Romo-Hualde та співавт. досліджували метаболічні зміни, які відбувалися при щоденному прийомі 1300 мг EПК або 300 мг AЛК, або 1300 мг EПК + 300 мг AЛК, або плацебо у 67 здорових жінок із надмірною вагою / ожирінням, які вели малорухливий спосіб життя і дотримувалися дієти з обмеженим калоражем протягом 10 тиж [30]. У результаті більш виражене зниження ІМТ і жирової маси було виявлено в усіх групах, які отримували АЛК, порівняно з групами, які отримували ЕПК і плацебо. Таким чином, введення АЛК може сприятливо впливати на зниження маси тіла, однак необхідні подальші дослідження.
Інші стани
Обнадійливі результати були отримані і при застосуванні АЛК у пацієнтів із шизофренією, розсіяним склерозом і патологічними станами вагітності [5]. Так, застосування АЛК у дозі 500-1800 мг/добу перорально протягом 12-16 тиж у пацієнтів із шизофренією, які отримували антипсихотичні препарати, супроводжувалося низкою позитивних ефектів, зокрема зниженням маси тіла, ІМТ та вмісту вісцерального жиру, достовірним покращенням нейрокогнітивних параметрів і підвищенням рівня адипонектину в плазмі крові. Прийом АЛК у дозі 1200 мг/добу пацієнтами з розсіяним склерозом протягом 12 тиж сприяв достовірному зниженню рівнів інтерферону-γ, ICAM‑1 TGF-β та IЛ‑4 у сироватці крові, а протягом 2 років – достовірному покращенню координації та параметрів ходьби.
Ефективність АЛК у запобіганні викидням також вивчали в кількох дослідженнях. Було встановлено, що застосування АЛК асоційоване з достовірним зменшенням частоти викиднів, швидшою резорбцією субхоріонічної гематоми та достовірним підвищенням рівня протизапальних інтерлейкінів у цервікальній і вагінальній рідині жінок при загрозі передчасних пологів [5].
Зважаючи на доведену ефективність АЛК при ДП, Gabriela Cassanego та співавт. вирішили дослідити ефективність АЛК у лікуванні різних типів болю шляхом проведення систематичного огляду і метааналізу рандомізованих клінічних досліджень. Після аналізу 1154 статтей до огляду увійшло 16 (9 стосувалися ДП та 7 – інших станів, що супроводжувалися больовим синдромом). Більшість включених в огляд досліджень мали низький ризик похибки. У результаті була встановлена ефективність АЛК при лікуванні головного болю, синдрому зап’ястного каналу та синдрому палаючого рота [31]. Утім, зважаючи на невеликі вибірки і дизайн досліджень, необхідні подальші масштабні випробування для оцінки застосування АЛК в лікуванні вищезгаданих станів.
Фармакокінетика та її вплив на практичні аспекти застосування АЛК в реальній практиці
У плазмі і клітинах людини міститься недостатньо АЛК для забезпечення всіх потреб організму, тому її надходження ззовні є надзвичайно важливим. Дослідження показали, що при пероральному прийомі суміші R- і S-ізомерів АЛК натщесерце її абсорбція збільшується на 40%, тоді як у разі прийому АЛК разом з їжею всмоктування знижується на 20%. Ураховуючи ще й те, що біодоступність АЛК значно знижується після прийому їжі, препарат рекомендовано приймати принаймні через 2 год після або за 30 хв до їди [32]. На користь цих рекомендацій свідчить і те, що кислий рН шлунка сприятливо впливає на всмоктування АЛК. Крім того, прийом АЛК натщесерце зменшує конкуренцію між всмоктуванням AЛК та інших поживних речовин [33].
Встановлено, що після перорального прийому 50-600 мг тіоктової кислоти максимальна концентрація досягається за 0,5-1 годину [34]. У роботі, метою якої була оцінка поглинання рацемічної композиції АЛК у дозі 600 мг, було виявлено, що після перорального прийому АЛК її концентрація швидко досягає максимальної 6,86±1,29 мкг/мл.
Біодоступність різних форм АЛК також порівнювали в багатьох дослідженнях. Одним із найбільш ілюстративних стало дослідження Hermann та співавт., які порівнювали біодоступність та інші фармакокінетичні параметри АЛК у дозі 200 мг після перорального і внутрішньовенного введення. У результаті АЛК можна було виявити в крові протягом 2 год після внутрішньовенного введення і впродовж 4 год після перорального введення. При цьому максимальна концентрація АЛК у плазмі була більшою при внутрішньовенному введенні порівняно з пероральним; однак кінцевий період напіврозпаду при пероральному і внутрішньовенному введенні АЛК був порівнянним [35]. Таким чином, зважаючи на швидке й активне поглинання АЛК після перорального прийому, а також кінцевий період напіврозпаду, порівнянний із таким у разі внутрішньовенного введення АЛК, пероральні форми АЛК ефективні так само, як парентеральні.
Висновки
АЛК – потужний антиоксидант, сфери терапевтичного застосування якого безперервно розширюються. Результати контрольованих клінічних досліджень підтверджують ефективність і доцільність використання АЛК при різноманітних захворюваннях і станах, у тому числі при ДП, ожирінні, шизофренії, розсіяному склерозі та аномаліях вагітності. Так, АЛК доведено покращує якість життя і зменшує вираженість нейропатичних симптомів у пацієнтів із ЦД і супутньою ДП і навіть дає можливість зменшити кількість ліків, які приймають пацієнти для контролю больового синдрому. Потенціал застосування АЛК при захворюваннях центральної нервової системи (шизофренії і розсіяному склерозі), окрім полегшення симптомів, полягає ще й у покращенні ліпідного обміну та сприянні зниженню ваги в пацієнтів з ожирінням. АЛК також може зменшити приріст маси тіла, спричинений застосуванням антипсихотичних засобів, а також позитивно вплинути на деякі метаболічні фактори ризику в пацієнтів із шизофренією.
Для максимального терапевтичного ефекту АЛК важливо пам’ятати про її фармакокінетичні параметри і фактори, які можуть на них впливати. Так, потрапляння АЛК в шлунок разом з іншими продуктами харчування може знизити її всмоктування та біодоступність, а отже й ефективність. Відповідно, АЛК необхідно приймати принаймні через 2 год після або за 30 хв до їди. Згадуючи фармакокінетику АЛК, треба сказати і про те, що фармакокінетичні параметри її абсорбції, біодоступності та напіврозпаду підтверджують, що пероральні форми АЛК не менш ефективні, ніж парентеральні.
***
На сьогодні на фармацевтичному ринку доступний препарат Альфа-ліпон – АЛК європейської якості від українського виробника АТ «Київський вітамінний завод». Цей засіб випускається у формі таблеток, вкритих плівковою оболонкою, що містять 300 або 600 мг АЛК. Ефективність і безпека засобу підтверджені не лише результатами вищезгаданих клінічних досліджень, а й тривалим використанням в умовах реальної клінічної практики, а обґрунтована ціна забезпечує доступність і підвищує прихильність пацієнтів до лікування.
Література
1. Dyck P.J., Kratz K.M., Karnes J.L., Litchy W.J., Klein R. et al. The prevalence by staged severity of various types of diabetic neuropathy, retinopathy, and nephropathy in a population-based cohort: the Rochester Diabetic Neuropathy Study. Neurology. 1993 Apr; 43(4):817-24.
2. Dianna Quan. Diabetic Neuropathy. Updated: Aug 24, 2021 Режим доступу: https://emedicine.medscape.com/article/1170337-overview#a7
3. Brownlee M. The pathobiology of diabetic complications: a unifying mechanism. Diabetes 2005; 54: 1615-1625.
....
32. Hermann R., Niebch G., Borbe H.O., Fieger-Büschges H., Ruus P., Nowak H., Riethmüller-Winzen H., Peukert M., Blume H. Enantioselective pharmacokinetics and bioavailability of different racemic α-lipoic acid formulations in healthy volunteers. Eur. J. Pharmacol. Sci. 1996;4:167-174. doi: 10.1016/0928-0987(95)00045-3.
Повний список літератури – у редакції.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (59) 2022 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
21 березня в рамках II Міжнародної школи «Сучасний лікар: від теорії до практики» професор кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, лікар-ендокринолог вищої категорії, доктор медичних наук Вікторія Олександрівна Сергієнко представила доповідь, присвячену хронічним ускладненням цукрового діабету (ЦД). Зокрема, було акцентовано увагу на причинах розвитку діабетичної полінейропатії (ДП), розглянуто клінічні варіанти цього ускладнення, діагностичні підходи та основні принципи лікування. Пропонуємо огляд цієї доповіді у форматі «запитання – відповідь»....
Останніми десятиліттями в усьому світі спостерігалося значне зростання поширеності цукрового діабету (ЦД), що зумовило серйозні наслідки стосовно якості життя населення, а також спричинило певний тягар для системи охорони здоров’я та економічні витрати [1]. За даними Діабетичного атласу Міжнародної діабетичної федерації (International Diabetes Federation Diabetes Atlas), у 2021 р. ≈537 млн людей мали ЦД і, за прогнозами, до 2045 р. цей показник досягне 783 млн [2]. Значна захворюваність і підвищена смертність асоційовані з пов’язаними із ЦД макросудинними (інфаркт міокарда, інсульт) і мікросудинними (сліпота, ниркова недостатність, ампутації) ускладненнями [3]....
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....