Порівняльна характеристика ефективності дидрогестерону і прогестерону в підтримці лютеїнової фази: систематичний огляд і метааналіз рандомізованих контрольованих досліджень
Жовте тіло відіграє провідну роль у підтриманні ранньої вагітності до лютеїно-плацентарного зсуву між 7-м і 8-м тижнями вагітності. У жінок, які отримують допоміжні репродуктивні технології (ДРТ), часто застосовують контрольовану стимуляцію яєчників для розвитку багатьох фолікулів. Відповідно, після аспірації яйцеклітини формуються кілька жовтих тіл. Надфізіологічні рівні естрадіолу, зумовлені стимуляцією яєчників, за механізмом негативного зворотного зв’язку діють на гіпофіз, що сприяє передчасному лізису жовтих тіл і зниженню рівня прогестерону в лютеїновій фазі.
Доведено, що підтримка лютеїнової фази (ПЛФ) прогестероном, хоріонічним гонадотропіном людини (ХГЛ) або агоністом гонадотропін-рилізинг-гормона (ГнРГ) покращує репродуктивні результати у жінок, які отримують ДРТ. Оскільки застосування ХГЛ асоціюється з підвищеним ризиком синдрому гіперстимуляції яєчників, а агоністи ГнРГ досліджували тільки у поєднанні з прогестероном, найкращим варіантом для ПЛФ сьогодні вважають прогестерон.
Прогестерон можна призначати перорально, внутрішньом’язово, вагінально або ректально з подібною ефективністю. Проте після перорального прийому прогестерон зазнає значного ефекту першого проходження, що зумовлює низьку біодоступність (<10%), через це пероральну форму прогестерону використовують приблизно 1% репродуктивних клінік. Прогестерон для внутрішньом’язового і вагінального застосування часто асоціюється з побічними ефектами. Основними проблемами, пов’язаними із внутрішньом’язовим введенням прогестерону, є біль, викликаний щоденними ін’єкціями, запальна відповідь і локальні абсцеси. У разі призначення вагінальної форми прогестерону побічні ефекти спостерігаються рідше, проте цей шлях введення супроводжується подразненням піхви, виділеннями і кровотечею. Крім того, після призначення прогестерону в формі вагінального гелю рекомендовано протягом кількох годин утримуватися від статевого акту, оскільки це може спричинити зміни абсорбції прогестерону.
Дидрогестерон – синтетичний прогестерон із покращеною біодоступністю при пероральному прийомі, що дозволяє вирішити зазначені проблеми. Препарат має доведену ефективність в лікуванні репродуктивних розладів, таких як загроза викидня, і є раціональною альтернативою прогестерону для ПЛФ. Основними перевагами дидрогестерону порівняно з прогестероном є простота застосування, нижча вартість терапії, а також менша кількість побічних ефектів і більша задоволеність пацієнток лікуванням, що покращує комплаєнс.
Мета цього систематичного огляду і метааналізу – ідентифікація, оцінка і підбиття підсумків рандомізованих контрольованих досліджень, які вивчали ефективність, безпечність і переносимість пероральної форми дидрогестерону порівняно з прогестероном для ПЛФ у жінок, які отримують ДРТ.
Методи
Пошук публікацій, проведений у жовтні 2015 р. у базах даних Cochrane CENTRAL, PubMed, Scopus, Web of Science, ClinicalTrial.gov, ISRCTN Registry і WHO ICTRP, виявив загалом 343 публікації про застосування прогестагенів із метою запобігання репродуктивним втратам. Для метааналізу відібрано 8 рандомізованих контрольованих досліджень (РКД), в яких порівнювали ефективність пероральної форми дидрогестерону і прогестерону (вагінальні капсули або вагінальний гель) у ПЛФ у жінок, котрі отримували ДРТ (перенесення свіжого або замороженого ембріона після запліднення in vitro або інтраплазматичної ін’єкції сперматозоїдів). Загалом у них було включено 3809 жінок: 1523 отримували дидрогестерон, 1388 – вагінальну форму прогестерону (капсули) і 898 – вагінальну форму прогестерону (гель). В усіх 8 дослідженнях здійснювалась оцінка ефективності застосування пероральної форми дидрогестерону в дозах від 20 до 40 мг/добу. У 6 з них порівнювали ефективність пероральної форми дидрогестерону і вагінальної форми прогестерону у вигляді капсул у дозах від 600 до 800 мг/добу. У дослідженні Tomic і співавт. (2015) порівнювали ефективність застосування дидрогестерону і вагінального гелю прогестерону в дозі 90 мг/добу. У дослідженні Ganesh і співавт. (2011) порівнювали ефективність застосування пероральної форми дидрогестерону і вагінальної форми прогестерону у вигляді капсул або гелю.
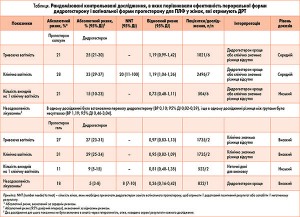
 Первинна кінцева точка, що характеризувала ефективність досліджуваних засобів, – частота живонароджень; як первинну кінцеву точку, що відображає небажані події, прийнято незадоволеність лікуванням. Крім того, оцінювали частоту триваючої вагітності (серцева активність плода за даними ультрасонографії після 10-12 тижнів гестації), клінічної вагітності, викиднів на одну клінічну вагітність і наявність будь-яких побічних ефектів.
Первинна кінцева точка, що характеризувала ефективність досліджуваних засобів, – частота живонароджень; як первинну кінцеву точку, що відображає небажані події, прийнято незадоволеність лікуванням. Крім того, оцінювали частоту триваючої вагітності (серцева активність плода за даними ультрасонографії після 10-12 тижнів гестації), клінічної вагітності, викиднів на одну клінічну вагітність і наявність будь-яких побічних ефектів.
Результати
Результати окремих досліджень, а також узагальнені дані схематично представлені на рисунках 1-3.
Триваюча вагітність
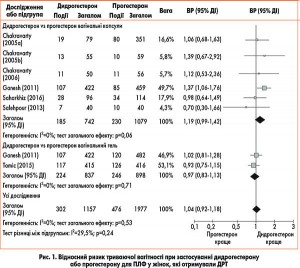
 За показником триваючої вагітності статистично значимої різниці ефективності застосування пероральної форми дидрогестерону і вагінальної форми прогестерону у підтриманні ЛФ не зафіксовано (відносний ризик – ВР – 1,04; 95% довірчий інтервал – ДІ – 0,92-1,18). Інакше кажучи, враховуючи частоту триваючої вагітності 24% у жінок, які отримували вагінальну форму прогестерону, у разі застосування дидрогестерону цей показник перебуває в межах 22-28%. Аналіз чутливості, з якого було виключено 4 дослідження з високим ризиком систематичної помилки, не вплинув на цей результат (ВР 1,02; 95% ДІ 0,84-1,25; 3 РКД, 2274 жінки).
За показником триваючої вагітності статистично значимої різниці ефективності застосування пероральної форми дидрогестерону і вагінальної форми прогестерону у підтриманні ЛФ не зафіксовано (відносний ризик – ВР – 1,04; 95% довірчий інтервал – ДІ – 0,92-1,18). Інакше кажучи, враховуючи частоту триваючої вагітності 24% у жінок, які отримували вагінальну форму прогестерону, у разі застосування дидрогестерону цей показник перебуває в межах 22-28%. Аналіз чутливості, з якого було виключено 4 дослідження з високим ризиком систематичної помилки, не вплинув на цей результат (ВР 1,02; 95% ДІ 0,84-1,25; 3 РКД, 2274 жінки).
Результати аналізу по підгрупах, в якому враховано порівняльні дослідження ефективності дидрогестерону і вагінальної форми прогестерону у вигляді капсул, показали ВР 1,19 (95% ДІ 0,99-1,42; 6 РКД, 1821 жінка) (табл.). У жінок, які отримували вагінальну форму прогестерону, частота триваючої вагітності склала 21%, тоді як при застосуванні дидрогестерону цей показник становив 21-30%. У дослідженнях, в яких порівнювали ефективність дидрогестерону і вагінальної форми прогестерону у вигляді гелю, ВР дорівнював 0,97 (95% ДІ 0,83-1,13; 2 РКД, 1735 жінок) (табл.). Для прогестерону частота триваючої вагітності становила 27%, для дидрогестерону – 23-31%.
Клінічна вагітність
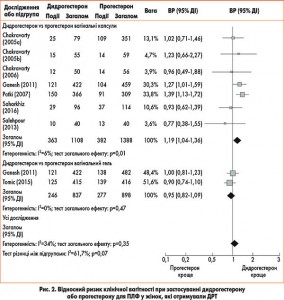 Показники частоти клінічної вагітності при застосуванні дидрогестерону або вагінальної форми прогестерону статистично не відрізнялися (ВР 1,07; 95% ДІ 0,93-1,23) (рис. 2).
Показники частоти клінічної вагітності при застосуванні дидрогестерону або вагінальної форми прогестерону статистично не відрізнялися (ВР 1,07; 95% ДІ 0,93-1,23) (рис. 2).
Результати аналізу по підгрупах, у який включено порівняльні дослідження ефективності дидрогестерону і вагінальної форми прогестерону у вигляді капсул, встановили ВР 1,19 (95% ДІ 1,04-1,36; 7 РКД, 2496 жінок). У жінок, які отримували вагінальну форму прогестерону, частота триваючої вагітності склала 21%, тоді як при застосуванні дидрогестерону цей показник становив 21-30%. У дослідженнях, в яких застосовували вагінальну форму прогестерону у вигляді гелю як препарат порівняння, ВР склав 0,95 (95% ДІ 0,82-1,09; 2 РКД, 1735 жінок) (табл.).
Викидень
За частотою викидня пероральна форма дидрогестерону і вагінальна форма прогестерону статистично не відрізнялися (ВР 0,77; 95% ДІ 0,53-1,10; 7 РКД, 906 клінічних вагітностей). Аналіз досліджень із вагінальною формою прогестерону у вигляді капсул показав ВР 0,73 (95% ДІ 0,48-1,11; 6 РКД, 504 клінічні вагітності), з вагінальною формою прогестерону у вигляді гелю – 0,81 (95% ДІ 0,48-1,35; 2 РКД, 523 клінічні вагітності).
Побічні ефекти
Два РКД, в яких оцінювали наявність побічних ефектів, мали значну гетерогенність (>50%), тому їх об’єднаний аналіз не проводили. У дослідженні за участю 80 жінок прийом пероральної форми дидрогестерону і застосування вагінальної форми прогестерону у вигляді гелю не відрізнялися за частотою випадків болю в животі. В іншому дослідженні (n=822) біль у животі, подразнення промежини, виділення з піхви і їх негативний вплив на статеве життя спостерігалися рідше у групі дидрогестерону порівняно з групою пацієнток, які отримували вагінальну форму прогестерону у вигляді гелю. Частота інших побічних ефектів (вагінальної кровотечі, нудоти, головного болю, запаморочення, сонливості, здуття живота і відчуття важкості у грудях) була подібною в обох групах.
Незадоволеність лікуванням
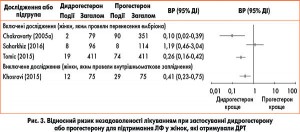 Його оцінювали в 3 дослідженнях. Chakravarty і співавт. та Saharkhiz і співавт. порівнювали ефективність дидрогестерону і вагінальної форми прогестерону у вигляді капсул, а Tomic і співавт. – дидрогестерону і вагінальної форми прогестерону у вигляді гелю. Через значну гетерогенність між РКД (I2=82%), навіть між 2 дослідженнями, в яких застосовували прогестерон у вигляді капсул (I2=91%), об’єднаний аналіз цих даних не проводили (рис. 3).
Його оцінювали в 3 дослідженнях. Chakravarty і співавт. та Saharkhiz і співавт. порівнювали ефективність дидрогестерону і вагінальної форми прогестерону у вигляді капсул, а Tomic і співавт. – дидрогестерону і вагінальної форми прогестерону у вигляді гелю. Через значну гетерогенність між РКД (I2=82%), навіть між 2 дослідженнями, в яких застосовували прогестерон у вигляді капсул (I2=91%), об’єднаний аналіз цих даних не проводили (рис. 3).
Saharkhiz і співавт. не виявили різниці у незадоволеності лікуванням між групою дидрогестерону і групою пацієнток, які приймали вагінальну форму прогестерону у вигляді капсул (8 vs 7% відповідно; ВР 1,19; 95% ДІ 0,46-3,04). Це дослідження було оцінено як таке, що має високий ризик систематичної помилки. В інших двох дослідженнях було продемонстровано значну перевагу дидрогестерону у зменшенні незадоволеності лікуванням. Chakravarty і співавт., порівнюючи ефективність дидрогестерону і вагінальної форми прогестерону у вигляді капсул, виявили незадоволеність у 3% жінок групи дидрогестерону vs 26% жінок групи прогестерону (ВР 0,10; 95% ДІ 0,02-0,39; 430 жінок). Tomic і співавт. повідомили про незадоволеність лікуванням у 5% пацієнток, які приймали пероральну форму дидрогестерону, і у 18% тих, котрі отримували вагінальну форму прогестерону у вигляді гелю (ВР 0,26; 95% ДІ 0,16-0,42; 822 жінки).
Ще в одному дослідженні, яке не включено в цей огляд, також спостерігали нижчу незадоволеність лікуванням у групі дидрогестерону. Її висловили 12/75 (16%) жінок, які приймали пероральну форму дидрогестерону (10 мг двічі на день), і 29/75 (39%) пацієнток, що отримували вагінальну форму прогестерону у вигляді капсул у дозі 400 мг 1 раз на день (ВР 0,41; 95% ДІ 0,23-0,75). Автори цього дослідження встановили подібну частоту вагітностей в обох групах терапії, проте відзначили тенденцію до нижчої частоти викидня у групі дидрогестерону.
Обговорення
У порівняльний аналіз ефективності дидрогестерону і вагінальної форми прогестерону включено 8 досліджень. У 6 РКД порівнювали ефективність дидрогестерону і вагінальної форми прогестерону у вигляді капсул, в одному РКД – дидрогестерону і вагінальної форми прогестерону у вигляді гелю, і ще в одному РКД застосовували обидві форми прогестерону (табл.).
Загалом застосування пероральної форми дидрогестерону забезпечувало таку саму ефективність у ПЛФ, як і вагінальна форма прогестерону, та асоціювалося з нижчою частотою незадоволеності лікуванням у пацієнток. Враховуючи відмінності в системах доставки прогестерону, було проведено аналіз по підгрупах, в результаті якого отримано важливі результати. Пероральна форма прогестерону забезпечувала вищу частоту клінічної вагітності порівняно з вагінальною формою прогестерону у вигляді капсул і не відрізнялася за цим показником від вагінального гелю прогестерону. Також дидрогестерон асоціювався з нижчою частотою викидня, проте невеликий обсяг даних не дозволяє зробити остаточний висновок.
Незадоволеність лікуванням була первинною кінцевою точкою, що характеризувала небажані події. Оцінку цього показника проводили в 3 РКД: у 2 дослідженнях показано значну перевагу дидрогестерону, тоді як у третьому показники у групах істотно не відрізнялися. В одному з цих 3 досліджень, яке було розцінено як таке, що має низький ризик систематичної помилки, встановлено значне і статистично достовірне зменшення частоти незадоволеності лікуванням у групі пацієнток, які приймали пероральну форму дидрогестерону, порівняно з групою тих, котрі застосовували вагінальну форму прогестерону у вигляді гелю. У дослідженні Khosravi і співавт. (2015), яке не ввійшло в цей огляд, також показано значне зниження незадоволеності лікуванням у тих жінок, котрі отримували дидрогестерон.
Дидрогестерон має унікальну стійку ретроструктуру, що забезпечує дуже високу селективність дії (зв’язування майже виключно з рецепторами прогестерону). На відміну від інших прогестогенів дидрогестерон позбавлений естрогенної, андрогенної та глюкокортикоїдної активності. Завдяки кращій біодоступності та прогестагенній активності основних метаболітів дидрогестерон можна призначати у значно нижчій (у 10-20 разів) дозі порівняно з пероральним мікронізованим прогестероном. У цей огляд увійшли лише 2 РКД, в яких оцінювали побічні ефекти дидрогестерону; нещодавно опублікований систематичний огляд, в якому йшлося про використання дидрогестерону для запобігання викидню, включив 13 досліджень, в яких повідомлялося про побічні ефекти. Загалом наявні дані свідчать про те, що застосування дидрогестерону асоціюється з мінімальними побічними ефектами.
Результати проведеного огляду узгоджуються з висновками недавнього Кокранівського огляду стосовно ПЛФ, згідно з якими синтетичний прогестерон має значні переваги порівняно з натуральним прогестероном (van der Linden et al., 2015). У нього увійшли 4 порівняльних дослідження, з яких 3 РКД також включено в наш огляд. Четверте ж дослідження не було включено, оскільки в ньому порівнювали ефективність перорального хлормадинону і внутрішньом’язового прогестерону. Проте в наш огляд додано ще 5 РКД, в яких порівнювали ефективність пероральної форми дидрогестерону і вагінальної форми прогестерону після переносу ембріона; крім того, проаналізовано ще одне порівняльне дослідження дидрогестерону і вагінальної форми прогестерону після внутрішньоматкового запліднення. Тож ми вважаємо, що отримані нами результати краще репрезентують наявну доказову базу порівняння ефективності застосування пероральної форми дидрогестерону і вагінальної форми прогестерону для ПЛФ у жінок, які отримують ДРТ.
У 2007 р. S. van Dulmen і співавт. встановили, що комплаєнс і задоволеність пацієнток лікуванням безпосередньо залежать від спрощення режиму терапії. Жінки, які отримують вагінальний прогестерон для ПЛФ, можуть скаржитися на вагінальний дискомфорт, який проявляється подразненням, запаленням, свербежем, сухістю і болем. Усі ці фактори можуть негативно впливати на комплаєнс. Іншими важливими характеристиками дидрогестерону, що дозволяють покращити комплаєнс, є нижча вартість порівняно з вагінальними лікарськими формами прогестерону. Краща прихильність до лікування при ПЛФ може пояснювати вищу частоту триваючої та клінічної вагітності, яка спостерігалася при застосуванні дидрогестерону порівняно з вагінальною формою прогестерону у вигляді капсул. Крім того, фізичний і психологічний дистрес, пов’язаний з використанням вагінальної форми прогестерону, міг сприяти достроковому припиненню лікування і, відповідно, зменшенню шансів завагітніти. Отже, пероральна форма дидрогестерону ймовірно є оптимальним варіантом для ПЛФ завдяки кращому комплаєнсу, який, своєю чергою, може реалізуватись у вищій кумулятивній частоті вагітності.
Висновки
У циклах ДРТ пероральна форма дидрогестерону, який застосовують для ПЛФ, забезпечує ефективність, порівнянну з вагінальною формою прогестерону. На нашу думку, пероральна форма дидрогестерону – це раціональний вибір для клінічної практики, оскільки дозволяє отримати такі самі результати за умови нижчої вартості та меншої незадоволеності лікуванням.
Список літератури знаходиться в редакції.
Стаття друкується в скороченні.
Barbosa M.W.P., Silva L.P., Navarro P.A. et al. Dydrogesterone vs progesterone for luteal-phase support: systematic review and meta-analysis
of randomized controlled trials. Ultrasound
Obstet Gynecol 2016; 48: 161-170.
Переклав з англ. Олексій Терещенко
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 1 (25), березень 2017 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...




