Ингибиторы PD-1 и PD-L1: в чем отличия?
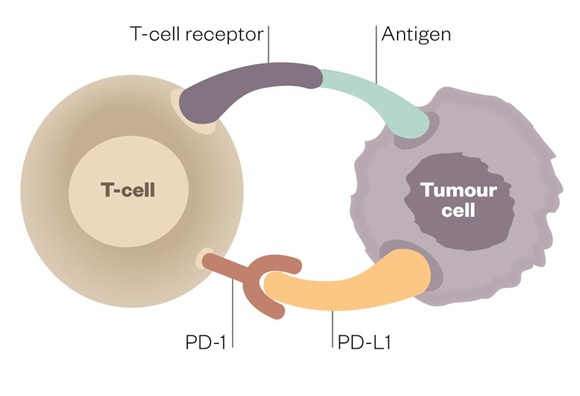
Одним из наиболее обсуждаемых методов, применяемых для лечения больных онкологического профиля, является усиление иммунной противоопухолевой активности путем блокирования иммунных контрольных точек. Воздействие на Т-лимфоцитарное звено иммунной системы онкологических больных обеспечивает долговременное клиническое преимущество. В доклинических и на ранних фазах клинических исследований подтверждено, что воздействие на лиганд запрограммированной клеточной смерти 1 типа (PD-L1) и его рецептор (PD-1) может обеспечивать продолжительный клинический ответ у пациентов с различными типами опухолей. Достигнутые результаты изменили парадигму лечения таких больных и понимание того, как иммунная система человека взаимодействует с опухолью.
Предпосылка к созданию PD-L1 или PD-1 – ускользание от иммунного ответа
Развитие злокачественного новообразования представляет собой многоступенчатый процесс, характеризующийся накоплением генетических и эпигенетических изменений. Эти изменения, специфические для злокачественных клеток, приводят к появлению антигенов, способных распознаваться иммунной системой. В результате циркулирующие иммунные клетки могут атаковать и уничтожать предраковые или злокачественные клетки подобно тому, как они атакуют возбудителей инфекций. Тем не менее, активация иммунной системы является сложным явлением, зависящим от баланса между стимулирующими и ингибирующими сигналами [1]. Последние необходимы, чтобы предотвратить аутоиммунные процессы в здоровом человеческом организме.
Ингибирующие иммунные контрольные точки связаны с сигнальными путями, которые снижают модуляцию ответов иммунной системы Т-лимфоцитов, блокируя неадекватное распознавание нормальной ткани активированными иммунными клетками и предотвращая аутоиммунные процессы. К настоящему времени идентифицированы различные молекулы иммунных контрольных точек, включая цитотоксический Т-лимфоцитарный антиген-4 (CTLA-4), рецептор запрограммированной клеточной смерти-1 (PD-1), Т-клеточный иммуноглобулин и домен муцина-3 (TIM-3), ген лимфоцитарной активации-3 (LAG-3) и другие [8].
Чтобы не быть уничтоженной иммунной системой, опухоль использует механизмы ускользания от иммунного ответа. Факторы, связанные с этим феноменом, включают:
– отсутствие сильных опухолевых антигенов или эпитопов, распознаваемых Т-лимфоцитами;
– минимальную активацию опухольспецифических Т-лимфоцитов;
– слабую инфильтрацию Т-лимфоцитов в пределы злокачественного новообразования;
– снижение регуляции основного комплекса гистосовместимости на опухолевых клетках;
– активацию иммуносупрессивных факторов и клеток в микроокружении опухоли [5].
Рецепторы PD-1 и B7.1 представляют собой отрицательные регуляторы активации Т-лимфоцитов. Связывание PD-L1 с этими рецепторами подавляет миграцию лимфоцитов, их пролиферацию и секрецию цитотоксических медиаторов и таким образом ограничивает способность иммунной системы уничтожать опухолевые клетки. Рецепторы PD-1 и B7.1 экспрессируются Т-лимфоцитами. Лиганд PD-L1 экспрессируется опухолевыми клетками, а также иммунными клетками, инфильтрирующими опухоль [2].
Экспрессия PD-L1 наблюдается при широком спектре солидных опухолей, онкогематологических заболеваний и коррелирует с неблагоприятным прогнозом. Эти результаты подтверждают гипотезу о том, что экспрессия PD-L1 является распространенным механизмом, позволяющим раковым клеткам избежать разрушения иммунной системой.
Предотвращение взаимодействия PD-1/PD-L1 способно значительно усилить функцию Т-лимфоцитов, приводя к возникновению у последних выраженной противоопухолевой активности. Эти данные свидетельствуют о том, что применение ингибиторов иммунных контрольных точек должно быть наиболее эффективным у пациентов, у которых ранее существовавший иммунитет был подавлен за счет экспрессии PD-L1, а значит, может быть снова активирован [3].
Разные мишени и терапевтическое воздействие
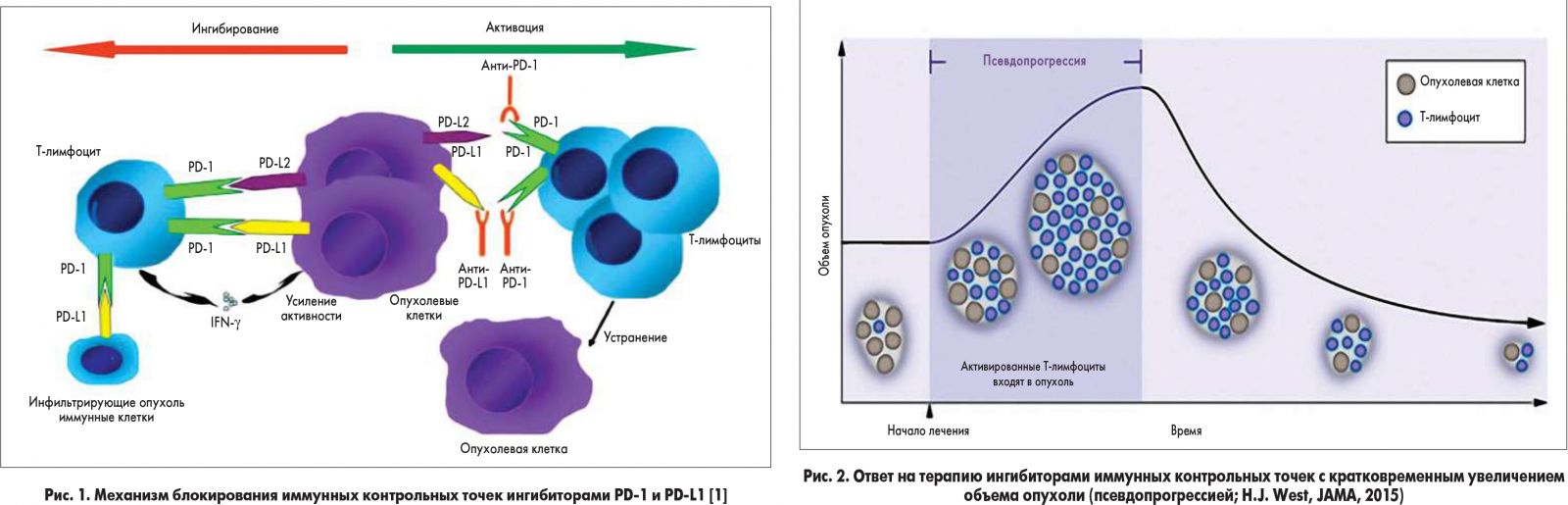
В современной онкологии используются две стратегии воздействия на сигнальный путь PD-1/PD-L1, которые привели к разработке двух соответствующих групп препаратов – ингибиторов иммунных контрольных точек (рис. 1). Без лечения действие PD-1 способствует подавлению функции Т-лимфоцитов.
Терапия, направленная на блокирование PD-1, делает невозможным его взаимодействие с лигандами PD-L1 и PD-L2, но допускает взаимодействие лиганда PD-L1 с рецептором В7.1 на поверхности Т-лимфоцита – то есть остается доступным один из путей подавления иммунной системы и ускользания от иммунного ответа.
Ингибирование PD-L1 устраняет угнетающее воздействие опухолевой клетки на Т-лимфоцит, но не препятствует взаимодействию PD-1 с лигандом PD-L2, необходимому для профилактики аутоиммунных явлений. Препарат Тецентрик (атезолизумаб) является единственным на сегодняшний день анти-PD-L1-препаратом.
Также установлено, что при назначении анти-PD-L1-терапии в течение первых 2 недель или даже первого месяца организм пациента активно перестраивает иммунный ответ. При первом введении ингибитора PD-L1 количество активированных Т-лимфоцитов в крови пациента резко повышается.
Затем активированные Т-лимфоциты мигрируют в периферические ткани и накапливаются в опухоли, вызывая явление псевдопрогрессии (рис. 2). При введении ингибитора PD-1 это явление не наблюдается.
Возрастающая активность Т-лимфоцитов после введения ингибитора PD-L1 отмечается у каждого пациента онкологического профиля, независимо от функционального статуса и исходного состояния иммунной системы. Разработчики предполагают, что эта особенность может обеспечивать преимущество в отдаленной выживаемости пациентов, в том числе тех, у которых исходный иммунный ответ на опухоль был очень низким.
Это подтверждается в исследованиях: пациенты с низким уровнем иммунного ответа на опухоль или даже его отсутствием (независимо от того, каким именно способом у них определялся иммунный ответ) все равно имеют преимущество в выживаемости при терапии ингибитором PD-L1, причем не только выживаемости без прогрессирования, но и общей выживаемости.
Структура молекулы
Ингибиторы PD-1/PD-L1 по структуре представляют собой моноклональные антитела, полученные с помощью биотехнологий. Большинство терапевтических моноклональных антител, которые в настоящее время используются для таргетной терапии в онкологии, содержат тяжелую цепь иммуноглобулина G1 (IgG1) человека. Домены Fc моноклональных антител могут быть определяющими для эффективности PD-L1/PD-1 [4].
В отличие от анти-PD-1-препаратов, среди которых есть IgG4-антитела, Тецентрик представляет собой полностью гуманизированное моноклональное антитело IgG1, которое нацелено на трансмембранный белок PD-L1, экспрессируемый на поверхности опухолевых и иммунных клеток. Это моноклональное антитело содержит модифицированный домен Fc, задача которого – ограничить антителозависимую и комплементарно-зависимую цитотоксичность. Специально введенная в структуру молекулы модификация (изменение Asp-Ala, введенное в положение 298) исключает способность домена связываться с человеческими Fcγ-рецепторами [6, 7].
Таким образом, ингибиторы PD-1 и PD-L1 представляют собой разные иммуноглобулины (IgG1 или IgG4), обладающие разной структурой молекулы, сайтами связывания, действие которых направлено на разные мишени [6, 7].
Безопасность
В целом терапия ингибиторами PD-1/PD-L1 хорошо переносится пациентами, проявления токсичности ниже, чем при лечении ингибитором другой иммунной контрольной точки – CTLA‑4.
Это связано с существенным различием в механизме содействия этих молекул (рис. 3) и влиянии на разные сигнальные пути. Токсичность лечения ингибиторами PD-1/PD-L1 может быть более выраженной у пациентов с аутоиммунными процессами, проявления которых контролируются лигандами PD-L1 и PD-L2.
Пациенты, получающие ингибиторы иммунных контрольных точек, нуждаются в тщательном мониторинге для своевременного выявления и устранения побочных эффектов, в том числе аутоиммунных процессов.
Большинство побочных эффектов не требуют прекращения терапии и могут быть устранены путем симптоматического лечения. В некоторых случаях они достаточно выражены и необходима их немедленная коррекция.
Вмешательство в иммунную систему может провоцировать осложнения с ее стороны. Преимуществом анти-PD-L1-терапии является более низкий риск аутоиммунных процессов, поскольку ингибирующее звено PD-1/PD-L2 остается активным. При развитии иммунной токсичности в большинстве случаев терапию не прекращают, но дополнительно назначают сопроводительное лечение (стероиды) для контроля этих побочных явлений. Следует учитывать, что пациенты могут получать иммунотерапию в течение многих лет без появления какой-либо дополнительной токсичности [4].
Персонализация иммунотерапии в будущем
Точная идентификация и понимание механизмов ускользания от иммунного ответа у отдельных больных онкологического профиля позволит проводить персонализированную противоопухолевую иммунотерапию, при которой моно- и комбинированную иммунотерапию выбирают исходя из наличия специфических особенностей состояния иммунной системы [3].
Предполагается, что широкий спектр фенотипов опухолей может требовать разных иммунотерапевтических стратегий. J. Kim и D. Chen (2016) предложили гипотетический алгоритм, в котором исследуются онкологические биомаркеры, связанные с резистентностью опухоли, включая наличие Th1-иммунитета, экспрессию PD-L1, исключение Т-лимфоцитов из опухоли, экспрессию молекул комплекса гистосовместимости, а также наличие или отсутствие других иммуномодулирующих факторов [5]. Эти данные сопоставляются с конкретными схемами иммунотерапии, которые устраняют основную причину неэффективного противоопухолевого иммунного ответа.
Для пациентов, опухоли которых демонстрируют воспалительный фенотип и признаки исходно существовавшего иммунного ответа, сильную экспрессию PD-L1, высокую мутационную нагрузку, может быть достаточной только монотерапия ингибиторами PD-L1 или PD-1.
Опухоли с воспалительным фенотипом, использующие другие механизмы ускользания от иммунного ответа, могут потребовать комбинированной терапии, например сочетания ингибитора PD-L1 или PD-1 с ингибитором индолеамин‑2,3-диоксигеназы (IDO).
Пациентам с невоспалительным фенотипом опухоли может быть назначена комбинация ингибитора PD-L1 или PD-1 с терапией, нацеленной на другие механизмы резистентности (например антиангиогенная, анти-OX40 или химиотерапия. Персонализированная иммунотерапия позволит использовать конкретные схемы, подбираемые исходя из биологических особенностей опухоли у конкретного пациента [5].
Сегодня комбинированные терапевтические стратегии, включающие иммунотерапию – это область, которая представляет значительный интерес. В настоящее время нет ни одного официально одобренного биомаркера, прогнозирующего ответ на анти-PD-1 / анти-PD-L1-терапию [3, 8]. Важно понимать, что экспрессия PD-L1 не является единственным фактором, определяющим терапевтический ответ.
Комбинированная иммунотерапия может быть использована при PD-L1-отрицательных опухолях или опухолях с неопределенным статусом и может включать химиотерапию и другие подходы, например, антиангиогенные соединения или лучевую терапию. Опухольспецифические антигены, большое количество которых высвобождается во время индуцированного химиотерапией некроза опухоли, потенциально способны увеличить иммуноспецифичность опухоли и, следовательно, повысить эффективность терапии ингибиторами иммунных контрольных точек [8].
Литература
1. Aydin A.M., Woldu S.L., Hutchinson R.C. et al. Spotlight on atezolizumab and its potential in the treatment of advanced urothelial bladder cancer. Onco Targets Ther. 2017; 10: 1487-1502.
2. Chen D., Mellman I., Herbst R. et al. Predictive correlates of response to the anti-PD-L1 antibody MPDL3280A in cancer patients. Nature. Nov 2014.
3. Meng X., Huang Z., Teng F., Xing L., Yu J. Predictive biomarkers in PD‑1/PD-L1 checkpoint blockade immunotherapy. Cancer Treat Rev, 41(10). 2015: 868-876.
4. Chen D.S., Irving B.A., Hodi F.S. Molecular pathways: next-generation immunotherapy – inhibiting programmed death-ligand 1 and programmed death‑1. Clin Cancer Res. 2012 Dec 15; 18 (24): 6580-7.
5. Kim J.M., Chen D.S.. Immune escape to PD-L1/PD‑1 blockade: seven steps to success (or failure). Annals of Oncology, Vol. 27, issue 8, 1 August 2016: 1492-1504.
6. www.invivogen.com.
7. Scapin G., Yang X., Prosise W. et al. Structure of full-length human anti-PD-1 therapeutic IgG4 antibody pembrolizumab. Nat Struct Mol Biol. 2015 Dec; 22 (12): 953-8. doi: 10.1038/nsmb.3129. Epub 2015 Nov 23.
8. Nguyen-Ngoc T., Reck M., Tan D., Peters S. Immunotherapy and Targeted Therapies in the Treatment of Non-small Cell Lung Cancer. European Oncology & Haematology, 2017; 13 (1): 35–52.
Подготовила Катерина Котенко
Тематичний номер «Онкологія» № 4 (50), жовтень 2017 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...





.jpg)

.jpg)

