Комплексный подход к лечению ВПЧ-индуцированных заболеваний кожи
11-13 октября 2017 г. при поддержке Украинской академии дерматовенерологии в UBI Conference Hall состоялось уже второе в этом году масштабное профессиональное мероприятие – 12-е «Киевские дерматологические дни». На этот раз в работе форума приняли участие более 700 специалистов со всех уголков Украины. Напомним, что на весеннем симпозиуме количество зарегистрированных участников составило более 500. Таким образом, в этом году ознакомиться с последними наработками, поделиться своим опытом и обсудить наиболее актуальные темы в области дерматовенерологии имели возможность более 1 300 человек, среди которых были ведущие отечественные эксперты в области дерматовенерологии, онкологии, а также врачи эстетической медицины, трихологи, косметологи и др. В рамках данных мероприятий было предлложено множество интересных докладов, тезисы которых мы хотели бы представить вниманию наших читателей. Предлагаем ознакомиться с кратким обзором одного из заинтересовавших нас докладов, поскольку значительный объем информации и формат издания не позволяют рассказать нашим читателям сразу обо всем.
Тему современных методов лечения эпидермальных образований аногенитальной области, ассоциированных с вирусом папилломы человека (ВПЧ), в своем докладе раскрыла доцент кафедры кожных и венерических болезней Винницкого национального медицинского университета им. Н.И. Пирогова, кандидат медицинских наук Марина Родионовна Анфилова.
– Аногенитальные кондиломы – заболевания, вызванные ДНК-содержащим вирусом, который относится к роду папилломавирусов (Papillomavirus) семейства папавирусов (Papavaviridae). Папилломавирусы – единственная группа вирусов, в отношении которых доказано, что они индуцируют образование опухолей у человека в естественных условиях. Большинство аногенитальных кондилом вызваны инфицированием ВПЧ 6 и 11-го типа (S. Syrjanen, 2003).
В свою очередь, ВПЧ представляет собой группу вирусов, чрезвычайно широко распространенных во всем мире. В странах со средним и низким уровнем дохода инфицированность населения достигает в среднем 85%.
Также достоверно известно, что наличие ВПЧ ассоциировано с высоким риском развития рака шейки матки, который, в свою очередь, является четвертой по распространенности формой рака у женщин и занимает одну из лидирующих позиций в структуре смертности от злокачественных процессов (Всемирная организация здравоохранения, 2012).
К факторам риска развития аногенитальных кондилом можно отнести: молодой возраст (около 25 лет), раннее начало половой жизни (до 16 лет), а также наличие большого количества половых партнеров. Кроме того, следует учитывать, что если партнер женщины ведет беспорядочную половую жизнь, это тоже является одним из основных факторов риска. Немаловажную роль в развитии аногенитальных кондилом играет наличие ВИЧ-инфекции (аногенитальные кондиломы отмечаются практически у четверти ВИЧ-инфицированных пациентов).
При диагностике ВПЧ в обязательном порядке необходимо придерживаться общепринятого алгоритма действий, первым этапом которого является осмотр кожи и слизистых оболочек наружных половых органов. Следующим этапом для выявления морфологических изменений в клетках, в том числе обусловленных ВПЧ, является цитологическое исследование мазков (взятых со слизистой поверхности шейки матки) по Папаниколау – PAP-тест.
Для более детального изучения поверхности шейки матки следует прибегнуть к кольпоскопии – инструментальному методу диагностики, благодаря которому врач-дерматовенеролог может провести осмотр состояния тканей шейки матки под тридцатикратным увеличением с дальнейшей оценкой наиболее характерных признаков субклинических форм ВПЧ (ацетобелый эпителий, мозаика, пунктация, аномальная зона трансформации).
На протяжении многих лет одним из наиболее информативных методов специфической диагностики ВПЧ является полимеразная цепная реакция, позволяющая определять ДНК ВПЧ, однако в некоторых случаях данный метод может давать ложноположительный результат. В связи с этим для более точного установления диагноза целесообразно проводить Digene-тест (метод гибридного захвата), который дает возможность не только выявить наличие ВПЧ, но и определить его тип, а также степень его онкогенности.
Таким образом, в арсенале врача должны быть наиболее информативные методы исследования, позволяющие своевременно диагностировать ВПЧ-инфекцию, что, в свою очередь, позволит подобрать наиболее рациональную тактику лечения в отношении проявлений данной инфекции (аногенитальных кондилом).
В первую очередь, метод терапии должен иметь высокий профиль безопасности и эффективности, а также характеризоваться низким риском развития рецидивов.
Тактика лечения считается оптимальной в том случае, если она позволяет достичь клинической и терапевтической эффективности в отношении всего поля дисплазии. Также важным фактором выбора является минимальные болезненность и дискомфорт.
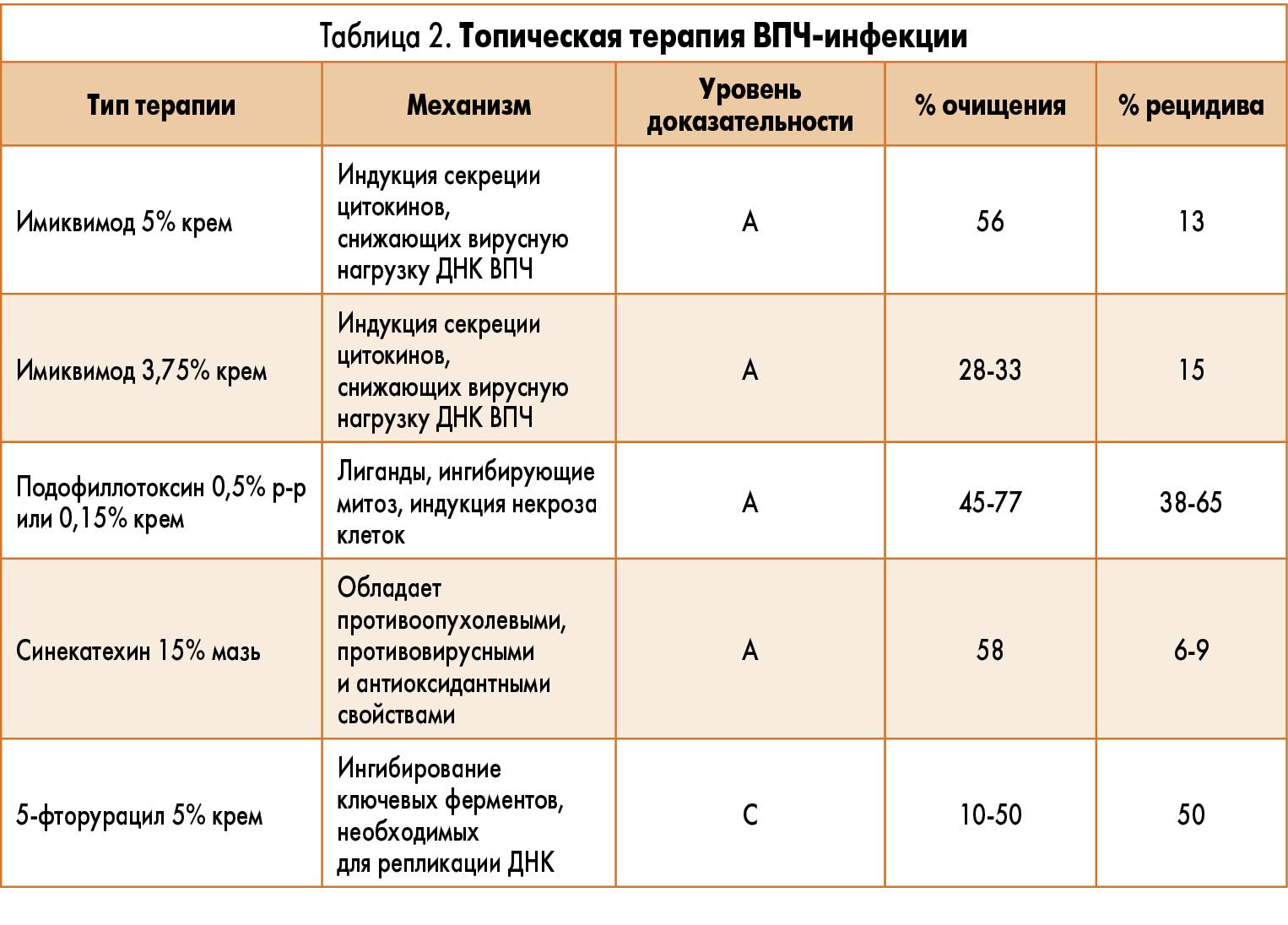
На сегодняшний день к оптимальным методам консервативного лечения ВПЧ-инфекции относится медикаментозная терапия, подразумевающая назначение препаратов для наружного применения (имиквимод крем 5% и 3,75%; подофиллотоксин 0,5% р-р или 0,15% крем; синекатехин мазь 15%) с целью устранения новообразований, ассоциированных с ВПЧ-инфекцией, на коже и слизистой оболочке наружных половых органов.
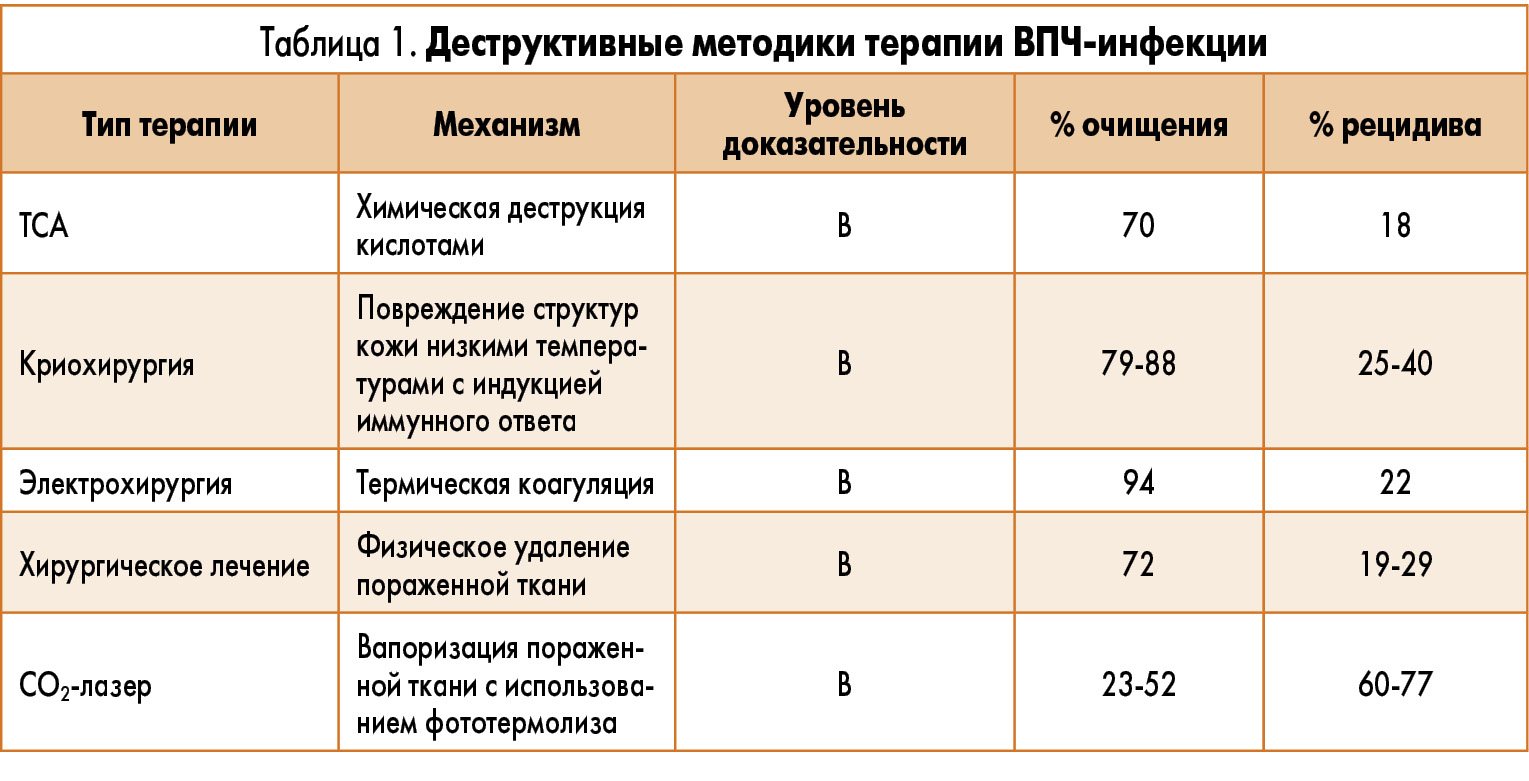
Терапевтическая эффективность и краткое описание механизма действия и характеристик применяемых на сегодняшний день методик лечения ВПЧ-инфекции представлены в таблицах 1 и 2.
При выборе средства следует обратить внимание на то, что высокая степень устранения клинических проявлений ВПЧ, в частности аногенитальных кондилом, не всегда гарантирует уменьшение частоты рецидивов. Так, например, имиквимод 5% в форме крема индуцирует секрецию цитокинов, снижающих вирусную нагрузку ДНК ВПЧ, характеризуется высоким уровнем устранения кондилом (56%) и низким уровнем их рецидивов (до 14%).
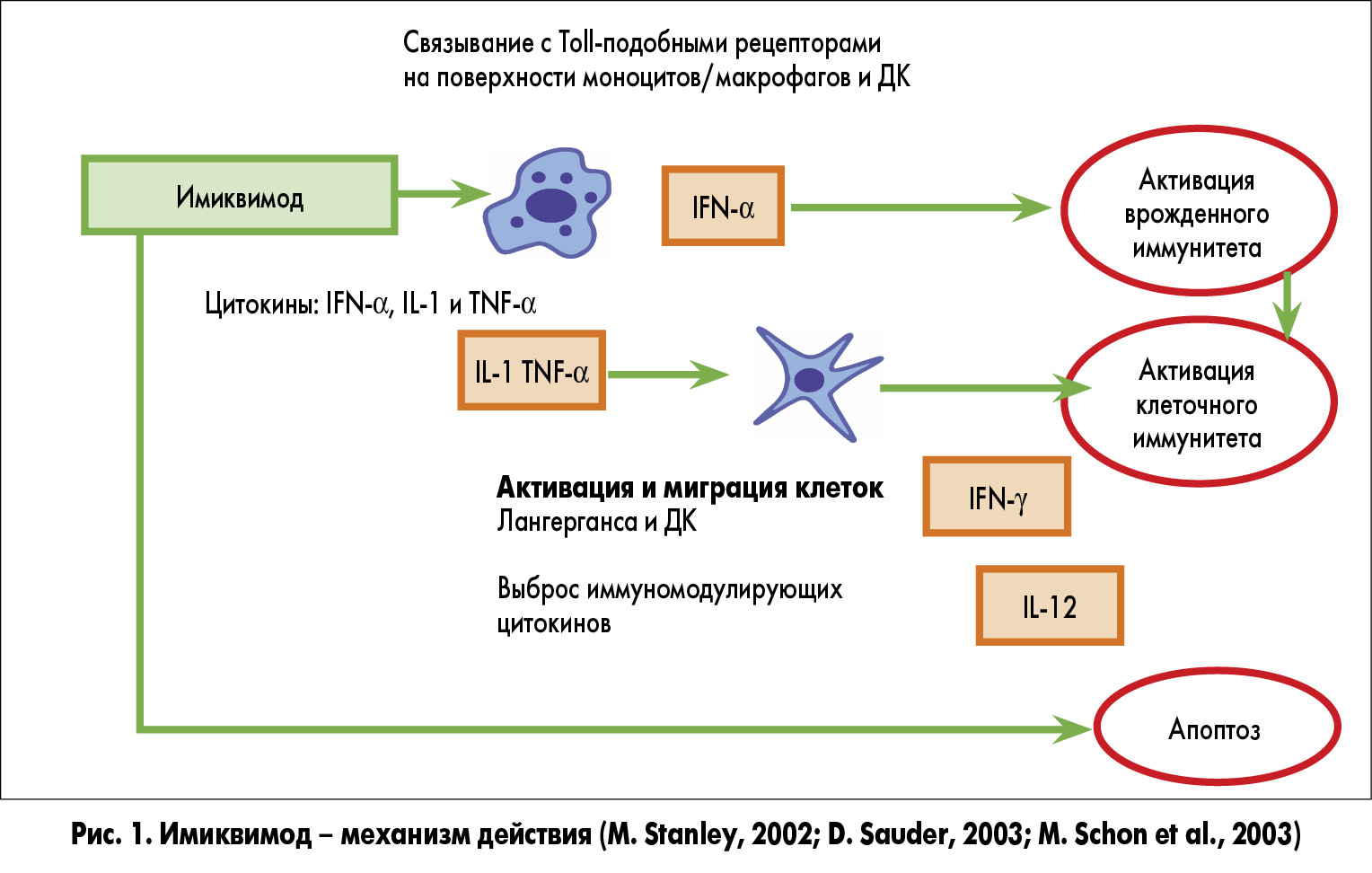
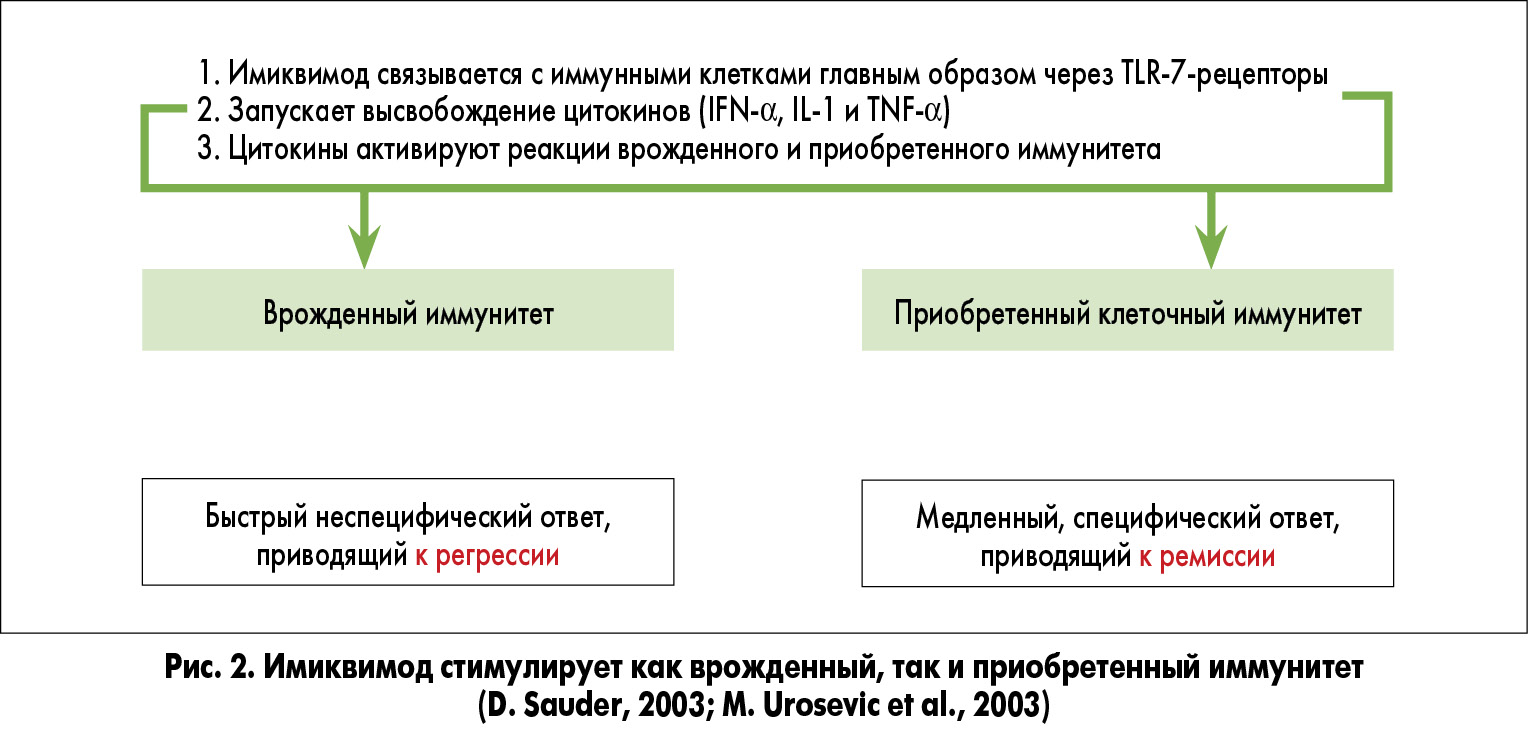
Механизм действия имиквимода позволяет ему связываться с иммунными клетками через TLR-7-рецепторы (Toll-подобные рецепторы), запуская высвобождение провоспалительных цитокинов (интерферон-α, интерлейкин-1, фактор некроза опухоли). В свою очередь, эти цитокины активируют реакции врожденного и приобретенного иммунитета (рис. 1). Таким образом, достигается быстрый неспецифический ответ, приводящий к регрессированию ВПЧ-инфекции, а также медленный специфический ответ, ведущий к ремиссии заболевания (рис. 2).
Имиквимод 5% крем рекомендован к применению различными международными руководствами по лечению кондилом наружных половых органов и широко применяется в клинической практике врачей-дерматовенерологов. Безусловным его преимуществом является возможность использования в домашних условиях, так называемая «home therapy» – пациент наносит препарат самостоятельно, что обусловливает его высокую приверженность к данному методу терапии.
Имиквимод 5% крем является эффективным средством в лечении аногенитальных кондилом с высокой степенью их устранения (50-61,8%) и низкой частотой рецидивов (9-14%) после 3-месячного курса лечения. Важно отметить, что результативность терапии не зависит от исходной площади поражения, длительности заболевания, предыдущего лечения (H.W. Buck et al., 2002; D.N. Sauder, 2002).
В настоящее время на фармацевтическом рынке Украины имиквимод 5% представлен препаратом Алдара компании Meda. Препарат выпускается в форме крема и имеет удобную расфасовку в пакетиках по 250 мг (№ 12). Частоту и длительность применения врач определяет индивидуально для каждого пациента. Особая форма упаковки позволяет самостоятельно в домашних условиях проводить лечение. При этом необходимо учитывать основные принципы применения крема Алдара:
- крем Алдара наносится на кожу перед сном;
- перед нанесением необходимо вымыть руки и зону обработки с применением мягкого моющего средства, после чего тщательно высушить кожу;
- крем следует наносить на зону поражения с захватом небольшого участка вокруг образования (не более 1 см) и мягко втирать в кожу;
- препарат должен находиться на коже около 8 ч, в течение которых следует избегать попадания воды на данный участок кожи;
- через 8 ч можно вымыть обработанную зону с использованием мягкого моющего средства.
Благодаря возможности лечить поле дисплазии частота рецидивов кондилом после 3 мес терапии препаратом Алдара составляет всего 9-14% в сравнении с криотерапией (21-37,5%), электрохирургией (25-33%) и хирургическим удалением кондилом – 13-18% (Challenor et al., 2002; Lacey et al., 2003).
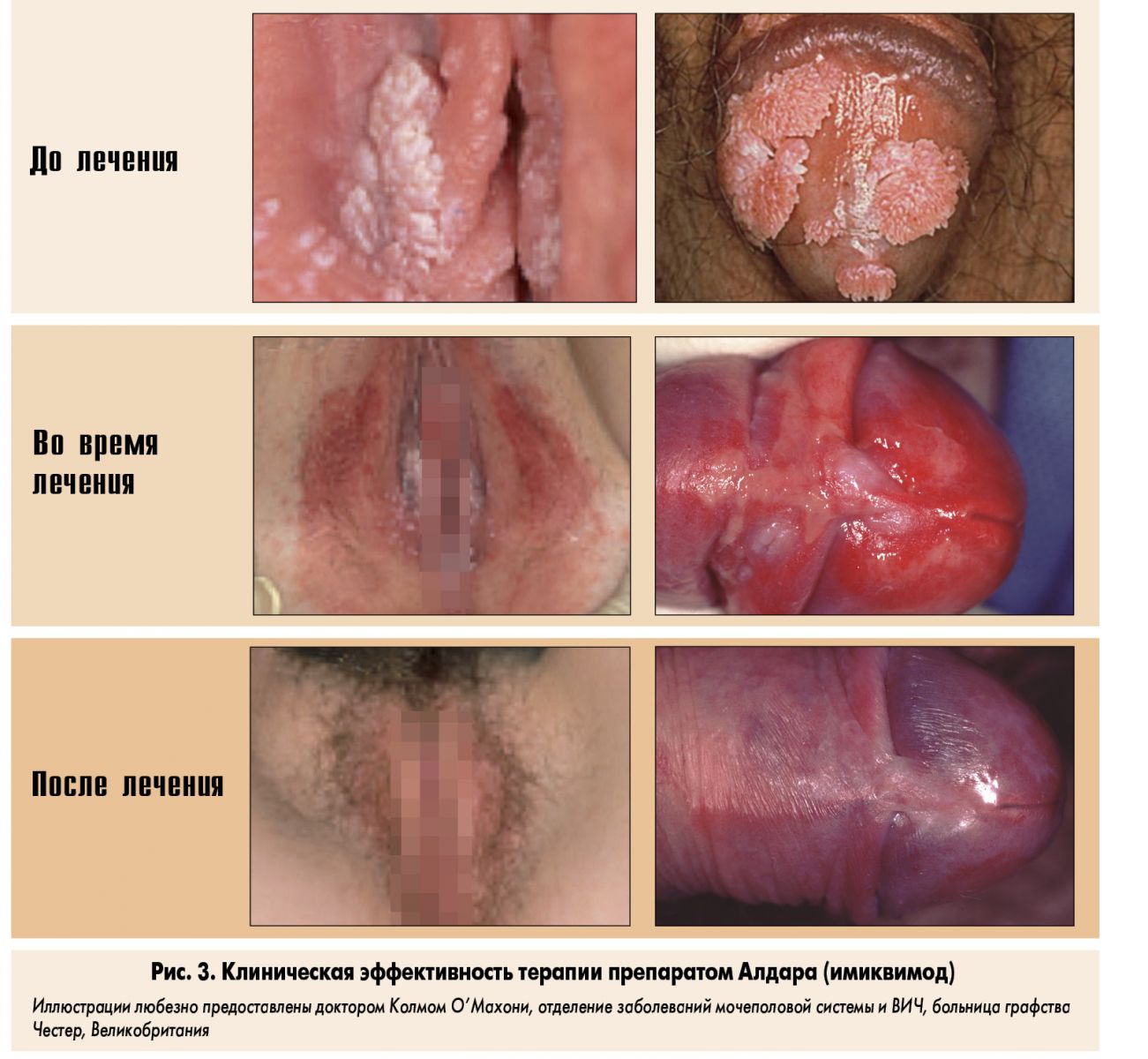
При использовании крема Алдара самое распространенное «нежелательное» явление – локальная эритема. В большинстве случаев она имеет легкую или умеренную степень выраженности и постепенно исчезает после прекращения лечения. Проявление эритемы следует рассматривать в качестве индивидуального иммунного ответа, что свидетельствует об ответе на лечение (L. Edvards et al., 1998) (рис. 3).
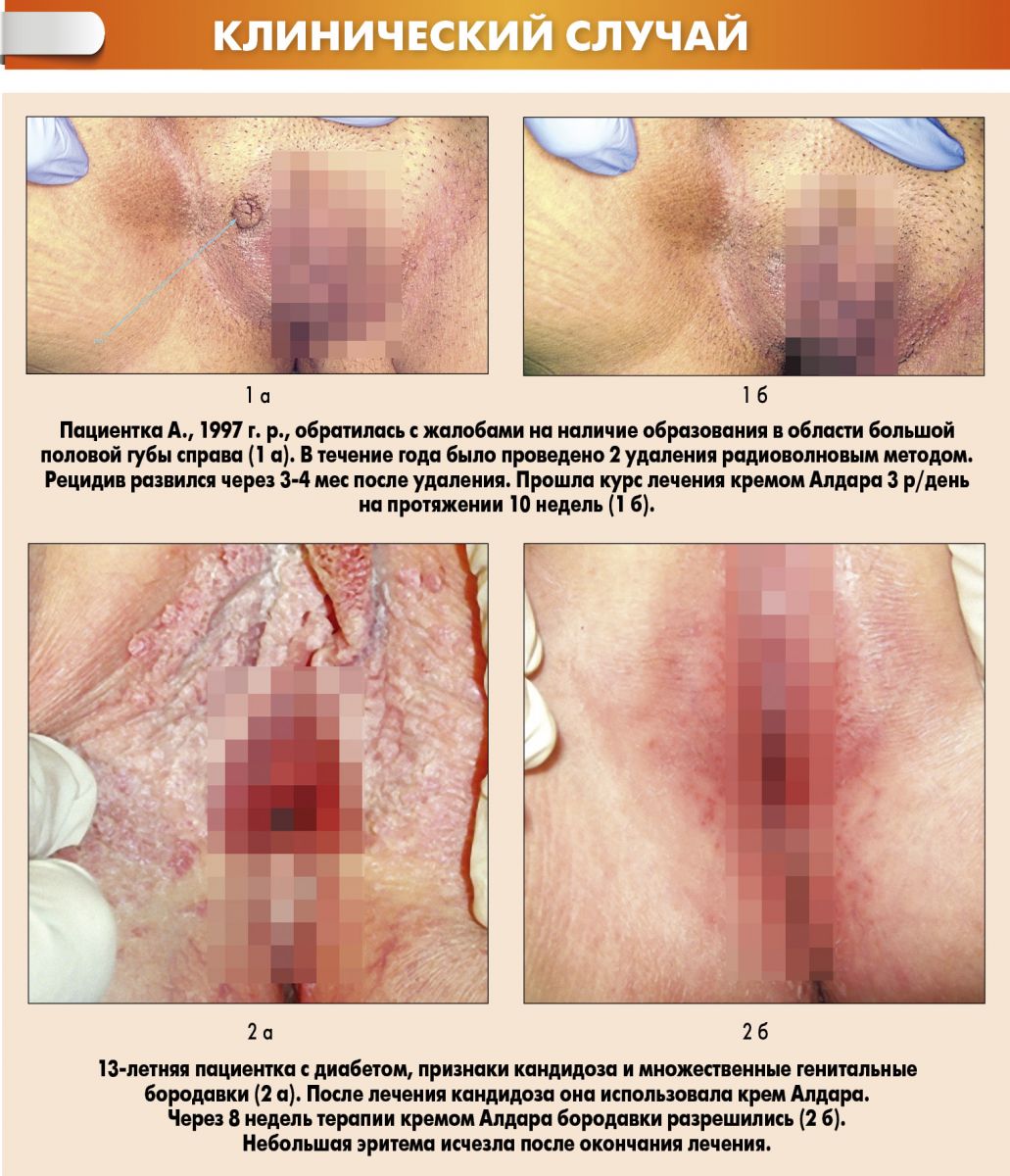
До начала лечения с применением препарата Алдара необходимо ликвидировать все сопутствующие инфекции. Рассмотрим данное утверждение на примере клинического случая.
Пациентка, 13 лет, диабет, множественные генитальные кондиломы в анамнезе, признаки кандидоза. После проведенного лечения кандидозной инфекции применение препарата Алдара курсом 3 раза в неделю позволило достичь полной ликвидации кондилом уже через 8 недель терапии. Небольшая эритема, появившаяся в процессе лечения, исчезла после его окончания. Важно, что в таких ситуациях врачу необходимо психологически настроить и расположить пациента к терапии, обязательно информируя его о возможных кожных реакциях.
Алдара (5% крем имиквимод):
- Стимулирует иммунитет там, где это необходимо!
- Возможно применение имиквимода с любыми деструктивными методами терапии.
- Единственный метод терапии «поля дисплазии»!
- Этиотропная терапия ОК имиквимодом обеспечивает «иммунную память клетки» по отношению к ВПЧ, что проявляется минимальным количеством рецидивов (всего 9-14%).
Таким образом, препарат Алдара (имиквимод 5% крем) является эффективным средством при лечении аногенитальных кондилом и характеризуется минимальным риском развития рецидивов. Удобные форма выпуска и упаковка позволяют пациенту осуществлять лечение самостоятельно в домашних условиях, что, в свою очередь, многократно увеличивает его приверженность к данному методу терапии.
Подготовила Марина Титомир
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...