Генеричні антиаритмічні засоби не є терапевтично еквівалентними для лікування тахіаритмій
Антиаритмічні препарати (ААП) залишаються основою лікування аритмій. При тяжких аритміях неефективність ААП може призвести до смерті. Якщо рівні ААП зменшуються нижче мінімальної ефективної концентрації, аритмія може рецидивувати [14]. І навпаки, надмірне підвищення концентрації препарату збільшує проаритмічний ризик. Терапевтичне вікно – це рівні препарату понад мінімальну ефективну концентрацію, але нижчі концентрації, що призводить до тяжких побічних ефектів. Для деяких препаратів або клінічних умов терапевтичне вікно може бути досить широким, натомість для інших – доволі вузьким (вузький терапевтичний індекс – ВТІ [5]). Отже, у разі використання препаратів з ВТІ коливання рівнів препарату можуть мати тяжкі наслідки [14].
Коливання сироваткових рівнів препарату можуть виникати при заміні оригінального препарату на генерик, одного генерика на інший або генерика на оригінальний препарат [1]. Для схвалення генеричної версії оригінального препарату Управлінням з контролю безпеки продуктів харчування та лікарських засобів США (FDA) потрібно продемонструвати «хімічну еквівалентність» (подібні вміст і розчинність активної речовини для оригінального та генеричного препаратів) та «біоеквівалентність» (параметри абсорбції генерика в межах 80125% від таких параметрів оригінального препарату за однакових умов дослідження) [5]. Багато експертів вважають неприйнятним настільки широкий діапазон біоеквівалентності для препаратів з ВТІ [69]. Щоб визначити реальний рівень стурбованості лікарів і ризики, пов’язані із заміною ААП, американські дослідники J. A. Reiffel та P. R. Kowey звернулися до 130 експертівелектрофізіологів (усі вони є членами Північноамериканського товариства кардіостимуляції та електрофізіології) із запитаннями щодо їхнього досвіду застосування генеричних ААП. Зокрема, респондентів детально розпитували про аритмічні події, пов’язані із заміною ААП, а також про нинішню практику стосовно таких замін.
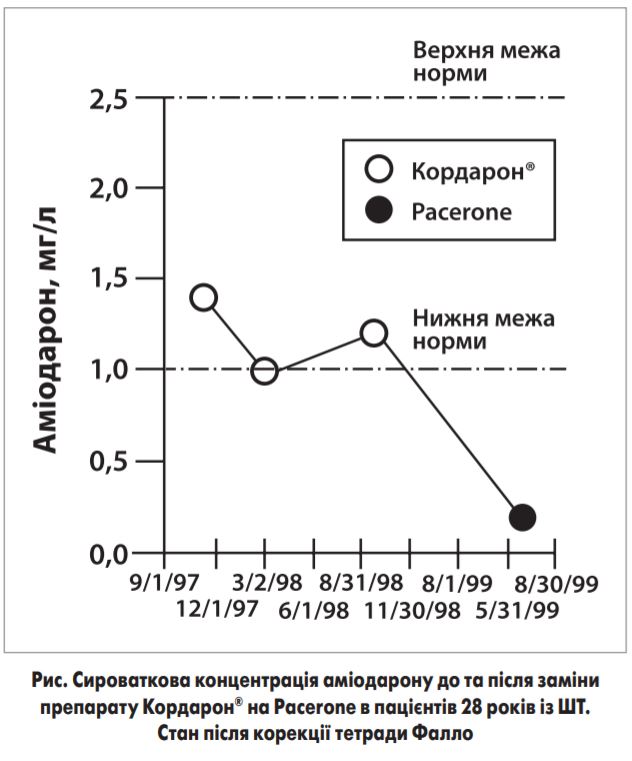 Зпоміж 130 лікарів 64 погодилися взяти участь в опитуванні (незвично високий показник для медичних опитувань). Із цих 64 лікарів 24 повідомили про певні та 7 – про ймовірні випадки рецидиву аритмії (фібриляції шлуночків, шлуночкової тахікардії – ШТ, фібриляції передсердь та передсердної тахікардії), асоційованих із заміною ААП. Двадцять один рецидив був пов’язаний із замінами препаратів хінідину, прокаїнаміду або дизопіраміду, 1 випадок – із заміною оригінального метопрололу генеричним та 32 випадки – із заміною оригінального аміодарону (Кордарон®) генеричним (Pacerone). Серед цих 54 рецидивів 3 мали летальний наслідок (фібриляція шлуночків при заміні хінідину та ШТ при заміні прокаїнаміду та аміодарону). Імовірно, смертей було б більше, якби пацієнти не мали імплантованого кардіовертерадефібрилятора (ІКД). П’ять рецидивів були верифіковані за допомогою провокаційної проби, 2 – опубліковані у вигляді абстрактів [7], принаймні про 3 ексцеси з аміодароном було повідомлено у FDA; при цьому багато з наведених випадків були верифіковані шляхом визначення сироваткових концентрацій препарату (рис.).
Зпоміж 130 лікарів 64 погодилися взяти участь в опитуванні (незвично високий показник для медичних опитувань). Із цих 64 лікарів 24 повідомили про певні та 7 – про ймовірні випадки рецидиву аритмії (фібриляції шлуночків, шлуночкової тахікардії – ШТ, фібриляції передсердь та передсердної тахікардії), асоційованих із заміною ААП. Двадцять один рецидив був пов’язаний із замінами препаратів хінідину, прокаїнаміду або дизопіраміду, 1 випадок – із заміною оригінального метопрололу генеричним та 32 випадки – із заміною оригінального аміодарону (Кордарон®) генеричним (Pacerone). Серед цих 54 рецидивів 3 мали летальний наслідок (фібриляція шлуночків при заміні хінідину та ШТ при заміні прокаїнаміду та аміодарону). Імовірно, смертей було б більше, якби пацієнти не мали імплантованого кардіовертерадефібрилятора (ІКД). П’ять рецидивів були верифіковані за допомогою провокаційної проби, 2 – опубліковані у вигляді абстрактів [7], принаймні про 3 ексцеси з аміодароном було повідомлено у FDA; при цьому багато з наведених випадків були верифіковані шляхом визначення сироваткових концентрацій препарату (рис.).
Крім того, було повідомлено про дві певні та 5 імовірних проаритмічних подій, асоційованих із заміною ААП: 6 для ААП I класу та одна для аміодарону. Дослідники також спостерігали рецидиви тахіаритмії, зумовлені заміною оригінального ААП генеричним: 2 – фібриляції передсердь і 2 – ШТ. Одна подія була пов’язана з хінідином (і супутньою зміною рівня дигоксину) і 3 події – із заміною препарату Кордарон® на Pacerone у пацієнтів з ІКД. Остання призвела до частих шоків (1 випадок – з фібриляцією шлуночків, 2 – із ШТ), які минули після відновлення лікування оригінальним препаратом.
П’ятнадцять респондентів вказали, що призначають лише оригінальні ААП, 8 лікарів зазвичай надавали перевагу генерикам (з них 4 спостерігали небажані події). Інші лікарі лише іноді допускали заміну оригінального препарату генеричним, переважно з фінансових причин.
Проведене дослідження чітко показало, що багато електрофізіологів стикаються з рецидивами аритмії або проаритмією (часто фатальними), пов’язаними із заміною ААП. Завдяки детальному аналізу було встановлено, що в усіх цих випадках мала місце заміна оригінального ААП генеричним. Навіть якщо припустити, що жоден із 66 лікарів, які відмовилися пройти опитування, не спостерігав подібних випадків (що малоймовірно, виходячи з досвіду респондентів та авторів дослідження), той факт, що 31 зі 130 експертів повідомив про 61 випадок проаритмії або рецидиву аритмії у відповідь на заміну ААП, є вражаючим і загрозливим. На національному або ж міжнародному рівні ця проблема має бути дуже значною, хоча її реальний масштаб встановити важко через труднощі з визначенням часового зв’язку між заміною ААП й аритмічною подією.
Велике занепокоєння викликає можливість значної шкоди від таких подій у сучасну еру, коли економічна складова в медицині спонукає державні органи та страхові компанії зменшувати витрати на лікування шляхом заміни оригінальних препаратів генеричними. З огляду на це абсолютно неприйнятними є публікації, які вводять в оману медичну спільноту і пацієнтів, якот звіт Medical Letter [10], де, зокрема, зазначено, що «генерична заміна є неважливою з медичного погляду, оскільки немає доказів, що це призводить до негативних наслідків». Подібні звіти є прикладом нехтування раніше опублікованих численних літературних джерел, де наводяться переконливі докази, що заміна оригінальних ААП генеричними асоціюється з ризиком рецидиву аритмій і неочікуваними економічними втратами [4, 1113].
Дійсно, схвалення генеричного препарату передбачає демонстрацію хімічної та біологічної еквівалентності, проте велика кількість спостережень і, зокрема, обговорюване дослідження переконливо свідчать, що це не гарантує терапевтичної еквівалентності, на яку заслуговують пацієнти [4, 11]. Імовірною причиною терапевтичної неспроможності є численні недоліки процесу тестування генериків, якот: неадекватність аналітичних методів; тестування після прийому однократної дози (замість досягнення рівноважного стану); тестування лише у невеликій групі здорових добровольців, а також неврахування впливу допоміжних речовин, їжі, статі та лікарських взаємодій [1416].
Оскільки обговорюване дослідження не є проспективним, подвійним сліпим чи рандомізованим, може здатися, що отримані результати не мають достатньої доказової ваги. Проте вони абсолютно переконливі для практикуючих лікарів, включно з авторами дослідження, і як мінімум є приводом для клінічної настороги та більш детального вивчення проблеми [11, 1719].
Якщо пацієнт із захворюванням, яке не є загрозливим для життя, отримує лікування препаратом із широким терапевтичним вікном, незалежно від біологічної еквівалентності оригінального препарату та генерика клінічна еквівалентність може й не бути важливою. Завдяки широкому терапевтичному вікну сироваткові рівні препарату, які досягаються за хімічної та біологічної еквівалентності, зазвичай є ефективними та безпечними. Якщо ж біоеквівалентність не дорівнює терапевтичній еквівалентності у пацієнта з небезпечним для життя захворюванням, який лікується препаратом з ВТІ, заміна оригінального препарату генеричним може спричинити дозозалежний проаритмічний ризик або навіть фатальний рецидив аритмії. Звісно, це не означає, що негативні наслідки заміни препарату виникнуть у більшості пацієнтів або що не слід брати до уваги конкретну клінічну ситуацію. Проте розуміння того, що заміна ААП може зашкодити пацієнтам, є дуже важливим, і лікарі мають усвідомлювати, що ця інформація може врятувати багато життів.
На думку авторів, при лікуванні станів, при яких надмірна або недостатня сироваткова концентрація препарату асоціюється зі значними ризиками, заміна оригінального засобу на генерик можлива виключно за умов наявності лише одного генерика (що унеможливлює безконтрольні повторні заміни), ефективність якого доведена клінічно і який є широкодоступним (у лікарнях та аптеках), а також якщо між оригінальним препаратом і генериком існує доведений і послідовний зв’язок, який дозволяє перенести клінічні дані для оригінального препарату на його генеричну копію.
Література
- Bauman J. L. Antiarrhythmics, drug concentrations, and generic substitution. Clinical Dialogues on Arrhythmias. 1990; 2: 14.
- 2. Berry N. S., Bauman J. L., Gallasatequi J. L. et al. Analysis of antiarrhythmic drug concentrations determined during electrophysiologic drug testing in patients with inducible tachycardias. Am J Cardiol 1988; 61: 922924.
- McCollam P.I., Bauman J. L., Beckman K. J., Hariman R. L. A simple method of monitoring antiarrhythmic drugs during short and longterm therapy. Am J Cardiol 1989; 63: 12731275.
- Grubb B. P. Recurrence of ventricular tachycardia after conversion from proprietary to generic procainamide. Am J Cardiol 1989; 63: 15321533.
- Criteria, and evidence to assess actual or potential bioequivalence problems. Federal Registrar 21 CFR320. 33 (c.1998).
- Strom B. L. Generic drug substitution revisited. N Engl J Med 1987; 316: 14561462.
- Ozahowski T. A., Greenberg M. L., Mock P. P. Clinical inequivalence of generic and brand name type IA antiarrhythmic drugs. PACE1998; 21: 809.
- Patnaik R. N., Lesko L. J., Chen M. L., Williams R. L., and the Individual Bioequivalence Working Group. Individual bioequivalence: new concepts in the statistical assessment of bioequivalence metrics. Clin Pharmcokinet 1997; 33: 16.
- Meyer B. M. FDA position on production selection from «narrow therapeutic index» drugs. Pharmacotherapy 1995; 54: 16301632.
- Anonymous. Generic drugs. The Medical Letter 1998; 41: 4748.
- Kowey P. R. What to do about prescribing generic antiarrhythmic drugs. Clinical Dialogues on Arrhythmias. 1990; 2: 13.
- RichtonHewett S., Foster E., Apstein C. S. Medical and economic consequences of a blinded oral anticoagulant brand change at a municipal hospital. Arch Intern Med 1988; 8: 806808.
- Sabatini S., Ferguson R. M., Heiderman J. H. et al. Drug substitution in transplantation: a National Kidney Foundation white paper. Am J Kidney Dis 1999; 33: 389397.
- Mojaverian M. X., Et L., Weinryb I. et al. The relative bioavailabilty of amiodarone HCL in healthy subjects in a fed and fasting state. NASPE1999; in press.
- Pereira J., Rebello J. Recipe Trouble: How Copley, making generic drug for asthma, let bacteria in an now faces lawsuit. The Wall Street Journal, Feb 2, 1995; CCXXV(23): A1 and A9.
- Grady D. In a survey the FDA is accused of nasty drug approval. The New York Times (National) Dec. 3, 1998; CXLVIII: A25.
- Murphy J. E. Generic substitution and optimal patient care. Arch Intern Med 1999; 159: 429433.
- Banahan B. F., Kolassa E. M. A physician survey on generic drugs and substitution of critical dose medications. Arch Intern Med 1997; 157: 20802088.
- Nolan P. E. Generic substitution of antiarrhythmic drugs. Am J Cardiol 1989; 69: 13711373.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 6 (427), березень 2018 р.
- Актуальна тема:
- Актуальна тема «Антиаритмічна терапія аміодароном»




