Раннее сокращение размеров опухоли как независимый маркер улучшенной общей выживаемости пациентов с метастатической карциномой почек
Алгоритм лечения метастатической карциномы почек (МКП) претерпел значительные изменения за последние 10 лет. Применение таргетной терапии МКП ингибиторами тирозинкиназы (иТК) не только увеличило общую выживаемость (ОВ) пациентов до 30 мес, но и, по данным последних исследований, было ассоциировано с частотой объективного ответа (ЧОО) 25-30%. Прогностическое значение раннего сокращения размеров опухоли (рСРО) и корреляция глубокой ремиссии с ОВ у пациентов с МКП были показаны в недавно проведенном анализе. А множество последних исследований продемонстрировали значимость ЧОО в прогнозе исходов у пациентов с МКП. Так, применение кабозантиниба, ниволумаба или комбинации ленватиниба и эверолимуса было ассоциировано с улучшенной ОВ и высокой ЧОО.
 |
 |
| Инструкция для медицинского применения |
Для поиска объективного предиктора ранней оценки эффективности лечения МКП осуществлен текущий анализ. Регрессия опухоли к 6-й нед терапии была определена в качестве предполагаемого раннего маркера для прогнозирования исходов у пациентов с МКП, поскольку, по данным предыдущего клинического исследования, включившего 4334 пациентов из базы данных Pfizer, было продемонстрировано, что уменьшение размеров опухоли на ≥10% связано с благоприятным прогнозом МКП. Однако оставался открытым вопрос: может ли более поздний регресс опухоли иметь такое же или более высокое прогностическое значение? Кроме этого в предыдущих фазах исследования использовались различные классы препаратов.
Возможность прогнозирования результата лечения еще на ранних этапах терапии открывает новые перспективы: потенциально снизить продолжительность клинических исследований и изменить тактику лечения на более ранних этапах. Учитывая валидацию проведенного исследования, рСРО может служить конечной суррогатной точкой для прогнозирования более поздних исходов – ОВ. В клинической практике лишь небольшая часть пациентов продолжает лечение и переходит к следующим линиям терапии, поэтому ранний выбор наиболее эффективного препарата для конкретного пациента может улучшить его исходы и снизить токсичность лечения.
Кроме этого рСРО помогает выделять пациентов с благоприятным прогнозом и правильно их консультировать, а также может использоваться в качестве основания к назначению интермиттирующего курса терапии. В рамках исследования COMPARZ была предпринята попытка оценить прогностическое значение рСРО на первом этапе лечения МКП в двух ранних временных точках: 42 дня и 90 дней от начала терапии.
Статистический анализ
Для оценки результатов на 42-й и 90-й дни от начала терапии использовался метод Каплана – Мейера. Выбор конечной точки для рСРО в 10% был основан на результатах предыдущих исследований. Чтобы дополнительно оценить применимость указанной точки отсечения (10%), был составлен график с нанесением значения мартингальных остатков относительно процентного сокращения размеров опухоли. Таким образом, изменения кривой LOESS указывали на участки, где точки отсечения могут быть наиболее приемлемыми.
Для определения влияния других прогностических факторов на ОВ через 42 дня и 90 дней терапии применялась модель пропорциональных рисков Кокса. Был проведен многовариантный анализ для оценки значимости сокращения размеров опухоли на ≥10% по сравнению с пациентами, не достигшими этой точки, после корректировки всех других потенциальных прогностических факторов.
Все тесты были двусторонними, статистическая значимость была определена как значение р≤0,05. Регрессионный анализ – стратифицирован полученным лечением. Данные оценивались в зависимости от полученной терапии.
Пациенты и методы
В анализ были включены пациенты с МКП из III фазы исследования COMPARZ (NCT00720941), спонсором которого выступила компания GlaxoSmithKline (GSK). Для участия в исследовании были отобраны пациенты в возрасте ≥18 лет с распространенным или метастатическим светлоклеточным раком почки, ранее не получавшие по этому поводу системную терапию.
Изучались данные 1110 пациентов, которые получали сунитиниб или пазопаниб в качестве препаратов первой линии и имели снимки опухоли на 42-й и 90-й день от начала курса терапии. Лечение, назначенное по протоколу, состояло из пазопаниба (800 мг 1 раз в день) или сунитиниба (50 мг 1 раз в день в течение 4 нед с последующими 2 нед без лечения).
Сокращение размеров опухоли
Снимки опухолей были сделаны во время проведения компьютерной томографии или магнитно-резонансной томографии, которые проводились каждые 6 нед до 24-й нед лечения, а затем каждые 12 нед согласно протоколу. Объективный ответ опухоли на лечение оценивался согласно критериям RECIST 1.0.
Была проведена оценка суммы наибольших диаметров опухоли в процентном соотношении для определения ранней регрессии. Критерием ответа на лечение было принято уменьшение размеров опухоли на ≥10% на 42-й и 90-й дни от начала терапии.
Результаты
В общей сложности все 1110 пациентов из исследования COMPARZ соответствовали критериям включения в анализ. Основные характеристики пациентов были хорошо сбалансированы между двумя группами терапии – пазопанибом или сунитинибом. Большинство участников были мужчины (71,5 и 75,1% соответственно), >50% из них находились в группе промежуточного риска (53,7 и 55,7% соответственно), примерно 25% – в группе благоприятного риска (25,5 и 24,8% соответственно) согласно прогностической модели категорий риска IMDC.
Аналогичное распределение наблюдалось для прогностической шкалы MSKCC. Примерно у 30% пациентов было больше чем 2 метастатически пораженных органа (33,6 и 33,1% соответственно). У большинства больных интервал от момента установления диагноза до начала системной терапии составлял <12 мес (56,6 и 55,7% соответственно). Медианная опухолевая нагрузка, представленная средней суммой диаметров поражений, была несколько ниже в группе пазопаниба (77,5 мм) по сравнению с группой сунитиниба (82 мм).
Раннее сокращение размеров опухоли на фоне терапии ингибиторами тирозинкиназы
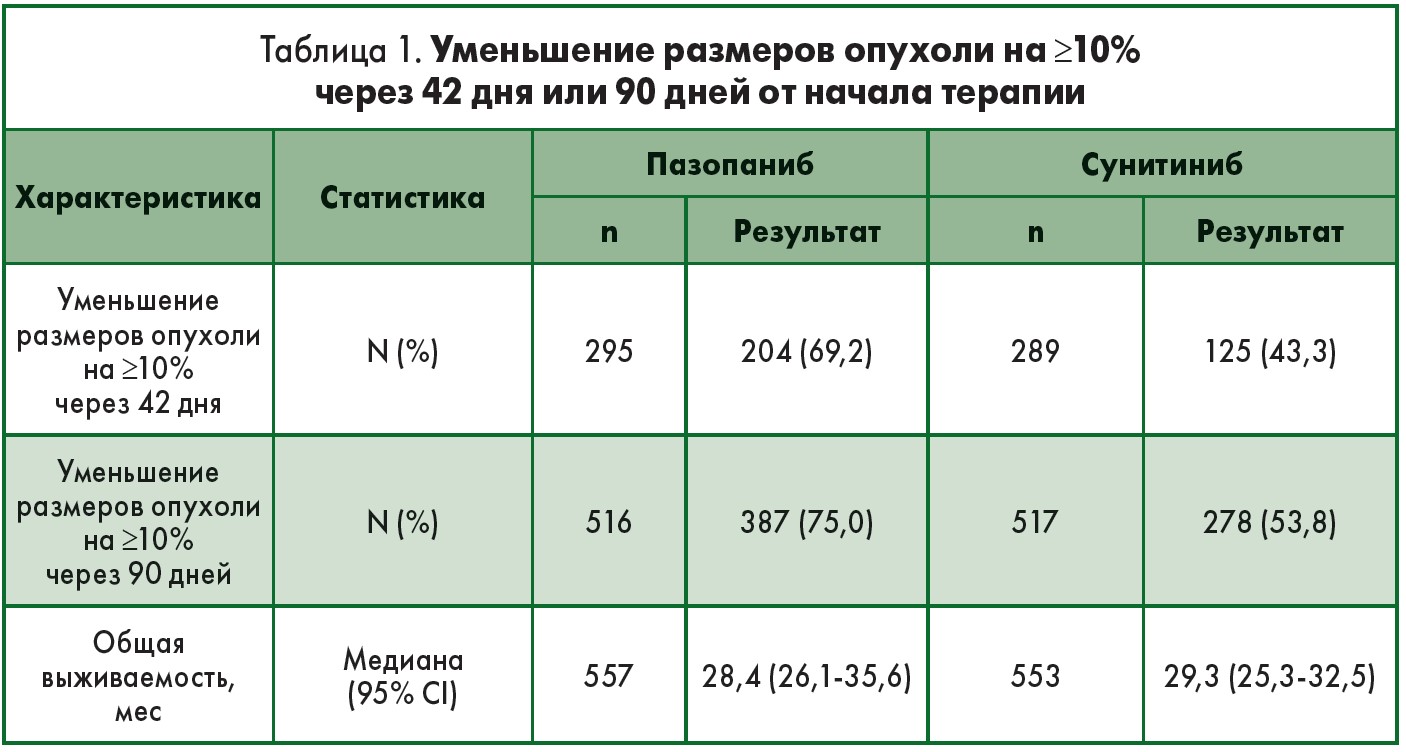
Критерий рСРО – уменьшение размеров на ≥10% через 42 дня или 90 дней от начала терапии. Выбранная точка отсечения в 10% была подтверждена согласно остаточному анализу Мартингейла.
рСРО ≥10% на 42-й и 90-й день составила 69,2 и 75,0% для пазопаниба и 43,3 и 53,8% для сунитиниба (табл. 1). Не было обнаружено связи между типом лечения и долей пациентов с рСРО как на 42-й (p=0,79), так и на 90-й день (p=0,37) от начала терапии.
Раннее сокращение размеров опухоли и клинический результат
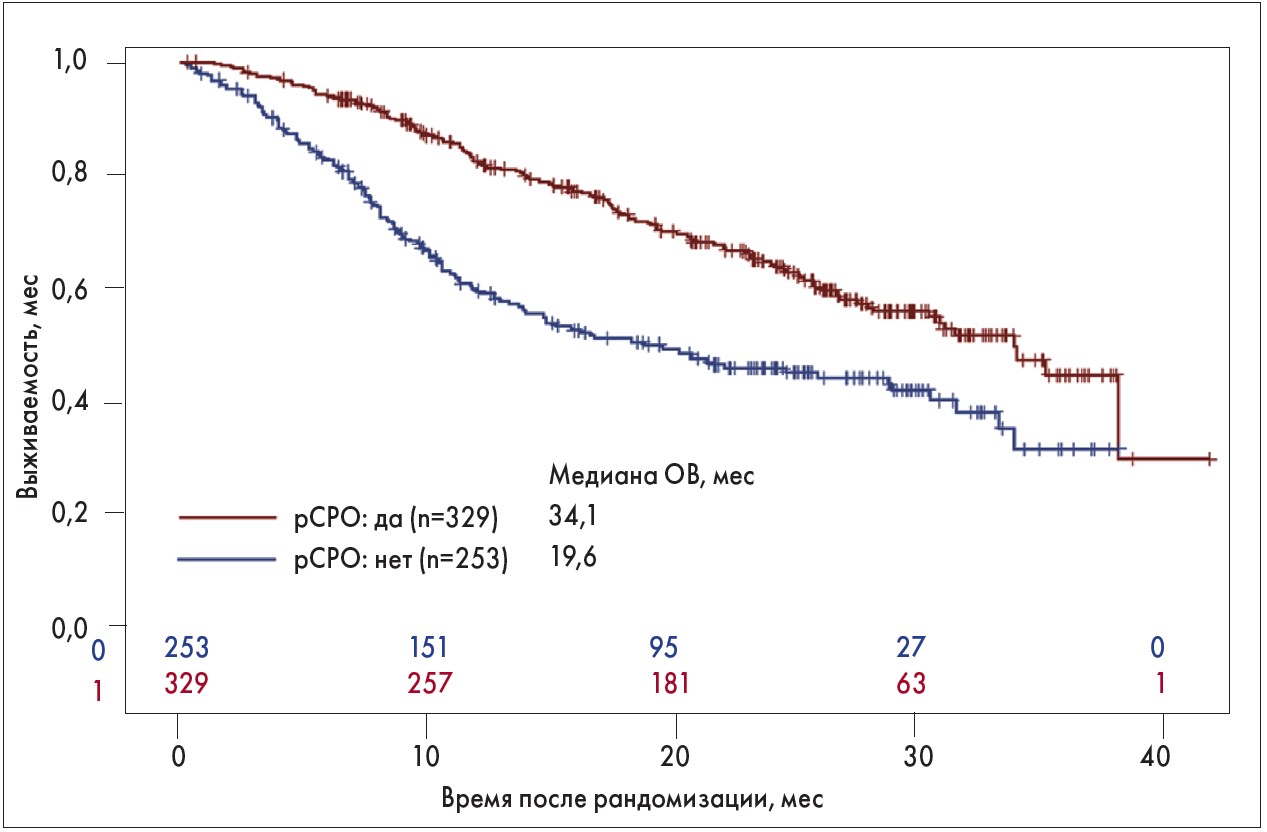
Медиана ОВ составила 34,1 и 19,6 месяца у пациентов с (n=329) и без (n=253) рСРО ≥10% на 42-й день (рис. 1). ОВ в течение года и двух лет оставалась выше у пациентов с рСРО ≥10% (82,5 и 64,7%) по сравнению с пациентами без рСРО (59,9 и 45,8%).
Рис. 1. Сравнительный анализ влияния рСРО на показатели ОВ у пациентов с ПКК в зависимости от сроков изменения размеров опухоли (рСРО на 42-й день)
Аналогичная ситуация отмечалась и при уменьшении размеров опухоли к 90-му дню наблюдения. Медиана ОВ составила 33,6 и 15,1 мес у пациентов с (n=657) и без (n=350) рСРО ≥10% на 90-й день соответственно (рис. 2). ОВ через 1 и 2 года: у пациентов с рСРО ≥10% на 90-й день – 80,8 и 62,8% соответственно, у тех, у кого не было отмечено регрессии опухоли, – 57,3 и 40,9% соответственно.
Рис. 2. Сравнительный анализ влияния рСРО на показатели ОВ у пациентов с ПКК в зависимости от сроков изменения размеров опухоли (рСРО на 90-й день)
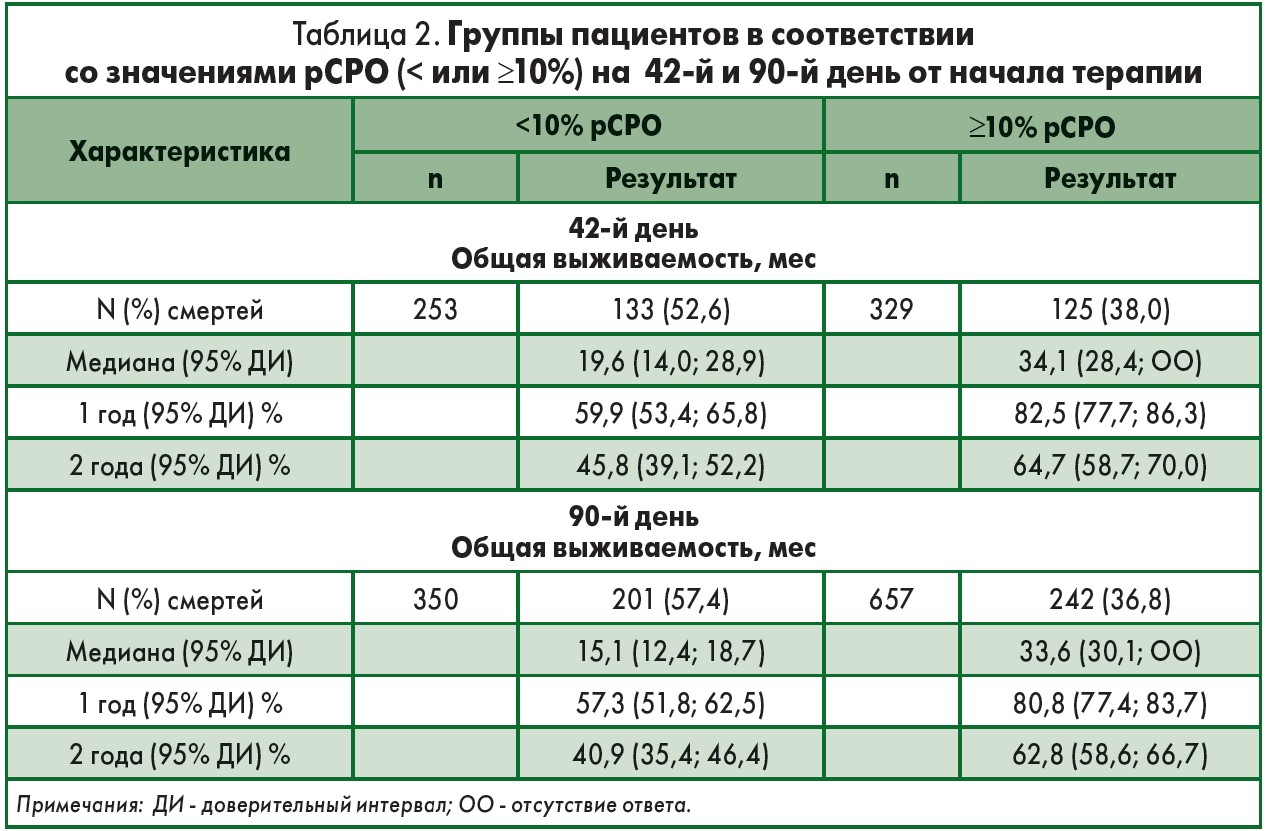
Демографические, клинические и лабораторные параметры, включая имеющие известную прогностическую ценность в отношении МКП, были включены в одно- и многофакторный анализы. Существенное значение рСРО на 42-й день по медиане ОВ было отмечено в однофакторном (ОР 0,55; 95% ДИ 0,43-0,70); p<0,001) и многофакторном анализах с применением модели пропорциональных рисков Кокса (ОР 0,53; 95% ДИ 0,41-0,69; p<0,001).
Аналогичные результаты были показаны и на 90-й день контроля (ОР 0,47; 95% ДИ 0,39-0,57; p<0,001 и ОР 0,49; 95% ДИ 0,40-0,60; p<0,001) для одно- и многофакторного анализа соответственно. В ходе исследования не было обнаружено преимущества одного лечения перед другим в улучшении ОВ (табл. 2).
А по данным многофакторного анализа, было отмечено существенное влияние на исходы заболевания таких переменных, как: пол; общее состояние; предшествующая нефрэктомия; количество метастатически пораженных органов; продолжительность лечения; уровень кальция и опухолевая н агрузка.
Обсуждение
Отсутствие прогнозирующего биомаркера в лечении МКП является основной дилеммой в выборе алгоритма лечения. Несмотря на то что до недавнего времени медикаментозная терапия назначалась до прогрессирования заболевания или непереносимости лечения с учетом сходных клинических эффектов у аналогичных групп препаратов, лишь 50% пациентов доходят до 2-й линии терапии и только 13-18% – до 3-й. Таким образом, большинство больных остаются на 1-й линии терапии.
Неизвестно, сможет ли получить пациент клиническую пользу от ранней оценки ответа на лечение, но при отсутствии благоприятного результата он своевременно может быть переведен на 2-ю линию терапии и получить шанс на хороший результат. В настоящее время проспективное исследование NIVOSWITCH (NCT02959554) немецкой междисциплинарной группы RCC (IAG-N) изучает, насколько эффективен в улучшении ОВ ранний переход (через 12 нед от начала терапии) от лечения иTK к ниволумабу.
Относительно недавно по данным II фазы проспективного клинического исследования было показано, что возможно применение интермиттирующего курса терапии сунитинибом в лечении МКП. Решение о назначении курса или его возобновлении принимается на основании уменьшения размеров опухоли или ее роста на 10% по сравнению с предыдущими образцами. Наши данные подтверждают эту концепцию, выделяя пациентов с благоприятным прогнозом в начале курса лечения и оправдывая 10% точку отсечения согласно проведенному анализу.
Интермиттирующее лечение имеет преимущества: улучшает качество жизни и снижает финансовую нагрузку как на пациента, так и в целом на систему здравоохранения. Продолжающееся исследование STAR оценивает переносимость и эффективность интермиттирующей терапии в лечении МКП, подчеркивая необходимость определения значения рСРО в качестве маркера для отбора пациентов.
Помимо предполагаемой роли интермиттирующей терапии в лечении МКП правильные критерии отбора являются ключом к консультированию больных и максимально эффективному их лечению. Однако остается открытым вопрос, смогут ли пациенты со стабилизацией заболевания получить столько клинических преимуществ и быть кандидатами на интермиттирующую терапию. В нашем предыдущем анализе отсутствие значимого уменьшения размеров опухоли при лечении с помощью иТК было связано с неблагоприятной ОВ (ОР 1,66; ДИ 95% 1,2-2,30; р=0,002). Это указывает на то, что доля пациентов со стабилизацией заболевания, согласно критериям RECIST 1,0, не демонстрирует улучшенной ОВ на фоне лечения иТК. В этом случае рСРО может стать критерием отбора в этой группе пациентов с потенциально хорошим ответом на терапию иТК.
Несмотря на то что метод раннего перевода на 2-ю линию терапии является экспериментальным, тем не менее ранние маркеры эффективности могли бы стать подходящим инструментом скрининга антиопухолевой активности. Было показано, что сокращение размеров опухоли служит независимым прогностическим маркером исходов МКП. Это указывает на ассоциацию глубокой ремиссии с лучшим прогнозом. В то же время, по данным анализа, отсутствие сокращения размеров опухоли ассоциировано с плохим результатом, что требует разработки новых, более эффективных алгоритмов лечения МКП. Например, таких как комбинация ленватиниба и эверолимуса.
рСРО спустя 6 нед от начала терапии может считаться критерием хорошего ответа и стать новым инструментом в ранней оценке эффективности лечения, дающим преимущество в отборе пациентов, которые смогут повысить ОВ. Нами была обнаружена высокая прогностическая ценность рСРО в оценке клинической эффективности на ранних этапах терапии, что коррелирует с другими наблюдениями и может быть более информативным по сравнению с ЧОО. рСРО связана с медианой ОВ 28,5 мес по сравнению с 16,0 мес для пациентов без рСРО.
Также этот критерий имеет более высокую прогностическую значимость (C-индекс 0,618; 95% ДИ 0,588-0,648) по сравнению с критериями RECIST 1.0 (C-индекс 0,597; 95% ДИ 0,566-0,627).
Чтобы дополнительно подтвердить эти выводы, мы проанализировали сравнительные данные по эффективности пазопаниба и сунитиниба из исследования COMPARZ. рСРО через 42 дня наблюдалась у 69 и 43% больных соответственно, тем самым обозначив большее количество перспективных пациентов по сравнению с обычной ЧОО (31% для пазопаниба и 25% для сунитиниба).
Не было отмечено достоверной разницы между выбором лекарственного средства и исходом заболевания. Оба препарата имели сходную клиническую активность.
Пациенты с рСРО продемонстрировали улучшение общей выживаемости (ОР 0,53; 95% ДИ 0,41-0,69; p<0,001), что сопоставимо с результатами нашего предыдущего исследования (ОР 0,615; 95% ДИ 0,568-0,677; p<0,0001). Основным различием между ними является изолированное применение только иТК в качестве 1-й линии терапии в текущем исследовании, тогда как в предыдущий анализ были включены и пациенты, принимавшие цитокины и ингибиторы мишени рапамицина млекопитающих (mTOR).
Следует отметить, что оптимальный уровень уменьшения размеров опухоли значительно варьировал между таргетными препаратами (10-12%) и цитокинами (1%), что указывает на зависимость этой конечной точки от механизма действия активного вещества. Но пока недостаточно информации, чтобы экстраполировать полученные результаты на другие иммунные препараты.
Так, использование ниволумаба было ассоциировано с лучшей ОВ, что указывает на его роль в стабилизации опухоли и сокращении ее размеров у пациентов с МКП. Пока остается открытым вопрос, имеет ли выраженность прогностическую ценность, что требует проведения дополнительных исследований.
Мы также провели оценку результатов и на 90-й день терапии, подтвердив высокую значимость этой точки. Фактически соотношение риска для ОВ на 90-й день (ОР 0,49; 95% ДИ 0,40-0,60; p<0,001) было даже лучше, чем на 42-й день, что указывает на ценность выбранной точки отсечения (уменьшение опухоли на 10%) как маркера ранней противоопухолевой активности между 42-м и 90-м днями терапии.
Основными ограничениями исследования являются его ретроспективный характер и вариабельность представленных данных. Кроме того, мы использовали критерии RECIST 1.0, которые на сегодняшний день обновлены до RECIST 1.1. Но, несмотря на внесенные изменения, RECIST 1.1 отличается лишь в нескольких пунктах от его предыдущей версии и остается весьма информативным в оценке ответа на лечение МКП.
Тем не менее, невзирая на свою простоту, оценка рСРО является основным преимуществом этого подхода ввиду своей универсальности и применимости в реальных клинических условиях.
World Journal of Urology
https://doi.org/10.1007/s00345-018-2297-4/ Springer-Verlag GmbH Germany, part of Springer Nature 2018
Реферативный пер. с англ. Ирины Чумак
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1 (12), березень 2018 р.