Прегабалін у лікуванні нейропатичного ракового болю
Практично всі онкологічні хворі відчувають біль на тому чи іншому етапі пухлинного процесу. У термінальній стадії раку біль відзначають 90-100% пацієнтів. Здебільшого раковий біль має змішаний механізм – ноцицептивний і нейропатичний, при цьому у третини пацієнтів домінує нейропатичний механізм (P. Reis-Pina et al., 2018).
Нейропатичний біль в онкології
Нейропатичний біль виникає внаслідок ушкодження або патологічних змін у сенсорному та модуляторному відділах нервової системи. Основними причинами нейропатичного болю в онкологічних пацієнтів є пухлинні ураження центральної нервової системи і периферичних нервів, ускладнення пухлинного процесу (переломи, виразки, лімфостаз та ін.), ускладнення протипухлинного лікування (фантомний біль після хірургічного втручання; променева мієлопатія; полінейропатія, індукована хіміотерапією), а також системні метаболічні порушення (неопластичні та паранеопластичні).
Пацієнти описують нейропатичний біль як «удар струмом», печіння, відчуття голок, скалок під шкірою, простріли, оніміння, «повзання мурашок», жар чи холод в кінцівках; ці прояви реєструють у половини хворих. На користь нейропатичного ракового болю свідчать локальні розлади чутливості (тактильної, больової, температурної), алодинія (біль у відповідь на небольові подразнення), гіпералгезія (підвищена чутливість до больового стимулу), гіперестезія (підвищена відповідь на тактильне подразнення), гіпестезія (випадіння тактильної чутливості), гіпалгезія (зменшення больової чутливості).
З метою оцінювання інтенсивності та характеру нейропатичного болю можна використовувати шкалу нейропатичного болю (NPS), Лідську шкалу оцінки нейропатичного болю (для заповнення лікарем – LANSS, для заповнення пацієнтом – S-LANSS), питальник нейропатичного болю (NPQ; коротка форма – NPQ-SF), діагностичний питальник нейропатичного болю (DN4), питальник painDETECT.
Нейропатичний біль – це не лише больові відчуття. Нейропатичний біль часто поєднується з тривожністю, депресією та розладами сну, які ще більше погіршують якість життя та функціональну активність пацієнтів. S.Y. Oh і співавт. (2017) у багатоцентровому дослідженні вивчали вплив нейропатичного болю на якість життя хворих онкологічного профілю. Нейропатичний раковий біль (НРБ) спостерігали у 722 з 2003 пацієнтів (36,0%), у більшості випадків (92,5%) він асоціювався з хіміотерапією. У пацієнтів з НРБ біль був більш вираженим (р<0,001), ніж у пацієнтів без НРБ. Якість життя, оцінена за питальником EQ‑5D, була значно гіршою в пацієнтів з НРБ (р=0,005). Щодо окремих доменів EQ‑5D, то НРБ асоціювався з більшою кількістю дуже тяжких проблем у доменах «біль/дискомфорт» і «тривожність/депресія» (р<0,001 та р=0,007 відповідно). Ад’ювантні аналгетики (антиконвульсанти, антидепресанти та ін.) отримували 49,6% пацієнтів з помірно тяжким і тяжким НРБ. У пацієнтів, які приймали ці препарати, НРБ менше впливав на повсякденне функціонування (р=0,041), і такі хворі мали значно кращу якість життя (р=0,043). Найбільш чітке покращення спостерігалося за доменами EQ‑5D «рухливість», «самообслуговування» та «повсякденні справи».
Прегабалін у лікуванні нейропатичного ракового болю
Механізм дії прегабаліну полягає у блокуванні α2δ-субодиниці потенціалзалежних кальцієвих каналів на мембранах нейронів у структурах центральної нервової системи, які залучені до оброблення больових сигналів із периферії, – задніх рогах спинного мозку, дорсальному шві, навколоводопровідній сірій речовині, locus coeruleus і мигдалеподібному тілі. Завдяки цьому препарат запобігає входженню в клітини іонів кальцію й вивільненню нейротрансмітерів збудження – глутамату, норадреналіну, серотоніну, дофаміну, субстанції Р. Таким чином припиняється циркуляція больового сигналу в структурах центральної нервової системи, зменшується відчуття тривоги і покращується сон.
Результати рандомізованих плацебо-контрольованих клінічних досліджень продемонстрували аналгетичну ефективність прегабаліну у пацієнтів із нейропатичним болем різного генезу, зокрема у хворих зі злоякісними новоутвореннями.
За даними M. Brasser і F. Leverkus, прегабалін достовірно зменшує інтенсивність нейропатичного болю при злоякісних новоутвореннях такою самою мірою, як і при діабетичній полінейропатії.
E. Raptis і співавт. (2014) порівнювали ефективність і безпеку прегабаліну та опіоїдного аналгетика фентанілу у формі трансдермального пластиру у пацієнтів зі злоякісними новоутвореннями різних локалізацій (рак грудної залози, легені, передміхурової залози, ендометрія, яєчника тощо). Первинної кінцевої точки – зменшення тяжкості болю за візуальною аналоговою шкалою (ВАШ) принаймні на 30% – досягли 73% пацієнтів групи прегабаліну та 37% хворих групи фентанілу. Зниження показника ВАШ принаймні на 50% при лікуванні прегабаліном і фентанілом було відзначено у 50 і 17% пацієнтів відповідно. Прегабалін також продемонстрував кращу переносимість порівняно з фентанілом: у групі прегабаліну спостерігали меншу кількість побічних явищ і більше пацієнтів повністю завершили лікування. Аналіз даних у підгрупах засвідчив перевагу прегабаліну над фентанілом незалежно від віку, статі пацієнтів і початкового показника ВАШ.
В іншому дослідженні НРБ отримано відповідь на лікування у 88% пацієнтів групи прегабаліну та у 44,2% хворих групи фентанілу (A. Vadalouca et al., 2010).
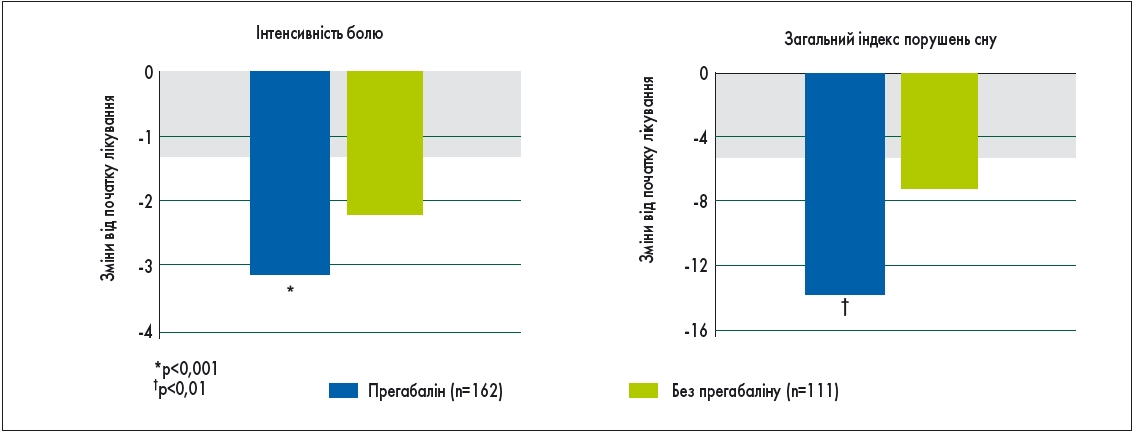
A. Manas і співавт. (2011) здійснили порівняльний аналіз результатів застосування прегабаліну і терапії без прегабаліну в рамках 8-тижневого епідеміологічного проспективного багатоцентрового дослідження у пацієнтів зі злоякісними новоутвореннями. У результаті в групі прегабаліну було констатовано значне зменшення інтенсивності болю та покращення сну (рис.). Крім того, завдяки анксіолітичному ефекту прегабаліну лікування цим препаратом дозволило майже вдвічі зменшити застосування бензодіазепінів.
Рис. Вплив прегабаліну на біль і розлади сну в пацієнтів з раковим нейропатичним болем (адаптовано з A. Manas et al., 2011)
K.-F. Sjolund і співавт. (2013) вивчали ефективність і безпеку прегабаліну у лікуванні ракового болю в кістках. У дослідженні 152 дорослих пацієнти з кістковими метастазами рандомізували для прийому прегабаліну в індивідуально підібраній дозі (100-600 мг/добу) або плацебо додатково до опіоїдних аналгетиків. Прегабалін значно ефективніше за плацебо зменшував біль і покращував сон.
Г.Р. Абузарова і Б.М. Прохоров (2008) продемострували, що в пацієнтів з НРБ прегабалін значно зменшує інтенсивність болю вже на 3-й день лікування з подальшим посиленням знеболювального ефекту на 7 і 14-й день.
У настановах Міжнародної асоціації з вивчення болю (IASP, 2010), Європейської федерації неврологічних товариств (EFNS, 2010), Американської академії неврології (AAN, 2011), інших національних і міжнародних організацій (CPS, 2014; CREST, 2008; SFETD, 2014 та ін.) прегабалін рекомендується як препарат першої лінії терапії нейропатичного болю.
Європейське товариство клінічної онкології (ESMO) рекомендує застосовувати прегабалін для лікування пацієнтів з НРБ (L. Jost, F. Roila, 2008).
За рекомендаціями Національної онкологічної мережі США (NCCN, 2018), при лікуванні НРБ початкова доза прегабаліну має становити 25 мг на ніч з наступним підвищенням частоти прийому до 2-3 разів на день. Дозу підвищують на 50-100% через кожні 3 дні до досягнення максимальної добової дози 600 мг. У пацієнтів похилого віку та/або з тяжким загальним станом дозу слід підвищувати повільніше.
Таким чином, прегабалін продемонстрував високу ефективність у лікуванні нейропатичного больового синдрому в хворих онкологічного профілю на всіх «сходинках» ВООЗ. Перевагами прегабаліну є високий профіль безпеки, швидкий початок дії, лінійна фармакокінетика та чіткий дозозалежний ефект, відсутність значущих фармакокінетичних взаємодій лікарських засобів. У пацієнтів з НРБ прегабалін забезпечує швидке (на 3-7-й день) і стійке полегшення больового синдрому, зменшення тривожності та покращення сну. Застосування прегабаліну дозволяє відмовитись від раннього призначення сильних опіоїдів або зменшити їх дозу та отримати стабільну аналгезію протягом тривалого часу.
Основні принципи медикаментозного лікування болю в онкологічних хворих (Всесвітня організація охорони здоров’я, 1986, 1996)
- Послідовне застосування аналгетиків різних груп – від ненаркотичних і нестероїдних протизапальних препаратів до слабких і сильних опіоїдів – відповідно до «сходів ВООЗ»; перехід на наступну «сходинку» здійснюється у разі недостатнього ефекту застосованого препарату в максимальній переносимій дозі та/або розвитку побічних ефектів.
- Індивідуальний підбір доз аналгетиків, моніторинг ефективності та безпеки лікування.
- Регулярний прийом/введення аналгетика з метою запобігання виникненню болю; застосування аналгетика «на вимогу» потребує значно вищих доз лікарських засобів і чинить негативний психологічний вплив.
- Активне застосування ад’ювантних аналгетиків (антиконвульсантів, антидепресантів та ін.) на будь-якій «сходинці» знеболення з урахуванням патофізіології болю (ноцицептивний або нейропатичний) і його локалізації (вісцеральний або кістково-суглобовий).
- Пріоритетне застосування неінвазивних форм лікарських засобів; перевагу слід надавати пероральному шляху введення як найбільш ефективному, простому, зручному і найменш болючому для більшості пацієнтів.
Підготував Олексій Терещенко
Тематичний номер «Онкологія» № 3 (54), червень-липень 2018 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...