Туберозный склероз как причина нейропсихических расстройств

Туберозный склероз, или туберозно-склерозный комплекс (TSC), связан с широким спектром поведенческих, психических, интеллектуальных, нейропсихологических и психосоциальных проблем, которые часто недооцениваются врачами в плане диагностики и лечения.
В этой статье представлены обновленные клинические данные касательно TSC-ассоциированных нервно-психических расстройств (TAND), которые могут быть использованы для усовершенствования скрининга, диагностики и лечения болезни на практике. Обзор предназначен для клинических генетиков, консультантов по генетике, педиатров и врачей общего профиля, которые участвуют в диагностике и лечении детей, подростков и взрослых с TSC и связанными с ним расстройствами.
 |
 |
| Инструкция для медицинского применения |
Туберозно-склерозный комплекс – это мультисистемное генетическое заболевание, ассоциированное с широким спектром патологических проявлений, поражением головного мозга, кожи, почек, глаз и легких (Curatolo, Moavero, de Vries, 2015; Henske, Jozwiak, Kingswood, Sampson, Thiele, 2016). Симптомы TSC имеют возрастзависимый характер и появляются в определенный период жизни человека (Curatolo, Bombardieri, Jozwiak, 2008). Основными мишенями болезни являются головной мозг, кожа и почки, которые поражаются у 80‑90% больных. Помимо патологических изменений в органах, у 90% пациентов с TSC возникают разного рода нейропсихические расстройства (Curatolo et al., 2015; de Vries et al., 2015). Эти проявления также имеют возрастзависимый характер и возникают на разных этапах развития болезни (de Vries, 2010a; de Vries et al., 2005; de Vries et al., 2015). Неврологические и нейропсихические симптомы являются наиболее тяжелыми для пациента с TSC (Curatolo et al., 2015; Hallett, Foster, Liu, Blieden, Valentim, 2011; Rentz et al., 2015). Несмотря на значительный прогресс в плане диагностики и лечения многих физических проявлений болезни, в том числе и субэпидермальной гигантоклеточной астроцитомы (SEGA), ангиомиолипомы (AML) и эпилепсии, психоневрологические расстройства остаются недостаточно изученными (Kingswood et al., 2017).
Концепция и уровни TAND
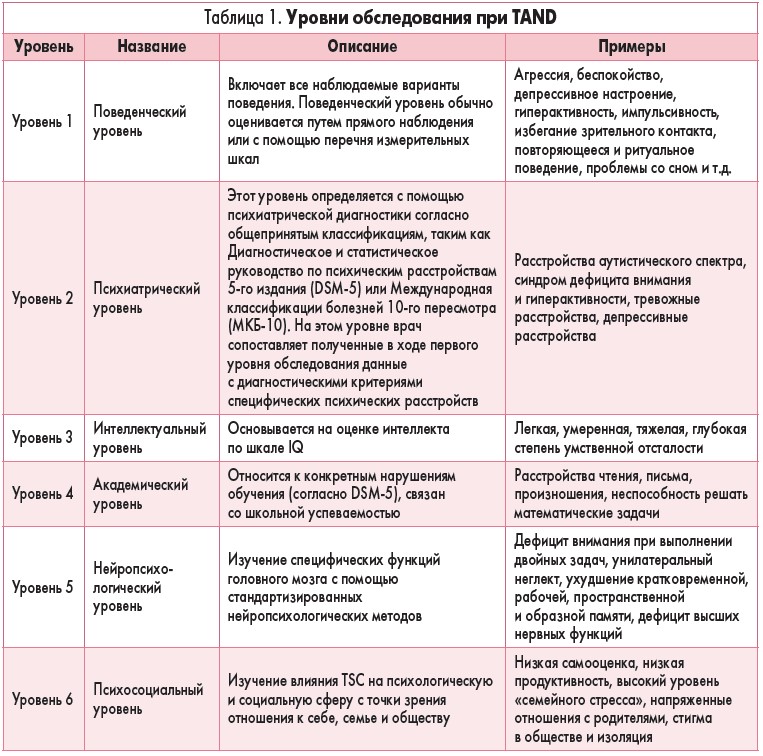
В рамках Международной консенсусной конференции по вопросам TSC (International TSC Consensus Conference) в 2012 г., целью которой являлся пересмотр диагностических критериев TSC (Northrup et al., 2013), а также рекомендаций касательно ведения и наблюдения за такими пациентами (Krueger et al., 2013), рабочая группа нейропсихиатров ввела новый термин – TAND, обозначающий весь спектр психомоторных, поведенческих, психиатрических и психосоциальных расстройств, ассоциированных с TSC (de Vries et al., 2015; Krueger et al., 2013). Рабочая группа также отметила, что такая сложная патология, как TSC, требует многопрофильного (когда в лечебном процессе участвуют специалисты по психотерапии, логопедии, трудотерапии и др.), мультидисциплинарного (привлечение медиков, педагогов, социальных работников) подходов, а также сотрудничества с юридическими и неюридическими организациями. Специалисты всех этих направлений раньше использовали различные термины для оценки одних и тех же аспектов развития патологии, состояния психического здоровья и психосоциальных потребностей. С целью оптимизации междисциплинарного сотрудничества был разработан 6-уровневый алгоритм обследования пациентов для специалистов, участвующих в ведении пациентов с TSC. Названия этих уровней и краткое изложение каждого из них представлены в таблице 1. Учитывая то, что для TAND характерна возрастная зависимость, как и для других физических симптомов TSC, согласно рекомендациям Международного консенсуса, пациенты с TSC должны проходить скрининговое обследование на TAND не реже 1 раза в год (Krueger et al., 2013). Нейропсихиатрическая комиссия определила скрининг как важное исследование для любых очевидных или возникающих TAND, которые могут потребовать комплексного обследования или лечения. В качестве поддержки ежегодного скрининга был разработан и апробирован контрольный список TAND – TAND Checklist (Le Clezio, Jansen, Whittemore, de Vries, 2015). Контрольный список TAND – это простой способ, который с помощью ручки и листа бумаги помогает клиницисту вести беседу с больным и его родственниками. Он подходит для пациентов любого возраста, с любой тяжестью болезни и предназначен для всех уровней обследования. Контрольный список состоит из серии вопросов, на которые в основном предлагаются два варианта ответа – «Да/Нет». За последние несколько лет контрольный список TAND переведен на испанский, немецкий, шведский, голландский, итальянский, польский и каталанский язык.
Последовательно мы обобщим текущие данные для каждого уровня обследования при TAND, включая основные рекомендации для дальнейшей оценки и интервенции.
Поведенческий уровень
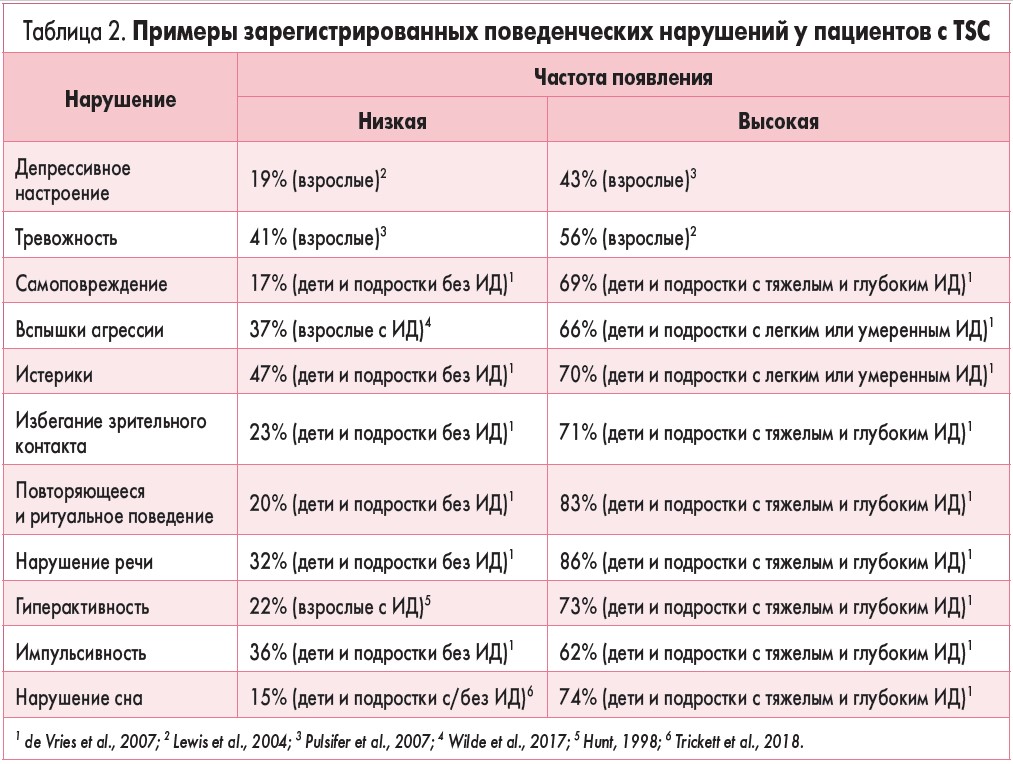
Поведенческий уровень TAND включает поведение, которое само по себе не является психическим расстройством, но вызывает беспокойство у пациента, его родственников и специалистов. Оно часто становится причиной для направления больного с TSC для психологического или психиатрического обследования. Согласно данным Регистра TSC для повышения осведомленности о болезни (TuberOus SClerosis registry to increase disease Awareness, TOSCA), 36% пациентов с TSC сообщают по крайней мере об одном случае поведенческого нарушения. Наиболее частыми расстройствами являются гиперактивность, импульсивность, нарушение сна (встречается у 20% больных). Среди других поведенческих нарушений у 11-14% пациентов возникали тревожность, перепады настроения, агрессия, у 6-8% больных были отмечены депрессивное настроение, самоповреждение, навязчивое поведение (Kingswood et al., 2017). Другие исследования показывают более высокую распространенность поведенческих нарушений, чем TOSCA, в котором представлены данные пациентов разного возраста и интеллектуального развития. Известно также, что возраст и интеллектуальные способности влияют на поведенческие реакции, поэтому эти расстройства зачастую проявляются у лиц с интеллектуальным дефицитом (ИД) и у детей (de Vries, Hunt, Bolton, 2007; Wilde et al., 2017). В таблице 2 проиллюстрирована корреляция между разными поведенческими расстройствами, уровнем интеллекта и возрастом.
Наивысшие показатели поведенческих расстройств наблюдаются у детей и подростков с ИД (у 2/3 пациентов этой категории наблюдают самоповреждение, вспышки агрессии и/или гнева). Частота самоповреждения гораздо ниже у детей и подростков без ИД или у взрослых пациентов с ИД. Поэтому дети с ИД имеют больший риск развития неблагоприятных последствий в результате поведенческих расстройств.
Учитывая сильную связь между расстройствами аутистического спектра (autism spectrum disorder, ASD) и TSC, описано много случаев социальной дезадаптации таких пациентов, что особенно ярко проявляется у детей и подростков с нарушениями интеллекта. Но даже при отсутствии ИД частота поведенческих нарушений у больных TSC в 10 раз выше, чем в общей популяции.
Гиперактивность и импульсивность следует рассматривать в контексте психиатрического диагноза – синдрома дефицита внимания с гиперактивностью (ADHD), а не в аспекте поведенческого нарушения. Представленные данные демонстрируют, что у детей и подростков ADHD зависит от наличия или отсутствия ИД, и с возрастом выраженность синдрома может уменьшаться.
Каждый пациент с TSC может иметь разные проявления TAND, которые становятся причиной дисгармонии в семейных отношениях и затрудняют лечение. Определение кластеров поведенческих нарушений TAND может помочь решить эту проблему.
Психиатрический уровень
Психиатрический уровень TAND включает разные проявления, которые могут возникнуть у больных с TSC (ASD или ADHD), чаще в детском возрасте, а также тревожные и депрессивные расстройства в юношестве и зрелости.
Нарушение развития нервной системы
Расстройства аутистического спектра. TSC является результатом мутации гена, с которым может быть связано возникновение ASD. В ряде исследований приводятся различные данные касательно распространенности ASD среди пациентов с TSC, которая в среднем составляет 40‑50% (Curatolo et al., 2015). К факторам риска развития ASD относят мутацию TSC-гена, структурные аномалии головного мозга и эпилепсию. Что касается ASD на фоне TSC, то такое сочетание чаще наблюдается при мутации гена TSC2.
Мутация одного из двух генов TSC приводит к внутриутробной активации гена mTOR (mammalian target of rapamycin), повышая риск развития как ASD, так и эпилепсии вследствие нарушения синаптогенеза, ГАМК-глутаматного баланса и других предполагаемых внутриклеточных аберраций (Curatolo et al., 2016). Кроме того, ранняя манифестация и высокая частота припадков, наличие патологических изменений (особенно в височных долях) при проведении эхоэнцефалографии (ЭЭГ) являются дополнительными факторами риска развития ASD (Bolton et al., 2002; Numis et al., 2011). Результаты недавних исследований показали, что нарушения нейронных связей в зонах, отвечающих за ASD (поясная извилина), наблюдаются у пациентов с ранней манифестацией припадков (Moavero et al., 2016). В таких ситуациях раннее начало противоэпилептической терапии существенно уменьшает риск наступления отдаленных последствий. В противном случае длительный временной промежуток между первыми припадками и началом терапии ассоциирован с более высоким риском развития ASD (Cusmai et al., 2011).
Первые признаки аутизма могут проявляться в возрасте до 1 года: изменение поведения ребенка во время игры, нарушение социального взаимодействия, избегание зрительного контакта (Jeste et al., 2008). С 2 лет наблюдаются разного характера поведенческие расстройства: гиперактивность, повторяющиеся и ритуальные формы поведения, приступы гнева (Jeste et al., 2008). Дети с TSC и ASD обычно имеют более низкие интеллектуальные способности в сравнении с детьми с TSC без ASD.
Синдром дефицита внимания с гиперактивностью. Распространенность ADHD среди пациентов с TSC составляет 30-50% (de Vries et al., 2007), что в 10 раз выше, чем в общей популяции (de Vries, 2010a). Пока до конца не известен патогенез возникновения ADHD при TSC, но было предложено несколько возможных причин, способствующих развитию этого варианта нарушения, например лобная эпилепсия и/или патологические изменения на ЭЭГ, особенно при наличии структурных изменений лобной доли головного мозга на фоне мутации гена TSC2 (D’Agati, Moavero, Cerminara, Curatolo, 2009; Muzykewicz et al., 2007). Локус, отвечающий за склонность к ADHD, расположен в 16p13 хромосоме, в которой также есть ген TSC2, кодирующий NMDA-рецепторы 2A и аномальную глутаматергическую передачу – они могут быть решающими факторами в развитии ADHD (Carrey, MacMaster, Gaudet, Schmidt, 2007; Ogdie et al., 2004; Turic et al., 2004). Остается также неизвестным, существует ли взаимосвязь между ASD и ADHD, вызванной мутацией гена TSC2, с ИД, и могут ли эти расстройства возникать независимо друг от друга.
Тревога и депрессивные расстройства
Несмотря на высокую частоту тревоги и депрессивных симптомов на поведенческом уровне у пациентов с TSC, данных о тревожных и депрессивных расстройствах в аспекте психиатрического уровня очень мало. В ходе обследования пациентов с TSC высокий уровень тревожности (56%) показывали взрослые пациенты с нормальным интеллектом, но никто из них не был достаточно обследован и, соответственно, не получал терапию (Lewis et al., 2004). В процессе систематического наблюдения выявлена высокая частота тревожных расстройств, соответствующих критериям МКБ‑10. Результаты ретроспективного исследования продемонстрировали, что при психиатрическом осмотре у 28% больных было выявлено тревожное расстройство, у 27% – депрессивное расстройство (Muzykewicz et al., 2007). В работах Lewis не обнаружено связи между возникновением тревожных и депрессивных расстройств и мутацией генов TSC1 и TSC2, но данные Muzykewicz показывают значимую корреляцию с TSC2-статусом. Следовательно, этот вопрос требует дальнейшего изучения.
Другие психические расстройства
Касательно других психических расстройств у пациентов с TSC собрано мало статистических данных. Психические болезни (в том числе шизофрения) у больных с TSC периодически регистрируются с низкой частотой, которая совпадает с таковой в общей популяции.
Интеллектуальный уровень
Пациенты с TSC демонстрируют разные интеллектуальные возможности. У 40-50% больных уровень IQ находится в нормальном диапазоне и в среднем составляет 93,6 (Joinson et al., 2003). Этот показатель на 12 пунктов ниже, чем средний уровень IQ у сестер и братьев пациентов без TSC (105,6).
Сегодня изучен ряд факторов, которые коррелируют с умственным развитием пациентов с TSC: большое количество опухолевых узлов, ранняя манифестация эпилептических приступов, инфантильные спазмы, недостаточный контроль над припадками, применение большого количества противоэпилептических средств, отражающее плохой контроль над приступами. Вероятно, существует также дозозависимая связь между эпилептической активностью и уровнем умственного развития. У детей с начальным средним уровнем IQ 92 в результате воздействия инфантильных спазмов менее 1 мес IQ снизился до показателя 72, больше 1 мес – до 63 (Humphrey et al., 2014). Наличие мутации гена TSC2 также ассоциировано с повышенным риском возникновения ИД (Dabora et al., 2001; Jansen et al., 2008; Jones et al., 1997; Kothare et al., 2014; Sancak et al., 2005).
С целью изучения корреляции между генотипом и интеллектуальным фенотипом было проведено исследование, в котором оценивались интеллектуальные способности 100 пациентов с известными TSC-мутациями с помощью стандартизованных шкал. У большинства лиц с мутацией TSC1 обнаружен нормальный уровень интеллекта, при этом 10% исследуемых показали глубокую степень ИД. Пациенты с мутацией TSC2 показали худшие результаты: у 34% исследуемых выявлен глубокий ИД (Wong et al., 2015).
Была изучена динамика умственного развития у больных с TSC на протяжении длительного времени. Обнаружено, что у большинства пациентов IQ практически не менялся (среднее снижение – 2 единицы), но у 9 из 66 исследуемых было отмечено улучшение интеллектуальных показателей, а у 11 из 66 – значительное ухудшение. Вместе с тем со временем наблюдается снижение адаптивных возможностей или практических жизненных навыков. Эта тенденция касается не потери уже имеющихся навыков, а, скорее, неспособности приобретать новые. Поэтому младенчество является критическим периодом, когда судороги могут крайне неблагоприятно воздействовать на формирование головного мозга (van Eeghen, Chu-Shore et al., 2012).
Следует отметить, что у лиц с ИД чаще наблюдаются поведенческие нарушения (АSD, ADHD, но не депрессивное настроение и тревожные расстройства), самоповреждение в сравнении с пациентами с нормальным уровнем интеллекта.
Академический уровень
Даже на фоне нормальных интеллектуальных способностей у детей с TSC часто наблюдаются разного рода академические трудности. Согласно современной терминологии DSM‑5 это нарушение идентифицируется как «специфические расстройства способности к обучению». У детей с TSC часто наблюдается дискалькулия, также имеет место нарушение чтения, письма. Наиболее часто проблемы с решением математических задач наблюдаются у детей с TSC и ADHD (de Vries, 2010a). Дети, имеющие разные академические трудности, подвержены высокому риску возникновения целого ряда вторичных проблем, таких как отказ от посещения школы, тревога, связанная с учебным заведением, недостаток социальных навыков, низкая самооценка.
При проведении опроса >2000 школьников 57,8% респондентов сообщили о трудностях в обучении, и только остальным (48,9%) была проведена официальная оценка этого расстройства (Kingswood et al., 2017). Сложившаяся ситуация обусловливает необходимость в совершенствовании образовательных систем и систематической оценке способности к обучению школьников с TSC даже при нормальном уровне интеллекта.
Нейропсихологический уровень
Пациенты с TSC даже при нормальном уровне интеллекта подвержены высокому риску возникновения нейропсихологических расстройств. Результаты недавнего исследования, проведенного TOSCA, показали, что из 510 пациентов 55% демонстрировали низкий уровень психоневрологических навыков, что указывает на специфический нейропсихологический дефицит (Kingswood et al., 2017).
Дефицит внимания
Постоянный дефицит внимания отмечается как у детей, так и у взрослых. Его выявляли при выполнении пациентами двойных задач, например визуального поиска при прослушивании звукового сигнала (de Vries et al., 2009; Tierney et al., 2011). Важно отметить, что дефицит внимания коррелирует с практическими трудностями в реализации жизненных навыков, низкой академической успеваемостью и возникновением чувства подавленности. Поэтому важно учитывать, что люди с TSC склонны к высокому риску развития нейропсихологического дефицита внимания, а не только расстройств внимания на поведенческом уровне.
Дефицит памяти
Помимо проблем с вниманием, у пациентов с TSC часто отмечается дефицит памяти вне зависимости от интеллектуальных способностей. Ridler и соавт. (2007) у взрослых с TSC обнаруживали нарушение вспоминания (при сохранении узнавания), а также дефицит вербальной и пространственной памяти.
Дефицит высших нервных функций
У взрослых пациентов с TSC наблюдаются проблемы с планированием, самоконтролем, когнитивной гибкостью и целенаправленными действиями. Prather и de Vries (2004) отметили, что у пациентов с TSC наиболее сильно повреждаются фронтальные зоны головного мозга, приводя к неспособности выполнения регулярных и целенаправленных действий. Этот вариант расстройств сопровождается негативными последствиями для человека в виде дезориентации в реальных жизненных ситуациях, также их довольно сложно идентифицировать в сравнении с ИД.
Психосоциальный уровень и влияние TAND
Учитывая пожизненность физических и нейропсихических проявлений TSC, болезнь оказывает существенное влияние на психосоциальное состояние больного, его семьи и общества. Сегодня доступно очень мало исследований относительно качества жизни таких пациентов и их семей, а также финансовой нагрузки и тяжести ухода, ложащегося на плечи опекунов.
Текущие результаты и перспективные направления
Ввиду разнообразия проявлений TAND у пациентов с TSC большой интерес представляет их четкая систематизация и сокращение этого перечня. Сегодня удалось все уникальные варианты TAND изобразить в виде шести кластеров (уровней). Создание 6-уровневой схемы TAND в ближайшие годы может стать очень полезным для клиницистов в плане скрининга, диагностики и лечения большинства TAND.
Растет интерес к потенциалу ингибиторов mTOR в лечении TAND. Кроме косвенных путей активации mTOR на фоне TAND, представленных в этом обзоре (например, через структурные изменения головного мозга, судороги), существует способ прямой активации mTOR при TAND (de Vries, 2010b; de Vries, Howe, 2007). Обнадеживающие результаты исследований на мышах демонстрируют, что на фоне применения ингибиторов mTOR может наблюдаться регрессия или уменьшение проявлений TAND. Данных о применении такого лечения у пациентов очень мало. В рамках исследования TESSTALL на фоне лечения ингибиторами mTOR у пациентов с TAND отмечалось улучшение памяти и когнитивных навыков (Davies et al., 2011; de Vries, 2010b).
В настоящее время пока нет данных, подтверждающих использование ингибиторов mTOR в качестве основного лечения при TAND, но применение этих препаратов может способствовать уменьшению интенсивности проявлений TAND и улучшению качества жизни таких пациентов за счет косвенного влияния. Например, эти лекарства уже разрешены к применению в Соединенных Штатах и Европе при SEGA, AML или эпилепсии (Bissler et al., 2013; Franz et al., 2013; French et al., 2016).
Заключение
TSC ассоциирован со многими физическими и психоневрологическими нарушениями. В этой статье изложена обновленная и актуальная информация о разных уровнях TAND. Обобщая приведенные выше данные, можно сказать, что TAND представляет собой распространенные и стойкие нарушения, возникающие у пациентов с TSC, которые зачастую не идентифицируются и не подлежат терапии. Проведение скрининга с помощью контрольного списка TAND может стать простым и эффективным методом удовлетворения потребностей пациентов и их родственников.
Список литературы находится в редакции.
Статья печатается в сокращении.
de Vries P.J., Wilde L., de Vries M.C., Moavero R., Pearson D.A., Curatolo P. A clinical update on tuberous sclerosis complex-associated neuropsychiatric disorders (TAND). Am J Med Genet Part C. 2018;178C:309-320.
https://doi.org/10.1002/ajmg.c.31637.
Перевела с англ. Илона Цюпа
Тематичний номер «Педіатрія» №1 (48), березень 2019 р.