Эффективность препаратов прогестерона в лечении угрожающего выкидыша
Самопроизвольный аборт является распространенным осложнением беременности, которое встречается в 15-20% случаев всех клинически подтвержденных беременностей [1] и может сопровождаться серьезными физическими и психологическими последствиями. Как правило, половина беременностей с угрозой аборта заканчиваются выкидышем, что оказывает большое психологическое влияние на женщин и их семьи [2]. В качестве стандартного препарата при лечении угрозы невынашивания в течение многих лет использовался прогестерон [4].
Угроза прерывания беременности манифестирует вагинальным кровотечением с абдоминальной болью или без нее при наличии закрытой шейки матки и жизнеспособного плода внутри полости матки. В физиологических исследованиях было показано, что прогестерон играет важную роль в процессах репродукции – начиная с предимплантационного этапа и в течение всей беременности: способствует трансформации и децидуализации эндометрия, регулирует инвазию ворсин трофобласта, контролирует сократительную активность матки, защищает полуаллогенный плод от иммунной системы матери и т. д. [3]. Поэтому прогестерон использовался в качестве стандартного лечения при угрозе невынашивания в течение последних десятилетий [4].
Эффективность прогестерона в лечении угрожающего аборта изучалась в ходе многочисленных клинических исследований, однако результаты их были неоднозначными. Такая ситуация существенно влияет на выбор тактики лечения пациенток с угрозой выкидыша, что в результате может привести к необратимым последствиям. Лучшее понимание этой проблемы может иметь важное значение для системы здравоохранения в целом и клинических исходов, поскольку терапия прогестероном позволила бы снизить количество потерь беременности при лечении угрожающих выкидышей.
С учетом недавно появившихся доказательств нашей целью было оценить эффективность прогестерона при угрозе прерывания беременности путем проведения метаанализа рандомизированных контролируемых исследований (РКИ).
Методы
Методы отбора статей, аналитических данных, отчетов по результатам метаанализов были первоначально определены на основании положений, указанных в рекомендациях «Предпочтительные пункты отчетности для систематических обзоров и метаанализов» (PRISMA) [5].
Метаанализ был проведен двумя исследователями (X.-x. Wang и Q. Luo) в соответствии с протоколом, рекомендованным для систематических обзоров [5]. Мы провели систематический поиск в базах данных PubMed, Embase, Кокрановской библиотеки и Web of Science, используя комбинацию из Медицинской предметной рубрики терминов, заголовков или абстрактов, в соответствии со следующими поисковыми запросами: «аборт, угроза», «аборты, угроза», «угрожающий аборт», «угрожающие аборты», «осложнения беременности», «аборт спонтанный», «аборт», «выкидыш», «прогестерон», «прегнандиол», «17-ОНРС», «17α-гидроксипрогестерона капроат», «17р», «17α-гидроксипрогестерон» и «гестагены» – с января 1980-го по июнь 2017 года. Во избежание упущений дополнительно использовали поиск вручную в перечне всех статей и более ранних обзоров по данной тематике.
В процессе отбора публикаций руководствовались следующими критериями включения:
(i) – РКИ, оценивающие эффективность прогестерона в лечении угрозы выкидыша в сравнении с плацебо или отсутствием лечения;
(ii) – беременные женщины, перенесшие угрозу выкидыша и симптомы угрожающего аборта, в зависимости от дизайна исследования и сроком гестации меньше 28 недель;
(iii) – без ограничений относительно типа прогестерона, включая микронизированный прогестерон и синтезированные гестагены, без учета пути введения, длительности и дозы (исключая профилактический прием прогестерона при привычном невынашивании или проведении ЭКО);
(iv) – первичным исходом был выкидыш, вторичным – преждевременные роды, уменьшение боли и другие задокументированные результаты;
(v) – не было языковых или географических ограничений.
Два автора (X.-x. Wang и Q. Luo) независимо друг от друга отобрали исследования, соответствующие критериям включения. Возникшие разногласия в выборе исследований были разрешены путем консенсуса и, при необходимости, привлечения третьего лица. Оригинальные данные из каждого выбранного исследования были сгруппированы в таблицы, включая исходные характеристики пациенток (возраст, регион проживания, период наблюдения, срок гестации, наличие выкидыша в прошлом и их количество в каждой группе) и общую информацию об использовании прогестерона, включая дозу, тип и путь введения.
Перед извлечением данных первичный исход был определен как случай самопроизвольного аборта, установленный автором исследования. Если в исследовании фиксировали осложнения беременности, исход беременности, состояние новорожденного и другие особые случаи, их также включали в таблицу анализа данных.
Мы оценивали качество исследований, используя Кокрановское руководство для систематических обзоров и вмешательств [6]. Для оценки риска системных ошибок были проанализированы семь доменов, включая генерацию случайной последовательности, скрытое распределение, ослепление исследования (в отношении участников и персонала), ослепление оценки исходов, неполные данные по исходам, избирательное информирование и другие отклонения [5].
Анализ данных проведен с использованием программ STATA 12.0 и Менеджер ревью 5.3 (Северный Кокрановский центр, Кокрановское сообщество, 2014) [6]. В связи с включением РКИ были использованы анализ модели случайных эффектов и статистический метод Мантеля – Хенцеля. Статистическая гетерогенность между исследованиями оценивалась путем определения I2 (Higgins JPT., 2011). Сводные данные были представлены как относительный риск (ОР) с 95% доверительным интервалом (ДИ). Статистически значимым считалось значение Р<0,05. Отчет по метаанализу был представлен в соответствии с положениями PRISMA [5].
Результаты
В соответствии с заданными поисковыми запросами в общей сложности было найдено 1113 исследований, в том числе 286 дублирующихся. При прочтении названия и реферата статьи были предварительно отобраны 18 источников [2, 4, 7-22]. При детальном изучении полного текста 10 исследований были исключены [7-11, 13, 16, 17, 20, 21]. Для окончательного анализа были выбраны восемь рандомизированных исследований, включающих 845 беременных женщин с угрозой выкидыша [2, 4, 12, 14, 15, 18, 19, 22].
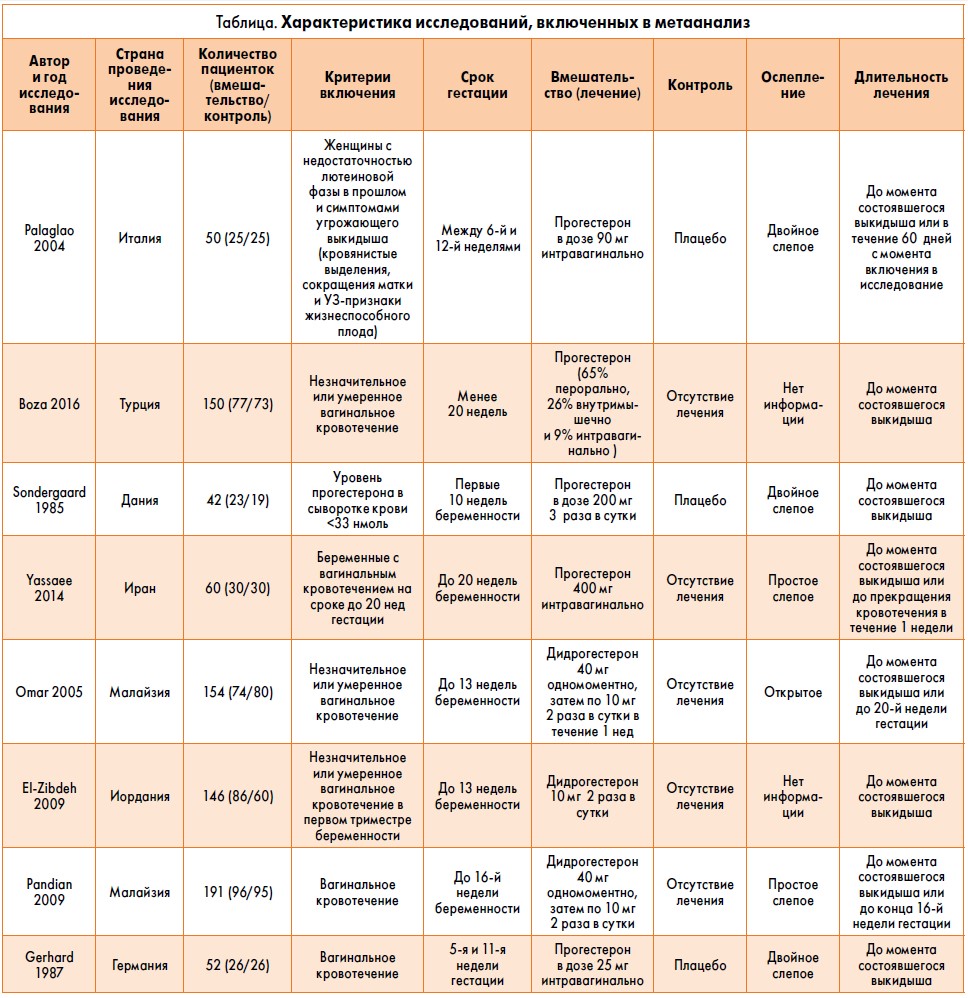
Характеристика исследований
В таблице представлены данные по включению, исключению и проводимым вмешательствам для каждого анализируемого исследования, а также исходные данные беременных женщин, включенных в исследование. Участницы четырех исследований получали лечение микронизированным прогестероном [2, 15, 18, 19]. В трех исследованиях беременным назначали дидрогестерон [4, 14]. В одном исследовании пациентки получали дидрогестерон и микронизированный прогестерон [22]. В двух исследованиях препарат применялся интравагинально [2, 18], в пяти – перорально [2, 4, 12, 14, 19] и в одном – перорально и интравагинально [22].
Результаты трех РКИ были опубликованы в Европейском регионе [15, 18, 19] и пяти РКИ – в Азиатском [2, 4, 14, 22]. Из восьми исследований три были двойными слепыми [15, 18, 19], два – простыми слепыми [2, 4,], одно было открытым [14] и в двух не было информации касательно ослепления [12, 22]. Три исследования включали плацебо-контролируемое лечение [15, 18, 19], а в пяти исследованиях лечение не проводилось [2, 4, 12, 14, 22].
Синтез результатов
Эффективность прогестерона в лечении угрожающего выкидыша
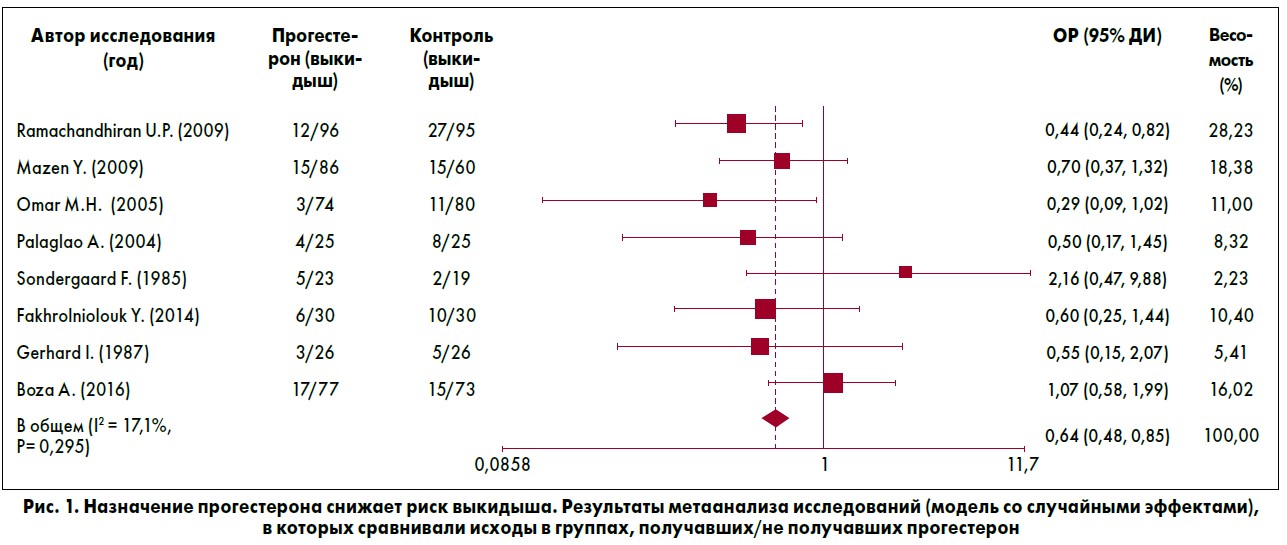
В целом, в метаанализ было включено 845 женщин. Обобщенный анализ первичных исходов (например, случаев выкидыша) представлен на рис. 1. Статистическая гетерогенность среди исследований была низкой (I2 =17%), что свидетельствует о том, что наши данные являются приемлемыми для метаанализа. Обобщенные данные восьми исследований показали, что у беременных с угрозой выкидыша, которых рандомизировали в группу приема прогестерона, риск потери беременности был меньшим (ОР=0,64; 95% ДИ 0,48-0,85) в сравнении с теми, кто получал плацебо или не получал лечения.
Анализ по подгруппам
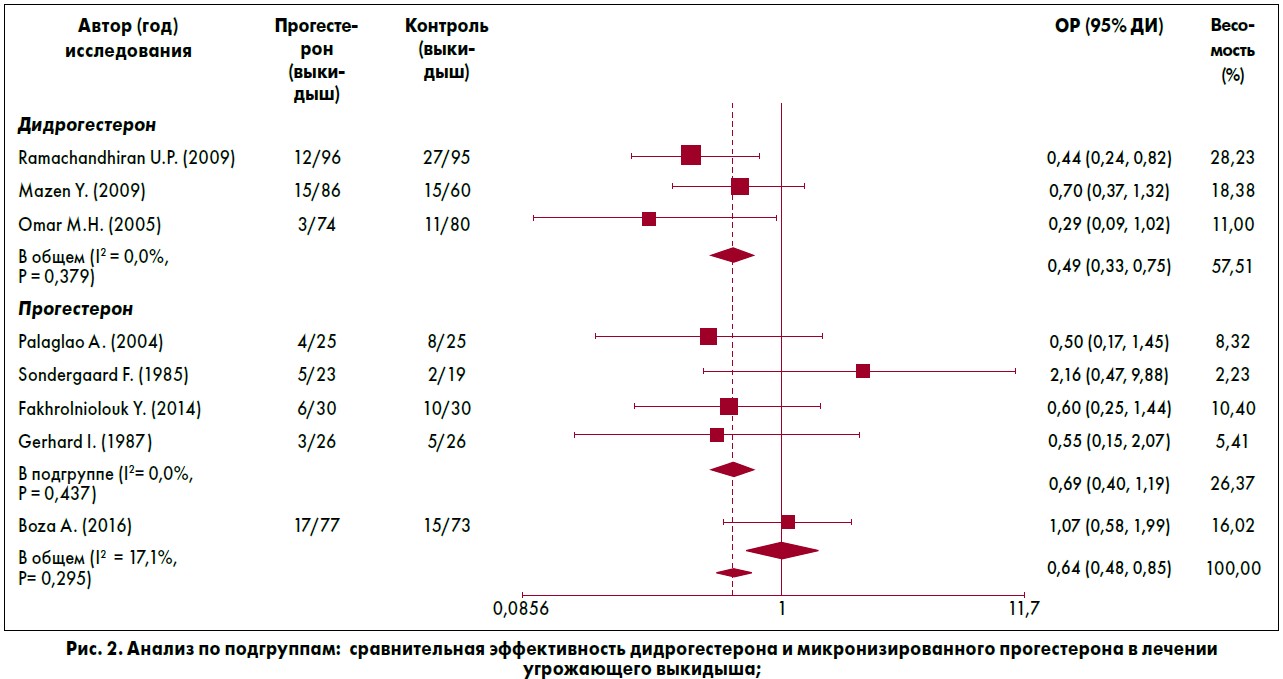
В целях получения более точных результатов мы провели более детальный анализ по отдельным подгруппам (рис. 2). Прием дидрогестерона сопровождался меньшим риском потери беременности (ОР=0,49; 95% ДИ 0,33-0,75) в сравнении с микронизированным прогестероном (ОР=0,69; 95% ДИ 0,40-1,19). Пероральное применение препарата ассоциировалось с меньшим риском спонтанного аборта (ОР=0,55; 95% ДИ 0,38-0,79) в сравнении с интравагинальным использованием (ОР=0,58; 95% ДИ 0,28-1,12). Были отмечены интересные результаты при проведении анализа в подгруппе участниц из различных географических регионов.
Применение прогестерона, как микронизированного, так и дидрогестерона достоверно снижало частоту самопроизвольного аборта в Азиатском регионе (ОР=0,62; 95% ДИ 0,45-0,85) в сравнении с Европейским (ОР=0,75; 95% ДИ 0,37-1,50). При применении микронизированного прогестерона в лечении беременных с угрожающим абортом (в странах Азиатского и Европейского регионов) терапевтический эффект не отмечался (ОР=0,62; 95% ДИ 0,45-0,85). Дальнейший анализ результатов показал, что в Европейском регионе не отмечено значимого эффекта ни при пероральном (ОР=0,85; 95% ДИ 0,37-1,94), ни при интравагинальном (ОР=0,55; 95% ДИ 0,15-2,07) применении микронизированного прогестерона.
В странах Азиатского региона микронизированный прогестерон также не имел эффекта при интравагинальном введении. Однако прием дидрогестерона сопровождался выраженным положительным эффектом (ОР=0,49; 95% ДИ 0,33-0,75) по сравнению с плацебо, что также подтверждает наши вышеизложенные выводы о том, что в общем эффект дидрогестерона в лечении угрожающего аборта превосходит таковой микронизированного прогестерона.
Предвзятость публикаций
Визуальная оценка, ранговый корреляционный тест Бегга и регрессионный анализ Эггера не выявили доказательств в пользу предвзятости публикаций среди исследований по применению прогестерона при угрожающем аборте (Бегг, Р=0,902; Эггер, Р=0,924).
Обсуждение
Угроза выкидыша – достаточно распространенная патология беременности, которая легко диагностируется, но лечение которой является сложной задачей. В течение более чем полувека мы применяли прогестерон и гестагены для лечения угрожающего аборта, не имея сильных доказательств, оправдывающих их применение. В различных метаанализах, изучавших эффективность прогестерона при угрозе выкидыша, были представлены противоречивые результаты. Так, в Кокрановском метаанализе 2011 года [23], включавшем четыре исследования, было показано, что назначение прогестерона при угрозе невынашивания снижает риск потери беременности на 47%. Однако в выводах Кокрановского метаанализа 2013 года [24] отмечалась неэффективность прогестерона, когда объект исследования расширялся и включал в себя беременных с выкидышем. Чтобы выяснить, значима ли роль прогестерона в лечении угрожающего выкидыша, мы провели этот обновленный метаанализ.
В него были включены 8 РКИ, отличных от предыдущих метаанализов (большинство из них включали данные, опубликованные 60 лет назад) [23-25]. Это позволило оценить более новые исследования и данные, а также принять во внимание более надежные выводы об эффективности. Результаты продемонстрировали, что назначение прогестерона женщинам с угрозой выкидыша ассоциировалось с меньшим риском потери плода (ОР=0,64; 95% ДИ 0,48-0,85), что соотносится с предыдущим Кокрановским системным обзором, опубликованным в 2011 году (ОР‑0,35; 95% ДИ 0,35-0,79) [23].
При нормальной беременности прогестерон стимулирует продукцию лимфоцитами прогестерон-индуцированного блокирующего фактора (ПИБФ). Это предотвращает иммунологическую реакцию в отношении плода, изменяя цитокиновый баланс от Th1 в сторону преобладания Т-хелперов 2-го типа (Th2), что приводит к снижению активности естественных Т-киллеров и обеспечивает таким образом защитную иммуномодуляцию [26, 27].
Cогласно результатам клинических исследований, включенных в метаанализ, прогестерон существенно снижал частоту выкидышей – на 36% в сравнении с контролем. Этот факт является достаточно серьезным основанием для назначения данного препарата в качестве эмпирического лечения при угрозе аборта.
В клинической практике обычно используют два типа препаратов прогестерона: микронизированный и дидрогестерон. В нашем анализе по подгруппам лечение дидрогестероном сопровождалось достоверным снижением (ОР=0,49; 95% ДИ 0,33-0,75) частоты выкидышей в сравнении с микронизированным прогестероном (ОР=0,69; 95% ДИ 0,40-1,19). Механизм защитного действия дидрогестерона при невынашивании был доказан в исследованиях на мышах и у людей. В условиях эксперимента на мышах под действием дидрогестерона происходило повышение процентного содержания рецепторов натуральных киллеров (NK‑1R+), в результате чего снижался уровень Th1 и увеличивалось содержание цитокинов Th2. В конечном итоге данные изменения сопровождались протективным эффектом при угрозе невынашивания [28].
Исследование с участием 27 пациенток с угрозой выкидыша и 16 – со здоровой беременностью выявило, что дидрогестерон проявляет защитные эффекты: повышение уровня ПИБФ и увеличение продукции противовоспалительных цитокинов [29].
Влияние на процессы синтеза оксида азота – это другой возможный механизм действия дидрогестерона, повышающий выживаемость эмбриона. Под действием дидрогестерона, в дополнение к его токолитическому эффекту на миометрий, может улучшаться кровоток и насыщение кислородом [30, 31]. Эффективность дидрогестерона также была отмечена в предыдущем систематическом обзоре (ОР=0,47; 95% ДИ=0,31-0,7), и, таким образом, наши выводы подкрепили достоверность более ранних результатов [25].
Более того, анализ по подгруппам показал, что в странах Европейского региона микронизированный прогестерон не эффективен при пероральном применении (ОР=0,85; 95% ДИ 0,37-1,94), так же как и при интравагинальном (ОР=0,55; 95% ДИ 0,15-2,07). Хотя только в одной статье в Азиатском регионе были представлены результаты лечения микронизированным прогестероном, авторы также склоняются к выводу о том, что он не оказывает значимого эффекта. Это может быть обусловлено особенностями процессов метаболизма микронизированного прогестерона, который мгновенно метаболизируется в печени и, как результат, характеризуется низкой биодоступностью.
Учитывая возможное влияние этнических факторов на действие препаратов, мы также провели анализ подгрупп в различных регионах. Применение обоих типов прогестерона (микронизированный и дидрогестерон) в странах Азиатского региона сопровождалось более низким риском (ОР=0,62; 95% ДИ 0,45-0,85), чем в Европейском регионе (ОР=0,75; 95% ДИ 0,37-1,50). Возможная причина этого, скорее всего, объясняется географическими различиями или этническим происхождением, что отражено в исследовании Schweikert et al. [32]. Авторы высказали предположение, что редко встречающийся аллель рецептора прогестерона может быть ассоциирован с повторными случаями невынашивания беременности, внося таким образом определенный вклад в мультифакторность данной патологии. Однако, учитывая, что во включенных в метаанализ исследованиях из Азиатского региона применяли в основном дидрогестерон, а в Европейском регионе выборка по применению микронизированного прогестерона была оносительно малой, мы все еще не можем утверждать, что эффекты прогестерона имеют этнические различия, поскольку это требует большей выборки и мультицентровых исследований в будущем.
Ограничения нашего исследования соответствуют ограничениям включенных РКИ. В проведенном нами метаанализе только три включенных исследования были двойными слепыми [15, 18, 19], а остальные являлись либо простыми слепыми, либо без детализации метода, что обуславливало риск погрешности.
Как известно, возраст матери и срок гестации – важнейшие факторы, которые следует учитывать при проведении таких исследований. Неоднородность сравниваемых групп по этим показателям может быть причиной различного ответа на прогестерон. Хотя оба эти фактора учитывались в исследованиях, к сожалению, участницы не были разделены на соответствующие группы. Кроме того, при проведении поиска в базах данных нами обнаружены исследования, в которых применяли прогестерон или дидрогестерон, без каких-либо упоминаний о других гестагенах.
Результаты проведенного метаанализа позволяют сделать вывод о том, что применение препаратов прогестерона эффективно в лечении угрожающего выкидыша. При этом действие дидрогестерона превосходит микронизированный прогестерон. Однако остается до конца не выясненным вопрос о наличии связи между эффективностью прогестерона и расовой принадлежностью. Учитывая небольшое количество включенных РКИ и трудности, связанные с дизайном исследований по угрозе выкидыша, необходимо проведение дальнейших исследований с большим количеством участниц и исследовательских центров.
Список литературы находится в редакции.
Xiao-xue Wang, Qing Luo,
Wen-pei Bai. Efficacy of progesterone on threatened miscarriage: Difference in drug types J. Obstet. Gynaecol. Res. 2019
Печатается с сокращениями.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 1 (33), березень 2019 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...