Особенности лечения болевого синдрома после кесарева сечения
17-20 апреля в Киеве, в клинической больнице «Феофания» прошел 11-й Британо-Украинский симпозиум (БУС‑11), который собрал более 1300 делегатов из разных стран. На этот раз ставший уже традиционным международный форум был посвящен теме «Инновационные технологии и методики в анестезиологии и интенсивной терапии».
В рамках симпозиума в отдельном зале заседаний рассматривались «Актуальные вопросы акушерской анестезиологии и интенсивной терапии», где обсуждались и проблемы обезболивания в гинекологии и после проведения кесарева сечения.
Доклад на тему «Новейшие аспекты послеоперационного обезболивания кесарева сечения» представил коллегам ассистент кафедры акушерства, гинекологии и репродуктологии НМАПО им. П.Л. Шупика, кандидат медицинских наук Вадим Витальевич Петриченко. Он также поделился опытом проведения исследования на базе центра.
В первую очередь докладчик отметил, что на сегодняшний день наблюдается общемировая тенденция к увеличению частоты проведения кесарева сечения. Рекомендации ВОЗ по идеальной частоте случаев не должны превышать 15% среди всех родоразрешений. Однако в некоторых странах показатель превышен в два и более раз. Так, в странах Европы, включая Украину, с 2004 года случаи кесарева сечения составили 25%.
Кесарево сечение – это операция, которая требует от врача-анестезиолога планирования вида обезболивания. Вмешательство может быть плановым и ургентным. Согласно категориям ургентности по Lukas et al. (2000), существует четыре категории ургентности:
- 1-я категория – немедленная угроза жизни матери и плоду;
- 2-я категория – нет угрозы жизни матери и плоду;
- 3-я категория – необходимо раннее выполнение оперативного вмешательства;
- 4-я категория – плановая операция в удобное время для женщины и медицинского учреждения.
При 1-й категории ургентности спинальная анестезия не выполняется, предпочтение отдается общей. При 2-й и 3-й категориях выполняется общая, спинальная или регионарная анестезия, при 4-й категории – регионарная.
В Киевском городском центре репродуктивной и перинатальной медицины (КМЦРПМ) специалистам удалось добиться снижения частоты проведения кесарева сечения с 32% в 2016 году до 25% в 2017 году. Прослеживается явное преобладание спинальной анестезии в сравнении с общей в процентном соотношении. Так, в 2016 году эпидуральное обезболивание составило 73,2%, а общее – 19,6% (другие виды анестезии – 7%). В 2017 году это соотношение было 78,8% против 18,2% соответственно (другие виды анестезии – 3%).
Далее докладчик сообщил, что в КМЦРПМ проводилось исследование, целью которого было определение времени, необходимого врачу для осуществления спинальной анестезии при ургентном кесаревом сечении. Выполнялось измерение периода от момента принятия решения об операции до разрешения анестезиолога хирургам на осуществление разреза кожи.
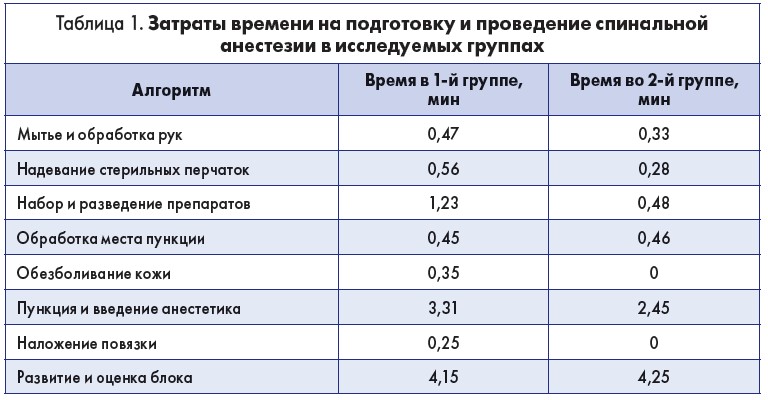
Оцениваемое время, которое отводилось на подготовку бригады анестезиолога к спинальной анестезии, разделили на этапы (табл. 1):
- мытье и обработка рук;
- надевание стерильных перчаток;
- набор и разведение препаратов (местные анестетики, адъюванты);
- обработка места пункции;
- обезболивание кожи;
- пункция и идентификация интратекального пространства, введение анестетика;
- наложение стерильной повязки на место пункции;
- развитие и оценка спинального блока.
Общее число пациенток, которым проводилась анестезия перед кесаревым сечением, составило 34. Они были разделены на две группы:
- 1-я группа – слепое проспективное исследование (n=16);
- 2-я группа – открытое проспективное исследование (n=18).
В 1-й группе опытный анестезиолог не был предупрежден о проведении испытания, расчет времени осуществления всех этапов проводился «вслепую». Во 2-й группе специалист был информирован об исследовании и необходимости оптимизировать процесс выполнения анестезии и ускорения проведения всех его этапов.
Средний показатель времени, затраченного на подготовку и выполнение спинно-мозговой анестезии в 1-й группе, составил 12 мин 11 с, во 2-й группе он сократился до 8 мин 25 с (р <0,05). Докладчик отметил, что по временным нормам в обеих группах наблюдалось попадание в рамки категории ургентности № 1 и не было ни одного случая задержки операции по вине анестезиолога и его бригады.
В.В. Петриченко отметил, что после любого оперативного вмешательства борьба с болью продолжается; при этом неадекватное интра- или послеоперационное обезболивание может стать причиной хронического болевого синдрома. Он сообщил, что, по данным проведенного исследования, частота возникновения постоперационной хронической боли через 3, 6 и 12 мес после кесарева сечения составила соответственно 18,3, 11,3 и 6,8%. Большинство пациенток ощущали легкую боль в состоянии покоя, которая усиливалась при движении. Это происходило до 3-го месяца после операционного вмешательства. Через 6-12 мес интенсивность боли постепенно снижалась. Этот факт подтверждает выводы о том, что спинальная анестезия обеспечивает полноценную защиту во время операции кесарева сечения, но имеет недостаточный анальгетический эффект в постоперационном периоде и рассматривается как компонент мультимодального обезболивания. Мультимодальная анестезия – это сбалансированная аналгезия, предусматривающая одновременное применение двух и более анальгетиков, которые обладают различными механизмами действия и позволяют достичь адекватного обезболивания.
Докладчик напомнил общеизвестный подход мультимодальной регионарной анестезии:
- опиаты;
- парацетамол (ацетаминофен);
- нестероидные противовоспалительные препараты (НПВП);
- метамизол натрия;
- антагонисты рецепторов N-метил-D-аспартата (NMDA-антагонисты);
- селективные ингибиторы циклооксигеназы 2-го типа (ЦОГ‑2);
- антагонисты центральных α‑2-адренорецепторов.
В.В. Петриченко привел данные Американского колледжа акушеров и гинекологов (ACOG, 2017), согласно которым одна из трехсот пациенток, принимавших опиатные анальгетики в послеродовом периоде, становится зависимой и продолжает принимать опиаты длительное время. Поэтому, отметил он, применение мультимодальных комбинаций препаратов для эффективной борьбы с послеоперационной болью является ключевым моментом ведения пациенток акушерского профиля в постоперационном периоде.
Докладчик сослался на опубликованный в 2017 г. в журнале Anesthesiology Clinics (Sutton C.D., Carvalho B.) американский «Протокол лечения боли в послеродовом периоде в условиях стационара», содержащий в своих алгоритмах морфин, который вводится преимущественно интратекально. Препарат добавляется к местному анестетику в дозе 100-150 мкг. В протоколе также есть ацетаминофен и всего два разрешенных НПВП: ибупрофен и кеторолак. В стандартах отмечены также наркотические анальгетики, которые добавляются при необходимости – если интенсивность боли по ВАШ (визуально-аналоговая шкала) превышает 4 балла.
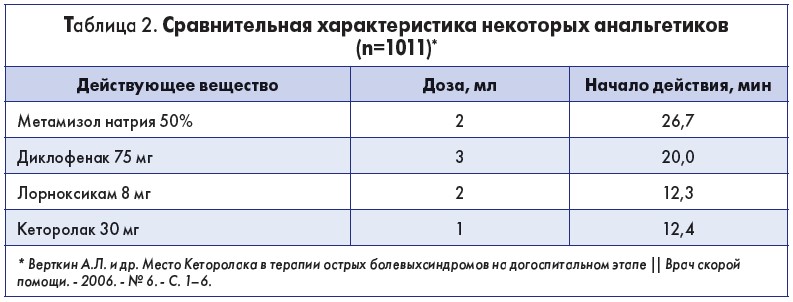
Кеторолак – это мощнейший анальгетик среди НПВП. Внутримышечное введение этого препарата обеспечивает быстрый аналгезирующий эффект в сравнении с метамизолом натрия, диклофенаком и лорноксикамом (табл. 2).
Докладчик обратил внимание коллег на то, что при использовании кеторолака нет необходимости в применении внутривенной формы, поскольку внутримышечное введение создает адекватное анальгетическое действие. Инъекция кеторолака, заметил он, является предупреждающей тактикой, поскольку, если известно, что пациентка будет испытывать боль через час, то препарат можно ввести заранее.
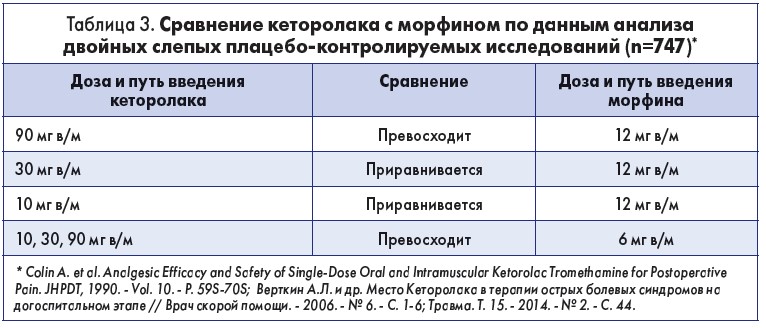
Докладчик отметил, что по уровню эффективности кеторолак сравним с морфином (табл. 3).
По данным исследования, в котором определялось количество экскреции кеторолака в грудное молоко, было зафиксировано, что его концентрация не превышала 5 нг/мл при условии суточной дозы 90 мг. Таким образом, максимальное потенциальное количество кеторолака, которое может получить ребенок при грудном вскармливании, колеблется от 3,16 до 7,9 мг при условии потребления им материнского молока в количестве от 400 мл до 1 л в сутки. В перерасчете на массу тела – это эквивалент от 0,16 до 0,4% общесуточной дозы для матери. Конечно же, новорожденный ребенок столько не потребляет, и только начиная от первого месяца жизни суточный объем потребляемого им молока может составлять 1 л.
В конце своего доклада В.В. Петриченко сформулировал выводы, сделанные в ходе представленного исследования:
- При условии внедрения в практику разработанного алгоритма удается сократить время, затраченное на подготовку и проведение спинальной анестезии как компонента мультимодального обезболивания при ургентном кесаревом сечении.
- Кеторолак (препарат Кеторол) может полноценно применяться как НПВП выбора для мультимодальной аналгезии при кесаревом сечении, учитывая его выраженный эффект, а также малую концентрацию в грудном молоке.
Таким образом, кеторолак можно использовать в акушерской практике. Доказана его безопасность при краткосрочном применении. Если придерживаться рекомендованных доз, то риск развития побочных эффектов от кеторолака соразмерен с риском при использовании кетопрофена или диклофенака (Forrest J.B. et al. Br J Anaesth. 2002;88(2)).
Подготовила Елена Марченко
Тематичний номер «Хірургія, Ортопедія, Травматологія, Інтенсивна терапія» № 3 (37), вересень 2019 р.
СТАТТІ ЗА ТЕМОЮ Хірургія, ортопедія та анестезіологія
Дисфагія є поширеним явищем у пацієнтів відділення інтенсивної терапії (ВІТ), але вона часто залишається недостатньо розпізнаною та неконтрольованою, незважаючи на те що пов’язана з небезпечними для життя ускладненнями, тривалим перебуванням у ВІТ та госпіталізацією. Запропонований у статті експертний висновок щодо діагностики й лікування дисфагії розроблений на основі доказових клінічних рекомендацій та думок лікарів-практиків. Автори рекомендують прийняти ці клінічні алгоритми для надання стандартизованої та високоякісної допомоги, яка передбачає своєчасний систематичний скринінг, оцінку та лікування дисфагії в екстубованих пацієнтів і пацієнтів із трахеостомою у ВІТ. ...
Больовий синдром при хронічних ранах є рутинним явищем хірургічної практики. Рана вважається такою, що тривало не загоюється, якщо, незважаючи на відповідну терапію та достатній термін лікування (4-6 міс), відсутні або практично відсутні ознаки загоєння. Неопіоїдні та опіоїдні анальгетики є основними препаратами, що застосовуються для лікування больового синдрому при ранах. На науково-практичній конференції «Міждисциплінарний підхід у лікуванні коморбідних хірургічних пацієнтів», що відбулася наприкінці 2023 року, тему менеджменту хронічної ранової хвороби представив у доповіді «Контроль болю в хірургії ран та трофічних дефектів м’яких тканин різної етіології» завідувач кафедри хірургії та судинної хірургії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Іванович Саволюк. Ключові слова: ранова хвороба, трофічна виразка, ВАК-терапія, больовий синдром, нестероїдні протизапальні препарати, Дексалгін®....
Актуальність проблеми переломів на сьогодні не залишає сумнівів, зокрема в контексті старіння населення та поширеності остеопорозу. Кальцій та вітамін D, виконуючи ключову роль у формуванні та підтриманні щільності кісткової тканини, є необхідними елементами для успішної профілактики переломів, особливо у вразливих груп населення. Також важливим є достатній рівень кальцію та вітаміну D в організмі для оптимального зрощення переломів і посттравматичної зміни кісток. У цьому контексті велике значення має вибір конкретного комплексу Са + D із позицій ефективності, безпеки та високого комплаєнсу. Ключові слова: остеопороз, крихкість кісток, кальцій, вітамін D, профілактика переломів. ...
З установленням центральних венозних катетерів (ЦВК) пов’язані різноманітні ускладнення, включаючи ті, що зумовлені безпосередньо введенням і/або доступом, через який уводиться катетер, а також віддалені (>1 тижня) ускладнення, такі як дисфункція катетера, стеноз або тромбоз центральної вени та розвиток інфекції. Кількість і тяжкість ускладнень зростають зі збільшенням розміру катетера, кількості використовуваних катетерів та часу їх перебування в організмі. У статті наведено огляд сучасних даних щодо ускладнень, пов’язаних із ЦВК, а також стратегії їх профілактики та лікування. Ключові слова: центральний венозний катетер, ускладнення, пункція артерії, пневмоторакс, тромбоз центральної вени, інфекції кровотоку, дисфункція катетера. ...