Анти-CD20 терапія при неходжкінських лімфомах
Особливу увагу учасників XI Науково-практичної конференції з міжнародною участю «Сучасні підходи до діагностики та лікування лімфопроліферативних захворювань», яка відбулася 9-11 жовтня 2019 року в м. Києві, привернула тема анти-CD20 терапії неходжкінських лімфом (НЛ). Українські науковці та запрошений іноземний гість поділилися результатами великих міжнародних рандомізованих клінічних досліджень, у яких порівнювали ефективність різних терапевтичних режимів у пацієнтів з НЛ, а також представили цікаві клінічні випадки.
 З доповіддю «Чи є анти-CD20 терапія провідною у лікуванні неходжкінських лімфом у 2019 році» виступила запрошена гостя з Хорватії доктор філософії та медицини Інга Мандак Рогуль.
З доповіддю «Чи є анти-CD20 терапія провідною у лікуванні неходжкінських лімфом у 2019 році» виступила запрошена гостя з Хорватії доктор філософії та медицини Інга Мандак Рогуль.
– Історія використання анти-CD20 антитіл у лікуванні пацієнтів з фолікулярними лімфомами (ФЛ) сягає початку 2000-х рр., коли вперше отримано позитивні результати застосування ритуксимабу у поєднанні з хіміотерапією у таких хворих. За 20 років досягнуто значного прориву у лікуванні пацієнтів з ФЛ. Якщо в недалекому 2001 р. перелік медикаментозних засобів для лікування таких хворих був істотно обмеженим, то можливості нинішніх лікарських препаратів стали справжньою революцією в онкогематології.
Більшість ФЛ є індолентними пухлинами. При визначенні стратегії ведення пацієнтів з цим діагнозом приблизно в 1/3 із них немає потреби в терміновому проведенні імунохіміотерапії, застосовується підхід активного спостереження. Що стосується групи пацієнтів, яким стартово проводилося лікування, через деякий час очікується рецидив патології або втрата адекватної відповіді на призначену терапію. Так через 18 років застосування ритуксимабу при ФЛ виникла проблема резистентності пухлини до цього препарату.
Ідентифікувати резистентність пухлини до ритуксимабу складно, адже вираженість цього явища може варіювати. Слід зазначити, що ритуксимаб призначають одночасно з цитотоксичними хіміопрепаратами, а отже визначити внесок конкретного лікарського засобу в загальну ефективність комплексної терапевтичної схеми майже неможливо. Тому загальноприйнятим визначенням резистентності до ритуксимабу є недостатня відповідь на лікування або прогресування хвороби на тлі застосування терапевтичних схем із включенням ритуксимабу через 6 міс.
Проаналізувавши доступні статистичні дані щодо результатів 1-ї лінії лікування пацієнтів з НЛ за схемами, які включають ритуксимаб, можна зробити такі висновки: у 10 зі 100 пацієнтів наявна рефрактерність до призначеної терапії, у 45 настає прогресування хвороби або смерть протягом 5 років лікування, і лише у 45 хворих відмічається адекватна відповідь на призначену терапію упродовж 5 років. Пацієнти з прогресуванням захворювання на тлі лікування ритуксимабом потребують застосування альтернативних підходів.
Протягом останніх років добре відомий бендамустин отримав «нове життя» у лікуванні хворих з рефрактерними до ритуксимабу індолентними В-клітинними НЛ. Є дані клінічних досліджень, які демонструють ефективність препарату у лікуванні таких пацієнтів. Проте важливим аспектом терапії гематологічних пацієнтів є збереження якості життя, що спонукає до пошуку нових лікувальних стратегій.
Безумовно, ритуксимаб є важливою опцією у терапії онкогематологічних хворих і при низці лімфопроліферативних захворювань вважається золотим стандартом. Проте разом з загальнонауковим прогресом лікарі прагнуть вищих результатів і в лікуванні хворих.
До нового покоління анти-CD20 препаратів належить обінутузумаб – моноклональне анти-CD20 антитіло 2 типу підкласу IgG1, яке характеризується більш вираженою прямою руйнівною дією проти пухлинних клітин, інтенсивнішими антитілозалежним клітинним фагоцитозом та цитотоксичністю порівняно з ритуксимабом.
У відкритому рандомізованому контрольованому дослідженні (РКД) III фази GADOLIN за участю пацієнтів з рефрактерною до ритуксимабу індолентною НЛ порівнювали дві схеми терапії: обінутузумаб + бендамустин та монотерапія бендамустином. Хворих (n=396) розподілили на дві групи: учасники 1-ї групи отримали 6 циклів за схемою обінутузумаб (1000 мг у 1-й, 8-й та 15-й дні 1-го циклу та у 1-й день 2-6-го циклів) + бендамустин
Метою дослідження B.D. Cheson та співавт. (2018) було оновлення результатів РКД III фази GADOLIN. До нього увійшли пацієнти з підтвердженою рефрактерною до ритуксимабу індолентною CD20+ НЛ (n=413). Рандомізація хворих і лікування проводилися за аналогією до РКД III фази GADOLIN. Слід зазначити, що у 335 пацієнтів була діагностована ФЛ (у 171 – 1-ї групи та 164 – 2-ї). Отримані результати підтвердили дані РКД GADOLIN: ВБП у групі обінутузумаб + бендамустин склала 25,8 міс, у групі монотерапії бендамустином – 14,1 міс (рис. 1). Тривалість загальної виживаності (ЗВ) у групі обінутузумаб + бендамустин також була більшою (рис. 2). У хворих з ФЛ динаміка ВБП та ЗВ були зіставні з загальними результатами. Побічні явища 3-5 ступеня реєстрували у 72,5% хворих 1-ї групи та у 65,5% – 2-ї. Найчастішими небажаними явищами були нейтропенія, тромбоцитопенія, анемія. Проте варто наголосити на тому, що ці побічні ефекти є очікуваними та контрольованими, а у великої частини пацієнтів тяжкість побічних явищ не перевищувала 3 ступеня.
Отже, обінутузумаб – це нова опція у лікуванні хворих з рефрактерними до ритуксимабу індолентними НЛ, особливо ФЛ. Застосування цього препарату дає змогу не лише підвищити ВБП та ЗВ у цих хворих, а й значно покращити якість життя.
Іншим важливим для онкологів питанням є те, чи можна застосовувати обінутузумаб у 1-й лінії терапії. У дослідженні GALLIUM порівнювали ефективність двох терапевтичних стратегій (із включенням у схему лікування обінутузумабу або ритуксимабу) у раніше не лікованих пацієнтів з CD20+ індолентними НЛ. Усі хворі (n=1202) були рівномірно розподілені на дві групи. Учасники 1-ї групи отримували обінутузумаб (1000 мг у 1-й, 8-й та 15-й дні 1-го циклу та 1-й день 2-6-го циклів), 2-ї групи – ритуксимаб (375 мг/м2 на добу у 1-й день кожного циклу) протягом 21-денного циклу (всього 6 циклів) разом з хіміотерапією (CHOP, або CVP, або бендамустин). Підтримувальну терапію проводили обінутузумабом або ритуксимабом через кожні 2 міс протягом 2 років. Після медіани спостереження 34,5 міс плановий проміжний аналіз показав, що ризик прогресування хвороби та смерті на 34% нижчий у пацієнтів, які разом з хіміотерапією отримували обінутузумаб, ніж у групі хіміотерапії з ритуксимабом. Трирічна ВБП у групах хіміотерапії з ритуксимабом та хіміотерапії з обінутузумабом становила 73,3 і 80,0% відповідно (рис. 3).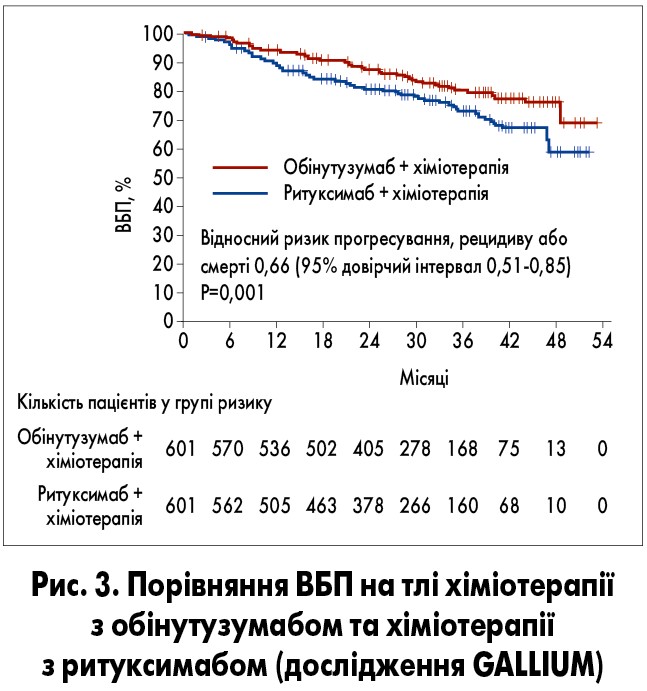
У дослідженні GALLIUM продемонстровано, що в осіб, які отримували обінутузумаб з хіміотерапією, частота прогресування, рецидиву хвороби чи смерті була нижчою, ніж у групі хіміотерапії з ритуксимабом (93 і 125 випадків відповідно). Частота летальних випадків у групах хіміотерапії з обінутузумабом та хіміотерапії з ритуксимабом склала 5,8 та 7,7% відповідно (R. Marcus et al., 2017).
Слід зазначити, що прогресування захворювання у пацієнтів з ФЛ протягом 24 міс від початку терапії вважається поганим прогностичним маркером. J.F. Seymour та співавт. (2019) провели аналіз результатів дослідження GALLIUM та порівняли режими хіміотерапії з обінутузумабом та ритуксимабом у пацієнтів з верифікованою ФЛ, які раніше не отримували лікування. У групі хіміотерапії з обінутузумабом раннє прогресування хвороби фіксували значно рідше, ніж у пацієнтів, які отримували хіміотерапію з ритуксимабом. Ризик смерті також був вищим у хворих, у яких патологія прогресувала протягом 24 міс від початку лікування. Крім того, ефективність обінутузумабу не залежала від призначеної схеми хіміотерапії.
Отже, застосування хіміотерапії з обінутузумабом як 1-ї лінії терапії при ФЛ дає можливість пролонгувати ВБП, характеризується різними механізмами дії та контрольованою безпекою для пацієнта.Крім того, що обінутузумаб забезпечує хороші результати як індукційна терапія, його можна призначати пацієнтам з індолентними НЛ для підтримання ремісії.
Препарати моноклональних антитіл є додатковою опцією у лікуванні хворих з хронічним лімфолейкозом (ХЛЛ), що продемонстровано у дослідженні CLL11. У це дослідження було включено 781 хворого з раніше не лікованим ХЛЛ. Пацієнтів розподілили на три групи: хлорамбуцил + обінутузумаб, хлорамбуцил + ритуксимаб, монотерапія хлорамбуцилом. Найвищі показники ВБП та ЗВ отримані у групі хлорамбуцил + обінутузумаб. Застосування хлорамбуцилу з обінутузумабом у пацієнтів з ХЛЛ знижує ризик прогресування хвороби та смерті на 51% порівняно з таким у групі, яка разом з хлорамбуцилом отримувала ритуксимаб (ВБП становила 28,9 та 15,7 міс відповідно; V. Goede et al., 2014). При фінальному аналізі результатів дослідження CLL11 виявлено, що у довготривалій перспективі комбінація хлорамбуцил + обінутузумаб знижує ризик смерті у пацієнтів з ХЛЛ на 24% порівняно з комбінацією хлорамбуцил + ритуксимаб.
 Про застосування обінутузумабу в 1-й та 2-й лініях терапії ФЛ та досвід використання препарату у своїй практиці розповіла професор кафедри гематології і трансфузіології Національної медичної академії післядипломної освіти імені П.Л. Шупика, доктор медичних наук Світлана Анатоліївна Гусєва.
Про застосування обінутузумабу в 1-й та 2-й лініях терапії ФЛ та досвід використання препарату у своїй практиці розповіла професор кафедри гематології і трансфузіології Національної медичної академії післядипломної освіти імені П.Л. Шупика, доктор медичних наук Світлана Анатоліївна Гусєва.
– Фолікулярна лімфома – це рідкісне лімфопроліферативне захворювання, поширеність якого в Україні становить близько 4% (у США та Західній Європі – 22%). Якщо донедавна хвороба вважалася невиліковною, то сучасні лікарські засоби дозволили істотно покращити виживаність пацієнтів із ФЛ.
Клінічний випадок 1
Пацієнт С., 65 років. У 2016 р. встановлений діагноз фолікулярна лімфома. Специфічного лікування не отримував, на власний розсуд застосовував методи народної медицини.
27.03.2019 госпіталізований до гематологічного відділення Головного військового клінічного госпіталю зі скаргами на різку загальну слабкість, нічну пітливість, дискомфорт у животі, нестачу повітря, печію, втрату маси тіла (10 кг протягом останнього року).
Фізикальне обстеження: загальний стан середнього ступеня тяжкості, збільшення розмірів селезінки (276×113×313 мм), при пальпації тверда, чутлива.
Аналіз крові: анемія середнього ступеня тяжкості, тромбоцитопенія (80×109/л), відносний лімфоцитоз (65,5%), незначне підвищення рівня лактатдегідрогенази.
Після дослідження стернального пунктату, імунофенотипування встановлено діагноз: неходжкінська В-клітинна фолікулярна лімфома з ураженням медіастинальних, внутрішньогрудних, черевних і заочеревинних лімфатичних вузлів, селезінки з лейкемізацією кісткового мозку IVВ стадії, FLIPI‑2 high risk factor; супутній діагноз – ішемічна хвороба серця, дифузний кардіосклероз, серцева недостатність 0 ступеня.
При виборі терапевтичної стратегії у цьому клінічному випадку за основу взято рекомендації Національної онкологічної мережі США (NCCN), згідно з якими як 1-й лінії терапії слід надавати перевагу комбінації бендамустину з обінутузумабом чи ритуксимабом. У зв’язку з масивним пухлинним ураженням лімфатичних вузлів пацієнту С. було призначено шість 28-денних циклів обінутузумабу (1-й цикл: по 1000 мг у 1-й, 8-й, 15-й дні,
Результати лікування: нормалізація рівня гранулоцитів (з 19,9 до 64,0%), зниження рівня лімфоцитів (з 65,5 до 23,1%), підвищення рівня гемоглобіну (зі 101 г/л до 124 г/л) та тромбоцитів; значне зменшення розмірів селезінки (до 134×70×86 мм) і лімфатичних вузлів; результати позитронно-емісійної томографії з комп’ютерною томографією (ПЕТ-КТ) – патологічних вузлів у шийній (білатерально) та аксилярній ділянках не виявлено; збільшення накопичення радіофармпрепарату в 5 медіастинальних вузлах (найбільший розмір вузла – 1,8 мм). Висновок: у пацієнта С. досягнуто часткової ремісії захворювання.
Під час лікування на 15-й хвилині введення обінутузумабу у пацієнта С. розвинулася інфузійна реакція легкого ступеня (підвищення температури тіла, озноб), яку незабаром вдалося купірувати шляхом сповільнення швидкості інфузії та проведення лікувальних заходів. Наступні введення препарату не викликали у пацієнта побічних реакцій.
Клінічний випадок 2
Пацієнтка Ш., 65 років. Вважає себе хворою з грудня 2016 р., коли вперше виявила збільшення шийних лімфатичних вузлів.
29.12.16 на підставі результатів гістологічного та імуногістологічного досліджень встановлено діагноз
Січень 2019 – рецидив захворювання. Після проведення повторної біопсії лімфатичного вузла з подальшим імуногістохімічним дослідженням встановлено діагноз фолікулярна лімфома.
На час госпіталізації у гематологічне відділення загальний стан хворої задовільний.
Фізикальне обстеження: збільшення розмірів правого підщелепного, шийних, лівого аксилярного лімфатичних вузлів до 2,0-2,5 см, селезінки.
Аналіз крові без особливостей.
Встановлений діагноз: неходжкінська В-клітинна фолікулярна лімфома IVА стадії з ураженням правого підщелепного, шийних, лівого аксилярного лімфатичних вузлів і селезінки, FLIPI‑2 проміжний ризик. Перший ранній рецидив. Стан після 6 курсів імунохіміотерапії. Супутнє захворювання: ішемічна хвороба серця, дифузний кардіосклероз, гіпертонічна хвороба ІІ стадії, серцева недостатність 1 ступеня.
Оскільки адекватна відповідь на хіміотерапію з ритуксимабом спостерігається лише у 45% хворих з ФЛ, то такі пацієнти потребують застосування сучасніших засобів, яким є обінутузумаб.
Відповідно до рекомендацій NCCN, 2-га лінія терапії при ФЛ представлена бендамустином з обінутузумабом або ритуксимабом. У цьому клінічному випадку застосування ритуксимабу є недоцільним, оскільки у пацієнтки розвинулась рефрактерність до нього. Хворій також було призначено комбінацію бендамустину з обінутузумабом – шість 28-денних циклів обінутузумабу (1-й цикл: по 1000 мг у 1-й, 8-й, 15-й дні, 2-6-й цикли: по 1000 мг на день) та бендамустину (90 мг/м2 у 1-й і 2-й день кожного циклу).
Результати лікування: зменшення розмірів лімфатичних вузлів (підщелепного з 2,0 до 1,5 см, лівого аксилярного з 2,5 до 1,7 см, правого шийного – з 2,1 до 1,6 см, лівого шийного – з 1,5 до 0,9 см); нормалізація розмірів селезінки (з 146 до 118 мм).
У пацієнтки Ш. не спостерігалося побічних реакцій на введення обінутузумабу.
Таким чином, дані великих рандомізованих досліджень та власний досвід застосування комбінації бендамустину з обінутузумабом свідчать про високу ефективність препарату у лікуванні первинних хворих з ФЛ, а також із рефрактерністю до попередньої терапії чи рецидивом захворювання на її тлі.
 Клінічний випадок гіперчутливості до анти-CD20 моноклональних антитіл та застосування обінутузумабу при непереносимості ритуксимабу від колективу науковців Національного інституту раку представила кандидат медичних наук Ольга Ігорівна Новосад.
Клінічний випадок гіперчутливості до анти-CD20 моноклональних антитіл та застосування обінутузумабу при непереносимості ритуксимабу від колективу науковців Національного інституту раку представила кандидат медичних наук Ольга Ігорівна Новосад.
Клінічний випадок
Пацієнтка А., 1989 р.н.
Скарги на біль у попереку, збільшення розмірів пахвинних лімфатичних вузлів, у зв’язку з чим пацієнтка отримала лікування за місцем проживання.
За результатами патогістохімічного дослідження (02.04.2019) морфологічна структура пухлини та імунофенотип клітин відповідає В-клітинній лімфомі з клітин фолікулярного центру ІІІА ступеня злоякісності з фолікулярним типом росту.
Методом магнітно-резонансної томографії виявлені конгломерати заочеревинних лімфатичних вузлів.
При зверненні пацієнтки до Національного інститут раку були призначені додаткові методи дослідження. За даними гістологічного дослідження пунктату кісткового мозку та імуногістохімічного дослідження морфологічні зміни відповідають ураженню В-клітин. Аналіз периферичної крові: 34% лімфоцитів, у кістковому мозку – 22% клітин з ознаками малих лімфоцитів.
З анамнезу відомо, що у дитинстві пацієнтка хворіла бронхіальною астмою, тобто у цьому клінічному випадку присутній алергічний компонент. У зв’язку з цим виникла потреба у проведенні алергопроб для уникнення можливих алергічних реакцій під час діагностики та лікування. У пацієнтки виявлена різко позитивна реакція на йодовмісні препарати, тому хворій проводилася ПЕТ-КТ без уведення йодовмісних засобів.
Шляхом ПЕТ-КТ виявлено множинне ураження лімфатичних вузлів: шийних, аксилярних, прекардіальних, наддіафрагмальних, заочеревинних та мезентеріальних, збільшені метаболічно активні клубові, пахвинні лімфатичні вузли, уражені ручка груднини та груднинні кінці ключиць.
Встановлений діагноз: фолікулярна лімфома IVА стадії (IIIА ступеня злоякісності) з ураженням шийних, аксилярних, внутрішньогрудних, заочеревинних, внутрішньочеревних, пахвинних лімфатичних вузлів, груднини та обох ключиць, кісткового мозку. Клінічна група 2.
Довідка
Ритуксимаб – моноклональне анти-CD20 антитіло 1 типу. Препарат став справжнім проривом у лікуванні хворих з В-клітинними лімфомами (у тому числі з ФЛ). Застосування препарату як індукційної та підтримувальної терапії дозволило істотно підвищити ВБП та ЗВ. Незважаючи на переваги ритуксимабу у лікуванні В-клітинних лімфом, у пацієнтів з ФЛ на тлі лікування цим лікарським засобом часто спостерігаються ранні рецидиви, які значно погіршують прогноз хвороби. Таким чином, існує потреба у застосуванні нових препаратів для терапії хворих на ФЛ.
Іншою проблемою застосування ритуксимабу є гіперчутливість до анти-CD20 моноклональних антитіл. Частота інфузійних реакцій на введення ритуксимабу коливається в межах 25-75%. Алергічні реакції варіюють від легких (кропив’янка, лихоманка, озноб) до тяжких (задишка, гіпотензія, анафілаксія, синдром Стівенса – Джонсона) проявів, що обмежує широке застосування ритуксимабу у 1-й лінії терапії.
У зв’язку з обтяженим алергологічним анамнезом перед призначенням лікування пацієнтці були проведені контрольні тести для визначення переносимості ритуксимабу, бендамустину та обінутузумабу. Результат реакції специфічного лейкоцитозу на ритуксимаб був різко позитивним, що є абсолютним протипоказанням для його застосування. Тому пацієнтці був призначений бендамустин + обінутузумаб.
Суперечливим питанням є частота виникнення побічних реакцій на введення обінутузумабу, які за результатами дослідження GALLIUM розвиваються частіше, ніж при застосуванні ритуксимабу (найчастішим побічним явищем є інфузійна реакція, яка виникає у 4,4% випадків при введенні обінутузумабу та у 1,8% – ритуксимабу).
У пацієнтки А. при першому введенні обінутузумабу розвинулася інфузійна реакція легкого ступеня (гіпертермія), яку вдалося купірувати шляхом зменшення швидкості інфузії та застосування медикаментозної корекції. Премедикацію проводили гідрокортизоном, димедролом, парацетамолом. Пізнім ускладненням специфічного лікування була нейтропенія 3 ступеня, яка виникла одноразово після 5-го курсу імунохіміотерапії і була купірувана введенням колонієстимулювального фактора.
Результат лікування після 3 курсів імунохіміотерапії: КТ (17.07.2019) – збільшені лімфатичні вузли не візуалізуються, уражень кісток не виявлено. Висновок: повна ремісія.
Трепанобіопсія (17.07.2019) – ураження кісткового мозку не виявлено.
Подальші рекомендації – продовження імунохіміотерапії до 6 курсів.
Отже, у лікуванні індолентних НЛ з’явився новий лідер – обінутузумаб, ефективність якого підтверджена результатами багатоцентрових РКД. Побоювання онкогематологів щодо застосування обінутузумабу у хворих з НЛ зазвичай пов’язані з ризиком розвитку побічних реакцій на введення препарату. Але, як свідчить практика, у більшості випадків ці небажані явища розвиваються одноразово та є контрольованими.
Підготувала Ілона Цюпа
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 4 (60), 2019 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...





