Экзокринная панкреатическая недостаточность при сахарном диабете 1 и 2 типа: необходимо ли лечение?
Экзокринная и эндокринная части поджелудочной железы (ПЖ) тесно связаны между собой как анатомически, так и функционально. У пациентов, страдающих диабетом, часто возникают абдоминальные симптомы, такие как тошнота, вздутие живота, диарея, стеаторея и снижение веса. Нарушения экзокринной функции ПЖ, по-видимому, являются частыми осложнениями сахарного диабета (СД). Тем не менее они в большинстве случаев упускаются из виду. В данном систематическом обзоре подытожена информация относительно распространенности и симптоматики экзокринной панкреатической недостаточности (ЭПН) при СД, патомеханизма и сложности диагностики и терапии ЭПН.
Введение
Как уже было отмечено, экзокринная и эндокринная части ПЖ тесно связаны между собой. Таким образом, патологические состояния в экзокринной ткани могут вызывать нарушения эндокринной функции и наоборот. Под ЭПН понимают дефицит экзокринных ферментов ПЖ, который приводит к неспособности поддерживать нормальные процессы пищеварения. Основной функцией ферментов ПЖ является гидролиз белков (трипсиногены, проэластаза, мезотрипсин), углеводов (a-амилаза), липидов (липаза) и нуклеотидов (ДНКаза, РНКаза). Хронический панкреатит – наиболее частая причина развития ЭПН. Резекции желудка и ПЖ, муковисцидоз, обструкция основного протока ПЖ (например, опухоли ПЖ и ампулярные опухоли), снижение ее стимуляции (например, целиакия) или инактивация кислотой панкреатических ферментов (например, синдром Золлингера-Эллисона) также могут привести к развитию ЭПН. Кроме того, было показано, что ЭПН присутствует у значительного количества (10-74%) пациентов с СД. Однако значение этих результатов было поставлено под сомнение, и неясно, является ли диабет причиной каких-либо симптомов ЭПН, или требует какого-либо лечения ЭПН при СД.
У пациентов с СД часто возникают абдоминальные симптомы, такие как тошнота, вздутие живота, диарея, стеаторея и снижение веса. Эти симптомы могут быть связаны с побочными эффектами принимаемого метформина, влиянием вегетативной невропатии на функцию кишечника, незначительным избыточным ростом кишечной микрофлоры, целиакией или ЭПН. Нарушения экзокринной функции ПЖ у больных СД в большинстве случаев упускаются из виду. Проведение тестирования и диагностики этого состояния требует больших знаний и осведомленности. Предыдущие исследования повысили вероятность того, что заместительная ферментная терапия при ЭПН улучшает родственные симптомы и может помочь контролировать выделение глюкозы.
Цель этой статьи – провести обзор существующих представлений об ЭПН при СД.
Стратегия поиска
Систематический обзор проводился в соответствии с критериями предпочтительных данных отчетности для систематических обзоров и метаанализов (PRISMA-P) 2015 года. Был осуществлен систематический поиск в трех базах данных: Pubmed, Embase и Cohraine по следующим предметным рубрикам (MeSH): «сахарный диабет» И «функция поджелудочной железы» ИЛИ «экзокринная панкреатическая недостаточность» ИЛИ «фекальная эластаза» ИЛИ «секретин» ИЛИ «холецистокинин» ИЛИ «стеаторея» или «заместительная ферментная терапия».
Клинические исследования отвечали критериям приемлемости, если в них сообщалось о данных экзокринной функции ПЖ у взрослых пациентов с СД 1 и 2 типа. Публикации о диабете типа 3с были исключены. Копии, публикации и повторные публикации, доступные только в форме реферата, обзорные статьи были исключены. Более того, в данный систематический обзор не вошли статьи с неправильным дизайном исследования и критериями включения пациентов.
Распространенность ЭПН при СД
В последние десятилетия появилось множество сообщений об ЭПН у больных СД. В ранних исследованиях экзокринную панкреатическую функцию оценивали по методу золотого стандарта прямых панкреатических функциональных тестов (панкреозимин-секретиновый тест). ЭПН была обнаружена у 52,4% пациентов (18-100%). Однако в этих исследованиях приняло участие только небольшое количества пациентов, поскольку прямые панкреатические функциональные тесты являются инвазивными, времязатратными и дорогостоящими.
Таким образом, для оценки экзокринной функции ПЖ при СД необходим менее инвазивный, экономически эффективный тест. Тест на фекальную эластазу‑1 (ФЭ‑1) позволяет измерять уровни эластазы‑1 – протеолитического фермента, продуцируемого ацинарными клетками ПЖ. Уровень ФЭ‑1 коррелирует с выбросом других ферментов ПЖ, эластаза в кале стабильна и легко измеряется. ФЭ‑1 продемонстрировала хорошую чувствительность и специфичность при умеренной и тяжелой ЭПН. Поэтому в настоящее время измерение уровня ФЭ-1 стало инструментом скрининга при определении ЭПН. При измерении ФЭ‑1 распространенность ЭПН составляла в среднем 40% (26-74%) при СД 1 типа и в среднем 27% (10-56%) при СД 2 типа.
По результатам многих исследований, распространенность ЭПН при обоих типах диабета очень гетерогенна. Тем не менее в большинстве из этих работ учитывались случаи с предшествующим заболеванием ПЖ, что могло привести к возможному искажению результатов. В двух последних исследованиях ЭПН при СД была менее распространена, нежели в предыдущих, вероятно, из-за того, что панкреатический диабет (тип 3c, согласно новой классификации Американской диабетической ассоциации – тип 4) был исключен. Низкий уровень ФЭ‑1 был отмечен только у 5,4% из 150 пациентов с СД 1 и 2 типа после исключения пациентов, злоупотребляющих алкоголем, с операциями брюшной полости в анамнезе, другими известными причинами мальабсорбции, предшествующего заболевания ПЖ и СД, длившегося <5 лет. В другом недавнем исследовании ЭПН диагностировали путем определения концентрации ФЭ‑1 у 16,8% пациентов с диабетом 2 типа после исключения пациентов с аномальной морфологией ПЖ. Действительно, распространенность хронических заболеваний ПЖ у пациентов с диабетом может быть высокой, поскольку в недавних дискуссиях было высказано предположение о недооценке в прошлом панкреатического СД (тип 4), который мог составлять около 8% всех случаев развития диабета.
Распространенность морфологических изменений экзокринной части ПЖ при СД
В нескольких исследованиях изучались морфологические изменения экзокринной части ПЖ при СД. При гистологическом исследовании у почти 50% пациентов с СД 1 типа ПЖ атрофичная и фиброзная, с жировой инфильтрацией и потерей ацинарных клеток. При УЗИ брюшной полости, КТ или МРТ у пациентов с СД отмечалось уменьшение размера ПЖ. Патологические изменения в протоках диагностируются при помощи эндоскопической ретроградной холангиопанкреатографии у 76% больных СД. Интересно, что эти изменения в протоках не связаны с типом СД, продолжительностью заболевания или возрастом.
Патофизиология
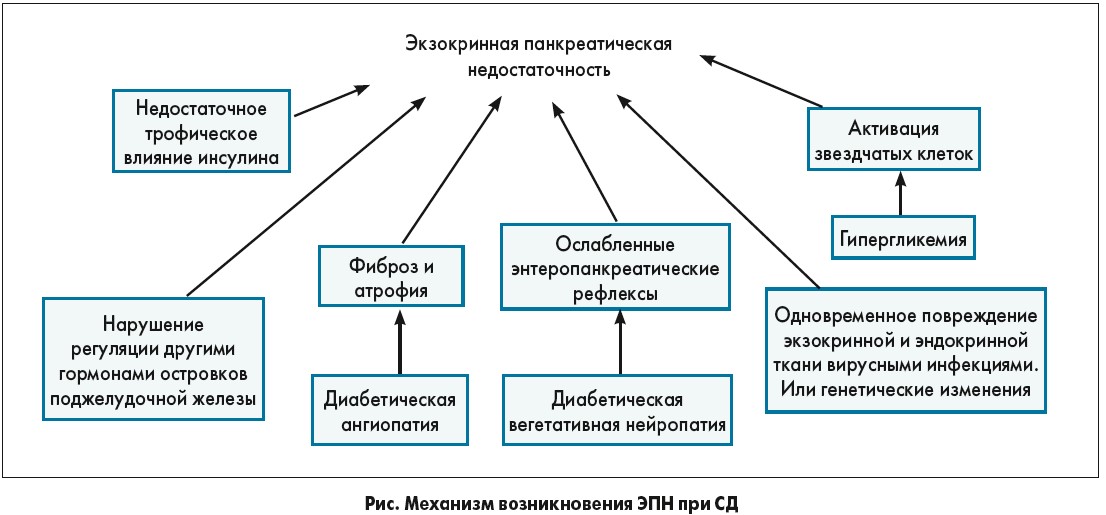
Механизм развития ЭПН при СД многофакторный (рис.). Атрофия ПЖ связана с СД и играет главную роль в развитии ЭПН.
Инсулин оказывает трофическое действие на ацинарную ткань ПЖ через инсуло-ацинарную портальную систему, поэтому уменьшение поступления инсулина может привести к атрофии ПЖ. Кроме того, было показано, что у пациентов с СД существует взаимосвязь между уменьшением объема ПЖ и ЭПН.
Установлено, что острая форма гипергликемии ингибирует базальную и стимулированную холецистокинином секрецию ферментов ПЖ посредством инсулиннезависимого механизма.
Панкреатические звездчатые клетки (ПЗК) играют решающую роль в развитии фиброза ПЖ. Было продемонстрировано, что гипергликемия способствует пролиферации и активации ПЗК и стимулирует образование коллагена ПЗК через пути протеинкиназы C и митоген-активируемой протеинкиназы p38, что приводит к фиброзу ПЖ.
Гормоны островков (например, глюкагон и соматостатин) оказывают влияние на экзокринную ткань, поэтому недостаток этих гормонов ведет к нарушению синтеза ферментов и экзокринной недостаточности.
Диабетическая микроангиопатия приводит к недостаточной перфузии через локальную микроангиопатию, к ишемии экзокринной части ПЖ, а также ее фиброзу, атрофии и ЭПН. Вегетативная нейропатия может вызвать нарушение рефлексов (энтеропатии) и ЭПН. Кроме того, вирусные инфекции, аутоиммунные реакции или генетические изменения в виде одноосновной делеции в переменном количестве тандемных повторов, содержащих экзон 11 в гене липазы эфира карбоновой кислоты, могут усиливать одновременное повреждение экзокринной и эндокринной ткани.
Более высокая распространенность ЭПН при СД 1 типа объясняется наличием более выраженного дефицита инсулина, более длительной продолжительностью заболевания и более высокой частотой микрососудистых осложнений, характерных для СД 1 типа.
Взаимосвязь между продолжительностью диабета и распространенностью ЭПН является противоречивой. В предыдущих исследованиях была описана зависимость или, по меньшей мере, небольшая взаимосвязь низкого уровня ФЭ‑1 при СД 2 типа и возраста, в котором развился диабет, продолжительностью болезни и относительно высокой концентрацией гликированного гемоглобина (HbA1c), что свидетельствует о том, что экзокринная дисфункция является долгосрочным осложнением диабета. Однако другие исследования показали, что нет никакой связи между концентрацией фекальной эластазы и продолжительностью диабета. В остальных случаях была описана обратная корреляция между продолжительностью СД и уровнем HbA1c, а также отмечалась положительная взаимосвязь уровней C-пептида и ФЭ‑1. Долгосрочное проспективное исследование обнаружило, что легкая и умеренная степени ЭПН развиваются при СД рано и не прогрессируют.
Сегодня больше внимания уделяется сигнальной функции белков при воспалении ПЖ и диабете, вызванном панкреатической недостаточностью. В предыдущем исследовании уровни общей PKB (протеинкиназы B), белков p70S6K, 4E-BP1, ERK1/2 и NF-kappa-B ПЖ у пациентов с диабетическим панкреатитом были значительно снижены по сравнению с контрольной группой, хотя благодаря фосфорилированию p70S6K1, 4E-BP1, ERK1/2 и убиквитинированию белка они существенно повысились по сравнению с контрольной группой. Можно предположить, что эти факторы отвечают за пониженный синтез ферментов и развитие атрофии ПЖ.
Симптомы ЭПН у пациентов с диабетом
Основными клиническими симптомами ЭПН являются нарушения пищеварения и мальабсорбция жиров, включая стеаторею, боль в животе, метеоризм, вздутие живота и потерю веса. Как следствие неполноценного питания ЭПН ассоциируется с низким содержанием микроэлементов в сыворотке, растворимых в липидах витаминов (витамины A, D, E и K), микроэлементов, альбумина, преальбумина и липопротеинов. Низкий уровень витамина D в сыворотке приводит к остеопорозу и повышенному риску переломов. Недостаток белков в питании и мальабсорбция витамина D и других микроэлементов имеют более высокий риск инфицирования из-за влияния на врожденные и приобретенные иммунные реакции.
Несмотря на то что ЭПН часто встречается при СД, данные о ее симптомах при диабете ограничены. Желудочно-кишечные (ЖК) симптомы часто встречаются у пациентов (27-87%) с СД 1 и 2 типов. В недавнем исследовании М.Н. Cummings и соавт. у 24% пациентов отмечались один или несколько ЖК симптомов, связанных с диагнозом ЭПН (согласно Бристольской шкале стула 5-7, стеаторея или потеря массы тела). У 42% этих пациентов был низкий уровень ФЭ‑1, что указывало на наличие ЭПН. Можно сделать вывод, что скрининг с помощью ФЭ‑1 эффективен у пациентов с ЖК симптомами, свидетельствующими об ЭПН. Более того, в этом исследовании стеаторея оказалась плохим маркером ЭПН при диабете, поскольку только у меньшего числа пациентов со стеатореей был низкий уровень ФЭ‑1. Было бы логично предположить, что у пациентов с ЭПН и диабетом снижается масса тела, то есть они имеют более низкий индекс массы тела (ИМТ). Однако существенных отличий ИМТ у пациентов с диабетом со сниженной или нормальной концентрацией ФЭ‑1 не было выявлено. Не согласовываясь с этими данными, результаты другого исследования свидетельствуют об отсутствии зависимости между размером ПЖ и ИМТ у пациентов с СД. Кроме того, ЭПН, обнаруженная при низких концентрациях ФЭ‑1, часто встречается у пациентов с диабетом и избыточной массой тела, а больные с СД и избыточной массой тела (ИМТ >25 м/кг2) могут подвергаться повышенному риску развития ЭПН.
Диагностика ЭПН
Диагностика ЭПН основывается на клинических симптомах или плохом гликемическом контроле, несмотря на сбалансированное питание, антидиабетическую терапию и соблюдение пациентом предписаний врача. Определение концентрации ФЭ‑1 – наиболее удобный способ диагностики ЭПН. Ранее было продемонстрировано, что снижение концентрации ФЭ‑1 является чувствительным методом при умеренной и тяжелой формах ЭПН (чувствительность 87% и 95% соответственно) и значительно коррелирует с прямыми панкреатическими функциональными тестами, усвоением жиров и степенью тяжести хронического панкреатита по Кембриджской классификации. Концентрация ФЭ‑1 коррелирует со степенью тяжести ЭПН: концентрация <200 мкг/г в кале указывает на наличие умеренной ЭПН, тогда как концентрация <100 мкг/г в кале свидетельствует о тяжелой степени ЭПН. Показатель активности ФЭ‑1 недостаточно чувствителен в отношении определения умеренной ЭПН, но если уровень ФЭ‑1 снижен, есть большая вероятность выявить изменения в протоках ПЖ и стеаторею.
ЭПН также может быть диагностирована с помощью дыхательного теста с использованием смешанных триглицеридов 13С путем измерения концентрации 13CO2 в выдыхаемом воздухе после употребления меченного радиоактивным изотопом пробного завтрака, содержащего известное количество жиров. Точность теста аналогична точности определения ФЭ‑1 при диагностике ЭПН.
Определение коэффициента абсорбции жиров (КАЖ) является еще одним золотым стандартом диагностики ЭПН, хотя его не определяют при СД. Во время 72-часового периода сбора кала пациент потребляет 100 г жира в сутки. Нарушение абсорбции жиров диагностируется при >7 г жира / 100 г стула в сутки, тяжелая форма стеатореи – при >15 г/сутки. Однако диагностика с помощью диеты достаточно трудоемка, 3-дневный сбор кала неудобен как для пациентов, так и для персонала лаборатории, поэтому КАЖ не применяется в рутинной клинической практике. Эту методику используют для оценки эффективности заместительной ферментной терапии (ЗФТ) при ЭПН.
Прямые панкреатические функциональные тесты считаются золотым стандартом диагностики ЭПН, и они, безусловно, имеют преимущества перед непрямыми тестами. Однако прямые тесты требуют много времени, они дорого стоят, неудобны для пациентов и доступны только в нескольких научных центрах.
Терапия
ЗФТ применяется при ЭПН для предотвращения симптомов мальабсорбции, таких как стеаторея, и для обеспечения физиологической потребности в получении питательных веществ путем коррекции нарушенного пищеварения. Вопросы эффективности ЗФТ при ЭПН, связанной с диабетом, рассматривались только в очень ограниченном количестве публикаций, и результаты исследований являются противоречивыми. В трех небольших исследованиях изучалась эффективность ЗФТ у пациентов с СД, вторичным по отношению к хроническому панкреатиту. В ходе лечения с применением ЗФТ через 6 мес у пациентов с СД, возникшим в результате тропического калькулезного панкреатита, уровень глюкозы после приема пищи и гликированного гемоглобина по сравнению с исходными данными значительно снизился. Напротив, как указывают другие авторы, при ЗФТ средние значения глюкозы не улучшались; ЗФТ вызвала потенциально опасные для жизни нарушения контроля глюкозы у инсулинозависимых пациентов с СД, возникшим на фоне хронического панкреатита.
Однако недавнее двойное слепое рандомизированное плацебо-контролируемое исследование ЗФТ у пациентов с ЭПН на фоне хронического панкреатита показало, что результаты эффективности и профиль нежелательных явлений для ЗФТ сопоставимы у пациентов с диабетом и без него. Более крупное многоцентровое двойное слепое рандомизированное плацебо-контролируемое исследование показало, что ЗФТ безопасна, но не оказывает влияния на гликемический контроль пациентов с СД, получавших инсулин, если ФЭ‑1 <100 мг/г. Уменьшение эпизодов легких и умеренных гипогликемических состояний было выявлено через 16 нед лечения при приеме четырех капсул по 10 000 ЕД ММФ панкреатина на один основной прием пищи и двух капсул по 10 000 ЕД МФФ панкреатина на один промежуточный прием пищи, что свидетельствует о более стабильном контроле влияния инсулинотерапии. Однако это исследование нельзя назвать безупречным. Во-первых, пациентов выбирали согласно наличию у них ЭПН, независимо от того, имеются ли у них симптомы, связанные с ЭПН. Во-вторых, применяемая доза панкреатина может быть низкой. В недавних клинических рекомендациях указывается, что начальная рекомендованная доза ЗФТ должна составлять 50 000 МЕ липазы на один основной прием и 25 000 МЕ на каждый перекус, титрование допускается согласно наличию симптомов. Однако недавно полученные результаты подтверждают, что даже такая доза ЗФТ может оказаться недостаточной для нормализации пищеварения.
Секреция глюкозозависимого инсулинотропного полипептида (ГИП), индуцированного в ответ на прием пищи, снизилась у пациентов с ЭПН. Было продемонстрировано, что ЗФТ оказывает обратное влияние на нарушенный ответ на ГИП и, следовательно, восстанавливает инкретиновый эффект жиров. Эффект ЗФТ может быть полезен при гликемическом контроле пациентов с СД и ЭПН.
Несмотря на то что пациенты с диабетом и пониженной концентрацией ФЭ‑1 могут не жаловаться на наличие ЖК симптомов, связанных с ЭПН, они все равно могут страдать от нарушенного обмена жиров, например от недостатка витамина D, как уже предполагалось ранее. Кроме того, у пациентов с СД имеется повышенный риск переломов костей. Показано, что ЗФТ повышает уровень витамина D в сыворотке крови у пациентов с СД и ЭПН, что важно для снижения повышенного риска переломов.
В нашем систематическом обзоре есть несколько ограничений. Во-первых, распространенность ЭПН при обоих типах диабета очень гетерогенна и варьирует от 5,1 до 80%. Во-вторых, примененный в исследовании золотой стандарт прямых панкреатических тестов для диагностики ЭПН, а именно секретин-панкреозиминовый тест, ограничивается небольшим числом пациентов из-за его инвазивности. В-третьих, в большинстве исследований учитывались случаи с предшествующим заболеванием ПЖ, что могло повлечь возможное искажение результатов. В-четвертых, несмотря на то что ЭПН часто встречается при СД, данные о симптомах ЭПН при диабете недостаточны. Кроме того, вопросы эффективности ЗФТ при ЭПН, связанной с диабетом, рассматривались только в очень ограниченном количестве публикаций, и результаты исследований являются противоречивыми.
Заключение
Имеющихся на сегодня данных недостаточно, чтобы ответить на вопрос об эффективности ЗФТ при гликемическом контроле у пациентов с СД и ЭПН. Несомненно, существует необходимость в дальнейших рандомизированных клинических исследованиях. Пока можно только предложить подбирать ЗФТ пациентам с СД в зависимости от абдоминальных симптомов, которые могут быть связаны с ЭПН, и с учетом результатов анализа сывороточных пищеварительных факторов и уровня витамина D.
В случае положительного ответа на прием ферментных препаратов рекомендуется продолжать ЗФТ.
Zsori G, et al., Exocrine pancreatic insufficiency in type 1 and type 2 diabetes mellitus: dowe need to treat it? Asystematic review // Pancreatology (2018). Р. 1-7.
Список литературы находится в редакции.
Сокращенный пер. с англ. Ирины Романовой
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (47) жовтень 2019 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....