Результаты исследования эффективности и переносимости препарата Тиворель® в комплексном лечении пациентов с острым коронарным синдромом без подъема сегмента ST и нестабильной стенокардией
Смертность при обострении ишемической болезни сердца (ИБС), в частности при остром коронарном синдроме (ОКС), остается сравнительно высокой. Назначение стандартной медикаментозной терапии, а так же использование методов реканализации инфаркт-зависимой коронарной артерии позволяют значительно улучшить результаты лечения данной категории больных, однако не всегда оправдывают ожидания клиницистов. Более того, восстановление кровотока в коронарных артериях может сопровождаться усугублением его повреждения, что актуализирует проблему защиты миокарда при ОКС. Для предупреждения возникновения осложнений ОКС необходимо уменьшить прогрессирующее повреждение кардиомиоцитов и выраженность нарушений метаболизма миокарда, возникающие с первых секунд развития ишемии.
Именно поэтому кардиологи в последнее время интенсивно разрабатывают методы метаболической коррекции состояний, обусловленных ишемией/реперфузией при лечении острых и хронических форм ИБС, в частности методы миокардиальной цитопротекции. Если ранее усилия исследователей концентрировались на изучении метаболических свойств гемодинамически активных лекарственных средств, то в последнее время все большее внимание уделяется препаратам, обладающим свойствами антиоксидантов, мембранопротекторов и ингибиторов катаболических ферментов. К их числу относятся аминокислоты левокарнитин (L-карнитин) и аргинина гидрохлорид.
L-карнитин играет важную роль в процессе β-окисления жирных кислот (ЖК), то есть в выработке энергии в митохондриях. При этом L-карнитин выступает в качестве специфического ко-фактора, контролирующего скорость окисления длинноцепочечных ЖК и облегчающего их перенос через внутреннюю мембрану митохондрий. Кроме того, L-карнитин участвует в удалении избытка ЖК из митохондрий, а затем и из цитоплазмы, предупреждая таким образом развитие цитотоксического эффекта. В условиях ишемии в митохондриях накапливается ацилкоэнзим А, баланс которого со свободным коэнзимом А поддерживается за счет работы так называемого карнитинового челнока, транспортирующего ацильные остатки ЖК. Удаляя из митохондрии избыток ацетильных групп, L-карнитин способствует образованию малонил-коэнзима А, который тормозит работу карнитинового челнока и тем самым в условиях ишемии снижает скорость β-окисления ЖК.
Показано, что уровень L-карнитина в миокарде снижается при ИБС, остром инфаркте миокарда (ОИМ) и сердечной недостаточности различного генеза. Аргинин относится к классу условно незаменимых аминокислот, является активным и разносторонним клеточным регулятором многочисленных жизненно важных функций организма и оказывает значимые протекторные эффекты: антигипоксический, мембраностабилизирующий, цитопротекторный, антиоксидантный, дезинтоксикационный. Аргинин участвует в регуляции промежуточного обмена и процессов энергообеспечения и играет определенную роль в поддержании гормонального баланса в организме. Известно, что аргинин увеличивает содержание в крови инсулина, глюкагона, соматотропного гормона и пролактина, принимает участие в синтезе пролина, полиамина агматина, включается в процессы фибриногенолиза и сперматогенеза. Аргинин является субстратом для образования NО-синтазы – фермента, катализирующего синтез оксида азота в эндотелиоцитах. Препарат активирует гуанилатци клазу и повышает уровень циклического гуанидинмонофосфата (цГМФ) в эндотелии сосудов, уменьшает активацию и адгезию лейкоцитов и тромбоцитов, угнетает синтез молекул адгезии VCAM-1 и MCP-1, подавляет синтез эндотелина-1, который является мощным вазоконстриктором и стимулятором пролиферации и миграции гладких миоцитов сосудистой стенки. Аргинин подавляет также синтез асимметричного диметиларгинина – мощного эндогенного стимулятора оксидативного стресса.
Есть основания полагать, что ургентная терапия с использованием внутривенного введения L-карнитина и аргинина гидрохлорида является патогенетически обоснованным методом, который позволит уменьшить выраженность нарушений метаболизма миокарда при ОКС и реперфузионном синдроме.
Вышеизложенное определяет актуальность и практическую значимость данного исследования, в котором оценивали эффективность и переносимость препарата Тиворель® (ООО «Юрия-Фарм»), содержащего L-карнитин (20 мг) и аргинина гидрохлорид (42 мг), в комплексном лечении пациентов c ОКС без стойкого подъема сегмента ST и нестабильной стенокардией в сравнении с группой больных, получавших только базисную терапию.
Объект и методы исследования
Дизайн исследования
Настоящее исследование было выполнено в соответствии с требованиями, предъявляемыми ГП «Государственный экспертный центр МЗ Украины» к клиническим испытаниям лекарственных средств. Исследование проводилось как открытое рандомизированное сравнительное параллельное в двух группах и включало следующие этапы: скрининг и период терапии (10 дней). В исследовании приняли участие 100 пациентов с ОКС без подъема сегмента ST, которые были распределены для лечения в основную и контрольную группы в соотношении 1:1.
Пациенты основной группы, кроме базисной терапии (согласно приказу МЗ № 164: нитроглицерин сублингвально, ацетилсалициловая кислота или клопидогрель, анальгетики, β-адреноблокаторы или ингибиторы АПФ), получали препарат Тиворель® 100 мл внутривенно капельно со скоростью 10 капель в минуту за первые 10-15 мин (затем скорость введения можно было увеличивать до 30 капель в минуту) 1 раз в сутки в течение 10 дней. Пациентам контрольной группы назначали только базисную терапию. В процессе проведения исследования не разрешалось назначать нейрометаболические и ноотропные препараты. Пациенты были госпитализированы в отделение реанимации и интенсивной терапии с диагнозом ОКС без подъема сегмента ST в первые 12 ч с момента развития заболевания.
Критерии включения в исследование: наличие типичного болевого синдрома в покое продолжительностью более 10 мин или учащение и утяжеление приступов стенокардии с отсутствием или уменьшением эффекта от приема нитроглицерина в течение последних 24 ч до госпитализации без подъема сегмента ST. Выбранным критериям включения в основном соответствовали больные с передней локализацией ИМ и нестабильной стенокардией.
Критерии невключения:
• повышенная чувствительность к компонентам исследуемого препарата;
• беременность и лактация;
• дегенеративные заболевания центральной нервной системы (болезнь Альцгеймера, болезнь Паркинсона, эссенциальный тремор);
• почечная и печеночная недостаточность;
• сахарный диабет;
• онкологические заболевания;
• злокачественные формы миастении;
• распространенные формы аллергических дерматитов;
• рассеянный склероз;
• нарушение функции печени и/или почек;
• острый тромбофлебит;
• выраженные нарушения сердечного ритма (тахикардия >100 уд/мин, частые суправентрикулярные и желудочковые экстрасистолы, мерцательная аритмия);
• тяжелая дыхательная недостаточность;
• тромбоэмболия легочной артерии;
• миокардит, эндокардит;
• эндокринные заболевания (диффузный токсический зоб, гипотиреоз, надпочечниковая недостаточность);
• участие в другом клиническом исследовании того же вещества или любого изучаемого препарата
в течение 30 дней до включения в данное исследование (любой препарат, способный повлиять на оценку терапевтического эффекта; прием до включения в исследование любого препарата, применение которого недопустимо на протяжении 2 мес перед визитом);
• вероятность не выполнения больными требований протокола или неспособность выполнить их, включая предоставление информированного согласия (неспособность дать информированное согласие из-за умственной отсталости или языкового барьера).
По данным эхокардиографии (ЭхоКГ), выполненной при поступлении больных, среднее значение
фракции выброса левого желудочка (ФВ ЛЖ) между группами достоверно не различалось: в основной группе этот показатель составил 55±10,6%, в контрольной – 54,1±10,5%. По выраженности субъективных жалоб и клинических проявлений ОКС группы статистически значимо не различались.
Таким образом, в клиническое исследование были включены две группы участников по 50 человек, которые соответствовали и были сопоставимы по основным критериям отбора.
Оценка эффективности лечения
Эффективность лечения оценивали с помощью следующих методов. Лабораторные методы: определение маркеров некроза миокарда – тропонина Т, общей креатинфосфокиназы (КФК), КФК-МВ – каждые 6 ч в течение первых суток госпитализации, в последующем учитывали максимальные значения маркеров.
Инструментальные методы исследования: ЭКГ в 12 отведениях, ЭхоКГ. С целью изучения внутри -сердечной гемодинамики проводили секторальную ЭхоКГ с расчетом основных показателей структуры и функции сердца в соответствии с рекомендациями Американской ассоциации эхокардиографии. Выполняли обязательный расчет конечно-диастолического и конечно-систолического индексов (КДИ и КСИ соответственно) и ФВ ЛЖ.
Конечные точки исследования
Главная переменная
отсутствие клинических признаков и ЭКГ-параметров ишемии миокарда;
• стабилизация состояния (отсутствие ИМ, внезапной смерти).
Вторичные переменные
• оценка динамики выраженности клинических признаков ишемии миокарда;
• динамика кардиологических ферментов и ЭКГ-критериев.
Общую эффективность лечения оценивали по категориальной переменной, описание которой представлено в таблице 1.

Оценка переносимости
Переносимость исследуемого препарата оценивали на основании:
• объективных данных, полученных исследователем в ходе проведения исследования. С этой целью во время каждого визита проводили объективный осмотр пациентов, включающий измерение частоты сердечных сокращений (ЧСС), уровня артериального давления (АД), ЭКГ, аускультацию сердца и легких; осмотр кожи и видимых слизистых оболочек;
• данных лабораторного обследования, производимого до начала и по завершении курса лечения исследуемым препаратом:
– общий анализ крови: эритроциты, гемоглобин, гематокрит, лейкоциты, тромбоциты, скорость оседания эритроцитов;
– общий анализ мочи;
– биохимический анализ крови (общий белок, уровни аланинаминотрансферазы, аспартатаминотрансферазы, холестерина крови, креатинина, глюкозы, сердечных тропонинов Т/І);
• субъективных ощущений пациента. Во время каждого визита исследователи проводили опрос пациента, при котором учитывали наличие и степень выраженности как прогнозируемых, так и неожиданных побочных реакций.
Критериями отмены препарата являлись увеличение активности трансаминаз в ≥3 раза по сравнению с верхней границей нормы, повышение уровня креатинина в крови, возникновение миалгий, мышечной слабости и других симптомов непереносимости препарата, а также отказ больного от продолжения лечения.
Методы статистического анализа полученных данных
Результаты исследований обрабатывали с помощью критериев Стьюдента, Шапиро-Уилка, χ2 Пирсона с поправкой Йетса, Манна-Уитни, Фишера.
Результаты исследования
Эффективность лечения
Установлено, что препарат Тиворель®, назначенный в составе комплексной терапии сразу же после поступления больных в стационар, улучшает электро-физиологические свойства миокарда и предупреждает появление временных нарушений ЭКГ. У пациентов основной группы уже в первые сутки после развития ОИМ реже регистрировались поздние потенциалы желудочков (ППЖ), маркеры так называемого аритмогенного субстрата – 9,6% по сравнению с 19,8% у больных контрольной группы. В ходе дальнейшего наблюдения ППЖ в контрольной группе исчезали, а на фоне лечения препаратом Тиворель® – не возникали. Это позволяет предположить наличие выраженного антиишемического эффекта препарата, что подтверждается и клиническими данными.
Нами отмечена достоверно выраженная положительная динамика изменений конечной части желудочкового комплекса под влиянием терапии с препаратом Тиворель®. При анализе стандартных ЭКГ и данных суточного мониторирования ЭКГ у ряда больных выявлялись нарушения ритма. Достоверных различий между группами по частоте встречаемости всех проявлений аритмического синдрома как исходно, так и после терапии не наблюдалось, однако в основной группе в процессе лечения достоверно уменьшилось количество случаев желудочковых нарушений ритма в виде групповой желудочковой экстрасистолии и пробежек желудочковой тахикардии.
За период стационарного лечения у всех пациентов отмечена положительная клиническая динамика: уменьшение частоты и тяжести приступов стенокардии, снижение уровня АД, повышение толерантности к физическим нагрузкам. Уже на третьи сутки лечения с использованием исследуемого препарата Тиворель® реже возникали рецидивы ангинозной боли (20,8% случаев в основной группе и 32,0% – в контрольной). При этом наблюдалось снижение потребности в использовании наркотических аналгетиков с целью купирования рецидивирующего болевого синдрома (22,1 и 36,2% случаев соответственно). Кроме того, на третьи сутки после развития ОИМ у больных основной группы по сравнению с контрольной регистрировали меньшую частоту случаев атриовентрикулярных блокад (4,2 и 12,6% соответственно). В ходе анализа всего госпитального периода установлено, что у больных, получавших Тиворель®, почти в 3 раза реже, чем в группе контроля, возникали атриовентрикулярные блокады. Частота регистрации желудочковой экстрасистолии снижалась на 7-е (на 36,2%) и 10-е сутки (на 44,6%) заболевания.
Основными факторами, определяющими летальность и неблагоприятный отдаленный прогноз
у больных ОКС, была масса некротизированного миокарда и скорость формирования зоны некроза.
Для выявления некроза в миокарде определяли уровень сердечных тропонинов, а также МВ фракции КФК. Пик КФК у больных основной группы составил 3,16±0,09 мккат/л, у больных контрольной группы – 3,21±0,12 мккат/л; МВ-КФК – 0,24±0,02 и 0,25±0,01 мккат/л соответственно, что свидетельствует о несущественных различиях объема изначально некротизированного миокарда. Введение препарата Тиворель® в первые часы на фоне стандартной терапии ОКС без подъема сегмента ST привело к уменьшению времени достижения пика активности КФК у больных основной группы (13,5±0,6 против 17,1±0,8 мккат/л у больных контрольной группы); уровень МБ-КФК составил 9,9±0,4 и 13,9±0,6 мккат/л соответственно. При этом зона некротического поражения (рассчитанная по изменениям активности МБ-КФК в сыворотке крови) была на 26,4% меньше у больных основной группы по сравнению с контрольной – 45,4±2,1 г/экв. и 61,6±2,9 г/экв. Это было обусловлено сокращением периода нормализации активности КФК и МБ-КФК в сыворотке крови в среднем на 8,1 и 9,4 ч соответственно. Сравнительно раннее наступление пика активности кардиоспецифических ферментов (КФК, МБ-КФК) свидетельствует о более быстром формировании зоны некроза, а сокращение сроков их вымывания – о предупреждении дальнейшего повреждения жизнеспособных кардиомиоцитов у больных основной группы.
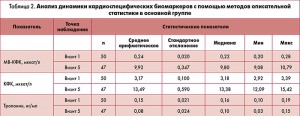
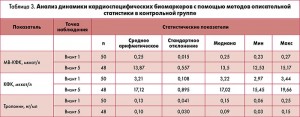
Анализ эффективности по динамике кардиоспецифических биомаркеров
Анализ динамики маркеров некроза миокарда – тропонина Т, общей КФК, КФК-МВ – в группах наблюдения с помощью методов описательной статистики представлен в таблицах 2 и 3.
В результате проведенного статистического анализа полученных данных выявлены значимые изменения кардиоспецифических биомаркеров в обеих группах. Повышенный уровень сердечных тропонинов отражает повреждение кардиомиоцитов, которое при ОКС без подъема сегмента ST может быть связано с дистальной эмболизацией тромбоцитарными тромбами, образующимися в области разрыва или эрозии бляшки.
У больных основной группы содержание тропонина в крови составляло 0,15±0,02 нг/мл, в контрольной – 0,13±0,05 нг/мл. Увеличение уровня тропонина сопровождалось клиническими проявлениями ишемии миокарда (боль в груди, изменения на ЭКГ и появление асинергии стенки сердца). У большинства пациентов, как в основной, так и в контрольной группе, через 48-72 ч уровень тропонина нормализовался и составил 0,08±0,02 и 0,1±0,03 нг/мл соответственно.
Анализ эффективности по степени выраженности субъективных жалоб больных, характерных для ОКС
В ходе исследования отмечен ряд позитивных общеклинических сдвигов, а также наблюдалось значимое уменьшение выраженности субъективных жалоб участников начиная со второго визита в обеих группах пациентов. В основной группе наблюдения быстрее происходило обратное развитие болевого синдрома, чем в контрольной. Так, в первые 12 ч с момента возникновения интенсивного болевого синдрома достоверной разницы в его выраженности между группами не наблюдалось. На 3-й день лечения в сравнении с 1-м днем в обеих группах интенсивность болевого синдрома значительно уменьшилась. С 7-го дня терапии степень болевого синдрома начала более выраженно снижаться в основной группе в сравнении с контрольной группой. К окончанию срока наблюдения эта тенденция сохранилась. Уменьшение интенсивности и снижение частоты ангинозных болей сопровождались уменьшением потребности больных основной группы в нитратах. Опрос пациентов в ходе исследования показал, что введение препарата Тиворель® с первых дней развития ОКС положительно влияет на выраженность субъективных жалоб больных.
У пациентов основной группы к 10-м суткам отмечалось значительное снижение степени выраженности таких субъективных ощущений, как чувство страха, внутреннее беспокойство, слабость, боль в области сердца или в других участках грудной клетки, ощущение нехватки воздуха. Применение препарата Тиворель® на фоне традиционной терапии ОКС без подъема сегмента ST оказало положительное влияние в комплексной терапии на основные клинические показатели.
Изменение ЭхоКГ-показателей у больных ОКС без подъема сегмента ST на фоне разных вариантов лечения
До поступления в стационар и через 10 дней с момента госпитализации при стабилизации состояния проводили ЭхоКГ. Определяли следующие параметры: конечные диастолический и систолический объемы и размеры ЛЖ (КДО и КСО; КДР и КСР), ФВ, ударный объем ЛЖ, оценивали диастолическую функцию ЛЖ. Согласно данным ЭхоКГ обе группы были исходно сопоставимы по всем изучаемым показателям, характеризующим как систолическую, так и диастолическую функции ЛЖ. В динамике наблюдения не выявлено существенных изменений величины полости ЛЖ (оценивали КДИ) в обеих группах. В то же время в основной группе в отличие от группы контроля отмечалось достоверное повышение ФВ ЛЖ уже через 7 суток лечения. При оценке результатов динамического исследования ЭхоКГ в основной группе на фоне стандартной терапии установлено, что раннее назначение препарата Тиворель® положительно влияет на гемодинамику, уменьшая дилатацию полости ЛЖ, что приводит к снижению КСО ЛЖ на 10-е сутки наблюдения. В то же время в контрольной группе отмечалась тенденция к повышению КДИ на 7-е и 10-е сутки ОИМ. ФВ ЛЖ увеличивается у больных обеих групп, но ее прирост на 10-е сутки ОИМ более значителен в о сновной группе: 9,3 и 6,1% соответственно.
Представленные ЭхоКГ-данные позволяют заключить, что применение препарата Тиворель® в составе базисной стандартной терапии достоверно и эффективно влияет на ремоделирование ЛЖ при ОКС без подъема сегмента ST.
Оценка общей эффективности лечения исследуемым и референтным препаратами
Оценка общей эффективности препаратов была проведена с помощью интегральной переменной,
которая включала стабилизацию состояния пациента, наличие осложнений, случаев повторного ИМ и внезапной смерти. У больных основной группы был зарегистрирован один Q-образующий ИМ и один ИМ без зубца Q в контрольной группе. Причины развития ИМ прямо не зависели от лечения и были связаны с длительностью и интенсивностью болевого синдрома до начала терапии и несоблюдением пациентами предписанного им ограничения двигательного режима. В обоих случаях ИМ протекал без осложнений и развился в первые 12 ч с момента поступления в стационар. В общем числе наблюдений (95) 2 случая ИМ составили 2,1%, по отношению к 47 больным основной группы – 2,1% и к 48 больным контрольной группы – 2,0%. Ни в одной из групп летальных исходов по причине ОКС не зарегистрировано.
На основании полученных результатов можно сделать вывод о том, что по эффективности лечения группы статистически значимо отличались.
Таким образом, применение препарата Тиворель® в основной группе пациентов, помимо достоверно более ранней стабилизации симптоматики ОКС, позволяло достичь достоверного снижения ранней постинфарктной стенокардии и жизнеугрожающей желудочковой тахиаритмии (фибрилляция желудочков/желудочковая тахикардия).
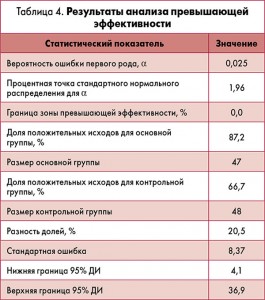
Оценка превышающей эффективности
Вывод о превышающей эффективности лечения с применением исследуемого препарата Тиворель® сделан с учетом доверительных интервалов (ДИ). Так как главная переменная эффективности – дихотомическая, то была вычислена разность долей положительных результатов в группах, оценены границы 95% ДИ для этой разности и выполнено сравнение нижней границы 95% ДИ с границей зоны превышающей эффективности (0%). Результаты вычислений приведены в таблице 4.
Таким образом, в связи с тем, что нижняя граница 95% ДИ для разности долей больше границы зоны превышающей эффективности (0%), можно сделать вывод, что комплексная терапия ОКС с применением исследуемого препарата Тиворель® (ООО «Юрия-Фарм») превосходит по эффективности стандартную терапию.
Анализ переносимости
Больные хорошо переносили внутривенное введение препарата Тиворель®. Лечение с применением исследуемого препарата в составе базисной терапии не оказало отрицательного влияния на количественные биохимические маркеры периферической крови, характеризующие состояние печени, углеводного, липидного и азотистого обмена. Разница показателей у пациентов основной и контрольной групп на всех этапах исследования была статистически незначимой. За время исследования показатели гемодинамики пациентов основной и контрольной группы были стабильными. Согласно полученным результатам ЧСС, систолическое и диастолическое АД у пациентов основной и контрольной групп существенно не отличались.
У всех пациентов как основной, так и контрольной групп переносимость препарата оценена как хорошая.
Ни у одного из пациентов не отмечались побочные явления, как местного, так и общего характера, развитие которых можно было бы связать с применением исследуемого препарата Тиворель®.
Выводы
1. Применение исследуемого препарата Тиворель® производства ООО «Юрия-Фарм» дополнительно к базисной терапии способствует оптимизации ведения больных ОКС без подъема сегмента ST. При комплексном лечении с применением препарата Тиворель® наблюдается более быстрый регресс клинических проявлений ОКС.
2. Использование в терапии ОКС без подъема сегмента ST препарата Тиворель® стабилизирует состояние больных и снижает частоту развития осложнений.
3. Препарат Тиворель® хорошо переносится пациентами, не вызывает серьезных побочных реакций и не оказывает отрицательного влияния на показатели лабораторных исследований крови и мочи.
4. Терапия с применением препарата Тиворель® по критерию общей эффективности превосходит стандартную терапию в лечении больных с ОКС без подъема сегмента ST.
Список литературы находится в редакции.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....