Чорнобильська катастрофа та тиреоїдна патологія: 30 років потому

26 квітня виповнилося 30 років з моменту аварії на Чорнобильській атомній електростанції (ЧАЕС) – катастрофи, що вважається найбільшою за всю історію ядерної енергетики як за кількістю потерпілих людей, так і за економічним збитком. Більш того, за масштабами рукотворного забруднення екосфери Чорнобильська катастрофа взагалі не має аналогів серед усіх трагедій, які пережило людство. І на жаль, питання Чорнобиля досі не закрите. Ще не одне покоління українців відчує на собі дію радіоактивних викидів, що мали місце в перші дні аварії. Отже, тема медичних наслідків аварії на ЧАЕС не втрачає своєї актуальності, і напередодні 30-ї річниці українські вчені та гості з закордону зібралися на Міжнародній науковій конференції «Радіологічні та медичні наслідки Чорнобильської катастрофи – тридцять років потому», щоб обговорити набутий досвід. Чимало доповідей, що прозвучали в межах цього наукового заходу, стосувались патології щитоподібної залози (ЩЗ) – органу, найбільш чутливого до радіоактивних ізотопів йоду. Огляд кількох з них пропонуємо нашим читачам.
 Про зв’язок аварії на ЧАЕС з ростом поширеності раку ЩЗ у дітей в Україні розповів директор ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка», академік НАМН України, член-кореспондент НАН України, доктор медичних наук, професор Микола Дмитрович Тронько.
Про зв’язок аварії на ЧАЕС з ростом поширеності раку ЩЗ у дітей в Україні розповів директор ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка», академік НАМН України, член-кореспондент НАН України, доктор медичних наук, професор Микола Дмитрович Тронько.
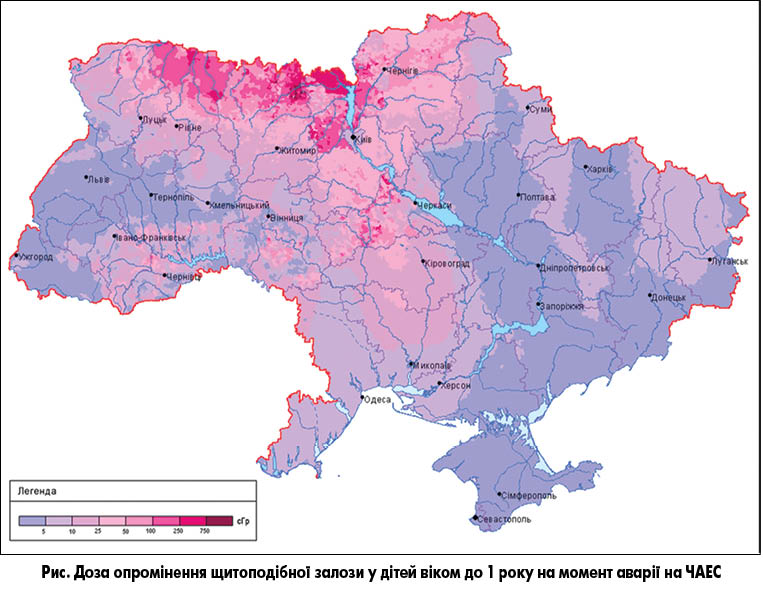
Доповідач нагадав, що більше 80% радіоактивних ізотопів, що потрапляють в атмосферу після вибуху атомного реактора, становлять ізотопи радіоактивного йоду (I131), який в організмі людини вибірково поглинається тільки клітинами ЩЗ. Саме цей орган є найбільш вразливою мішенню для радіаційного опромінення, особливо у дітей і підлітків (рис.).
Після аварії на ЧАЕС витік I131 був надзвичайно високим (40-50 млн Кюрі) – у 10 разів вищим, ніж після аварії станції Фукусима (2011) та в сотні й тисячі разів більшим, ніж після інших аварій на атомних станціях. Найбільш забрудненими I131 виявилися Київська, Чернігівська, Житомирська, Черкаська та Рівненська області. Діти, що проживали в цих областях, отримали в середньому по 0,2-0,3 Гр навантаження на ЩЗ, а в епіцентрі – більше 0,6 Гр.
Наслідки аварії на ЧАЕС відносно здоров’я ЩЗ у дітей та підлітків, що проживали на момент аварії у найбільш забруднених регіонах, було вивчено у рамках українсько-американського тиреоїдного проекту. З метою визначення ризику розвитку раку та іншої патології ЩЗ (гіпотиреоз, аутоімунний тиреоїдит, доброякісні пухлини) в проспективне когортне дослідження включали жителів України, що були опромінені у дитячому та підлітковому віці внаслідок аварії на ЧАЕС і мали прямі виміри активності ЩЗ в травні-червні 1986 року.
До дослідження було залучено 13 243 дитини, що були умовно розділені на три групи залежно від дозового навантаження на ЩЗ: дозова група А (низька доза – менше 0,3 Гр) – 57%, дозова група В (середня доза – 0,3-1 Гр) – 26,1%, дозова група С (висока доза – більше 1 Гр) – 16,9%. Ця когорта була відібрана у 1998 р., після чого в її учасників кожні два роки проводили скринінг на захворювання ЩЗ.
З початку спостереження і до теперішнього часу в учасників дослідження, що проживали в Київській, Чернігівській та Житомирській областях, було діагностовано 179 випадків раку ЩЗ. За морфологічною характеристикою це були переважно папілярні карциноми (близько 93%), рідше – фолікулярні (5%) та медулярні (2%).
Після першого скринінігу було виявлено 45 випадків раку ЩЗ з наступною поширеністю по групах: 1,7% у групі А (14 випадків), 3,2% у групі В (10 випадків) та 10,6% у групі С (21 випадок). Отримані дані свідчать, що захворюваність на рак ЩЗ зростає із збільшенням дозового навантаження на ЩЗ. Ця тенденція зберігалась і на етапі другого скринінгу, однак різниця між захворюваністю на рак ЩЗ в групах дещо зменшилась, склавши – 1,7; 2,8 та 6% у групах А, В і С відповідно. Після третього та четвертого скринінгу захворюваність на рак ЩЗ у досліджуваних групах виявилася приблизно однаковою. Нещодавно були отримані результати п’ятого скринінгу, однак вони потребують статистичної обробки.
Таким чином, перший скринінг продемонстрував чітку залежність захворюваності на рак ЩЗ від індивідуальної дози опромінення ЩЗ. Показник відносного ризику в досліджуваній когорті становив 5,25 на кожен Гр опромінення (95% ДІ від 1,70 до 27,5). Тобто при відсутності впливу радіації внаслідок аварії на ЧАЕС в досліджуваній когорті на момент проведення першого скринінгу можна було б очікувати 11,2 випадку раку ЩЗ порівняно з 45 виявленими. В подальшому відносний ризик раку ЩЗ залежно від дози опромінення поступово зменшувався та, за даними подальших скринінгів, сягав у середньому 1,9 на кожен Гр опромінення (95% ДІ від 0,43 до 6,34).
На завершення своєї доповіді академік М.Д. Тронько зазначив, що поширеність раку ЩЗ й досі залишається високою, в основному за рахунок осіб, які на момент Чорнобильської катастрофи були дітьми чи підлітками. Нарізі спільно з американськими колегами проводиться вивчення механізмів радіоіндукованого раку ЩЗ та пошук нових біомаркерів, що могли б передбачити ризик розвитку цього захворювання ще до появи його клінічних симптомів.
 Керівник відділу епідеміології ендокринних захворювань ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук, професор Віктор Іванович Кравченко присвятив доповідь питанням йодного забезпечення дитячого населення постраждалих після аварії на ЧАЕС регіонів, представивши відповідні результати українсько-американського проекту.
Керівник відділу епідеміології ендокринних захворювань ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук, професор Віктор Іванович Кравченко присвятив доповідь питанням йодного забезпечення дитячого населення постраждалих після аварії на ЧАЕС регіонів, представивши відповідні результати українсько-американського проекту.
Дослідження йодного статусу проводили у осіб, що були дітьми на період аварії та проживали у постраждалих після аварії регіонах (Київська область: Іванківський район, евакуйовані діти в м. Києві; Житомирська область: Народицький та Овруцький райони; Чернігівська область: м. Чернігів, Козелецький, Ріпкинський, Чернігівський райони). У якості основного критерію оцінки йодного статусу використовували середній рівень його екскреції з сечею (медіана йодурії): нормальне забезпечення йодом – понад 100 мкг/л, йодний дефіцит легкого ступеня – 50-100 мкг/л, середнього ступеня – 20-50 мкг/л, тяжкий – менше 20 мкг/л.
Дослідження складалося з чотирьох циклів. У першому циклі (1998-2000) проводили аналіз зразків сечі 11 926 пацієнтів, у другому (2001-2003) – 11 997, у третьому (квітень 2003 – березень 2005) – 10 868, у четвертому (квітень 2005 – квітень 2007 року) – 8083. Загальна чисельність української когорти, що брала участь у проекті, становила 13 243 осіб віком 0-18 років на момент аварії на ЧАЕС.
Результати першого циклу показали, що для всього північного регіону вкрай актуальною була проблема йододефіциту. Показники медіани йодурії становили в середньому 40-50 мкг/л. Найгіршою ситуація виявилась в Житомирській і Чернігівській областях, в деяких районах цих областей мода йодурії (значення показника, що зустрічається найбільш часто) становила менше 20 мкг/л. На актуальність проблеми йодної недостатності в північному регіоні України вказувало і те, що тільки 12,7% проб мали нормальний (>100 мкг/л) вміст йоду, тоді як більше половини проб знаходились в зоні тяжкого і середнього йодного дефіциту. Опитування обстежених у цьому проекті дітей та їх батьків показало, що в період 1998-2000 рр. харчову йодовану сіль вони майже не використовували. Це яскраве свідчення практично повної відсутності йодної профілактики на той час.
В подальшому був проведений аналіз зв’язку даних медіани йодурії з дозами опромінення ЩЗ. Виявилося, що в першому циклі дослідження у групі з рівнем дозового навантаження >1 Гр була найменша йодна забезпеченість (медіана йодурії 41,2 мкг/л) та, навпаки, в групі з найменшою дозою опромінення ЩЗ (<0,3 Гр) був найвищий йодний статус (медіана йодурії – 47,0 мкг/л). Група із середньою дозою опромінення (0,3-0,99 Гр) мала проміжний порівняно з іншими групами показник медіани йодурії з вірогідною відмінністю від першої групи.
Результати оцінки йодного статусу у другому циклі дослідження незначно відрізнялися від попередніх. В цілому вираженість йодної недостатності залишалася близькою до першого циклу, оскільки трохи більше 50% проб продовжували знаходитися в зоні тяжкого і помірного дефіциту, і тільки 17,8% показників йодурії були вищими за 100 мкг/л.
У третьому циклі дослідження йодна забезпеченість як у цілому по регіону, так і по окремих районах зросла на 50% і більше, причому в середньому по північному регіону України медіана йодурії становила близько 70 мкг/л. Суттєве поліпшення ситуації щодо йодного забезпечення підтверджують також результати розподілу даних йодурії. На цей час дослідження третина результатів (37,2%) знаходилася в зоні слабкого йодного дефіциту, а ще в третині зразків були нормальні показники. Такі зміни в йодному статусі збігаються в часі з прийняттям Державної програми профілактики йодної недостатності в Україні. Йодовану сіль згідно з результатами опитування на той момент вживали вже 20-60% домогосподарств.
У четвертому циклі дослідження майже по всіх районах, як і в попередньому циклі, зберігався йодний дефіцит слабкого ступеня, 34% зразків демонстрували нормальні показники і тільки 4,5% відповідали критеріям тяжкої йодної недостатності. В межах когорти найкраща ситуація спостерігалася в окремих районах Київської та Чернігівської областей з відносно високою частотою нормалізації йодного статусу.
Та на жаль, дослідження, проведені у 2011-2014 рр. в Київській, Житомирській та Чернігівській областях, показали, що на цих територіях йодний дефіцит все ще зберігається та чинить додатковий негативний вплив на здоров’я мешканців, які зазнали впливу радіаційного опромінення після аварії на ЧАЕС. Частота вузлового та дифузного зобу у населення цього регіону сягає 20%.
На завершення доповідач підкреслив, що ліквідація йододефіциту – важливий шлях до запобігання захворюванням ЩЗ та поліпшення здоров’я населення північного регіону Уркаїни, що найбільше постраждав після аварії на ЧАЕС. На думку професора, розв’язання проблеми йододефіциту та пов’язаних з ним захворювань у першу чергу потребує прийняття відповідних законодавчих актів щодо масової і групової йодної профілактики.
 Про сучасні підходи до ведення хворих з вузлами та раком ЩЗ, ризик яких значно підвищений у осіб, що постраждали внаслідок аварії на ЧАЕС, розповів заступник директора з клінічної роботи ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук Андрій Миколайович Кваченюк.
Про сучасні підходи до ведення хворих з вузлами та раком ЩЗ, ризик яких значно підвищений у осіб, що постраждали внаслідок аварії на ЧАЕС, розповів заступник директора з клінічної роботи ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук Андрій Миколайович Кваченюк.
Доповідач нагадав, що поширеність вогнищевих утворень ЩЗ в загальній популяції є досить високою. Пальпаторно їх виявляють у 3-7% в загальній популяції, а при проведенні скринінгового УЗД – у 20-76%.
Що стосується тактики ведення пацієнтів з вузлами та раком ЩЗ, то сучасні рекомендації, зокрема від Європейської тиреоїдної асоціації (ETA) 2006 року, консенсусу ЕТА та Американської тиреоїдної асоціації (АТА) 2010 року та нещодавно оновленого керівництва АТА (2015), суттєво відрізняються між собою.
Згідно з консенсусом ЕТА/АТА проведення тонкоголкової аспіраційної пункційної біопсії (ТАПБ) з наступним виконанням цитологічного дослідження показане при:
- розмірі вузлів >1 см в діаметрі, якщо вони солідні або гіпоехогенні;
- вузлах будь-якого розміру з ознаками інвазивного росту через капсулу або при підозрі на шийні метастази;
- вузлах будь-якого розміру при вказівках на опромінення голови і шиї, особливо в дитинстві; наявності папілярного або медулярного раку ЩЗ або МЕН-2 синдрому у родичів; після попередніх операцій з приводу раку ЩЗ; підвищеному рівні кальцитоніну крові;
- вузлах <1 см за наявності УЗД-ознак малігнізації (гіпоехогенні, нерівні і нечіткі краї, мікрокальцифікати, хаотична інтранодулярна васкуляризація).
В оновлених рекомендаціях АТА покази до виконання ТАПБ дещо змінено. Зокрема, діагностична ТАПБ рекомендується:
а) для вузлів >1 см з високим ступенем сонографічної підозри на рак;
b) для вузлів >1 см з проміжним ступенем сонографічної підозри на рак;
с) для вузлів >1,5 см з низьким ступенем сонографічної підозри на рак.
Діагностична ТАПБ може бути показаною для:
d) вузлів >2 см з дуже низьким ступенем сонографічної підозри на рак (наприклад – губчастої структури); спостереження без ТАПБ може бути виправданою опцією.
Діагностична ТАПБ не показана:
е) для тих вузлів, що не відповідають зазначеним вище критеріям;
f) для чисто кістозних вузлів.
У випадку цитологічного підтвердження раку ЩЗ рекомендується хірургічне лікування. Але нові рекомендації АТА менш категоричні, ніж інші керівництва. Зокрема, допускається можливість динамічного спостереження без операції навіть у випадках доведеного раку ЩЗ низького ризику (наприклад, папілярна мікрокарцинома без інвазії та метастазів, а також за відсутності морфологічних чи генетичних ознак агресивності захворювання) Крім того, активне спостереження може розглядатись в якості альтернативи для негайної операції, якщо пацієнт належить до групи високого хірургічного ризику через супутні захворювання, має відносно коротку очікувану тривалість життя (через тяжкі хвороби або дуже похилий вік), має більш нагальні медичні проблеми терапевтичного або хірургічного профілю.
Відрізняються і рекомендації щодо об’єму оперативного втручання. Згідно з ЕТА-2006 показом до виконання тотальної тиреоїдектомії є наявність будь-якого раку ЩЗ, а в АТА-2015 допускається можливість гемітиреоїдектомії у випадку неагресивного тиреоїдного раку (T2N0M0). За АТА-2015 показанням до центральної та латеральної дисекції лімфатичних колекторів шиї є наявність цитологічно або гістологічно доведених метастазів, причому мікрометастази центральної групи не вважаються загрозливими для життя.
Є також відмінності у показах до радіойодтерапії. За ЕТА-2006 радіойодтерапію можна не застосовувати тільки в групі дуже низького ризику – солітарна інтратиреоїдна мікрокарцинома без метастазів у пацієнтів старших за 18 років. Відповідно до рекомендацій АТА-2015 від призначення радіойодабляції можна утриматись навіть при інтратиреоїдній пухлині менше 4 см або мікрометастазах папілярного раку ЩЗ у центральній групі лімфатичних вузлів.
При визначенні доцільності супресивної терапії препаратами тироксину та цільових рівнів тиреотропного гормону при її проведенні АТА наголошує на ретельному зваженні серцево-судинних ризиків.
Також слід зазначити, що АТА вводить принципово нове поняття – динамічна стратифікація (переоцінка) ризику рецидивів відповідно до первинного статусу та відгуку на лікування. Це регламентує прискіпливість подальших діагностично-лікувальних заходів та визначає актуальний ризик рецидиву та смерті. В рекомендаціях АТА-2015 чітко окреслюється перелік адекватних заходів у випадку рецидиву або персистенції захворювання, викладаються показання щодо повторних операцій чи малоінвазивних маніпуляцій, а також застосування нових таргетних хіміотерапевтичних препаратів.
 Чорнобильска катастрофа призвела до значного зростання частоти не тільки раку, але й незлоякісної патології ЩЗ. Про її поширеність та фактори ризику у постраждалих внаслідок аварії на ЧАЕС осіб розповів завідувач відділу радіаційної ендокринології ДУ «Національний науковий центр радіаційної медицини НАМН України», доктор медичних наук Олексій Валентинович Камінський.
Чорнобильска катастрофа призвела до значного зростання частоти не тільки раку, але й незлоякісної патології ЩЗ. Про її поширеність та фактори ризику у постраждалих внаслідок аварії на ЧАЕС осіб розповів завідувач відділу радіаційної ендокринології ДУ «Національний науковий центр радіаційної медицини НАМН України», доктор медичних наук Олексій Валентинович Камінський.
Доповідач навів результати спостереження 20 087 дітей, постраждалих внаслідок аварії на ЧАЕС (період 1992-2012 рр.) і включених до клініко-епідеміологічного реєстру ДУ «Національний науковий центр радіаційної медицини НАМН України». Діти були опромінені головним чином за рахунок І131, тому найбільш значущими були саме тиреоїдні ефекти іонізуючого випромінювання. Середня доза опромінення ЩЗ учасників зазначеної когорти знаходилась в межах 0,1-1,55 Гр.
Серед дітей, постраждалих внаслідок аварії на ЧАЕС, найбільш поширеною патологією ЩЗ був дифузний нетоксичний зоб, виявлений у 50,5% осіб, що значно вище, ніж у загальній популяції.
Найвищий ризик тиреоїдної патології відмічено в групі дітей, евакуйованих з 30-кілометрової зони відчуження і опромінених у віці 3-6 років.
У групі дітей, опромінених іn utero, не було виявлено вірогідного збільшення загальної частоти захворювань ЩЗ порівняно з безпосередньо постраждалими дітьми, але частота аутоімунного тиреоїдиту в них була значно вищою і сягала 9,9-12,8%.
Серед дітей, народжених від опромінених батьків (перше покоління), тиреоїдні захворювання виявляли у 42,64%, що перевищувало частоту в контрольній групі.
Також доповідач розповів про результати ретроспективного аналізу незлоякісних ефектів іонізуючого опромінення на ендокринну систему у 18 192 дорослих осіб, постраждалих внаслідок аварії на ЧАЕС і включених до клініко-епідеміологічного реєстру ДУ «Національний науковий центр радіаційної медицини НАМН України». Було встановлено, що частота тиреоїдної патології у осіб, постраждалих внаслідок аварії на ЧАЕС, була в 1,5-2 рази вищою, ніж у групі контролю.
Особливо вираженою ця різниця була у постраждалих, що мали ожиріння. Крім того, у обстежених осіб була виявлена низка міжсистемних гормональних зв’язків, зокрема на розвиток дифузного нетоксичного зобу значно впливали такі гормони, як серотонін, лептин, кортизол, а також наявність інсулінорезистентності; на розвиток вузлового зобу – α-меланоцитстимулюючий гормон, мелатонін, субклінічне порушення функції ЩЗ, інсуліно- і лептинорезистентність; хронічного аутоімунного тиреоїдиту – інсулін, лептин, С-пептид, кортизол, інсуліно- та лептинорезистентність.
Отримані результати дозволили зробити висновок, що ризик розвитку неонкологічної тиреоїдної патології у осіб, що зазнали впливу іонізуючого опромінення, можуть підвищувати такі фактори, як ожиріння та інсулінорезистентність.
Довідка ЗУ
Глобальні наслідки аварії у цифрах
Після 1991 р. радіоактивно забрудненими визнано 11 областей, 74 адміністративних райони і 2293 населених пункти України.
Постраждалими від катастрофи визнано більше 3,4 млн громадян країни, з них більше 1,2 млн дітей.
З 1991 по 2014 р. з мапи України зникло 700 сіл, причому більше 250 з них – в зонах радіоактивного забруднення.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....