Використання пробіотиків при гострому гастроентериті у дітей
Оновлені рекомендації ESPGHAN-2020
Робоча група (РГ) з питань пре- та пробіотиків Європейського товариства дитячої гастроентерології, гепатології та нутриціології (European Society for Paediatric Gastroenterology, Hepatology and Nutrition, ESPGHAN) у 2020 році розробила оновлені рекомендації щодо застосування пробіотиків при гострому гастроентериті (ГГЕ) у раніше здорових немовлят і дітей. Ці рекомендації не стосуються дітей із хронічними захворюваннями та імунодефіцитними станами.
Методи
При розробленні рекомендацій використовували дані систематичних оглядів та/або метааналізів, а також пізніше опубліковані результати рандомізованих контрольованих досліджень (РКД) за вересень 2013 – серпень 2019 р., у яких порівнювалися пробіотики у будь-якій лікарській формі та дозуванні з плацебо чи відсутністю лікування.
Учасниками досліджень були діти з клінічно діагностованим ГГЕ (незалежно від визначення патології, що застосовували дослідники), які лікувалися амбулаторно або у стаціонарі. У фокусі уваги експертів були діти, які проживали у Європі. Загалом увага експертів була сконцентрована на тривалості діареї, необхідності госпіталізації амбулаторних хворих або тривалості періоду госпіталізації стаціонарних пацієнтів, а також на частці дітей, котрі одужали протягом 48 год лікування (або наявності діареї на 2-й день лікування).
Враховуючи те, що виробники можуть змінювати склад та технологію виробництва власної продукції, РГ вирішила оцінювати лише пробіотичні штами, а не торгові марки. РГ усвідомлює, що різні виробники можуть постачати таксономічно еквівалентні пробіотичні мікроорганізми. Залежно від країни одні й ті самі пробіотики можуть бути доступні як харчові добавки чи входити до складу інших продуктів, що пов’язано з різними регуляторними процесами та контролем якості. Крім виробничого процесу, на характеристики та функціональність штаму може впливати матрикс. Таким чином, у цьому документі дані про таксономічно еквівалентні пробіотики об’єднані незалежно від виробника. Нежиттєздатні мікроорганізми, тобто ті, що не відповідають визначенню пробіотика [5], не розглядалися.
Ефективність пробіотиків LGG, Lactobacillus reuteri DSM 17938, Saccharomyces boulardii, Bacillus clausii O/C, SIN, N/R і T, L. helveticus R0052 та L. rhamnosus R0011, L. rhamnosus 19070 та L. reuteri DSM 12246 була оцінена у 2 та більше РКД, тому створення рекомендацій щодо них було можливим.
Загальні положення
Пробіотики з рекомендацією
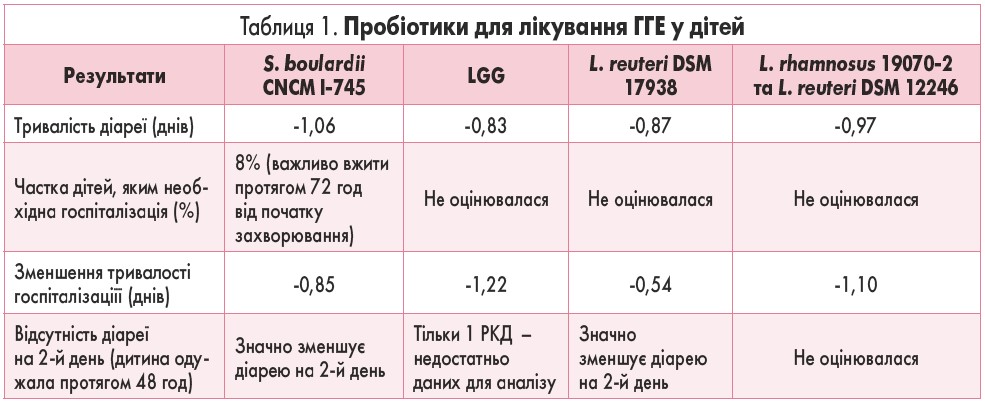
Нижче наведені пробіотики зі слабкою рекомендацією щодо застосування в клінічній практиці обговорюються у порядку зменшення кількості досліджень, у яких оцінююється штам (або штами; табл. 1). У разі прийняття рішення про включення пробіотика у схему лікування дитини з ГГЕ його слід використовувати як допоміжну терапію разом з регідратацією та дієтотерапією, а не замість них.
Saccharomyces boulardii
Нещодавно був опублікований систематичний огляд з метааналізом 29 РКД, який загалом охопив 4217 пацієнтів, котрі були рандомізовані на досліджувану (n=2152) та контрольну (n=2065) групи [22]. Застосування пробіотика S. boulardii сприяє зменшенню тривалості діареї (23 РКД; n=3450; середня різниця – СР – 1,06 дня; 95% довірчий інтервал – ДІ – від -1,32 до -0,79), періоду госпіталізації (8 РКД; n=999; СР – 0,85 дня; 95% ДІ від -1,35 до -0,34), потребу в госпіталізації амбулаторних пацієнтів (2 РКД; n=233; коефіцієнт ризику – КР – 1,08; 95% ДІ 0,62-1,87) та ризик діареї уже на 2-й день лікування (2 РКД; n=463; КР – 0,75; 95% ДІ 0,67-0,84).
У 13 дослідженнях (n=1599) було використано штам S. boulardii CNCM I-745, щодо решти 10 (n=1851) відомості про застосування конкретного штаму відсутні. Незалежно від призначеного штаму S. boulardii, тривалість діареї була зменшена: СР -0,99 дня; 95% ДІ від -1,27 до -0,70 проти -1,12 дня; 95% ДІ від 1,68 до -0,57 відповідно. Тест на різницю підгруп показав відсутність істотної різниці (р=0,66). У цьому дослідженні підтверджено ефективність S. boulardii (ретроспективно визначено як S. boulardii CMCM I-745) у зменшенні тривалості діареї при застосуванні пробіотика протягом 72 год після початку захворювання.
Lactobacillus rhamnosus GG
Від 2014 р. був проведений один систематичний огляд 18 РКД (n=4208), який стосувався лише LGG [18]. Застосування пробіотика асоціювалося зі зменшенням тривалості діареї (16 РКД; n=3949; СР – 0,83 дня; 95% ДІ від -1,13 до -0,53). Вища ефективність пробіотика була в країнах Європи, ніж у неєвропейських країнах. Слід зазначити, що аналіз 5 РКД (n=2409), які мали низький ризик упередженості, показав, що порівняно з контролем пробіотик LGG не впливав на тривалість діареї (СР -0,68 дня; 95% ДІ від -1,82 до 0,45). Метааналіз 5 РКД (n=1790) продемонстрував зменшення тривалості госпіталізації серед пацієнтів, які приймали LGG, порівняно з контрольною групою (СР -1,22 дня; 95% ДІ від -2,33 до - 0,10). Однак аналіз 3 РКД (n=1328) з низьким ризиком упередженості не виявив впливу на тривалість госпіталізації (СР -1,68 дня; 95% ДІ від -4,62 до 1,26). Обмежені дані засвідчили, що порівняно з плацебо пробіотик LGG знижував ризик діареї на 2-й день (1 РКД; n=36; КР 0,37; 95% ДІ 0,17-0,84). Однак зазначений результат не враховувався у цих рекомендаціях.
Lactobacillus reuteri DSM 17938
Крім опублікованих раніше результатів 2 РКД, які стосувалися L. reuteri DSM 17938 [30, 31], стали доступні дані ще 2 РКД [32, 33]. Усі вони увійшли до нещодавно проведеного метааналізу [24]. Так, результати 4 РКД (n=347) показали зменшення тривалості діареї на 0,87 дня (95% ДІ від -1,43 до -0,31) у пацієнтів, які отримували L. reuteri DSM 17938, порівняно з плацебо. Застосування пробіотика сприяло зменшенню тривалості госпіталізації порівняно з контрольною групою, однак різниця мала пограничну статистичну значимість (3 РКД; n=284; СР -0,54 дня; 95% ДІ від -1,09 до 0). Застосування пробіотика також супроводжувалося пришвидшенням одужання уже на 2-й день терапії (3 РКД; n=256; КР 4,54; 95% ДІ 2,02-10,18).
L. rhamnosus 19070-2 та L. reuteri DSM 12246
Рекомендація про застосування цієї комбінації ґрунтується на результатах лише 2 РКД [34, 35], проведених у Данії, з невеликою вибіркою пацієнтів (n=112), тому вона з найбільшою ймовірністю може бути переглянута при отриманні нових даних. Зведений аналіз 2 РКД показав, що застосування комбінації L. rhamnosus 19070-2 та L. reuteri DSM 12246 по 2×1010 колонієутворювальних одиниць (КУО) протягом 5 днів зменшує тривалість діареї (СР -0,97 дня; 95% ДІ від -1,72 до -0,22). У госпіталізованих дітей, які приймали пробіотики, тривалість госпіталізації була на 1 день коротшою, ніж у контрольній групі (1 РКД; n=69; СР -1,10 дня, 95% ДІ від -1,82 до -0,38).
Безпека пробіотиків
Як правило, застосування пробіотиків є безпечним у здорових осіб [52]. До факторів ризику виникнення побічних явищ, таких як бактеріємія або грибкова хвороба, належать критичні захворювання, імуносупресія, недоношеність, органічна патологія серця, госпіталізація, наявність центрального венозного катетера та потенціалу транслокації пробіотиків через стінку кишечнику [54, 55]. Наслідки тривалого прийому пробіотиків залишаються невідомими. При ГГЕ пробіотики застосовуються протягом короткого часу.
У таблиці 2 представлені рекомендації РГ з питань пре- та пробіотиків ESPGHAN щодо застосування пробіотиків у дітей з ГГЕ (перелік подано у порядку зменшення кількості досліджень).
РГ не надає жодних рекомендацій за чи проти застосування інших пробіотичних штамів. У країнах з обмеженою доступністю пробіотиків із позитивною рекомендацією медичні працівники можуть розглядати застосування інших пробіотиків за наявності доказів щонайменше в одному дослідженні про їх ефективність та безпеку у лікуванні дітей з ГГЕ.
Список літератури знаходиться в редакції.
Szajewska H., Guarino A., Hojsak I., Indrio F., Kolacek S., Orel R., Salvatore S., Shamir R., van Goudoever J.B., Vandenplas Y., Weizman Z., Zalewski B.M. Use of Probiotics for the Management of Acute Gastroenteritis in Children. An Update. Journal of Pediatric Gastroenterology and Nutrition. Publish Ahead of Print.
DOI: 10.1097/MPG.0000000000002751.
Переклала з англ. у скороченні Ілона Цюпа
Тематичний номер «Педіатрія» №3 (54) 2020 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Метаболічноасоційована жирова хвороба печінки (МАЖХП) є однією з найактуальніших проблем сучасної гепатології та внутрішньої медицини в цілому. Стрімке зростання поширеності ожиріння та цукрового діабету (ЦД) 2 типу в популяції призвело до істотного збільшення кількості хворих на МАЖХП, яка охоплює спектр патологічних станів від неускладненого стеатозу до алкогольної хвороби печінки та цирозу, що розвиваються на тлі надлишкового нагромадження ліпідів у гепатоцитах. ...
Інфекція Helicobacter pylori (H. pylori) офіційно визнана інфекційним захворюванням і включена до Міжнародної класифікації хвороб (МКХ) 11-го перегляду, тому рекомендовано лікувати всіх інфікованих пацієнтів. Проте, зважаючи на широкий спектр клінічних проявів, пов’язаних із гастритом, викликаним H. pylori, лишаються специфічні проблеми, які потребують регулярного перегляду для оптимізації лікування. ...
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...