Оцінка ефективності застосування пробіотиків при гастроінтестинальних розладах на тлі атопічного дерматиту в дітей
Останніми десятиліттями спостерігається зростання алергологічних захворювань у всьому світі, особливо в західних країнах [1]. Серед них атопічний дерматит (АД) є найпоширенішим хронічним запальним захворюванням шкіри, що з’являється в ранньому дитячому віці й уражає близько 20% дітей, а також значно впливає на якість життя як маленького пацієнта, так і всіх членів його сім’ї [2].
 Останніми роками спостерігається неабиякий інтерес до визначення ролі мікробіоти кишечнику в етіопатогенезі АД. Відомо, що нормальна мікрофлора травного каналу створює мікробну плівку на поверхні кишок, перешкоджаючи так надходженню алергенів і токсинів до внутрішнього середовища організму. Крім того, сьогодні доведено, що мікробний фактор визначає також кількість вільного гістаміну в біологічних середовищах і тканинах організму. Отже, стан кишкової мікрофлори є одним із факторів, що визначають патогенез алергічних проявів. Незважаючи на вищезазначені дані, слід визнати, що сьогодні не існує єдиних поглядів на роль мікрофлори у формуванні здоров’я і розвитку різноманітної, зокрема алергічної, патології [3].
Останніми роками спостерігається неабиякий інтерес до визначення ролі мікробіоти кишечнику в етіопатогенезі АД. Відомо, що нормальна мікрофлора травного каналу створює мікробну плівку на поверхні кишок, перешкоджаючи так надходженню алергенів і токсинів до внутрішнього середовища організму. Крім того, сьогодні доведено, що мікробний фактор визначає також кількість вільного гістаміну в біологічних середовищах і тканинах організму. Отже, стан кишкової мікрофлори є одним із факторів, що визначають патогенез алергічних проявів. Незважаючи на вищезазначені дані, слід визнати, що сьогодні не існує єдиних поглядів на роль мікрофлори у формуванні здоров’я і розвитку різноманітної, зокрема алергічної, патології [3].
Мікробіота кишечнику урізноманітнюється весь час, але найбільше – протягом перших 5 років життя. Кишковий бактеріальний склад є унікальним для кожного індивіда [4]. У шлунково-кишковому тракті дорослої людини міститься кілька трильйонів мікробних клітин. Дослідження виявили загалом 9,9 млн мікробних генів у кишечнику дорослої людини [5].
Мікробіота кишечнику бере участь у регуляції широкого спектра фізіологічних процесів, як-от кишкова ендокринна функція, проліферація клітин, васкуляризація, біосинтез різних сполук та елімінація токсинів [4]. Клітинно-опосередковані імунні реакції та розвиток і підтримка слизової оболонки кишечнику також здійснюються під впливом мікробіоти кишечнику [6]. Дисбаланс або дисбактеріоз мікробіоти кишечнику людини на ранніх етапах дитинства може бути фактором ризику для широкого спектра захворювань, пов’язаних зі способом життя й імунітетом, як-от бронхіальна астма, метаболічні захворювання та запальні захворювання кишечнику [7-9]. Дослідження на мишах, які не містять мікробів, свідчать про те, що відсутність кишкових бактерій може спричинити імунну дисфункцію, а це збільшує ризик захворювання в подальшому житті [10-12].
Відповідно до гігієнічної гіпотези, наслідки сучасної медичної практики, які знижують стимуляцію імунної системи різними мікробами, роблять дітей чутливішими до алергічних захворювань [13, 14]. Малодітні сім’ї, відмова від щеплень та широке застосування антибіотиків – усе це сприяло зменшенню контакту дітей з патогенами, здатними стимулювати саме Th1, тому активною залишається лише ланка активації Th2-лімфоцитів, що може зумовити розвиток алергічних захворювань. Задля розширення гігієнічної гіпотези було запропоновано «гіпотезу про мікрофлору алергічного захворювання», аби підкреслити роль мікробіоти кишечнику у формуванні імунної системи дитячого організму в ранньому віці [15]. Фактично рання мікробна колонізація кишечнику зміщує баланс Th1 і Th2 до фенотипу Th1 [16, 17]. І навпаки, відсутність нормальної кишкової бактеріальної колонізації при атопічних захворюваннях, особливо під час розвитку імунної системи слизової оболонки, зміщує баланс Th1/Th2 до фенотипу Th2 [18, 19]. Цитокіни Th2, як-от IL‑4, IL‑5 та IL‑13, індукують синтез імуноглобулінів класу Ig E. Модуляція цієї відповіді через збільшення Th2 або регуляторних Т-клітин є новою стратегією профілактики та лікування АД шляхом призначення пробіотиків [20]. Пробіотики визначаються як живі мікроорганізми, які після прийому всередину приносять користь здоров’ю господаря [21]. При атопічних захворюваннях вони можуть діяти як імуномодулятори, що стимулюють Th1-опосередковані реакції [22].
Якщо незбалансований склад кишкової мікрофлори має змогу сприяти розвитку атопічних захворювань, то пробіотики можуть бути корисними завдяки їхній здатності поліпшувати імунологічні функції кишечнику шляхом зменшення вироблення прозапальних цитокінів і відновлення нормальної проникності кишечнику [3].
Крім того, було висловлене припущення, що позитивні ефекти пробіотиків у запобіганні запуску атопічних захворювань пов’язані зі стимуляцією ними Toll-подібних рецепторів (TLRs) [3, 23]. У відповідь на стимуляцію цих рецепторів кишкові епітеліальні клітини виробляють різні рецептори розпізнавання структур; вони є клітинно-специфічними, які, своєю чергою, розпізнають певні мікробні антигени (патоген-асоційовані молекулярні структури – PAMPs). Стимуляція TLRs різними PAMPs індукує диференціювання Т-клітин у клітини Th1, що опосередковують клітинні та запальні реакції, і Th2-клітини, які опосередковують гуморальну відповідь, антипаразитарний захист й алергічні реакції. Взаємодія мікрофлори дитини із TLRs може відігравати певну роль у реалізації схильності до харчової алергії [3].
Лактіалє® – сучасний синбіотик (пробіотик + пребіотик), який містить комплекс 7 корисних бактерій (біфідобактерій, лактобактерій та стрептокока), що в нормі присутні в мікрофлорі кишечнику здорової людини, і пребіотик – фруктоолігосахариди. Кожен пакетик містить 7 корисних штамів пробіотичних мікроорганізмів: Lactobacillus casei, Lactobacillus rhamnosus, Streptococcus thermophylus, Bifidobacterium breve, Lactobacillus acidophylus, Bifidobacterium longum, Lactobacillus bulgaricus (сумарно 5,0×108 КУО на 1 пакет у Лактіалє® Малюк формула і 1,00×109 КУО на 1 пакет у Лактіалє® для дітей) та фруктоолігосахариди.
Мета роботи – вивчити ефективність пробіотичних продуктів Лактіалє® Малюк формула та Лактіалє® для дітей щодо дітей віком від 6 міс до 9 років з гастроінтестинальними розладами на тлі АД.
Матеріали та методи
Пацієнти
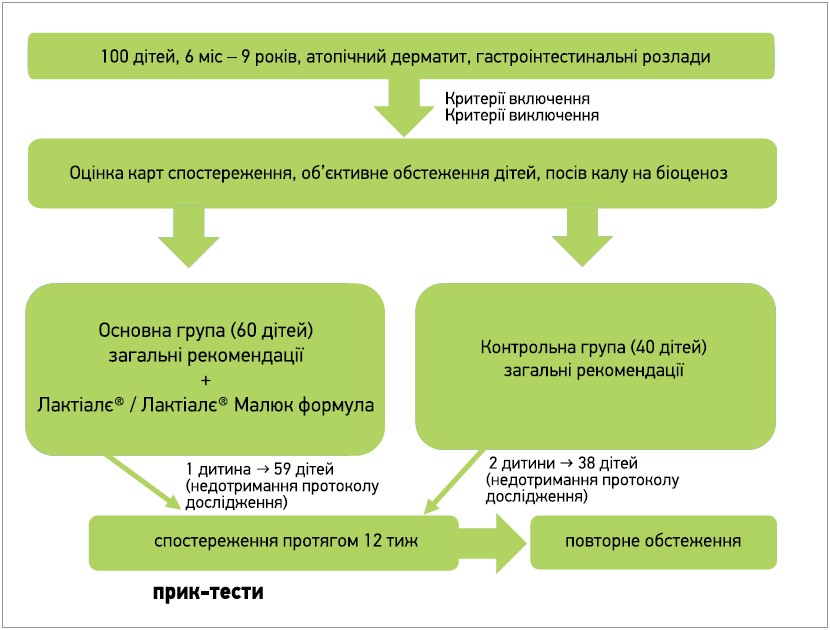
До клінічного дослідження, яке проводилося у 2018-2019 рр., було залучено 100 дітей віком від 6 міс до 9 років з діагнозом АД (рис. 1).
Рис. 1. Дизайн дослідження
Критерії включення до випробування: вік – від 6 міс до 9 років; діагноз – АД; доношена дитина (термін гестації – 37-42 тиж); маса при народженні – понад 2500 г; згода батьків на отримання пробіотичного продукту та повторний огляд й обстеження під час і після завершення терапії.
Критерії виключення з дослідження: непереносимість пробіотичних продуктів або їхніх компонентів; недотримання протоколу призначеної терапії; наявність тяжких супутніх захворювань, вроджених вад розвитку; гостра кишкова інфекція.
Отже, під спостереженням перебувало 97 дітей віком від 6 міс до 9 років (середній вік – 4,5±2,2 року) з діагнозом АД; серед них 36% хлопчиків і 64% дівчаток, які лікувалися на базі міської дитячої клінічної лікарні м. Львова.
Дітей було розподілено на 2 групи. Основна група – 59 дітей (42% хлопчиків і 58% дівчаток, середній вік – 3,62±2,1 року, діти до 2 років – 30,5%), які отримували пробіотичний продукт Лактіалє® чи Лактіале® Малюк формула (залежно від віку дитини: діти від 6 міс до 2 років – Лактіалє® Малюк формула, діти віком понад 2 роки – Лактіалє®) протягом 12 тиж по 1 пакетику 1 р/день (після основного прийому їжі, розчинивши у воді). Група контролю – 38 дітей (26% хлопчиків і 74% дівчаток, середній вік – 5,9±1,7 року), котрі не отримували пробіотичного продукту; їм було надано лише загальні рекомендації щодо режиму, дієти та догляду за шкірою.
Статистичні розрахунки проведені з використанням електронних таблиць Excel 2009 (Microsoft, USA), статистичного пакета прикладних програм STATISTICA For Windows v.6.0 (StatSoft, USA). При проведенні розрахунків обчислювали відносні (інтенсивні й екстенсивні показники) величини. Насамперед оцінювали характер змінних (кількісні, якісні) та нормальність розподілу варіаційного ряду. За умови непараметричного (неправильного) розподілу змінних для порівняння двох груп застосовували метод кутового перетворення Фішера (розрахунок критерію φ). Різницю двох середніх величин вважали достовірною при значеннях р≤0,05 (ймовірність помилки <5%). Отже, ці дані можна перенести на генеральну сукупність з достовірністю 95%.
Результати та обговорення
Гастроінтестинальні прояви харчової алергії не є рідкістю в немовлят і дітей. До них належать блювання, гастроезофагеальний рефлюкс, болі в животі, діарея, метеоризм і закрепи. Клінічний діагноз вимагає виключення неімунологічних захворювань, які мають схожу гастроінтестинальну симптоматику [24].
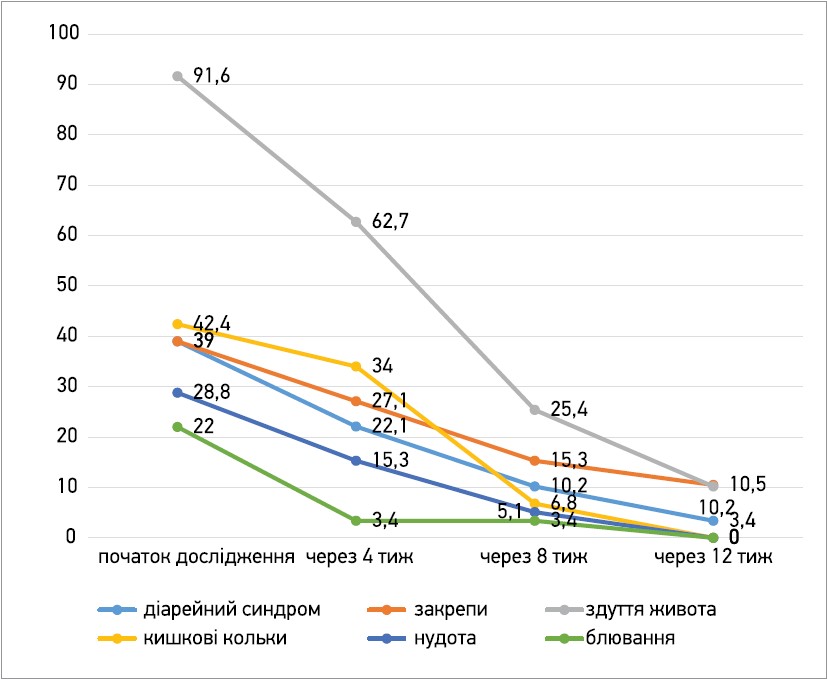
Діти з АД часто скаржаться на шлунково-кишкові розлади [25]. Було встановлено, що діарейний синдром без температури на початку дослідження спостерігався у 39% дітей основної групи та 31,6% дітей контрольної проти 3,4% дітей основної групи через 12 тиж, закрепи на початку випробування – у 39% дітей основної групи та 47,4% дітей контрольної проти 3,4% і 10,5% дітей відповідно через 12 тиж, здуття живота на початку дослідження – в 91,6% дітей основної групи та 50% дітей контрольної проти 10,2% дітей основної групи через 12 тиж, кишкові кольки на початку випробування – в 42,4% дітей основної групи та 21% дітей контрольної, а через 12 тиж не спостерігалися в жодній із груп, нудота на початку дослідження – у 28,8% дітей основної групи та 50% дітей контрольної, блювання – у 22% і 7,9% дітей відповідно, а через 12 тиж не спостерігалося в жодній із груп (табл., рис. 2, 3).
Рис. 2. Динаміка частоти гастроінтестинальних симптомів у дітей основної групи
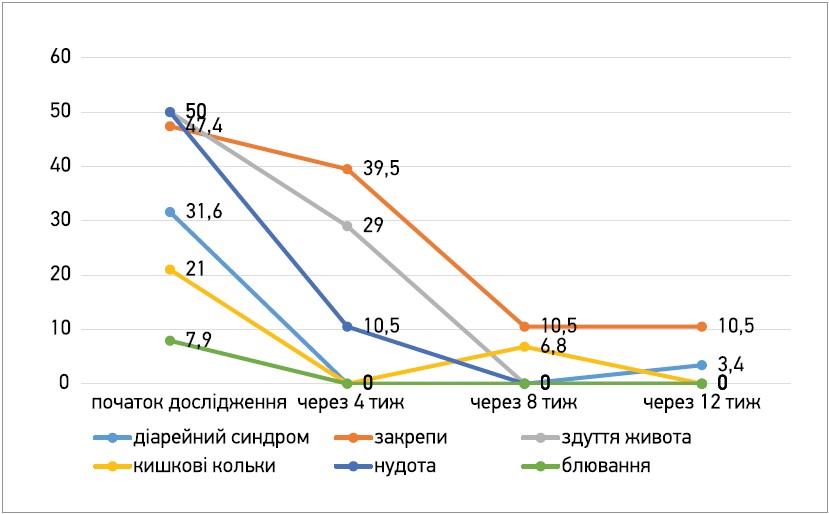
Рис. 3. Динаміка частоти гастроінтестинальних симптомів у дітей контрольної групи
Можна зробити висновок, що після проведеного лікування відсоток дітей з діарейним синдромом без температури, закрепами, синдромом кишкових кольок, здуттям живота та нудотою достовірно зменшився в обох групах, хоча тяжкість прояву деяких симптомів (синдром кишкових кольок, здуття живота) була достовірно вищою в дітей основної групи на початку дослідження.
При дослідженні калу на мікробіоценоз на початку дослідження було виявлено патологічні зміни у складі кишкової мікрофлори в значної кількості дітей.
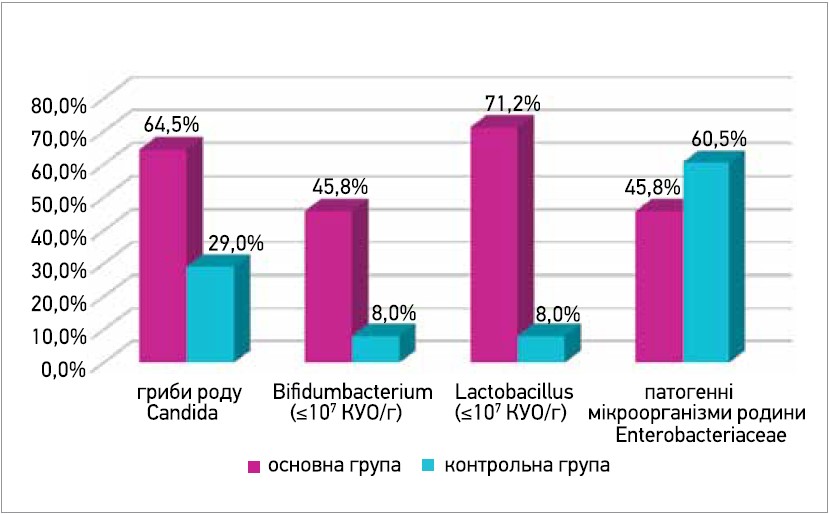
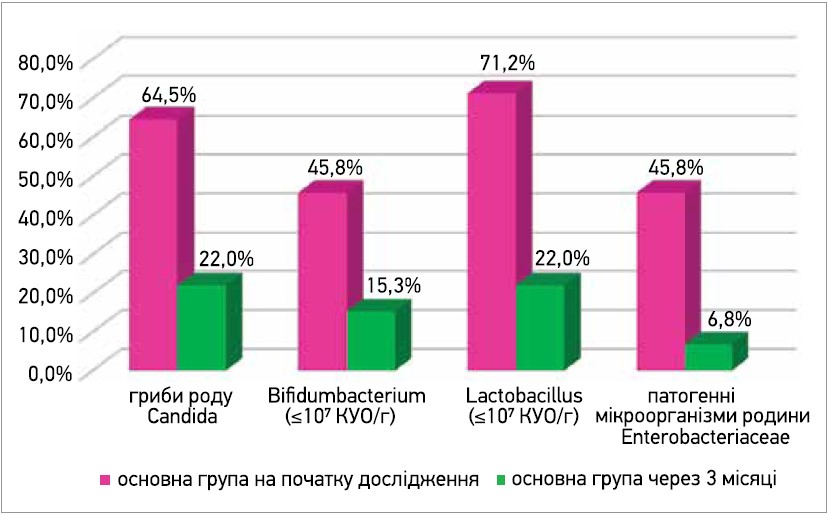
Так, дріжджоподібні гриби роду Candida виявлено в 64,5% дітей основної групи та 29% дітей контрольної (р<0,01), недостатня кількість Bifidumbacterium (≤107 КУО/г) – у 45,8% і 8% дітей відповідно (р<0,01), дефіцит Lactobacillus (≤107 КУО/г) – у 71,2% і 8% дітей відповідно (р<0,01). Патогенні мікроорганізми родини Enterobacteriaceae на початку дослідження було виявлено в 45,8% дітей основної групи та 60,5% дітей контрольної (рис. 4).
Рис. 4. Патологічні зміни у складі кишкової мікрофлори в дітей досліджуваних груп
Отже, в дітей основної групи були достовірно гірші результати при дослідженні калу на мікробіоценоз.
Через 12 тиж після випробування спостерігалася позитивна динаміка в дітей обох груп, проте в дітей основної групи вона була достовірно кращою.
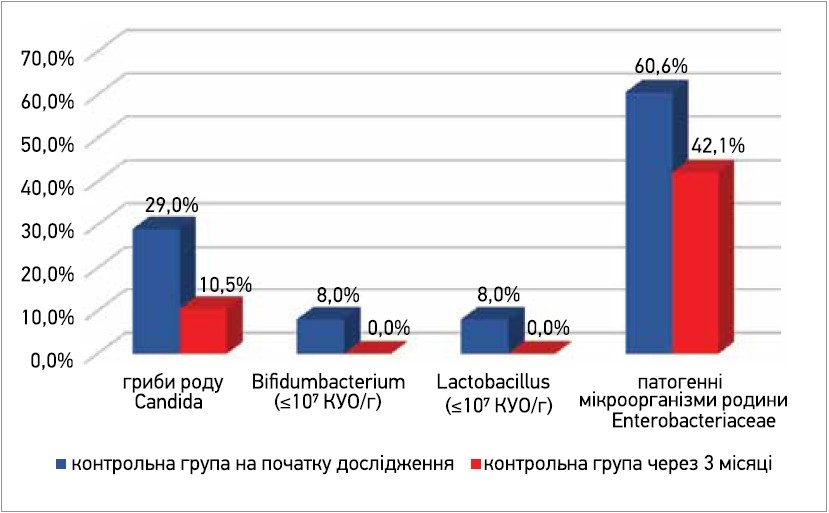
Так, дріжджоподібні гриби роду Candida виявлено у 22% (р<0,05) дітей основної групи та 10,5% дітей контрольної проти 64,5% і 29% дітей відповідно на початку дослідження, недостатня кількість Bifidumbacterium (≤107 КУО/г) – у 15,3% (р<0,05) дітей основної групи проти 45,8% дітей основної та 8% дітей контрольної групи (р<0,01) на початку випробування, дефіцит Lactobacillus (≤107 КУО/г) – у 22% (р<0,05) дітей основної групи проти 71,2% дітей основної та 8% дітей контрольної групи (р<0,01) на початку дослідження, патогенні мікроорганізми родини Enterobacteriaceae – в 6,8% (р<0,05) дітей основної групи та 42,1% дітей контрольної проти 45,8% і 60,5% дітей відповідно на початку випробування (рис. 5, 6).
Рис. 5. Динаміка патологічних змін у складі кишкової мікрофлори в дітей основної групи
Рис. 6. Динаміка патологічних змін у складі кишкової мікрофлори в дітей контрольної групи
Отже, в більшості дітей основної групи на початку дослідження основні показники мікробіоценозу випорожнень були достовірно незадовільнішими, проте через 12 тиж після лікування вони стали достовірно кращими.
Висновки
Гастроінтестинальні розлади на тлі АД залишаються однією з актуальних проблем сучасної педіатрії, оскільки зустрічаються доволі часто, можуть мати тяжкий перебіг і не завжди піддаються звичайним методам корекції. В етіопатогенезі АД, зокрема й гастроінтестинальних розладів на його тлі, має значення кількісний та якісний склад мікробіому кишечнику.
Тривале застосування (протягом 12 тиж) пробіотичного продукту Лактіалє® для дітей / Лактіалє® Малюк формула (відповідно до віку дітей) по 1 пакетику 1 р/день істотно покращує ефективність комплексної терапії АД, що супроводжується достовірним зменшенням функціональних розладів травної системи та покращенням мікробіоценозу кишок, а це свідчить про його ефективність й доцільність включення до схем лікування.
В дослідженні не визначено ознак непереносимості чи побічних дій цього пробіотичного препарату.
Медична газета «Здоров’я України 21 сторіччя» № 17 (486), 2020 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...