Бригатиниб в лечении немелкоклеточного рака легкого
В структуре онкологической заболеваемости и смертности рак легкого длительное время занимает лидирующие позиции. По данным B.A. Chan и B.G.M. Hughes (2015), около 1/5 всех летальных исходов вследствие онкологической патологии обусловлены раком легкого. Согласно бюллетеню Национального канцер-регистра № 20 «Рак в Украине, 2017-2018», в структуре заболеваемости и смертности рак трахеи, бронха и легкого занимает соответственно 1-е место у мужчин, 6-е и 9-е место у женщин. Рак легкого является прогностически неблагоприятной формой злокачественного новообразования с низкой выживаемостью пациентов (более половины больных раком легкого умирают на протяжении года после постановки диагноза). Наиболее распространенным типом рака легкого является немелкоклеточный рак легкого (НМРЛ), который составляет до 90% всех злокачественных опухолей органа (T. Sher et al., 2008). За последние годы осуществлен значительный прорыв в лечении больных НМРЛ, главным образом благодаря внедрению таргетной терапии, что позволило достичь беспрецедентного увеличения выживаемости.
Около 5% пациентов с НМРЛ имеют мутацию гена киназы анапластической лимфомы (ALK), кодирующего соответствующий онкогенный гибридный белок (W. Pao et al., 2011; L.M. Sholl et al., 2015). Белок ALK (также известен как CD246) – трансмембранная киназа тирозинового рецептора, участвует как в обеспечении некоторых физиологических функций (передача внеклеточных сигналов, контроль пролиферации, дифференциации клеток, в частности в центральной нервной системе), так и в онкогенезе при некоторых видах рака (за счет транслокации гена ALK и образования комбинированного гена NPM‑ALK либо путем увеличения репликации или дублирования реального кода ДНК). Ген NPM-ALK или комбинация генов ответственны за 75% случаев анапластической крупноклеточной лимфомы (R. Chiarle et al., 2008). У 2-7% больных аденокарциномой при НМРЛ также определяют другой слитый белок – ALK-EML4 (D.W. Wong et al., 2009). Таким образом, ALK является привлекательной терапевтической мишенью у пациентов с НМРЛ.
С 2007 г. начался активный поиск простых молекул, угнетающих ALK. Представители ингибиторов ALK первого и некоторые препараты второго поколения были одобрены для лечения пациентов с НМРЛ. Вскоре оказалось, что применение перорального ингибитора тирозинкиназы (ИТК) первого поколения кризотиниба не приносило достаточного успеха. Причинами отсутствия эффективности были формирование устойчивости к ALK-ингибитору в течение 1-2 лет терапии за счет модификации мишени или передачи сигналов обходными путями (R. Katayama et al., 2012), а также тяжелая токсичность из-за воздействия препарата на центральную нервную систему (ЦНС; D.B. Costa et al., 2011). Некоторые представители ИТК второго поколения (церитиниб, алектиниб) в условиях клинического испытания показали более высокую эффективность, но на практике к этим препаратам также развивалась резистентность (L. Friboulet et al., 2014; А. Tanimoto et al., 2014).
Бригатиниб – ALK-ингибитор второго поколения, проявляет двойную ингибирующую активность против CD246 (ALK) и трансмембранного белка EGFR (рецептора эпидермального фактора роста) или HER‑1 (Huang et al., 2016). В 2016 г. Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) признало бригатиниб орфанным препаратом для лечения НМРЛ. В 2017 г. FDA разрешило ускоренное одобрение бригатиниба для лечения пациентов с раком легкого, вызванным мутациями ALK и EGFR (табл. 1), в том числе пациентов с уже имеющейся резистентностью к другим ингибиторам.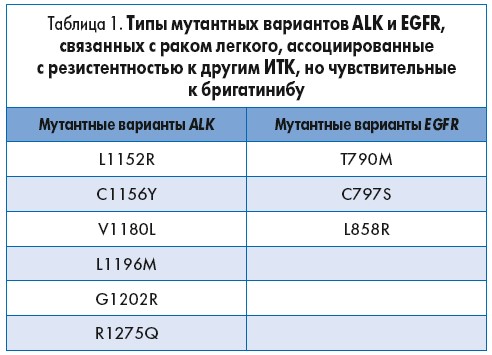
Основными характеристиками бригатиниба, которые отличают его от других ALK-ингибиторов и способствуют взаимодействию препарата с ALK, являются наличие бис-анилин-пиримидинового фрагмента вместо аминопиридинового каркаса (как у кризотиниба); две группы NH2, присоединенные к фенильному кольцу (дополнительно присоединено к углероду 2 и 4), – группы OCH3 и атом хлора на углероде 5 (W.S. Huang et al., 2014; W.S. Huang et al., 2016). Наличие в молекуле бригатиниба оксида диметилфосфина (DMPO) обусловливает профиль селективности препарата по отношению ALK.
В экспериментальном исследовании in vitro S. Zhang и соавт. (2014) обнаружили, что применения бригатиниба в концентрации 500 нмоль/л достаточно для преодоления резистентности к другим ингибиторам ALK. Результаты следующего эксперимента S. Zhang и соавт. (2016) с использованием клеточных линий, содержащих мутагенные субстанции, которые могут вызывать резистентность, показали, что бригатиниб более эффективен против мутагенных вариаций, чем другие ALK-ингибиторы.
Бригатиниб является активным пероральным ИТК, который подавляет киназу ALK с силой, в 12 раз превосходящей таковую кризотиниба (Zhang et al., 2016), и дополнительно ингибирует киназу ROS1. В доклинических исследованиях бригатиниб проявил активность в отношении нескольких мутаций ALK, которые лежат в основе клинически обусловленной резистентности к кризотинибу. В клиническом исследовании I-II фазы, в котором оценивали разные дозы бригатиниба (30-300 мг), частота объективного ответа (ОО) на лечение составила 72% у 71 включенного в исследование пациента с прогрессирующим ALK+ НМРЛ, который ранее получал лечение кризотинибом (Gettinger et al., 2016).
В рандомизированном клиническом исследовании ІІ фазы ALTA была изучена эффективность и переносимость двух вариантов дозирования бригатиниба у пациентов с рефрактерным к кризотинибу НМРЛ. Пациенты были стратифицированы по наличию метастазов в мозге и уровню ответа на предыдущую терапию кризотинибом, а затем распределены случайным образом на группы (1:1) с целью перорального применения бригатиниба в дозах 90 мг 1 раз в сутки (группа A) или 180 мг 1 раз в сутки с предшествующим подготовительным периодом (90 мг в течение 7 дней; группа B). Первичной конечной точкой была подтвержденная частота ОО.
Исходно у 71 и 67% пациентов групп A и B соответственно наблюдались метастазы в головном мозге. После
Бригатиниб продемонстрировал высокую эффективность при использовании обеих схем (90 и 180 мг/сутки). Частота ОО была высокой, ответ достигался быстро и был стойким в обеих группах. Показатели эффективности свидетельствовали о преимуществе более высокой дозы, особенно в отношении ВБП и ответа на терапию со стороны внутричерепных метастазов. У пациентов с измеримыми интракраниальными метастазами при приеме дозы 180 мг (после начальной дозы 90 мг в течение подготовительного периода) частота ОО со стороны внутричерепных метастазов составила 67% в сравнении с 50% у пациентов, которые принимали бригатиниб в дозе 90 мг. По данным независимого экспертного комитета, медиана ВБП в когорте пациентов с метастазами в ЦНС составила 12,8 мес (95% ДИ 9,2-18,3) в группе А и 18,7 мес (95% ДИ 12,6-23,9) в группе В (R.M. Huber et al., 2020).
В исследовании I-II фазы, проведенном в 9 университетских госпиталях США и Испании, изучали эффективность и безопасность бригатиниба у пациентов с распространенными метастатическими стадиями ALK+ НМРЛ. Частота ОО у больных, которые ранее принимали кризотиниб, составила 74%. Серьезными побочными эффектами (за исключением прогрессирования новообразования), возникшими в связи с лечением, были одышка, пневмония и гипоксия, которые отмечались у 5% пациентов. Бригатиниб демонстрировал приемлемый профиль безопасности у больных НМРЛ, ранее получавших кризотиниб, и пациентов, нечувствительных к кризотинибу. Во II фазе исследования были выделены 5 когорт пациентов, у которых получена разная частота ОО (табл. 2; S.N. Gettinger et al., 2016).
Рандомизированное клиническое исследование III фазы ALTA‑1L. Целью исследования III фазы ALTA‑1L было сравнение активности и безопасности бригатиниба и кризотиниба в лечении больных распространенным ALK+ НМРЛ, которые ранее не получали терапию ALK‑ингибиторами. 275 пациентов с ALK+ НМРЛ были распределены в группы бригатиниба (n=137) и кризотиниба (n=138). Первые данные, полученные в 2018 г., свидетельствовали о существенном преимуществе бригатиниба по сравнению с кризотинибом: 12-месячная БПВ – 67 против 43%; соотношение рисков (CР) 0,49; р<0,001; частота подтвержденного ОО 71 и 60% соответственно. Большое различие показателей ответа со стороны интракраниальных метастазов на терапию между группами свидетельствовало в пользу бригатиниба – 78 против 29% (D.R. Camidge et al., 2018).
Недавно получены обновленные результаты исследования ALTA‑1L. Согласно оценкам независимого контрольного комитета, медиана ВБП в группе бригатиниба составила 24,0 мес (95% ДИ 18,5 – не достигнут), в группе кризотиниба – 11,0 мес (95% ДИ 9,2-12,9); СР 0,49; 95% ДИ 0,35-0,68; p=0,0001. По оценке исследователей СР ВБП составляло 0,43 (95% ДИ 0,31-0,61), медиана ВБП – 29,4 и 9,2 мес. Применение бригатиниба способствовало продлению среднего времени до ухудшения общего состояния здоровья/показателей качества жизни по сравнению с кризотинибом (СР 0,70; 95% ДИ 0,49-1,00; р=0,049; D.R. Camidge et al., 2020).
Таким образом, бригатиниб – препарат для лечения поздних стадий ALK+ НМРЛ. Широкий спектр ингибирующей активности бригатиниба в отношении ALK позволяет использовать его при резистентности опухоли к другим ингибиторам ALK. Результаты клинического исследования ALTA‑1L показывают, что прием бригатиниба в первой линии терапии существенно увеличивает ВБП и поддерживает качество жизни пациентов с ALK+ НМРЛ по сравнению с кризотинибом. В исследованиях ALTA и ALTA‑1L бригатиниб продемонстрировал высокий уровень общего ответа и ответа со стороны интракраниальных метастазов, что, несомненно, важно для пациентов с метастазами в ЦНС.
Подготовила Илона Цюпа
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 5 (66) 2020 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




