Сравнение бригатиниба и кризотиниба у больных ALK+ немелкоклеточным раком легкого, ранее не получавших терапию по поводу распространенного заболевания
Второй промежуточный анализ результатов исследования III фазы ALTA-1L
Онкогенная мутация гена киназы анапластической лимфомы (ALK) встречается примерно у 3-5% пациентов с немелкоклеточным раком легкого (НМРЛ; J.F. Gainor, 2013; J.P. Koivunen, 2008). У пациентов, получающих терапию ингибитором ALK первого поколения кризотинибом, наблюдается прогрессирование болезни, в том числе с поражением центральной нервной системы (ЦНС). Вероятно, это связано с плохим проникновением кризотиниба через гематоэнцефалический барьер, а также c возникновением экстракраниальных метастазов вследствие приобретенных мутаций ALK или активации других сигнальных путей.
Бригатиниб – мультитаргетный ингибитор ALK второго поколения, обладающий повышенной активностью против различных мутаций, обусловливающих устойчивость к другим ингибиторам ALK (R. Katayama, 2011; W.S. Huang, 2016; S.tN. Gettinger, 2016).
В исследовании I/II и II фазы ALTA у пациентов с рефрактерностью к кризотинибу бригатиниб обеспечивал высокий уровень общего ответа, в том числе со стороны ЦНС. Медиана выживаемости без прогрессирования (ВБП) в группах кризотиниба и бригатиниба достигала 16,3 и 16,7 мес соответственно (R.M. Huber, 2020; D.R. Camidge, 2018; L.A. Bazhenova, 2017).
В клиническом исследовании III фазы ALTA‑1L сравнивали эффективность бригатиниба и кризотиниба в лечении больных распространенным НМРЛ с мутацией ALK (ALK+), которые ранее не получали ALK-ингибиторы. Медиана наблюдения составила 11 мес в группе бригатиниба и 9,3 мес в группе кризотиниба. Медиана ВБП была выше в группе бригатиниба по сравнению с группой кризотиниба (соотношение рисков – СР – 0,49; р<0,001).
Согласно промежуточному анализу данных исследования ALTA‑1L, у пациентов, принимавших бригатиниб, отмечено значительное улучшение состояния по сравнению с исходным уровнем показателей общего состояния здоровья/качества жизни, физических, когнитивных функций и эмоциональной сферы. Выявлено также уменьшение таких симптомов, как усталость, тошнота/рвота, потеря аппетита и запор, по сравнению с пациентами, принимавшими кризотиниб (р<0,05; R.G. Campelo, 2019).
Первичной конечной точкой была ВБП, которую вслепую оценивал независимый контрольный комитет (BIRC). Вторичные конечные точки включали подтвержденную BIRC частоту объективного ответа (ОО), частоту ОО со стороны интракраниальных метастазов и «интракраниальную» ВБП, а также общую выживаемость, продолжительность ответа, безопасность, изменения по сравнению с исходным показателя общего состояния здоровья/качества жизни с использованием опросника по качеству жизни С30 Европейской организации по исследованию и лечению рака (EORTC QLQ-C30).
С апреля 2016 по август 2017 г. 275 пациентов были включены в исследование и рандомизированы на две группы в соотношении 1:1: группу бригатиниба (n=137) и группу кризотиниба (n=138).
ВБП. На момент оценки промежуточных данных исследования зафиксировано 150 случаев прогрессирования заболевания в ITT (Intention-to-treat) популяции1: у 63 (46%) пациентов в группе бригатиниба и у 87 (63%) в группе кризотиниба. По оценке BIRC бригатиниб продемонстрировал достоверное превосходство в отношении двухлетней ВБП с отсутствием прогрессирования у 48% лиц, принимавших препарат (95% доверительный интервал – ДИ – 39-57%), по сравнению с 26% в группе кризотиниба (95% ДИ 18-35%; СР 0,49; 95% ДИ 0,35-0,68; р<0,0001; рис. 1А). По оценкам исследователей также имелось превосходство бригатиниба в отношении двухлетней ВБП с отсутствием прогрессирования у 56% принимавших его пациентов (95% ДИ 46-64%) по сравнению с 24% в группе кризотиниба (95% ДИ 16-32%; СР 0,43; 95% ДИ 0,31-0,61; р<0,0001; рис. 1Б).
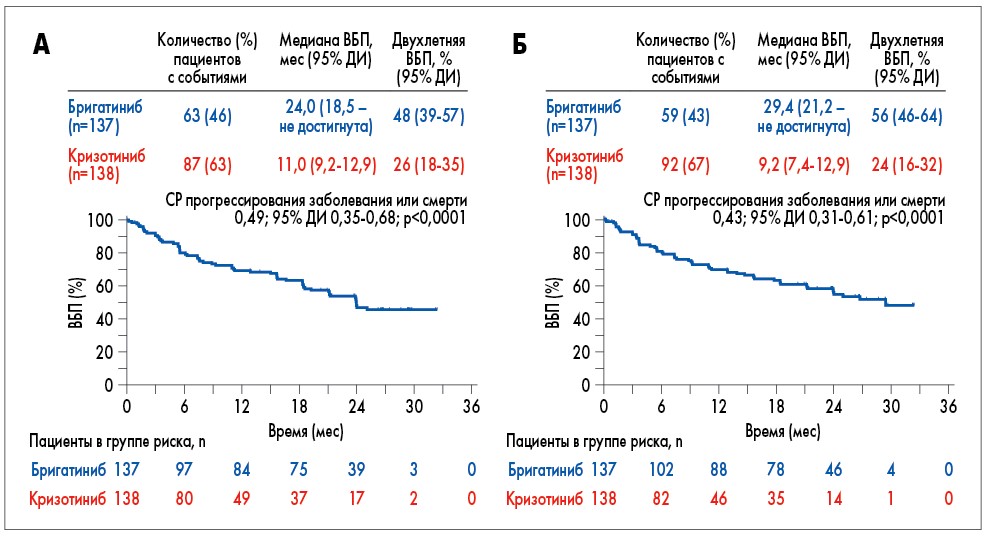 Рис. 1. ВБП при использовании бригатиниба и кризотиниба в лечении ALK+ НМРЛ согласно оценкам BIRC (А) и исследователей (Б)
Рис. 1. ВБП при использовании бригатиниба и кризотиниба в лечении ALK+ НМРЛ согласно оценкам BIRC (А) и исследователей (Б)
Частота и продолжительность ответа. Частота подтвержденного BIRC ОО на терапию составила 74% (95% ДИ 66-81%) в группе бригатиниба и 62% (95% ДИ 53-70%) в группе кризотиниба. Медиана продолжительности ответа на прием бригатиниба не была достигнута (95% ДИ 19,4 мес – не достигнута), для кризотиниба этот показатель составил 13,8 мес (95% ДИ 9,3-20,8).
Общая выживаемость. На момент оценки данных 70 пациентов умерли (33 (24%) в группе бригатиниба и 37 (27%) в группе кризотиниба). Двухлетняя общая выживаемость составила 76% (95% ДИ 67-82%) в группе бригатиниба и 74% (95% ДИ 65-80%) – кризотиниба (СР 0,92; 95% ДИ 0,57-1,47; р=0,771).
Эффективность лечения пациентов с метастатическим поражением головного мозга и без него. У 81 пациента с метастатическим поражением ЦНС (40 в группе бригатиниба и 41 в группе кризотиниба) двухлетняя ВБП по оценке BIRC составила 43% (ДИ 95% 25‑59%) у принимавших бригатиниб и 10% (ДИ 95% 2-25%) – кризотиниб (СР 0,25; 95% ДИ 0,14-0,46; р<0,0001; рис. 2А).
У пациентов без метастазов в головном мозге до лечения (по 97 в каждой группе) ВБП не достигла статистической значимости по проценту событий, но была выше в группе бригатиниба (СР 0,65; 95% ДИ 0,44-0,97; р=0,030; рис. 2Б).
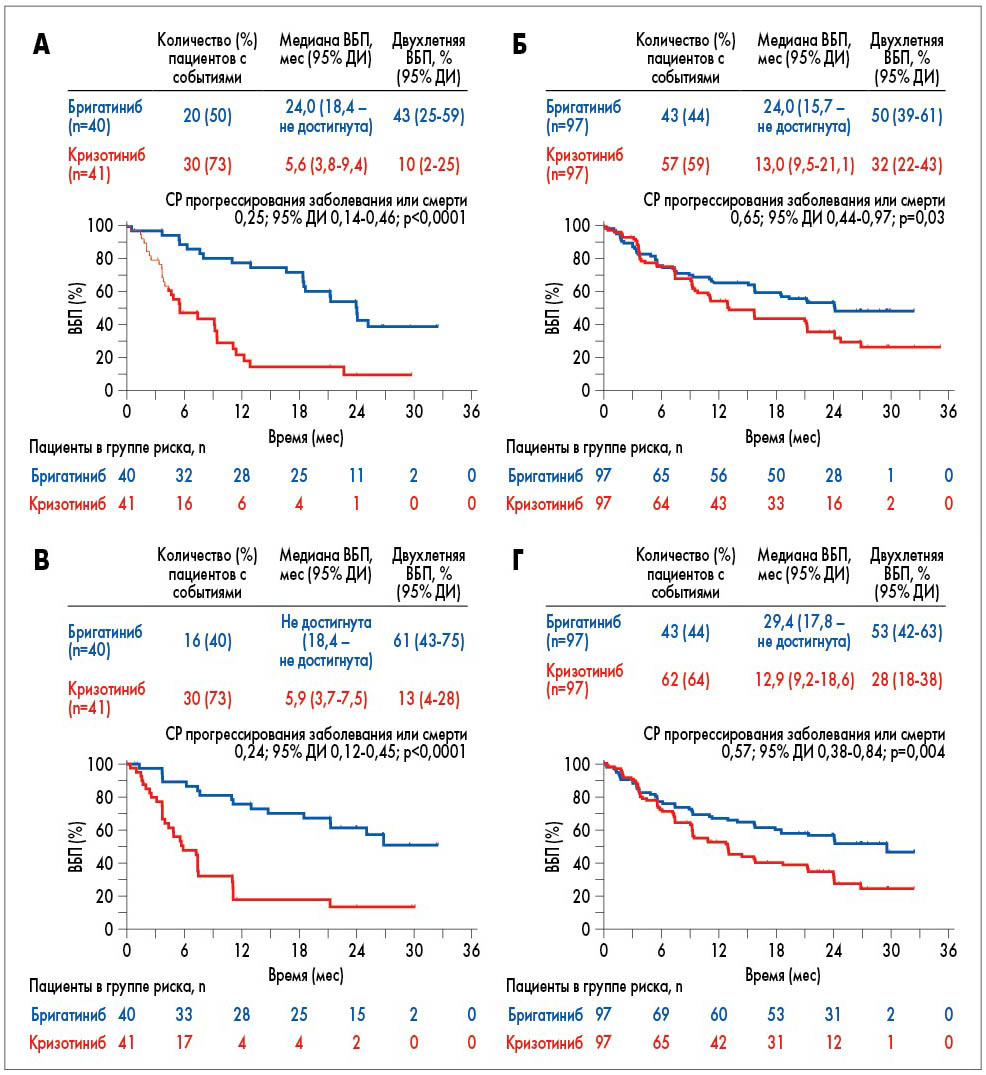 Рис. 2. ВБП по оценкам BIRC (А, Б) и исследователей (В, Г) при использовании бригатиниба и кризотиниба в лечении ALK+ НМРЛ при наличии (А, В) и отсутствии (Б, Г) метастазов в ЦНС
Рис. 2. ВБП по оценкам BIRC (А, Б) и исследователей (В, Г) при использовании бригатиниба и кризотиниба в лечении ALK+ НМРЛ при наличии (А, В) и отсутствии (Б, Г) метастазов в ЦНС
У 41 из 96 пациентов с метастатическим поражением ЦНС согласно оценке BIRC метастазы были измеряемыми (≥10 мм в диаметре). При измеряемых метастазах в головном мозге подтвержденная частота интракраниального ОО на терапию составила 78% (14 из 18 пациентов; 95% ДИ 52-94%) у принимавших бригатиниб и 26% (6 из 23 пациентов; 95% ДИ 10-48%) – кризотиниб. Согласно оценке BIRC, двухлетняя ВБП у пациентов с исходным метастатическим поражением ЦНС составила 48% (95% ДИ 30-63%) для бригатиниба и 15% (5-32%) для кризотиниба, а у больных без метастазов в головном мозге до лечения – 74 (95% ДИ 62-83%) и 67% (95% ДИ 52-79%) соответственно.
Безопасность. Наиболее частыми (>25% пациентов) нежелательными реакциями на лечение различной степени тяжести были гастроинтестинальные расстройства, повышение уровня креатинфосфокиназы (КФК), кашель и повышение содержания аминотрансфераз.
Частота нежелательных явлений 3-5 степени тяжести составила 73 и 61% в группах бригатиниба и кризотиниба соответственно. Данных о клинически диагностированном панкреатите или рабдомиолизе не поступало. Симптомы, которые могут быть связаны с повышением уровня КФК в крови (такие как миалгии или мышечная боль), между группами не отличались.
Качество жизни. Медиана времени до ухудшения показателя общего состояния здоровья/качества жизни у всех пациентов составила 26,7 мес (95% ДИ 8,3 – не достигнуто). в группе бригатиниба и 8,3 мес (95% ДИ 5,7‑13,5) – кризотиниба (СР 0,70; 95% ДИ 0,49-1,00; р=0,049; рис. 3).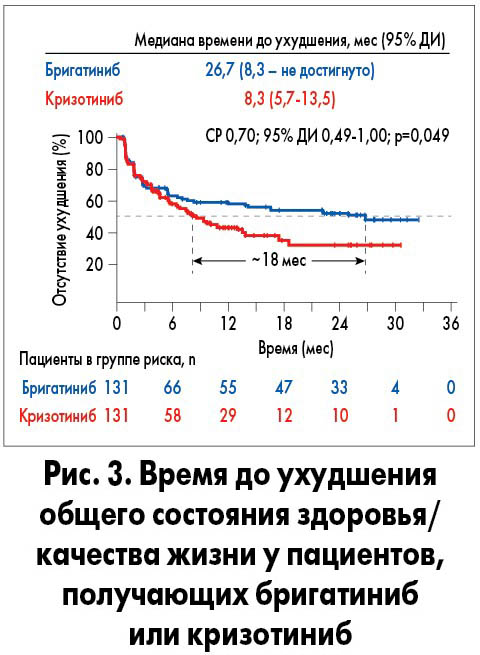
У больных, ранее не получавших химиотерапию, медиана времени до ухудшения общего состояния здоровья/качества жизни не была достигнута (95% ДИ 13,9 – не достигнуто) для бригатиниба. В группе кризотиниба данный показатель составил 8,3 мес (95% ДИ 6,4-18,5; СР 0;68; 95% ДИ 0,44-1,04; р<0,0695).
Среди пациентов с улучшением общего состояния здоровья медиана продолжительности улучшения не была достигнута в группе бригатиниба по сравнению с 12,0 мес (95% ДИ 7,7-17,5) в группе кризотиниба (СР 0,27; 95% ДИ 0,14-0,49; р<0,0001). У больных, ранее не получавших химиотерапию, медиана продолжительности улучшения общего состояния здоровья не была достигнута в группе бригатиниба vs 9,9 мес в группе кризотиниба (95% ДИ 7,3 – не достигнуто; СР 0,26; 95% ДИ 0,12-0,56; р=0,0002).
Бригатиниб – ингибитор ALK для перорального применения, обеспечивающий значительно более высокую эффективность лечения, лучшую переносимость и качество жизни по сравнению с кризотинибом. Следовательно, бригатиниб можно рекомендовать для первой линии терапии при ALK+ НМРЛ.
Camidge D.R., Kim H.R., Ahn M.-Ju et al. Brigatinib in ALK Inhibitor-Naive ALK-Positive NSCLC: Second Interim Analysis of the Phase III ALTA‑1L Trial. Journal of Clinical Oncology. Volume 38, Issue 31.
DOI https://doi. org/10.1200/JCO.20.00505.
1Расчет показателей в ITT-популяции предусматривает анализ результатов исследования с учетом исходно назначенного препарата.
Перевела с англ. в сокращении Ольга Нестеровская
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (67) 2020 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




