Застосування поліненасичених жирних кислот омега‑3 у пацієнтів із гіпертригліцеридемією
Гіпертригліцеридемія – це підвищений рівень тригліцеридів (ТГ) у плазмі крові натще. Серед факторів, які можуть чинити суттєвий вплив на зростання даного показника, – використання ліків, генетичний чинник, загальний стан здоров’я, спосіб життя, режим харчування, низка супутніх захворювань тощо. Відповідно до рекомендацій Американської асоціації серця (АНА), в осіб із підвищеним рівнем ТГ доцільно застосовувати поліненасичені жирні кислоти (ПНЖК) омега‑3. Робоча група АНА проаналізувала й узагальнила наукові дані щодо впливу ПНЖК омега‑3 на плазмові концентрації ТГ й інших ліпідів, ліпопротеїнів у пацієнтів із надмірним вмістом ТГ. Автори мали на меті детально розглянути ефекти засобів, які містять ПНЖК омега‑3, зокрема як додаткового терапевтичного варіанта, особливо у поєднанні зі статинами. Отримані результати опубліковані у виданні Circulation (2019; 140: e673-e691). Пропонуємо до вашої уваги огляд основних положень даного документа.
Концентрацію ТГ у плазмі крові натще класифікують як нормальну (<150 мг/дл), граничну (150‑199 мг/дл), високу (200‑499 мг/дл) і дуже високу (≥500 мг/дл) (Miller et al., 2011). У пацієнтів із дуже високим рівнем ТГ (особливо при ≥1000 мг/дл) імовірність розвитку гострого панкреатиту збільшується (Ewald et al., 2009). Основною метою за такої клінічної ситуації є зниження рівня ТГ до <500 мг/дл (Jacobson et al., 2015).
Клінічні стани, асоційовані з підвищенням рівня ТГ
- надмірна вага або ожиріння
- інсулінорезистентність або метаболічний синдром
- цукровий діабет, особливо при поганому глікемічному контролі
- надмірне вживання алкоголю, цукру, насичених жирів
- гіпотиреоз
- хронічна хвороба нирок
- нефротичний синдром
- малорухливий спосіб життя
- вагітність (особливо 3-й триместр)
- ліпоатрофія
- системні запальні захворювання (як-от ревматоїдний артрит, системний червоний вовчак, інфекційні патології)
Інтерес до ПНЖК омега‑3, зокрема ейкозапентаєнової (ЕПК) та докозагексаэнової (ДГК) кислот, останнім часом значно підвищився, адже вони впливають на життєво важливі процеси в організмі. У масштабних випробуваннях, в яких вивчали ефект засобів із ПНЖК омега‑3 у дозі 4 г/добу, вміст холестерину (ХС) ліпопротеїнів невисокої щільності (не-ЛПВЩ) та аполіпопротеїну В (апо-В) помірно знижувався, що свідчить про зменшення загальної кількості атерогенних ліпопротеїдів. У рандомізованому плацебо-контрольованому дослідженні REDUCE-IT щодо використання ЕПК у хворих групи високого ризику, які отримували статини, позитивний вплив ПНЖК омега‑3 (4 г/добу) для скорочення ризику розвитку атеросклеротичних серцево-судинних захворювань (АССЗ) у пацієнтів із гіпертригліцеридемією підтвердився зниженням частоти основних несприятливих серцево-судинних (СС) подій на 25%.
Оптимальні терапевтичні заходи для зниження вмісту ТГ
У разі наявності підвищення рівня ТГ будь-якого ступеня, перш ніж розпочинати терапію, необхідно виявити й усунути зворотні вторинні причини розвитку такого стану, як-то гіпотиреоз або погано контрольований цукровий діабет 2-го типу. Крім того, спершу варто запровадити інтенсивну корекцію раціону харчування та способу життя (Grundy et al., 2019). Такі зміни включають втрату ваги, збільшення фізичної активності, обмеження споживання алкоголю, ініціювання різних практик здорового харчування, таких як зниження вживання рафінованих вуглеводів та простих цукрів, заміщення насичених і трансжирів ненасиченими, збільшення споживання морепродуктів (особливо з високим вмістом ПНЖК омега‑3).
У рекомендаціях AHA (2002) йшлося про доцільність збільшення споживання омега‑3 з їжею та дієтичних добавок із ПНЖК омега‑3 для досягнення їхньої концентрації в організмі 2‑4 г/добу (загальної кількості ЕПК + ДГК) з метою зниження рівня ТГ під наглядом лікаря (Kris-Etherton et al., 2002). У документі 2011 р. детально висвітлені варіанти оптимального режиму харчування, способу життя та коротко – медикаментозні методи лікування гіпертригліцеридемії (Miller et al., 2011). Зокрема, зазначено, що помірне збільшення вмісту ТГ часто асоційоване з підвищеним ризиком розвитку АССЗ (Nordestgaard, Varbo, 2014; Stitziel, 2017; Dewey et al., 2017). У рекомендаціях AHA (2017) розглянуте питання використання дієтичних добавок із ПНЖК омега‑3 для зменшення ризику АССЗ з акцентом на їхньому призначенні при високому і дуже високому рівні ТГ (Siscovick et al., 2017).
У 2002 р. Агентство з санітарного нагляду за якістю продуктів харчування та медикаментів США (FDA) затвердило рецептурні засоби, що містять ЕПК + ДГК або лише ЕПК, для лікування хворих із гіпертригліцеридемією. У 2004 р. було схвалено низку препаратів на основі ПНЖК омега‑3 при дуже високому рівні ТГ. Стандартна доза становить чотири капсули по 1 г/добу, що забезпечує >3 г/добу ЕПК + ДГК в організмі.
Застосування ПНЖК омега‑3 за дуже високого рівня ТГ
У межах чотирьох досліджень (Harris et al., 1997; Pownall et al., 1999; Bays et al., 2011; Kastelein et al., 2014) було проаналізовано ефективність засобів на основі ПНЖК омега‑3, як-то етилові ефіри омега‑3-кислот (О3КЕЕ) ЕПК + ДГК, лише ЕПК та карбонові кислоти омега‑3 (О3КК), у дозі 4 г/добу в пацієнтів із дуже високим вмістом ТГ (≥500 мг/дл). Цей показник знижувався на 30‑35% в осіб із вихідним рівнем ТГ від 600 до 800 мг/дл. У субаналізі випробування Bays et al. (2011) плацебо-скоригований ефект зменшення концентрації ТГ при >750 мг/дл становив 45%. У дослідженні, де вивчали вплив ПНЖК омега‑3 у пацієнтів із загальним середнім рівнем ТГ ~900 мг/дл, мало місце зниження рівня ТГ із поправкою з урахуванням плацебо на 60% (Harris et al., 1997).
Зміни ліпопротеїнів в інших класах також важливі для оцінки ефектів засобів, що містять ПНЖК омега‑3. Однак слід зазначити, що вимірювання ХС ліпопротеїнів низької щільності (ЛПНЩ) у хворих із підвищеним рівнем ТГ може бути неточним. Так, у пацієнтів із дуже високим вмістом ТГ, які отримували засоби з EПК + ДГК, концентрація ЛПНЩ збільшилася на ~15‑36% (Pownall et al., 1999; Kastelein et al., 2014). Проте в останньому дослідженні зростання рівня апо-B не спостерігалося. Тож, імовірно, підвищення рівня ЛПНЩ може відображати збільшення середнього розміру часток ЛПНЩ, а не їхньої концентрації.
Такий вплив на розмір часток ЛПНЩ підтверджується результатами нещодавніх досліджень (Dunbar et al., 2015; Maki et al., 2011). У пацієнтів із дуже високим вмістом ТГ (500‑2000 мг/дл) при застосуванні ЕПК рівень ЛПНЩ не підвищився, а апо-В – зменшився, що свідчить про різницю в ефекті порівняно з EПК + ДГК (Bays et al., 2011). Щодо ХС ліпопротеїнів високої щільності (ЛПВЩ), у більш ранніх дослідженнях із використанням О3КЕЕ повідомлялося про зростання показника на ~12% (Harris et al., 1997; Pownall et al., 1999). Однак, за даними Bays et al. (2011) та Kastelein et al. (2014), ані ЕПК, ані О3КК суттєво не вплинули на концентрацію ЛПВЩ.
Деякі пацієнти із дуже високим рівнем ТГ потребують призначення декількох засобів на додаток до корекції режиму харчування, способу життя та потенційної зміни терапії. У низку досліджень ЕПК та О3КК були включені хворі, що додатково приймали статини (Bays et al., 2011; Kastelein et al., 2014). Дані рандомізованих контрольованих випробувань щодо впливу ПНЖК омега‑3 у поєднанні з нестатином у цій популяції хворих обмежені. Так, у пацієнтів, які отримували комбінацію 130 мг/добу фенофібрату та 4 г/добу O3КEE, спостерігали зниження рівня ТГ на 61%. У відкритому додатковому дослідженні додавання O3КEE до фенофібрату зменшило концентрацію ТГ ще на 18%, а загалом показник становив 71% (Roth et al., 2009).
Ефективність монотерапії ПНЖК омега‑3
Були проаналізовані дані шести випробувань щодо застосування 3‑4 г/добу ПНЖК омега‑3 в осіб із високим рівнем ТГ, які не приймали інших ліпідознижувальних засобів (Mackness et al., 1994; Grundt et al., 1995; Skulas-Ray et al., 2011; Oh et al., 2014; Minihane et al., 2000; Leigh-Firbank et al., 2002). У чотирьох дослідженнях призначали O3КEE по 4 г/добу (що відповідало 3,4 г/добу ЕПК + ДГК) та у двох – ЕПК + ДГК в аналогічних дозах як лікувальне харчування або дієтичну добавку. В середньому зниження рівня ТГ становило ~27%. У більш ранній роботі з вивчення ефекту дієтичної добавки із ПНЖК омега‑3 у вищій дозі (4,5 г/добу ЕПК + ДГК) повідомлялося про зниження рівня ТГ на 39% через шість місяців (Bairati et al., 1992).
Додавання ПНЖК омега‑3 до інших ліпідознижувальних препаратів
У восьми випробуваннях вивчали застосування засобів із ПНЖК омега‑3 у дозі 4 г /добу в осіб із високим рівнем ТГ на тлі статинотерапії. У двох дослідженнях ЕПК та одному – ОЗКК ці ПНЖК омега‑3 сприяли зниженню показника на ~21% (Nordestgaard, Varbo, 2014). У 2 із 5 досліджень результатом поєднання O3КEE зі статинами стало зменшення вмісту ТГ на 17‑19%, ХС не-ЛПВЩ – на 5‑7%, а рівень ХС ЛПНЩ залишався незмінним порівняно з контролем лише статинами (Bays et al., 2010; Maki et al., 2008). У роботі M.H. Davidson et al. (2007) всі хворі отримували статин у стабільній дозі перед початком приймання O3КE. Як наслідок, спостерігалося незначне зростання рівня ЛПНЩ порівняно із плацебо (у середньому на 3,5%).
За нещодавно опублікованими даними REDUCE-IT, повідомлялося про скореговане за плацебо зниження рівня ТГ на 20%, ХС ЛПВЩ – 7%, ХС не-ЛПВЩ – 12%, апо-В – 10% та ХС ЛПНЩ – 7% через чотири місяці приймання ПНЖК омега‑3 і статинів (Bhatt et al., 2019). При використанні ОЗКК як доповнення до лікування статинами вміст ТГ зменшувався на 15%, ХС ЛПВЩ – 6% та апо-В – 2%, тоді як ХС ЛПНЩ лишався незмінним, а розмір часток ЛПНЩ дещо збільшувався (Maki et al., 2013; Dunbar et al., 2015).
Таким чином, усі три зазначені засоби на основі ПНЖК омега‑3 були ефективними щодо зниження рівня ТГ та атерогенних ліпопротеїдів у комбінації зі статинотерапією.
У трьох дослідженнях оцінювали дієтичні добавки із ПНЖК омега‑3 у нижчих дозах (2,4‑2,7 г/добу ЕПК + ДГК) при сумісному використанні зі статином або езетимібом. Згідно з отриманими даними, автори повідомили про зниження рівня ТГ на 22‑31% (Hedengran et al., 2015; Makiet al., 2014; Vecka et al., 2012). В одній із робіт, де учасники приймали чи не приймали статини, мало місце загальне зниження рівня ТГ на 28% у результаті застосування ЕПК + ДГК по 2,6 г/добу, яке не відрізнялося між двома групами (Vecka et al., 2012). Це підтверджує концепцію, що зменшення вмісту ТГ на тлі використання ПНЖК омега‑3 не залежить від одночасної терапії статинами.
Дані випробувань комбінованого приймання засобів із ПНЖК омега‑3 та фібратами/ніацином у пацієнтів із високим рівнем ТГ обмежені. У роботі K.K. Koh et al. (2016) сумісне застосування фенофібрату та O3КEE (2 г/добу) привело до значного зменшення ТГ на 11% порівняно з лише фенофібратом. У меншому дослідженні (n<20 на групу) хворих із метаболічним синдромом та високою концентрацією ТГ лікували 4 г/добу O3КEE, 2 г/добу ніацину із пролонгованим вивільненням, їхнім поєднанням або плацебо протягом 16 тижнів (Shearer et al., 2012). Вміст ТГ зменшився на 13% у групі O3КEE, на 21% – ніацину із пролонгованим вивільненням та на 33% – у комбінованій групі.
Порівняльна міжгрупова оцінка застосування ПНЖК омега‑3 у хворих із високим рівнем ТГ
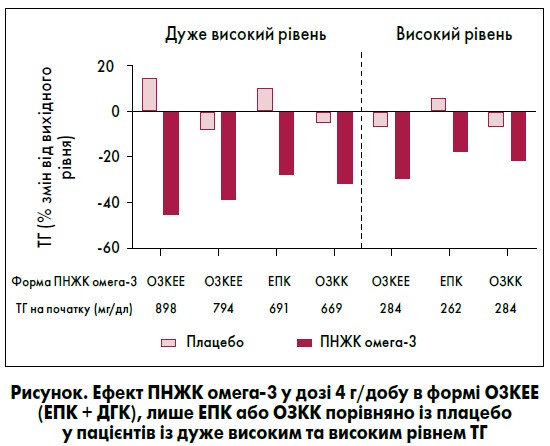
За даними масштабних досліджень, порівняльний аналіз впливу засобів, що містять ПНЖК омега‑3, на рівень ТГ в осіб із високим його вмістом показаний на рисунку (Davidson et al., 2007; Ballantyne et al., 2012; Bhatt et al., 2019; Maki et al., 2013). У додатковому випробуванні вивчали зіставний ефект O3КEE (2 або 4 г/добу) та ЕПК (2 г/добу) в ~600 пацієнтів, 40% з яких отримували фонові ліпідознижувальні засоби (переважно статини) (Tatsuno et al., 2013). Зменшення концентрації ТГ становило ~11% у групах O3КEE та ЕПК через 12 тижнів, дещо більше зниження показника спостерігалося через один рік.
 На додаток, у деяких дослідженнях за участю пацієнтів із високим вмістом ТГ вивчали вплив препаратів із ПНЖК омега‑3 на інші показники атерогенних ліпопротеїнів, як-то ХС не-ЛПВЩ та апо-B. За даними трьох найбільших робіт, на тлі приймання 4 г/добу O3КEE рівень ХС не-ЛПВЩ знизився на 5‑7%, у двох із них апо-B – на 2‑3% (Kastelein et al., 2014; Skulas-Ray et al., 2015). При використанні O3КК та ЕПК концентрація ХС не-ЛПВЩ зменшилася на 6 і 14% та апо-B – на 2 і 9% відповідно (Maki et al., 2013; Oh et al., 2014). Аналогічним чином, у REDUCE-IT зниження ХС не-ЛПВЩ становило 12,2%, апо-В – 9,7% (Bhatt et al., 2019).
На додаток, у деяких дослідженнях за участю пацієнтів із високим вмістом ТГ вивчали вплив препаратів із ПНЖК омега‑3 на інші показники атерогенних ліпопротеїнів, як-то ХС не-ЛПВЩ та апо-B. За даними трьох найбільших робіт, на тлі приймання 4 г/добу O3КEE рівень ХС не-ЛПВЩ знизився на 5‑7%, у двох із них апо-B – на 2‑3% (Kastelein et al., 2014; Skulas-Ray et al., 2015). При використанні O3КК та ЕПК концентрація ХС не-ЛПВЩ зменшилася на 6 і 14% та апо-B – на 2 і 9% відповідно (Maki et al., 2013; Oh et al., 2014). Аналогічним чином, у REDUCE-IT зниження ХС не-ЛПВЩ становило 12,2%, апо-В – 9,7% (Bhatt et al., 2019).
Вплив ПНЖК омега‑3 на кардіоваскулярні наслідки пацієнтів при застосуванні статинотерапії
У великому рандомізованому плацебо-контрольованому клінічному випробуванні REDUCE-IT вивчали вплив 4 г/добу ПНЖК омега‑3 (ЕПК) на клінічні наслідки АССЗ в осіб із високим вмістом ТГ на тлі лікування статинами (Bhatt et al., 2017). Загалом до спостереження було залучено 8179 пацієнтів з 11 країн, середній рівень ТГ яких становив 216 мг/дл. Критеріями включення у дослідження були вік ≥45 років із наявним АССЗ (71%) або вік ≥50 років із цукровим діабетом та принаймні ще одним основним фактором ризику (29%). Усі хворі отримували статин у стабільній дозі та мали вихідний показник ХС ЛПНЩ 41‑100 мг/дл.
На тлі застосування ЕПК спостерігалося зниження комбінованої первинної кінцевої точки на 25%, що включала СС-смерть, нефатальні інфаркт міокарда й інсульт, коронарну реваскуляризацію та нестабільну стенокардію (Bhatt et al., 2019). Ризик для кожного окремого компонента первинної комбінованої кінцевої точки також значно знизився (зокрема СС-смерть на 20%).
Зниження ризику ССЗ не відрізнялося у пацієнтів за показників ТГ >150 або <150 мг/дл протягом одного року. Однак у підгрупі хворих, які розпочали випробування при ТГ >200 мг/дл та ХС ЛПВЩ ≤35 мг/дл (~20% від загальної когорти), спостерігалося більш значуще зниження ризику первинної кінцевої точки, ніж у тих, хто не відповідав цьому критерію (38 та 21% відповідно). Отримані результати свідчать про те, що високий рівень ТГ (особливо у поєднанні з низьким ХС ЛПВЩ) являє собою потенційний корисний біомаркер для виявлення пацієнтів, які можуть мати найбільші переваги від призначення засобів із ПНЖК омега‑3. Однак зниження ризику АССЗ може не залежати від досягнення конкретної мети щодо ТГ натще.
Висновки
За результатами проведеного аналізу наукових даних, призначення засобів, що містять ПНЖК омега‑3 у дозі 4 г/добу, сприяє суттєвому зниженню у пацієнтів високого або дуже високого рівня ТГ плазми крові. Зокрема, цей ефект є більш значущим в осіб із дуже високою концентрацією ТГ (зниження на ≥30%). У контексті високого вмісту ТГ (200‑499 мг/дл) ПНЖК омега‑3 ефективно знижує цей показник на ~20‑30% і несуттєво збільшує ХС ЛПНЩ. Підсумкові положення ефектів ПНЖК омега‑3 у контексті зниження високого рівня ТГ наведені в таблиці. На додаток, використання ПНЖК омега‑3 безпечне та зазвичай добре переноситься. Також застосування ЕПК + ДГК або лише ЕПК як доповнення до статинотерапії помірно знижує вміст ХС не-ЛПВЩ та апо-B. Це свідчить про зменшення загальної кількості атерогенних ліпопротеїнів.
Таким чином, засоби, що містять ПНЖК омега‑3 (ЕПК + ДГК або ЕПК) у дозі 4 г/добу, являють собою ефективний та безпечний окремий варіант зниження рівня ТГ, а також як доповнення до інших гіполіпідемічних засобів. Окрім того, у всіх пацієнтів слід дотримуватися рекомендацій щодо належного режиму харчування та здорового способу життя.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (73) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...





