Діагностика та лікування фібриляції передсердь
Фібриляція передсердь (ФП) – суправентрикулярна тахіаритмія з некоординованою електричною активністю передсердь та, як наслідок, прогресивним погіршенням їхньої електромеханічної функції. ФП становить значний тягар для пацієнтів, лікарів і систем охорони здоров’я загалом у всьому світі. Необхідний багатогранний, цілісний та мультидисциплінарний підхід до ведення пацієнтів із ФП з їхнім активним залученням та співпрацею з клініцистами. Оптимізація медичної допомоги хворим на ФП у щоденній клінічній практиці є складною, але важливою вимогою для ефективного лікування ФП. Останніми роками було досягнуто значного прогресу в діагностиці й терапії ФП. Цьогоріч на основі сучасних доказових даних Європейське товариство кардіологів (ESC) та Європейська асоціація кардіоторакальної хірургії (EACTS) розробили рекомендації щодо ведення пацієнтів із ФП. Документ покликаний допомогти лікарям у виборі й реалізації найліпших профілактичних, діагностичних чи терапевтичних стратегій відповідно до індивідуальних потреб хворих.
Діагностика та скринінг ФП
Для встановлення діагнозу ФП необхідна документована реєстрація електрокардіограми (ЕКГ). Діагностику клінічної ФП проводять шляхом стандартного запису ЕКГ у 12 відведеннях або одноканальної ЕКГ тривалістю ≥30 с, що показує серцевий ритм без помітних повторюваних зубців Р та нерегулярних інтервалів RR (коли атріовентрикулярну провідність не порушено) (І, В).
У пацієнтів віком ≥65 років потрібно виконувати позапланове обстеження із приводу наявності ФП за допомогою вимірювання пульсу або моніторингу ЕКГ (І, В). Рекомендовано регулярно перевіряти кардіостимулятори та імплантовані кардіовертери-дефібрилятори щодо епізодів високої передсердної частоти (І, В).
Під час скринінгу щодо ФП необхідно (І, В):
- інформувати осіб, які проходять обстеження, про важливість та наслідки виявлення ФП для призначення лікування;
- у разі виявлення ФП організувати структуровану взаємодію спеціалістів для подальшої клінічної оцінки з метою підтвердження діагнозу та забезпечення оптимального ведення пацієнтів;
- на основі первинних результатів скринінгу лікар має встановити точний діагноз ФП лише після ретельного аналізу записів одноканальної
ЕКГ тривалістю ≥30 с або ЕКГ у 12 відведеннях.
У пацієнтів із ФП рекомендовано проаналізувати симптоми, пов’язані з ФП, що включають слабкість, швидку стомлюваність, задишку при фізичному навантаженні, надмірне серцебиття та біль за грудиною, за допомогою модифікованої шкали оцінки тяжкості симптомів Європейської асоціації серцевого ритму (EHRA) до та після початку лікування (І, С). Крім того, необхідно оцінити асоційовані з ФП симптоми до й після проведення кардіоверсії персистувальної ФП, аби прийняти рішення щодо шляхів оптимального контролю частоти серцевого ритму (І, С).
В осіб з епізодами високої передсердної частоти / субклінічною ФП, виявленою за допомогою імплантованого кардіального електронного пристрою або вставного кардіомонітора, рекомендовано виконати всебічну оцінку серцево-судинної системи із реєстрацією ЕКГ, аналізом клінічних факторів ризику та/або супутніх патологій, а також імовірності тромбоемболічних подій із використанням шкали CHA2DS2-VASc (І, В). На додаток, слід проводити безперервне спостереження та моніторинг пацієнта (бажано дистанційний) для виявлення прогресування клінічної ФП, контролю навантаження епізодів високої передсердної частоти / субклінічної ФП та визначення основних клінічних змін (І, В).
Діагностична оцінка й терапія для профілактики інсульту та інших ускладнень, пов’язаних із ФП, для жінок та чоловіків є однаковою (І, А).
Комплексне лікування пацієнтів із ФП
При прийнятті спільного рішення клініцистом та хворим щодо конкретних варіантів лікування ФП рекомендовано інформувати пацієнта про переваги/обмеження і співвідношення користі/ризику, пов’язані з розглянутою терапією, та враховувати його думку із приводу вищенаведеного при визначенні оптимальних втручань (І, С). Доцільно проводити регулярне опитування хворих щодо результатів лікування для поліпшення його якості та догляду за пацієнтами (І, С).
Профілактика тромбоемболічних подій при ФП
Для профілактики інсульту в осіб із ФП, яким показане лікування оральними антикоагулянтами (ОАК), перевагу слід віддавати ОАК, що не є антагоністами вітаміну К (НОАК), перед антагоністами вітаміну К (АВК). Виняток становлять пацієнти з механічними клапанами серця або мітральним стенозом від середньої до тяжкої форми (І, А). Для оцінки імовірності виникнення інсульту рекомендований підхід, що ґрунтується на факторах ризику з використанням шкали CHA2DS2-VASc. Спершу потрібно виявити пацієнтів із низьким ризиком розвитку інсульту (бал за CHA2DS2-VASc 0 у чоловіків та 1 у жінок), яким недоцільно призначати антитромботичну терапію (І, А). OAК слід застосовувати для профілактики інсульту в пацієнтів із ФП з показником за CHA2DS2-VASc ≥2 у чоловіків та ≥3 у жінок (І, А).
У всіх пацієнтів із ФП рекомендовано провести структуровану оцінку для виявлення немодифікованих та врахування модифікованих факторів ризику кровотечі. Також необхідно визначити хворих із потенційно високою імовірністю кровотечі, які мають перебувати під більш ретельним спостереженням якомога раніше (І, В).
Слід періодично виконувати переоцінку ризику інсульту та кровотеч для корегування лікування (наприклад, ініціація ОАК у пацієнтів, які більше не мають низького ризику інсульту) та усунення модифікованих чинників ризику кровотечі (І, В). При використанні АВК цільове міжнародне нормалізоване відношення (МНВ) має становити 2,0‑3,0 з індивідуальним періодом у терапевтичному діапазоні (ПТД) ≥70%. Пацієнтів, що отримують лікування АВК, із низьким показником ПТД (наприклад, <70%) доцільно перевести на НОАК, але контролювати належний комплаєнс та регулярність терапії (І, В).
Застосування антиагрегантів у монотерапії або комбінації ацетилсаліцилової кислоти (АСК) та клопідогрелю для профілактики інсульту при ФП не рекомендоване (ІІІ, А). Потенційний ризик кровотечі, за відсутності абсолютних протипоказань до використання ОАК, сам по собі не має впливати на прийняття рішення щодо призначення лікування ОАК для профілактики інсульту (ІІІ, А). Клінічна картина ФП (вперше виявлена, пароксизмальна, персистувальна, тривало персистувальна, стійка) не повинна зумовлювати показання для проведення тромбопрофілактики (ІІІ, В).
Контроль серцевого ритму в пацієнтів із ФП
Терапевтичні заходи щодо контролю серцевого ритму є доцільними для зменшення симптомів та поліпшення якості життя у симптомних пацієнтів із ФП (І, А). Для регулювання частоти серцевих скорочень (ЧСС) у хворих на ФП із фракцією викиду (ФВ) лівого шлуночка (ЛШ) ≥40% як препарати першого вибору рекомендовані β-блокатори, дилтіазем або верапаміл, із ФВ ЛШ <40% – β-блокатори та/або дигоксин (І, В). Селективні β-блокатори слід застосовувати для контролю ЧСС у вагітних із ФП (I, C).
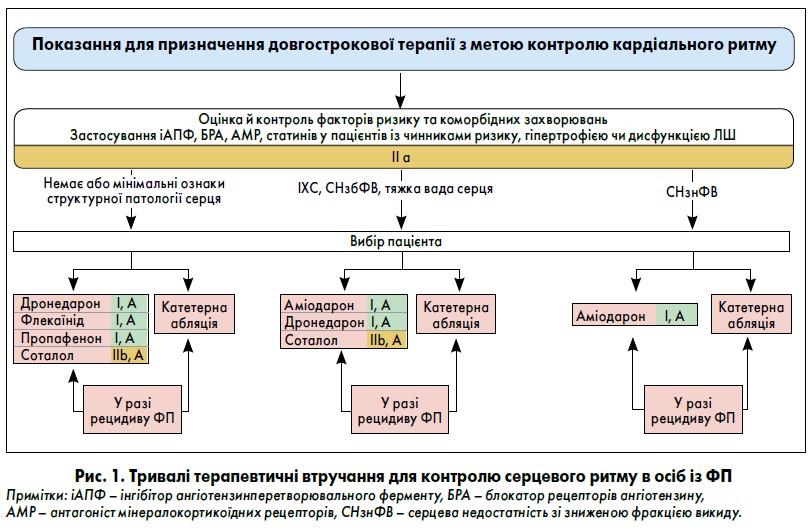
Довгострокове лікування антиаритмічними препаратами
Флекаїнід або пропафенон рекомендовані для тривалого контролю кардіального ритму у хворих на ФП із нормальною функцією ЛШ та без структурних захворювань серця, включно з виразною гіпертрофією ЛШ та ішемією міокарда (І, А). Дронедарон призначають для довгочасного контролю ритму в пацієнтів із ФП, що мають нормальну або помірно знижену (але стабільну) функцію ЛШ, серцеву недостатність зі збереженою фракцією викиду (СНзбФВ), ішемічну хворобу серця або ваду серця (І, А). Аміодарон доцільно використовувати для тривалого контролю ритму в усіх осіб із ФП, зокрема з СНзбФВ. Однак через екстракардіальні побічні явища, асоційовані з цим препаратом, за можливості слід призначити інші антиаритмічні препарати (ААП) (І, А).
У пацієнтів із ФП, які отримують лікування соталолом, рекомендований ретельний моніторинг інтервалу QT, рівня калію в сироватці крові, кліренсу креатиніну та інших факторів ризику розвитку проаритмії (І, В). Терапію ААП не варто призначати хворим на стійку ФП за контролю ЧСС та пацієнтам із серйозними порушеннями провідності, якщо не передбачено антибрадикардичної стимуляції (ІІІ, С).
Алгоритм тривалих терапевтичних втручань для контролю серцевого ритму в пацієнтів із ФП представлений на рисунку 1.
Катетерна абляція із приводу ФП
Катетерна абляція рекомендована для усунення дисфункції ЛШ у хворих на ФП, коли ймовірність розвитку кардіоміопатії, індукована тахікардією, є високою незалежно від тяжкості симптомів (І, В). При прийнятті рішення щодо проведення катетерної абляції в осіб із ФП слід враховувати асоційовані з нею потенційні негативні наслідки й основні фактори ризику рецидиву ФП після процедури та обговорити їх із пацієнтом (І, В). Катетерну абляцію при ФП для ізоляції легеневих вен рекомендовано з метою контролю кардіального ритму після одного застосування ААП I або III класу, що виявилося неефективним або непереносимим. Процедуру виконують для зменшення рецидиву симптомів ФП у пацієнтів із пароксизмальною ФП (І, А), персистувальною формою без основних факторів ризику рецидиву ФП (І, А) або персистувальною формою за наявності основних чинників ризику рецидиву ФП (І, В).
Повну електричну ізоляцію легеневих вен рекомендовано проводити під час усіх процедур катетерної абляції у пацієнтів із ФП (І, А).
Модифікація способу життя, зокрема, зниження ваги є важливою для всіх пацієнтів із ФП, що страждають на ожиріння, особливо тих, кому показано катетерну абляцію. У межах стратегії моніторингу серцевого ритму необхідні строгий контроль факторів ризику та уникання тригерів для поліпшення результатів процедури (І, В).
Контроль ризику інсульту після катетерної абляції
В осіб із ФП та факторами ризику інсульту, які не приймають ОАК перед катетерною абляцією, рекомендовано ініціювати антикоагулянтну терапію, бажано ОАК, принаймні за три тижні до операції (І, С). У пацієнтів, яким показано катетерну абляцію із приводу ФП, і при цьому вони отримували антикоагулянти варфарин, дабігатран, ривароксабан, апіксабан або едоксабан, процедуру треба проводити без переривання застосування ОАК (І, А).
Після катетерної абляції рекомендованими є (І, С):
- системна антикоагулянтна терапія варфарином або НОАК тривалістю щонайменше два місяці після операції;
- довгострокове системне використання антикоагулянтів через два місяці після процедури, що має базуватися на профілі ризику інсульту пацієнта, а не на успішному чи невдалому виконанні катетерної абляції.
У хворих після операції із приводу ФП та закриття вушка лівого передсердя необхідне довгочасне лікування ОАК на основі індивідуального тромбоемболічного ризику за шкалою CHA2DS2-VASc (І, С).
Контроль ризику інсульту після кардіоверсії
У пацієнтів із ФП, які перенесли кардіоверсію, рекомендовано застосовувати НОАК із принаймні такою самою ефективністю та безпекою, як варфарин (І, А). При проведенні кардіоверсії з приводу ФП / тріпотіння передсердь доцільною є дієва антикоагулянтна терапія щонайменше за три тижні до процедури (І, В). При плануванні ранньої кардіоверсії слід виконати трансезофагеальну ехокардіографію (ЕхоКГ) для виключення серцевого тромбу як альтернативу 3-тижневій допроцедурній антикоагуляції (І, В).
Хворим із ризиком інсульту рекомендовано продовжувати довгострокову терапію OAК після кардіоверсії згідно з відповідними рекомендаціями з антикоагулянтної терапії, незалежно від методу кардіоверсії, очевидного підтримання синусового ритму або характеристики ФП як вперше діагностованого епізоду (І, В).
При виявленні тромбу на трансезофагеальній ЕхоКГ слід провести ефективне антикоагулянтне лікування принаймні за три тижні до кардіоверсії з приводу ФП (І, В). Важливо настійно наголошували пацієнтам на необхідності дотримання режиму терапії та регулярного приймання НОАК як до, так і після кардіоверсії (І, С).
Вторинна профілактика в пацієнтів із ФП після гострого ішемічного інсульту
У хворих на ФП, що перенесли ішемічний інсульт або транзиторну ішемічну атаку (ТІА), слід проводити тривалу вторинну профілактику інсульту із застосуванням ОАК у разі відсутності строгих протипоказань (І, А). При цьому перевагу мають НОАК перед АВК за наявності показань. У пацієнтів із ФП після гострого ішемічного інсульту дуже рання антикоагулянтна терапія (<48 год) із використанням нефракціонованого, низькомолекулярного гепарину або АВК не рекомендована (ІІІ, В).
Медикаментозна та електрична кардіоверсія
Кардіоверсія ФП (електрична/фармакологічна) рекомендована особам із симптомами персистувальної або тривало персистувальної ФП як частина терапії для контролю серцевого ритму (I, В).
Медикаментозну кардіоверсію при ФП показано лише для гемодинамічно стабільного хворого з урахуванням тромбоемболічного ризику (I, В). Для фармакологічної кардіоверсії вперше діагностованої ФП рекомендоване внутрішньовенне (в/в) введення вернакаланту (крім пацієнтів із нещодавно перенесеним гострим коронарним синдромом [ГКС] або тяжкою формою СН), флекаїніду або пропафенону (за виключенням осіб із тяжким структурним захворюванням серця) (I, А).
Застосування аміодарону в/в слід розглянути для кардіоверсії з приводу ФП у хворих на СН та структурні патології серця, якщо відстрочена процедура відповідає клінічній ситуації (I, А). У пацієнтів із синдромом слабкості синусового вузла, порушенням атріовентрикулярної провідності або подовженим інтервалом QTc (>500 мс) не слід виконувати фармакологічну кардіоверсію, якщо не враховано ризики проаритмії та брадикардії (IІІ, С).
Екстрену електричну кардіоверсію проводять у пацієнтів із ФП із гемодинамічною нестабільністю, що є гострою або погіршується (I, В). Вагітним пацієнткам із ФП вона показана у разі гемодинамічної нестабільності або попереднього збудження шлуночків (I, С).
Інші терапевтичні умови
 У пацієнтів із ФП, яким показане лікування НОАК, потрібно віддавати перевагу НОАК перед АВК у поєднанні з антиагрегантами (І, А). В осіб із ФП та ГКС, які перенесли неускладнене черезшкірне коронарне втручання (ЧКВ), рекомендовано раннє припинення (на 1-му тижні) приймання АСК і продовження подвійної терапії OAК та інгібітором P2Y12 (переважно клопідогрелем) протягом 12 місяців. При цьому ймовірність тромбозу стенту має бути низькою, або ж побоювання щодо ризику кровотечі переважає над таким щодо тромбозу стенту незалежно від його типу (І, В).
У пацієнтів із ФП, яким показане лікування НОАК, потрібно віддавати перевагу НОАК перед АВК у поєднанні з антиагрегантами (І, А). В осіб із ФП та ГКС, які перенесли неускладнене черезшкірне коронарне втручання (ЧКВ), рекомендовано раннє припинення (на 1-му тижні) приймання АСК і продовження подвійної терапії OAК та інгібітором P2Y12 (переважно клопідогрелем) протягом 12 місяців. При цьому ймовірність тромбозу стенту має бути низькою, або ж побоювання щодо ризику кровотечі переважає над таким щодо тромбозу стенту незалежно від його типу (І, В).
У хворих із ФП та хронічним коронарним синдромом після неускладненого ЧКВ доцільним є передчасне (впродовж ≤1 тижня) приймання АСК, а також продовження подвійної терапії OAК і клопідогрелем до шести місяців. При цьому ймовірність тромбозу стенту має бути низькою, або ж побоювання щодо ризику кровотечі переважає над таким щодо тромбозу стенту незалежно від його типу (І, В).
Алгоритм післяопераційного ведення пацієнтів із ФП, ГКС та тих, що перенесли ЧКВ, представлений на рисунку 2.
НОАК протипоказані пацієнтам із механічним протезом клапана (III, С). Не рекомендовано застосовувати НОАК в осіб із ФП і мітральним стенозом середньої та тяжкої форми (III, С). У пацієнтів із ФП та великою активною кровотечею рекомендовано перервати використання OAК до встановлення її причини й зупинки. Для цього необхідне проведення оперативних діагностичних та лікувальних заходів (І, С).
У вагітних хворих на ФП доцільно проводити антикоагулянтну терапію гепарином або АВК залежно від стадії вагітності (І, С).
Передопераційна терапія аміодароном або β-блокатором рекомендована для профілактики ФП після кардіохірургічних втручань (І, А). Бета-блокатори не слід регулярно застосовувати для профілактики післяопераційної ФП у пацієнтів, які перенесли некардіальну операцію (ІІІ, В).
Корекція способу життя, контроль факторів ризику та супутніх захворювань у пацієнтів із ФП
Виявлення та контроль факторів ризику й коморбідних патологій є невід’ємною частиною лікування хворих на ФП (І, В). Модифікація способу життя й таргетна терапія інтеркурентних станів рекомендовані для зменшення навантаження ФП та тяжкості симптомів (І, В). У пацієнтів з артеріальною гіпертензією (АГ) слід проводити позапланове обстеження із приводу ФП (І, В). Також в осіб з супутніми ФП та АГ необхідний належний контроль артеріального тиску для зниження ризику рецидиву ФП, інсульту та кровотечі (І, В). Лікарі мають інформувати професійних спортсменів, що тривалі інтенсивні фізичні навантаження можуть спричиняти ФП, помірні ж, навпаки, запобігають її розвитку (І, В).
Підготувала Олена Коробка
Оригінальний текст документа, включно зі списком літератури, читайте на сайті
www.academic.oup.com
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (73) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...