Застосування фебуксостату в пацієнтів із хронічною хворобою нирок та гіперурикемією
Гіперурикемію визначають як збільшення концентрації уратів у сироватці крові до більш ніж 6,8‑7,0 мг/дл. Цей клінічний симптом є дуже поширеним у всьому світі й асоційований із розвитком низки захворювань і станів, як-от метаболічний синдром і серцево-судинна патологія, включно з артеріальною гіпертензією (АГ) та основними кардіоваскулярними подіями. Доведено, що безсимптомна гіперурикемія є незалежним фактором ризику хронічної хвороби нирок (ХХН), що визначається як порушення функції або структури нирок тривалістю більш ніж три місяці з негативними наслідками для здоров’я. Однак роль гіперурикемії у прогресуванні ХХН лишається не до кінця зрозумілою. T.-C. Lin et al. провели аналіз досліджень для оцінки ефективності та безпеки фебуксостату – уратознижувального засобу першого вибору для лікування осіб із ХХН і гіперурикемією. Отримані результати опубліковані у виданні Medicine (2019; 98 (29): e16311).
Відповідно до настанови Американського коледжу ревматологів (ACR, 2012), фармакологічну уратознижувальну терапію (УЗТ) рекомендовано пацієнтам із поточною гіперурикемією та перенесеними нападами подагри (Khanna et al., 2012). Однак через відсутність досліджень причинно-наслідкового зв’язку між гіперурикемією та прогресуванням системних захворювань, включно з АГ, кардіоваскулярними патологіями та ХХН, досі неясно, чи слід лікувати гіперурикемію за наявності хвороб, що не пов’язані з подагрою (Stamp, Dalbeth, 2011).
Стосовно ХХН, дослідження на тваринах показали, що зниження рівня сечової кислоти може поліпшити роботу нирок (Kosugi et al., 2009; Kang, 2002). За результатами деяких клінічних випробувань, гіперурикемія є незалежним фактором ризику хвороби нирок, і зменшення концентрації сечової кислоти може уповільнити її прогресування (Bellomo et al., 2010; Obermayr et al., 2008). Інші ж дані свідчать про те, що цей показник пов’язаний із ХХН, але не обов’язково її прогресуванням (Madero et al., 2009; Sturm et al., 2008; Eleftheriadis et al., 2017).
У межах УЗТ першої лінії в пацієнтів із подагрою застосовують інгібітори ксантиноксидази, зокрема алопуринол та фебуксостат (Khanna et al., 2012). Алопуринол використовують із 1960-х рр. минулого століття для лікування гіперурикемії, однак слід зауважити, що він асоційований із низкою побічних ефектів (Li et al., 2016). Окрім незначних подій, як-то шлунково-кишкові розлади та легкий висип, алопуринол може призводити до розвитку тяжких станів, включно з еритродермією, синдромом Стівенса – Джонсона, токсичним епідермальним некролізом тощо (Ramasamy et al., 2013). На додачу, ризик реакції гіперчутливості до алопуринолу вищий у популяції пацієнтів, що страждають на ССЗ або хворобу нирок (Yang et al., 2015).
На противагу, фебуксостат є новим інгібітором ксантиноксидази, що затверджений Управлінням з контролю за якістю продуктів харчування та медикаментів США (FDA) 2009 р. Мережевий метааналіз показав, що фебуксостат має вищу ефективність, ніж алопуринол в осіб із гіперурикемією з/без подагри (Li et al., 2016). Крім того, дослідження продемонстрували, що фебуксостат рідше спричиняє побічні явища порівняно з алопуринолом (Tayar et al., 2012). Фебуксостат переважно метаболізується у печінці, тоді як алопуринол здебільшого виводиться через нирки, тож у пацієнтів із ХХН може знадобитися корекція дози останнього (El-Zawawy et al., 2010; Stamp, Chapman, 2014). Фебуксостат же показав доведену ефективність та безпеку в осіб із помірною і тяжкою нирковою недостатністю, тому корегування дози у цих хворих не потрібне (Shibagaki et al., 2014; Hira et al., 2015).
C. Lin et al. (2019) виконали систематичний огляд досліджень та метааналіз даних для детальнішої оцінки ефективності та безпеки фебуксостату в пацієнтів із ХХН та гіперурикемією.
Матеріали й методи дослідження
Критерії включення та виключення, аналіз даних
У базах даних MEDLINE, PubMed, EMBASE та Cochrane автори провели пошук рандомізованих контрольованих досліджень (РКД), опублікованих із 2015 до 2018 рр., в яких оцінювали ефективність фебуксостату порівняно з контролем в осіб із ХХН та гіперурикемією. Загалом було знайдено 528 випробувань; до аналізу увійшли 11 робіт із загальною кількістю 1317 учасників, що відповідали наступним критеріям (Alshahawey et al., 2017; Kimura et al., 2018; Mukri, 2018):
- проводилася оцінка ефективності та безпеки фебуксостату в осіб із ХХН;
- чітко зафіксовані критерії включення та виключення для відбору пацієнтів;
- належним чином задокументовані дозування та тривалість лікування в основній та контрольній групах;
- РКД.
Дослідження були виключені з аналізу, якщо необхідні результати не були чітко зафіксовані або отримання чи обчислення відповідних даних виявилося неможливим.
Для оцінки ефективності та безпеки фебуксостату при гіперурикемії у хворих на ХХН використовували такі показники: рівень сечової кислоти та креатиніну в сироватці крові, розрахункову швидкість клубочкової фільтрації (рШКФ), високочутливий C-реактивний білок (вчСРБ), систолічний і діастолічний артеріальний тиск (АТ), несприятливі явища протягом періоду лікування та спостереження. Ризик систематичної похибки у кожному дослідженні аналізували за допомогою спеціального інструмента з кокранівських рекомендацій щодо систематичних оглядів втручань (Higgins, Green, 2011).
Дозування фебуксостату в усіх включених до метааналізу роботах становило від 10 до 80 мг/добу. У групі контролю в більшості досліджень пацієнти отримували плацебо. У двох дослідженнях порівнювали ефективність та безпеку фебуксостату з алопуринолом, в одному – із бензбромароном (Sezai et al., 2015; Tanaka et al., 2015; Yu et al., 2018).
Статистичний аналіз
Метааналіз із використанням моделі випадкових ефектів проводили у разі доступності даних щодо результату з ≥1 дослідження. Величину ефекту визначали як різницю середніх значень (РСЗ) між групами лікування та контролю. За потреби стандартні відхилення було оцінено на основі наданих меж довірчого інтервалу (ДІ), стандартної похибки або показників діапазону. Середнє значення та стандартну похибку визначали за допомогою методу оцінки перцентилів. Гетерогенність фіксували за допомогою кокранівських критеріїв Q та I2, зведену статистику було надано з 95% ДІ. Для аналізу використовували двосторонній тест, значення р<0,05 вважалося статистично значущим.
Результати дослідження
Оцінка рівня уратів, креатиніну сироватки та АТ
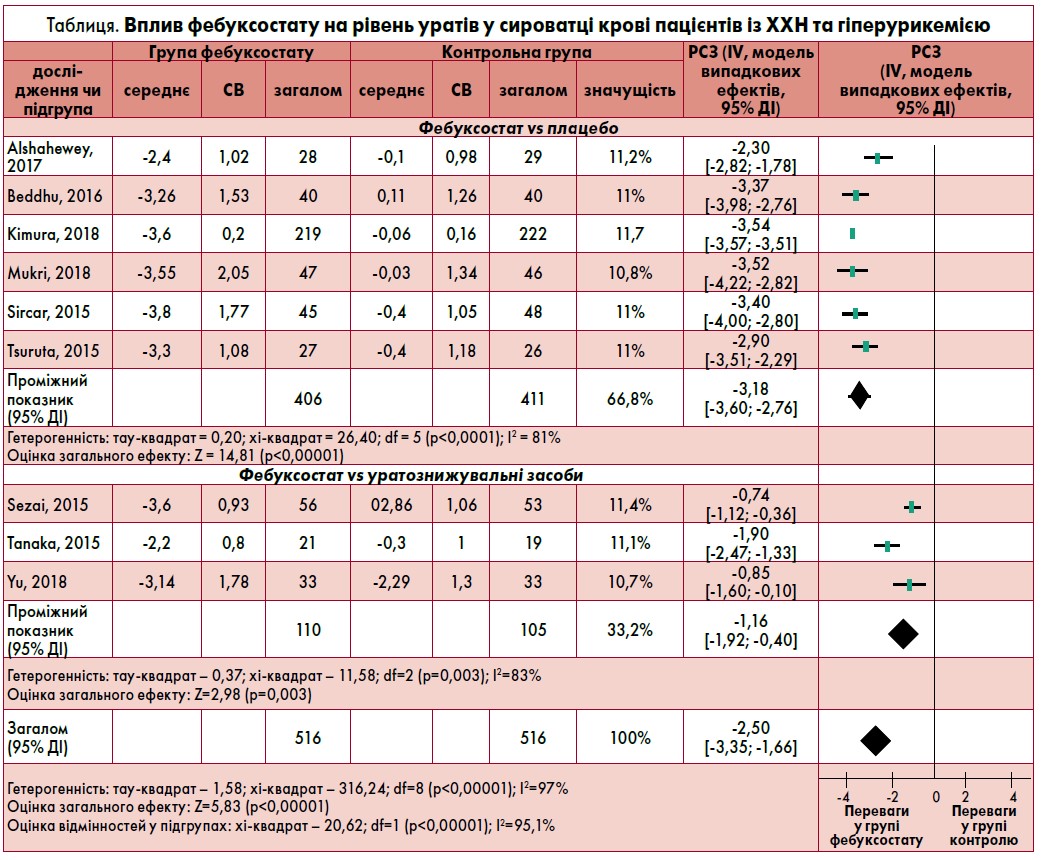
У низці досліджень було отримано результати зміни концентрації уратів у сироватці крові (Sircar et al., 2015; Tsuruta et al., 2015; Beddhu et al., 2016). У пацієнтів, які застосовували фебуксостат, спостерігалося суттєвіше зниження даного показника, ніж у групі контролю та при порівнянні з іншими препаратами УЗТ (Sezai et al., 2015; Yu et al., 2018). За переважною більшістю даних статистично значущої різниці щодо зміни показника вчСРБ між групами фебуксостату та алопуринолу не відзначено (Sezai et al., 2015; Alshahawey et al., 2017). Результати щодо впливу фебуксостату на рівень уратів у сироватці крові пацієнтів із ХХН та гіперурикемією порівняно із плацебо та іншими уратознижувальними засобами представлені у таблиці.
Також у дослідженнях оцінювали функцію нирок за зміною рШКФ та рівня креатиніну в сироватці крові (Saag et al., 2016; Sircar et al., 2015). У пацієнтів із ХХН 3-ї та 4-ї стадії, що отримували фебуксостат і плацебо, було підтверджено користь лікування фебуксостатом. Аналіз даної популяції хворих показав, що у групі терапії спостерігався вищий показник рШКФ. Зміну сироваткового креатиніну оцінювали у випробуваннях за участю хворих, які приймали фебуксостат або інші уратознижувальні засоби (Tanaka et al., 2015; Yu et al., 2018). Істотної різниці між результатами не спостерігалося. Однак статистично значущий нижчий рівень креатиніну в сироватці крові було відзначено у групі фебуксостату за тривалості лікування ≥6 місяців.
При оцінюванні змін рівня АТ суттєво нижчий показник систолічного АТ спостерігався у групі фебуксостату порівняно з контролем. Значущої міжгрупової різниці щодо діастолічного АТ не виявлено (Tsuruta et al., 2015; Alshahawey et al., 2017).
Безпека лікування
Безпеку терапії фебуксостатом у межах досліджень оцінювали шляхом оцінки рівня аланін-, аспартатамінотрансферази (АСТ) у сироватці крові, розвитку панцитопенії, серцево-судинних подій, кількості летальних випадків або будь-яких побічних явищ, пов’язаних із лікуванням (Kimura et al., 2018; Mukri, 2018). Не було виявлено суттєвої різниці між групами щодо серйозних ускладнень чи смерті, або ж їхній зв’язок із препаратом протягом подальшого спостереження (Saag et al., 2016). Загалом у роботах зафіксовані поодинокі випадки несприятливих явищ у групі фебуксостату: по одному – підвищеної активності печінкових ферментів, зниження АТ і висипу, а також легка діарея у двох суб’єктів (Sircar et al., 2015; Beddhu et al., 2016). Крім того, мали місце випадки вищої частоти болю в суглобах, зростання рівня АСТ і гемоглобіну (Yu et al., 2018). У більшості досліджень повідомлення про будь-які побічні ефекти при застосуванні фебуксостату протягом періоду спостереження відсутні.
Висновки
C. Lin et al. провели систематичний огляд та метааналіз для оцінки ефективності, ренопротекторного впливу та безпеки фебуксостату в пацієнтів із ХХН. Пацієнти, які отримували лікування цим препаратом, продемонстрували суттєвіше зниження рівня уратів сироватки порівняно з контрольною групою. Аналіз змін показника рШКФ в осіб із ХХН 3-ї та 4-ї стадії показав значний ренопротекторний ефект фебуксостату. Також спостерігалося виразне зниження рівня креатиніну в сироватці крові у хворих при застосуванні фебуксостату порівняно із групою контролю за тривалості лікування ≥6 місяців.
Таким чином, отримані результати показали, що, крім уратознижувального ефекту, фебуксостат чинить ренопротекторний вплив у хворих на ХХН. Проведене дослідження розширило уявлення про причинно-наслідковий зв’язок гіперурикемії з прогресуванням ХХН та вказує на можливі варіанти лікування у вищезазначеній популяції. Крім того, фебуксостат можна застосовувати для уповільнення погіршення стану пацієнтів із ХХН. Для з’ясування ролі фебуксостату в прогресуванні ХХН потрібні додаткові РКД із більшими вибірками та вищою якістю.
Підготувала Олена Коробка
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (73) 2020 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....