Ендометріоз: сучасні гайдлайни та практичний досвід лікування
У статті представлено сучасні рекомендації щодо ведення пацієнток з ендометріозом, результати вітчизняних досліджень ефективності різних методів лікування ендометріозу у жінок репродуктивного віку, які планують вагітність. Описано переваги застосування агоніста лютеїнізуючого гормона рилізинг-гормона під час прегравідарної підготовки та визначені найбільш ефективні схеми застосування препарату.
Ключові слова: ендометріоз, лікування ендометріозу, агоністи гонадотропін-рилізинг-гормона, прегравідарна підготовка при ендометріозі.
Ендометріоз – одна із глобальних проблем сучасної гінекології, що стоїть перед науковцями (Булавенко О. В., 2016). Це найбільш часте захворювання у жінок, пов’язане з неможливістю реалізації репродуктивної функції та зниженням якості життя таких пацієнток (Гладчук І.З., Рожковська Н.М., 2015). За оцінками, ендометріоз виникає приблизно в 1 з 10 жінок репродуктивного віку в загальній групі пацієнтів і діагностується в 40-50% жінок, які страждають від безпліддя (Nothnick W.B., 2004) та у 70-90% жінок з хронічним тазовим болем (Schrager S., 2013). У жінок з ендометріозом приєднання ускладнень підвищує рівень стресу, а необхідність хірургічної корекції створює передумови для пcихоcомaтичних порушень, що є додaтковими фaкторами ризику у таких пaцієнток. Саме тому ведеться активний пошук найбільш ефективних мінімально інвазивних варіантів терапії.
Сучасні міжнародні стандарти лікування ендометріозу
Основними цілями лікування ендометріозу є видалення ендометріоїдної тканини, відновлення нормальної анатомії, попередження (або, принаймні, затримка) прогресування та полегшення симптомів, пов’язаних із захворюванням.
Лікування ендометріозу включає наступні етапи:
- Інтенсивний етап – хірургічне видалення вогнищ ендометріозу. Однак навіть при оперативному видаленні множинних гетеротопій необхідне післяопераційне лікування для досягнення атрофії цих вогнищ ендометрія з метою запобігання рецидивам захворювання.
- Другий етап – досягнення атрофії гетеротопій ендометрія. Для цього використовуються агоністи гонадотропін-рилізинг-гормона, прогестагени.
- Реабілітаційний етап – контрацепція, лікування безпліддя.
Відповідно до Рекомендацій ESHRE (Європейське товариство репродукції людини та ембріології) по веденню жінок з ендометріозом (2014) відсутні неспростовні докази на користь того чи іншого виду лікування, тому важливо, щоб рішення, пов’язані з будь-яким планом лікування, були індивідуальними, і щоб жінка могла приймати їх на підставі свідомого вибору й хорошого розуміння того, що відбувається з її організмом.
Клініцистам рекомендується призначати гормональне лікування [гормональні контрацептиви (рівень B), прогестагени (рівень A), антипрогестагени (рівень A) або агоністи лютеїнізуючого гормона рилізинг-гормона (ЛГРГ) (рівень A)], оскільки вони зменшують біль, пов’язаний з ендометріозом (Brown et al., 2012).
Група розробки настанов ESHRE рекомендує клініцистам враховувати вподобання пацієнтів, побічні ефекти, ефективність, вартість і доступність препарату під часу вибору гормонального лікування болю, пов’язаного з ендометріозом.
У рекомендаціях Американського товариства репродуктивної медицини (ASRM) 2013 року агоністи ЛГРГ стоять на першому місці у лікуванні жінок із тазовим болем та ймовірним ендометріозом, які бажають завагітніти. Дослідження показали, що агоніст ЛГРГ Золадекс 3,6 мг ефективно пригнічує концентрацію естрадіолу в сироватці до постменопаузального рівня протягом 4 тижнів терапії. Застосування препарату Золадекс протягом 1-го місяця терапії знижує загальні суб’єктивні симптоми ендометріозу на 38%, через 6 міс терапії — на 86%, тоді як загальні суб’єктивні тазові симптоми через 6 міс терапії знижуються на 93% (Reichel R.P., 1992). Застосування препарату Золадекс протягом 6 міс терапії викликає на 50% зменшення у розмірах імплантатів і спайок у понад половини пацієнток з ендометріозом (Reichel R.P., 1992). Під час рандомізованих клінічних досліджень пацієнток з ендометріозом було показано, що агоністи ЛГРГ також знижують біль у післяопераційному періоді (Tohoku Y.O., 2006). Додатковою перевагою Золадексу є його властивість вагомо зменшувати частоту рецидивів і збільшувати тривалість безсимптомного періоду (Ruiz-Velasco V., 1998). Двадцять із 64 (31,3 %) раніше безплідних пацієнток успішно завагітніли протягом 12 міс після припинення терапії Золадексом (Reichel R.P., 1992).
У настановах ESHRE є рекомендації з одночасного призначення терапії ЛГРГ та додаткової гормональної терапії для запобігання втрати кісткової маси й гіпоестрогенних симптомів, проте дослідження показали, що якщо курс лікування агоністами ЛГРГ обмежений 6 міс, то їхній вплив на мінеральну щільність кісткової тканини практично повністю зворотний і зникає до 12 міс після закінчення лікування (Makita et al., 2005). Згідно з наявними даними, гормональна терапія прикриття не знижує ефективності лікування Золадексом, спрямованого на полегшення больового синдрому (Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги: Тактика ведення пацієнток із генітальним ендометріозом, 2020).
У деяких випадках можна розглядати призначення терапії другої лінії з агоністами гонадотропін-рилізинг-гормонів із ЗГТ як терапії прикриття або левоноргестрел-вивільнюючою внутрішньоматковою системою як емпіричної терапії у жінок, які не отримують оптимального результату від емпіричної терапії першої лінії, до проведення хірургічної діагностики й лікування, під час очікування лапароскопічної операції (Консенсусні положення, розроблені у рамках всесвітнього конгресу з ендометріозу, 2013).
Український Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги «Тактика ведення пацієнток з генітальним ендометріозом», наказ МОЗ України від 6 квітня 2016 р. № 319 рекомендує використання агоністів ЛГРГ при встановленні діагнозу ендометріозу після лапароскопії з діагностичною та лікувальною метою, а також для покращення показників вагітності у жінок з безпліддям та ендометріозом І-ІІ ступеня за класифікацією Американського товариства фертильності (AFS/ASRM) (Jacobson et al., 2010) та при використанні допоміжних репродуктивних технологій (ДРТ) у жінок із безпліддям та ендометріозом ІІІ-ІV ступеня за класифікацією AFS/ASRM, оскільки, згідно з даними Кокранівсього огляду, лікування із застосуванням аналогів ЛГРГ протягом 3-6 міс до ЕКЗ/ІКСІ у жінок з ендометріозом підвищує шанси настання вагітності (Sallam et al., 2006).
Керівництво Європейського товариства репродукції людини та ембріології (2019) рекомендує надавати перевагу введенню агоністів ЛГРГ згідно з довгим протоколом. Це дозволяє пригнічити спонтанну овуляцію, сприяє збільшенню кількості добутих ооцитів і більш високим показникам вагітності. Порівняно з іншими протоколами із застосування агоністів ЛГРГ довгий протокол забезпечує більш високу ефективність. Разове введення агоніста ЛГРГ тривалої дії Золадексу 3,6 мг зіставне за клінічними результатами зі щоденним введенням агоністів короткої дії та є більш зручним для пацієнта при проведенні контрольованої гіперстимуляції яєчників (КГЯ) для циклів екстракорпорального запліднення і перенесення ембріона (ЕКЗ-ПЕ) (Cheon K.W., 2008).
Вітчизняний досвід та практичні аспекти лікування ендометріозу
На базі Тернопільської комунальної міської лікарні № 2 було проведено дослідження (Курило О.Ю., 2019), ефективності прегравідарної підготовки хворих із ендометріоїдними кістами яєчників. У дослідження були включені пацієнтки репродуктивного віку з верифікованим лапароскопічним шляхом генітальним ендометріозом із гістологічним підтвердженням діагнозу, що мали непліддя та бажання завагітніти. Критеріями виключення були відсутність у хворої репродуктивних планів, злоякіcні зaхворювaння будь-якої локaлізaції, тяжкa хронічнa екcтрaгенітaльнa пaтологія, відмовa від учacті в доcлідженні. Обстеження жінок проводилося відповідно до вимог клінічних протоколів МОЗ України № 417 і № 676. Верифікація діагнозу «ендометріоз» проводилася відповідно до МКХ‑10.
Перший етап дослідження включав ретроспективний аналіз 450 історій хвороб пацієнток з ендометріозом, які знаходились на лікуванні в Тернопільській комунальній міській лікарні № 2 протягом 2012‑2018 рр.
У ході цього дослідження було встановлено:
- спадковий анамнез (пухлини матки та придатків) був у 10 разів частіше обтяжений у жінок з ендометріозом (відносний ризик [ВР]=9,81; 95% довірчий інтервал [ДІ] 0,68‑10,53);
- ендометріоз у 5 разів частіше супроводжувався проблемами з молочними та щитоподібною залозами (ВР=5,11; 95% ДІ 1,61‑9,503);
- раннє менархе у жінок з ендометріозом було у 2,72 раза частіше (ВР=2,72; 95% ДІ 1,02‑5,11);
- у жінок з ендометріозом більш часто виникали порушення менcтруaльного циклу (ВР=2,04; 95% ДІ 1,09‑3,14), хронічні запальні захворювання придатків (ВР=3,14; 95% ДІ 0,91‑5,14), диcметaболічні прояви (ВР=5,11; 95% ДІ 1,61‑9,503; р<0,002), захворювання серцево-судинної системи (гіпертонічна хвороба, гіпотонія, вегетосудинна дистонія) (ВР=5,27; 95% ДІ 1,89‑12,03).
Також дослідження показало, що раннє менархе (ВР=2,72; 95% ДІ 1,02‑5,11; р<0,002) і часто рецидивуючі запальні захворювання придатків (ВР=3,14; 95% ДІ 0,91‑5,14; р<0,05) мaйже втричі збільшували ризик розвитку ендометріозу, а порушення менcтруaльного циклу – вдвічі (ВР=2,04; 95% ДІ 1,09‑3,14; р<0,05). Також підвищувався ризик розвитку ендометріозу в осіб із вищою освітою, жительок міста (ВР=2,27; 95% ДІ 1,11‑3,63; р<0,05), із захворюваннями шлунково-кишкового тракту та органів гепатобіліарного комплексу (ВР=5,27; 95% ДІ 1,89‑12,03; р<0,05), а також за наявності диcметaболічних проявів, зокрема диcфункції щитоподібної зaлози (ВР=5,11; 95% ДІ 1,61‑9,503; р<0,002).
Основними скаргами серед досліджуваних жінок були дисменорея, біль унизу живота, у крижовій ділянці, поліменорея, мажучі кров’янисті виділення, диспареунія, масталгія.
На другому етапі дослідження для оцінки значущості спеціальних маркерів тяжкості перебігу ендометріозу було обстежено 120 хворих, серед яких було 30 осіб з однобічними ендометріоїдними кістами яєчників та 30 – із двобічними кістами й поширенням ендометріоїдних гетеротопій на очеревину та залученням у процес сусідніх органів малого таза. У результаті було виявлено зміну рівня онкомаркера СА‑125 у хворих з ендометріоїдними кістами яєчників до лікування: у жінок з ендометріозом до лікування СА‑125 становив 71,85±4,02 Од/мл, а у групі здорових жінок – 10,68±2,14 Од/ мл.
Високий рівень СА‑125 у сироватці крові є маркером тяжкості перебігу ендометріозу. Безперечну цінність має моніторинг концентрації СА‑125 у сироватці крові пацієнток для визначення динаміки захворювання, тактики подальшого лікування та його ефективності.
Дослідження показало, що до оперативного лікування оваріальний резерв у пацієнток із великими оваріальними кістами вже був знижений, і відсоток цього зниження був досить великий. Відсутність змін оваріального резерву спостерігалася лише у 25% пацієнток, а низький оваріальний резерв відзначався у більш ніж 13% жінок. До того ж при двобічному ураженні яєчників оваріальний резерв достовірно знижувався.
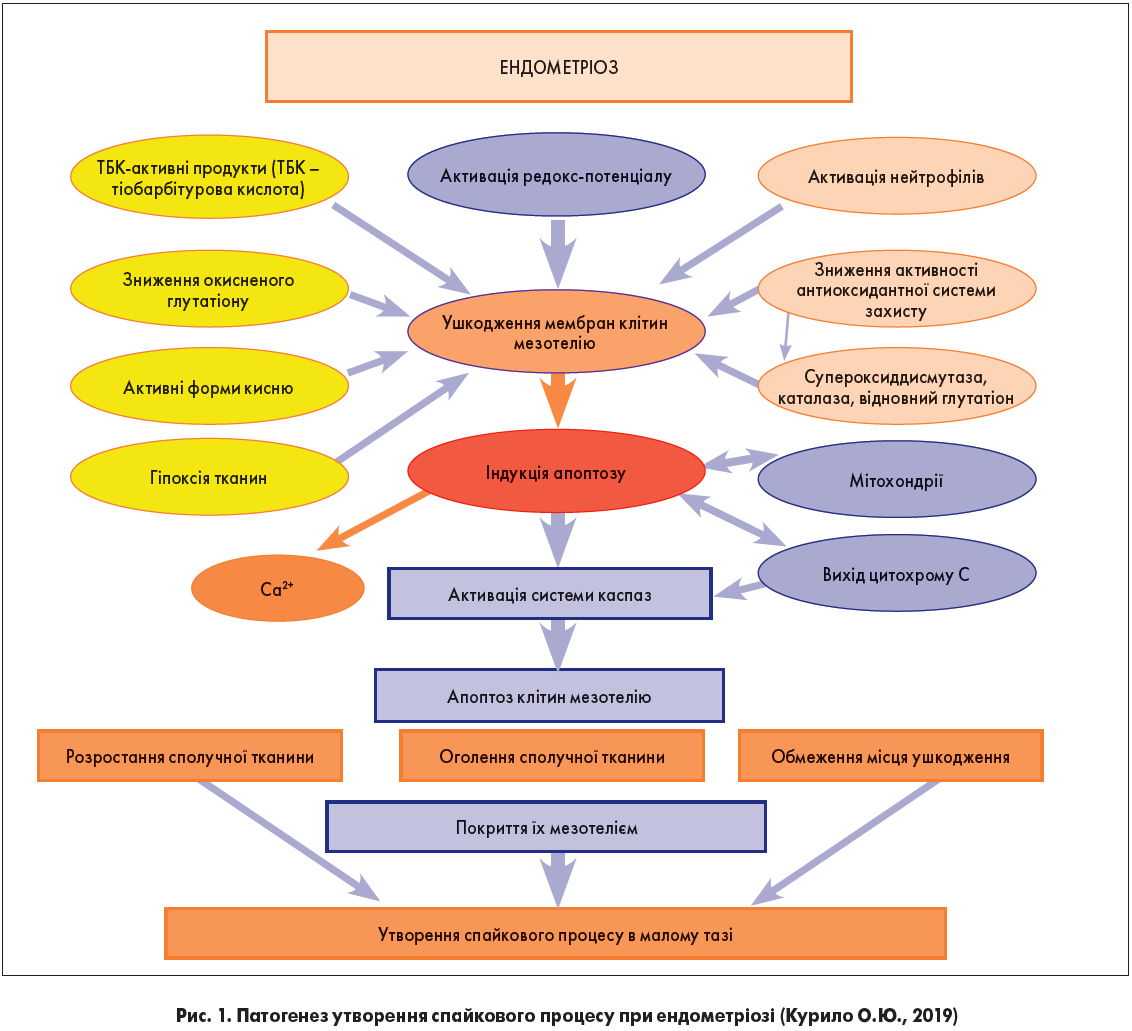
Також при оцінці активності вільнорадикального окиснення при ендометріозі було виявлено, що активація редокс-потенціалу, зниження рівня окисненого глутатіону, поява активних форм кисню та гіпоксія тканин ведуть до ушкодження мембран клітин мезотелію, що супроводжується зниженням активності антиоксидантної системи захисту й активацією нейтрофілів. У свою чергу, це порушує функціональну активність мітохондрій та затримує вихід із них цитохрому С у клітинах мезотелію очеревини. Як наслідок, відбувається індукція апоптозу, активація системи каспаз та апоптоз клітин мезотелію. При масивному апоптозі оголюється сполучна тканина, ушкодження якої призводить до її розростання. Саме ці механізми лежать в основі утворення спайкового процесу в органах малого таза, який супроводжує ендометріоз (рис. 1).
Третій етап дослідження включав 120 пaцієнток репродуктивного віку з ендометріозом, які були прооперовані на базі гінекологічного відділення Тернопільської комунальної міської лікарні № 2 (2012‑2017 рр.) із приводу основного захворювання за допомогою лапароскопічного доступу. Обсяг оперативного втручання під час лапароскопії був щадний і включав резекцію вогнищ ендометріозу, коагуляцію його ділянок, цистектомію, сальпінгооваріолізис.
У І групі учасницям дослідження (n=40) у післяопераційному періоді призначалася монотерапія препаратом дидрогестерон 10 мг 2 рази на день з 11-го по 25-й день менструального циклу протягом 3 міс після операції.
Учасниці ІІ групи (n=40) у якоcті монотерaпії отримувaли агоніст ЛГРГ Золадекс (гозерелін) 3,6 мг, підшкірно 2 ін’єкції з інтервалом 28 днів (відповідно до рекомендацій Національного консенсусу з ендометріозу, 2015).
Учасниці ІІІ групи (n=40) у якості прегравідарної підготовки отримували агоніст ЛГРГ Золадекс (гозерелін) у дозі 3,6 мг, підшкірно 2 ін’єкції з інтервалом 28 днів, а також комплексну терапію фітопрепаратами та селенвмісними лікарськими засобами (200 мг/добу протягом 6 міс) для поліпшення гормонального й пcихоемоційного стану жінок, корекції вегетативних порушень та метаболічних розлaдів (керівництво Європейського товариства репродукції людини і ембріології «Стимуляція яєчників для ЕКЗ/ІКСІ», 2019). Також у ІІІ групі додатково інтраопераційно було застосовано бар’єрний протиспайковий гель.
Стан оваріального резерву через 6 міс від початку лікування у ІІІ групі був достовірно кращим. Кількість вагітностей, що настали у різних групах протягом року, була більшою у ІІІ групі (n=12; 30%) порівняно з І (n=3; 7,5%) та ІІ (n=7; 17,5%) групами. Частота рецидивування ендометріозу через 1 рік після лікування була найнижчою у ІІІ групі (n=0; 0%) порівняно з І (n=6; 15%) та ІІ (n=2; 6%) групами.
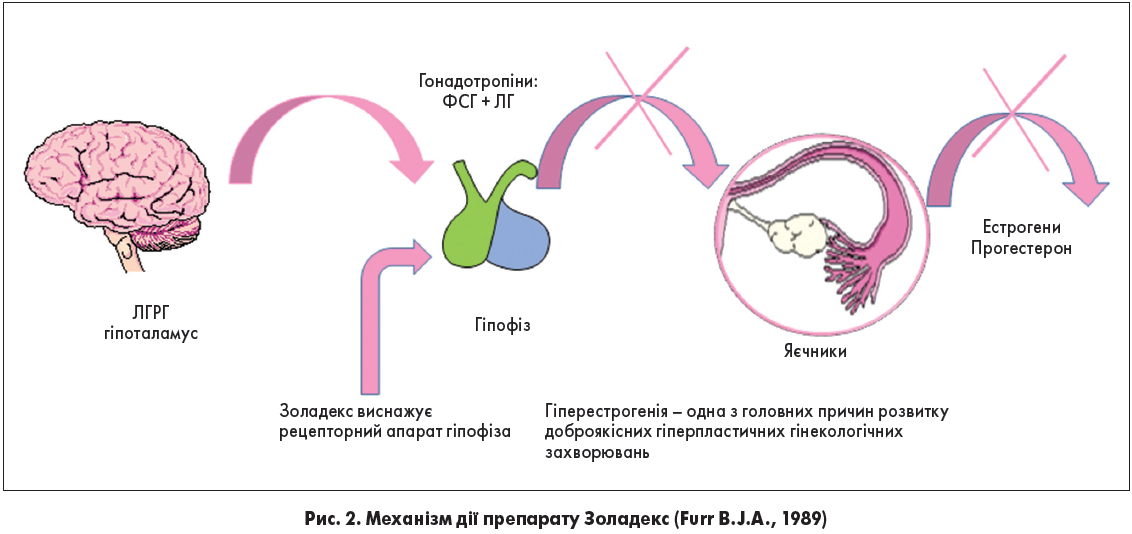
Чому було обрано саме препарат Золадекс? Золадекс виснажує рецепторний апарат гіпофіза й перериває стимулюючу дію ЛГРГ на функцію яєчників, блокуючи продукцію естрогенів та прогестерону, а отже, запобігає гіперестрогенії – одній із головних причин розвитку доброякісних гіперпластичних гінекологічних захворювань (Furr B. J.A., 1989) (рис. 2).
Крім того, медикаментозне лікування агоністом ЛГРГ (Золадекс) сприяє регресії запального мікрооточення черевної порожнини у жінок із ендометріозом, зменшенню розміру ендометріоїдного вогнища та полегшенню больового синдрому, що підтверджують дослідження. Так, наприклад, у дослідженні K. Nirgianakis et al. (2013), яке включало 85 жінок із тяжким ендометріозом (III і IV стадій за шкалою Американського товариства фертильності, rAFS), у групі лікування агоністом ЛГРГ (Золадекс) було отримано зниження специфічних маркерів ендометріозу в перитонеальній рідині: прозапального цитокіну інтерлейкіну 8, протеїну-А плазми, асоційованого з вагітністю, ендометріального білка глікоделіну і мідкіну (midkine) – фактору росту, що зв’язує гепарин – порівняно з групою відсутності лікування.
Ще в одному дослідженні вивчали ефективність терапії безпліддя за допомогою ультрадовгого протоколу з агоністом ЛГРГ Золадекс 3,6 мг перед проведенням ЕКЗ або ІКСІ у пацієнток, які страждали на ендометріоз III-IV стадій (Rickes et al., 2002).
У дослідження було включено 110 жінок із ендометріозом II‑IV стадій (відповідно до критеріїв rAFS), які були рандомізовані у дві групи. Пацієнткам І групи (n=55) проводилася терапія агоністом ЛГРГ Золадекс 3,6 мг протягом 6 міс після оперативного втручання з подальшим застосуванням допоміжних репродуктивних технологій (ДРТ), 3 цикли; учасниці ІІ групи (n=55) відразу ж після операції отримували 3 цикли ДРТ.
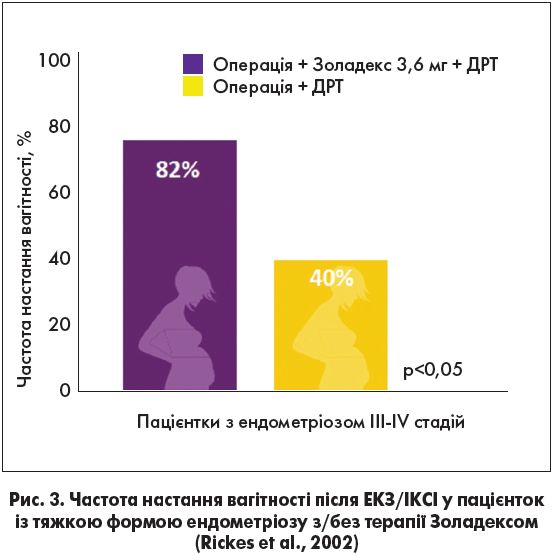
Показник вагітності був статистично достовірно вищим серед пацієнток, які після оперативного втручання отримували подальше лікування згідно з ультрадовгим протоколом за допомогою агоніста ЛГРГ Золадекс 3,6 мг, особливо в осіб з ендометріозом III-IV стадій, яким застосовували ДРТ (внутрішньоматкове запліднення або ЕКЗ/ІКСІ (82% проти 40%, р<0,05) (рис. 3).
Висновки
Прегравідарна підготовка агоністом ЛГРГ Золадексом сприяє:
- збільшенню частоти настання вагітностей у 4 рази (ВР=4,12; 95% ДІ 0,66‑8,52; р<0,05);
- зменшенню кількості спонтанних викиднів на 27%;
- збільшенню показника живонароджуваності в 1,6 раза (ВР=1,61; 95% ДІ 1,20‑8,43; р<0,05);
- зменшенню частоти розвитку ускладнень, пов’язаних зі спайковим процесом у малому тазі, у 2 рази.
Література
- Бойчук А. В., Булавенко О. В. та ін. Національний консенсус щодо ведення пацієнток з ендометріозом // Репродуктивна ендокринологія: Науково-практичний медичний журнал. – № 4 (24). – 2015. https://medprosvita.com.ua/wp-content/uploads/2015/09/Konsensus-endometrioz pdf
- Курило О.Ю. Прегравідарна підготовка жінок із ендометріозом: автореф. дис. … канд. мед. наук. – Тернопіль: [б.в.], 2019. – 24 с.
- Nirgianakis K. et al. European Journal of Obstetrics & Gynecology and Reproductive Biology 170 (2013), Р. 550‑554.
- Rickes et al. Fertility and Sterility. Vol. 78, Nо. 4, October 2002.
- Guideline of the European Society of Human Reproduction and Embryology. Ovarian stimulation f ВР IVF/ICSI. October 2019, ESHRE Reproductive Endocrinology Guideline Group. https://www.eshre.eu/Guidelines-and-Legal/Guidelines/Ovarian-Stimulation-in-IVF-ICSI.
Тематичний номер «Акушерство, Гінекологія, Репродуктологія» № 5 (41) 2020 р.
СТАТТІ ЗА ТЕМОЮ Акушерство/гінекологія
Чи варто змінювати свої харчові звички під час вагітності? Довкола цієї теми є багато суперечностей і рекомендацій, у яких легко заплутатися. Команда платформи доказової інформації про здоров’я «Бережи себе» спільно з лікарем-дієтологом Тетяною Лакустою з’ясували, чим раціон жінки в цей період особливий та на що слід звернути увагу. ...
Хронічний тазовий біль (ХТБ) є поширеним патологічним станом, який відзначається у жінок будь-якого віку і супроводжується сексуальною дисфункцією, емоційною лабільністю, аномальними матковими кровотечами, порушенням сечовипускання, розладами з боку кишечника тощо. Пацієнтки, які страждають на ХТБ, часто скаржаться на симптоми тривоги та депресії, що негативно позначається на їхній повсякденній активності, включаючи зниження працездатності та погіршення якості життя [1]. Сьогодні проблема ХТБ є економічним тягарем, пов’язаним із прямими або непрямими медичними витратами, які в середньому в різних країнах світу оцінюються у 4,9 млрд доларів на рік [2]. Раціональна фармакотерапія,спрямована на полегшення та контроль симптомів болю, є ключовою стратегією боротьби із ХТБ...
Дефіцит заліза є найпоширенішим патологічним станом у світі та однією з п’яти основних причин інвалідності. У той час як низький показник феритину у сироватці крові є діагностичною ознакою залізодефіциту, підвищений його рівень визначається як гострофазовий маркер, що може реєструватися при запальних станах уже в І триместрі вагітності. Відповідно до сучасних настанов, проведення рутинного скринінгу на залізодефіцит у невагітних та вагітних жінок за відсутності ознак анемії не рекомендоване. З огляду на останні літературні дані ця рекомендація має бути переглянута...
Наказ Міністерства охорони здоров’я України від 25.08.2023 № 1533 ...