Індивідуальна дієтотерапія при метаболічному синдромі
23-24 березня відбувся ІІ Міжнародний конгрес «Від народження до зрілості: міждисциплінарний підхід у збереженні здоров’я людини». Питанню корекції маси тіла при метаболічному синдромі, особливостям патогенезу та можливостям ефективного впливу на різні ланки проблеми присвятив свою доповідь президент Асоціації дієтологів України, кандидат медичних наук Олег Віталійович Швець.
 Метаболічний синдром – це комбінація вісцерального ожиріння, підвищеного артеріального тиску (АТ), інсулінорезистентності, підвищення тригліцеридів і зниження ліпопротеїнів високої щільності (ЛПВЩ). Діагностичними критеріями метаболічного синдрому є вісцеральне ожиріння (окружність талії (ОТ) ≥94 см для чоловіків і ≥80 см для жінок), АТ ≥130/85 мм рт. ст. або антигіпертензивна терапія, гіперглікемія (рівень глюкози натще ≥5,6 ммоль/л або діагностований діабет), тригліцериди 1,7 ммоль/л або фармакотерапія, ЛПВЩ <1,0 ммоль/л для чоловіків і <1,3 ммоль/л для жінок. Дослідження STEPS «Поширеність факторів ризику неінфекційних захворювань», що проводилося у 2019 році в Україні, продемонструвало такі результати: середній індекс маси тіла (ІМТ) становив 26,8 кг/м²; надмірну масу тіла (ІМТ ≥25 кг/м²) було виявлено в 59,0% осіб (60,2% із них становили жінки, 58,0% – чоловіки), ожиріння (ІМТ ≥30 кг/м²) – у 24,8% досліджуваних (29,8% – жінки, 20,1% – чоловіки). Частка осіб із підвищеним рівнем загального холестерину (≥5,0 ммоль/л) або осіб, які приймають медикаменти від підвищеного холестерину крові, становила 40,7%, частка осіб із підвищеним рівнем глюкози – 15,9%, з яких 8,8% складали особи з порушеною глікемією (концентрація глюкози в крові ≥6,1 та 7 ммоль/л), а також 7,1% становили особи з підвищеною концентрацією глюкози ≥7 ммоль/л або особи, які вживають медикаменти від підвищеного рівня глюкози в крові. Середнє споживання солі на добу – 12,6 г, 86,9% осіб уживають >5 г солі на добу.
Метаболічний синдром – це комбінація вісцерального ожиріння, підвищеного артеріального тиску (АТ), інсулінорезистентності, підвищення тригліцеридів і зниження ліпопротеїнів високої щільності (ЛПВЩ). Діагностичними критеріями метаболічного синдрому є вісцеральне ожиріння (окружність талії (ОТ) ≥94 см для чоловіків і ≥80 см для жінок), АТ ≥130/85 мм рт. ст. або антигіпертензивна терапія, гіперглікемія (рівень глюкози натще ≥5,6 ммоль/л або діагностований діабет), тригліцериди 1,7 ммоль/л або фармакотерапія, ЛПВЩ <1,0 ммоль/л для чоловіків і <1,3 ммоль/л для жінок. Дослідження STEPS «Поширеність факторів ризику неінфекційних захворювань», що проводилося у 2019 році в Україні, продемонструвало такі результати: середній індекс маси тіла (ІМТ) становив 26,8 кг/м²; надмірну масу тіла (ІМТ ≥25 кг/м²) було виявлено в 59,0% осіб (60,2% із них становили жінки, 58,0% – чоловіки), ожиріння (ІМТ ≥30 кг/м²) – у 24,8% досліджуваних (29,8% – жінки, 20,1% – чоловіки). Частка осіб із підвищеним рівнем загального холестерину (≥5,0 ммоль/л) або осіб, які приймають медикаменти від підвищеного холестерину крові, становила 40,7%, частка осіб із підвищеним рівнем глюкози – 15,9%, з яких 8,8% складали особи з порушеною глікемією (концентрація глюкози в крові ≥6,1 та 7 ммоль/л), а також 7,1% становили особи з підвищеною концентрацією глюкози ≥7 ммоль/л або особи, які вживають медикаменти від підвищеного рівня глюкози в крові. Середнє споживання солі на добу – 12,6 г, 86,9% осіб уживають >5 г солі на добу.
Ожиріння – захворювання, зумовлене порушенням регуляції енергетичного балансу, що спричиняє надмірне накопичення жиру (як джерела енергії). Особливостями харчування, котрі, ймовірно, асоційовані з підвищенням маси тіла, є надмірна калорійність, значне вживання цукру (>50 г/день), високий уміст жирів (а також споживання переважно насичених та омега‑6 жирних кислот) і вуглеводів, нездорова харчова поведінка (швидке вживання їжі, багато перекусів); при цьому зв’язок їжі й ожиріння не є безумовним. Їжа бере участь у маніфестації ожиріння, але не є наслідком порушення регуляції енергетичного балансу та безпосередньою причиною ожиріння. На енергетичний баланс впливають генетичні, психологічні фактори, недосипання, навколишнє середовище, відсутність фізичної активності, а також певний вплив чинять гормони (на апетит). У зв’язку з цим можливості вольового контролю енергетичного балансу мають серйозні обмеження, адже існує низка фізіологічних факторів, які діють на енергетичний баланс і спрямовані на забезпечення запасів енергії. Нетривалий контроль споживання й витрат енергії (крім центрів головного мозку) регулюється також за рахунок синтезу гормона греліну (регулює відчуття голоду), гормонів насичення ГПП‑1 (глюкагоноподібний пептид) і PYY (пептид тирозин-тирозин). Середньостроковий контроль реалізується завдяки продукції лептину в жировій тканині (з відповідними сигналами центральної нервової системи); композиція кишечного мікробіому динамічно впливає на отримання додаткової енергії з їжі. Тривалий контроль включає коричневу жирову тканину, яка може утилізувати чи накопичувати енергію; фермент ліпопротеїнліпазу, що регулює надходження тригліцеридів у жирову та м’язову тканину (в останньому випадку відбувається витрата енергії).
Одним із популярних оманливих уявлень є інтерпретація набирання зайвої маси тіла (як різниця між надходженням і витратою калорій); наприклад, для набирання 1 кг потрібно спожити ≈8000 «зайвих кілокалорій». Однак випробування Bouchard, яке досліджувало набирання маси тіла в ідентичних близнюків, продемонструвало, що, незважаючи на аналогічний енергетичний дисбаланс, деякі суб’єкти демонстрували значну резистентність до накопичення енергії, тоді як інші були схильними до набирання маси тіла. Крім того, різниця в збільшенні маси тіла була помітнішою між парами близнюків, аніж усередині пар. Це дослідження підтверджує значення спадкової схильності в набиранні маси тіла. Останніми роками також виявлено можливий вплив мікробіому кишечнику та циркадних ритмів на механізм виникнення надмірної маси тіла.
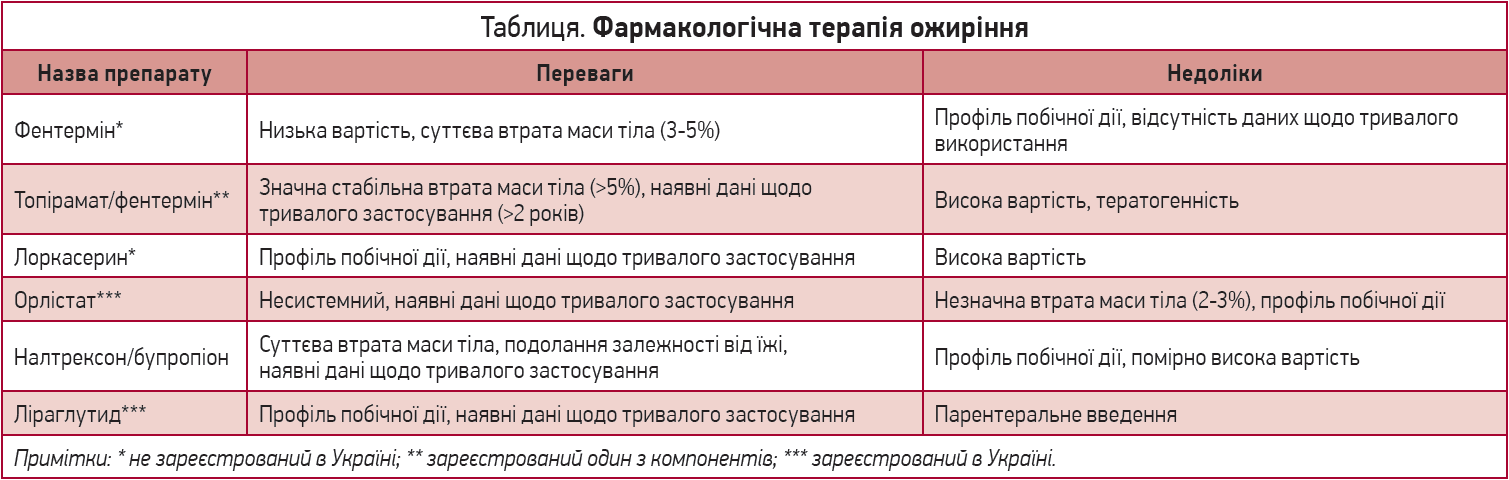
Ведення пацієнта з ожирінням включає індивідуальний підхід і вплив на різні ланки патогенезу. Принципи ведення такого пацієнта – антропометрична оцінка (ІМТ, ОТ), оцінка звичного харчування (відтворення дієти за попередні 24 год), метаболічні тести, оцінка кардіометаболічного ризику, нутритивний супровід (дієтотерапія) легкого, помірного, а також тяжкого ожиріння, фізична активність, поведінкова терапія, фармакотерапія (табл.), баріатрична хірургія (обов’язковою є оцінка кардіометаболічного ризику). Шкала SCORE дозволяє швидко та легко оцінити загальний ризик серцево-судинної смертності для кожної людини, спрогнозувати його динаміку на майбутнє та визначити конкретні шляхи його зниження (в цій шкалі враховано 5 факторів ризику – 2 з них не підлягають модифікації: вік (від 40 до 65 років) і стать; 3 фактори ризику належать до категорії тих, що модифікуються: систолічний АТ, статус куріння та рівень холестерину в крові, в т. ч. холестерин ЛПВЩ). Слід пам’ятати, що лише 3 категорії населення, котрі автоматично належать до групи високого ризику, не потребують оцінки ризику за шкалою SCORE: хворі з діагностованою ішемічною хворобою серця, цукровим діабетом, а також особи, які мають надзвичайно високі рівні індивідуальних факторів ризику. Решта пацієнтів підлягає оцінці ризику за шкалою SCORE.
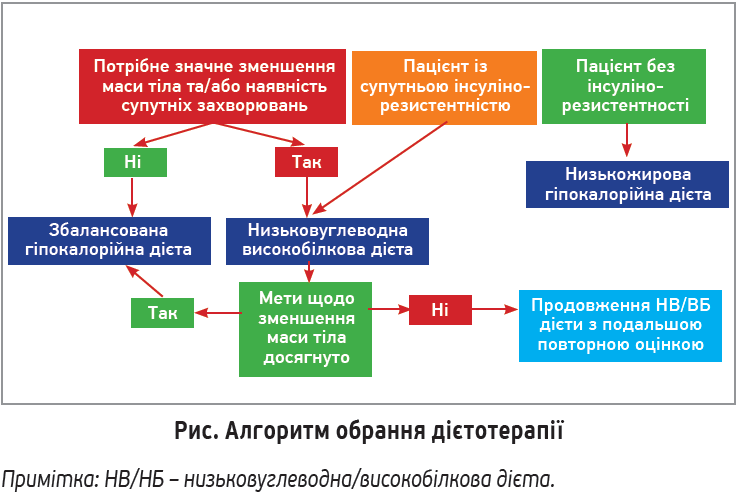
Обрання дієти (рис.) має ґрунтуватися на наявності переконливих доказів ефективності з огляду на досягнення стабільного зниження маси тіла, позитивного впливу на метаболічні показники, покращення якості життя. Не існує універсальної дієти, яка дозволила би досягти й утримувати бажану масу тіла. Рестриктивні дієти дають змогу зменшити масу тіла, але результат часто є нестабільним і супроводжується ризиком дефіциту нутрієнтів. Також проблемою в дотриманні дієтичного харчування є т. зв. тригери. Тригери, які спонукають до вживання їжі за відсутності голоду, – навколишнє середовище (запах і вигляд їжі), розумові (думки та згадки про їжу), емоційні (вживання їжі для комфорту чи як винагорода), соціальні (зустріч із друзями, свята із застіллям), звичні тригери (сталий час прийому їжі, режим харчування), фізіологічні порушення сну, гормональні розлади.
Нутритивний супровід легкого та помірного ожиріння включає дієтичну, а також метаболічну оцінку, гіпокалорійну дієту з дефіцитом 500-1000 ккал/добу, збалансовану індивідуальну дієту, питний режим, дієтичну саплементацію за калорійності <1200 ккал/добу.
Супровід тяжкого ожиріння – супергіпокалорійна дієта (<800 ккал/добу), супровід дієтолога, мультидисциплінарне ведення зі щотижневим оглядом, уживання сумішей із фіксованою калорійністю та/або білкових сумішей, дієтична саплементація (призначення вітамінів і мінералів). Базові зміни харчової поведінки мають включати неквапливе споживання їжі (20-30 хв на основний прийом), уживання їжі лише за обіднім столом, триразовий режим харчування (уникнення перекусів), скорочення проміжків між сніданком і вечерею.
Дослідження Hutchinson (2019) продемонструвало ефективність комбінування гіпокалорійної дієти з інтервальним голодуванням. У випробуванні, що включало жінок із надмірною масою тіла, котрі дотримувалися гіпокалорійної дієти та голодували 3 р/тиж, було доведено кращу динаміку зменшення маси тіла та нормалізації кардіометаболічних маркерів. У групах, де практикувалося інтервальне голодування, учасниці не вживали їжу з 08:00 до 08:00 наступного дня протягом 3 непослідовних днів тижня. Інтервальне голодування + обмеження калорійності їжі мали кращі результати в зниженні маси тіла, жирової маси, загального холестерину та ліпопротеїнів низької щільності порівняно з групами, де призначалося або лише обмеження калорій, або тільки інтервальне голодування (p≤0,05 для всіх).
Консервативне лікування ожиріння є низькоефективним у хворих з ІМТ >40 кг/м² або ІМТ >35 кг/м² і супутніми захворюваннями. Досвід застосування баріатричних операцій довів, що вони можуть суттєво коригувати порушення вуглеводного та ліпідного обміну в хворих з ожирінням і розглядатись як патогенетично обґрунтований метод лікування ожиріння. На сьогодні баріатричні операції можна розподілити на 3 групи: мальабсорбтивні втручання; операції, що зменшують об’єм шлунка (гастрорестриктивні), та комбіновані оперативні втручання (гібридні). Найпоширенішими є оперативні втручання, що включають рестриктивне оперативне втручання зі зменшенням обсягу шлунка, шунтувальні операції зі зменшенням всмоктування в тонкому кишечнику, комбіноване оперативне втручання з рестриктивним і шунтувальним компонентом. За даними Fisher і співавт. (2018), після виконання бандажування шлунка в 46,2% пацієнтів спостерігається втрата надмірної маси тіла, в 56,7% – зникнення цукрового діабету 2 типу, в 59% – ремісія гіперліпідемії, в 43% – зникнення артеріальної гіпертензії; після виконання шунтування шлунка відзначається втрата надмірної маси тіла – в 59,5%, зникнення цукрового діабету 2 типу – у 80,3%, ремісія гіперліпідемії – в 59%, зникнення артеріальної гіпертензії – в 68%; проведене біліопанкреатичне шунтування дозволяє втратити надмірну масу тіла в 63,3%, зумовлює зникнення цукрового діабету 2 типу – в 95,1%, ремісія гіперліпідемії з’являється в 99%, зникнення артеріальної гіпертензії – у 83% пацієнтів.
Підготувала Тетяна Ведмідь
Медична газета «Здоров’я України 21 сторіччя» № 9 (502), 2021 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Після десятиліть, а часом і запеклих суперечок про переваги та недоліки застосування глюкокортикоїдів (ГК) досягнута певна конвергенція. Сучасні рекомендації лікування таких захворювань, як ревматоїдний артрит (РА), ревматична поліміалгія (РПМ) та васкуліт великих судин відображають поточний стан консенсусу терапії ГК. Однак залишаються відкритими питання щодо можливості тривалого лікування дуже низькими дозами ГК у пацієнтів із РА, а також успішності пошуку інноваційних ГК (лігандів ГК-рецепторів) із покращеним співвідношенням користь/ризик....
Серед препаратів, які мають велику доказову базу щодо лікування пацієнтів із захворюваннями дихальних шляхів з алергічним компонентом, особливий інтерес становлять антагоністи лейкотрієнових рецепторів (АЛТР). Ці препарати мають хорошу переносимість у дорослих та дітей, а також, на відміну від інгаляційних кортикостероїдів (ІКС), характеризуються високим комплаєнсом, тому посідають чільне місце в лікуванні пацієнтів із респіраторною патологією. У лютому відбувся міждисциплінарний конгрес із міжнародною участю «Життя без алергії International» за участю провідних вітчизняних міжнародних експертів. Слово мав президент Асоціації алергологів України, професор кафедри фтизіатрії та пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук Сергій Вікторович Зайков із доповіддю «Місце АЛТР у лікуванні пацієнтів із респіраторною патологією». ...
Розбір клінічного випадку...