Потенціал бактерій роду Bacillus як пробіотиків
Бактерії роду Bacillus завдяки здатності утворювати спори широко розповсюджені в природі й трапляються повсюдно – в ґрунті, воді, повітрі, харчових продуктах, а також в організмі людини та тварин [1, 2]. Характерною особливістю бацил є також їхня висока й різнобічна біологічна активність. Вони характеризуються вираженим антагонізмом до широкого спектра збудників захворювань людини та тварин, синтезують різні за своєю природою й механізмом дії сполуки з протимікробною активністю, а також ферменти, амінокислоти, полісахариди, вітаміни.
Рід Bacillus налічує близько 217 видів і об’єднує численну групу аеробних або факультативно анаеробних грампозитивних мікроорганізмів паличкоподібної форми. Типовий вид – B. subtilis (Ehremberg) Cohn 1872, 174.
Бактерії роду Bacillus характеризуються стійкістю до несприятливих умов зовнішнього середовища, в тому числі й у шлунково-кишковому тракті, тому мають перевагу перед мікроорганізмами інших таксономічних груп при використанні їх у біотехнології та медицині [3]. Вони є одними з домінувальних видів мікроорганізмів на Землі. У процесі еволюційного розвитку людства бацили вступали в симбіотичні відносини з організмом людини й інших ссавців і є важливими компонентами їхньої екзогенної мікрофлори, а також виконують комплекс корисних для макроорганізму функцій, найважливішою з яких є здатність запобігати колонізації кишечнику патогенами.
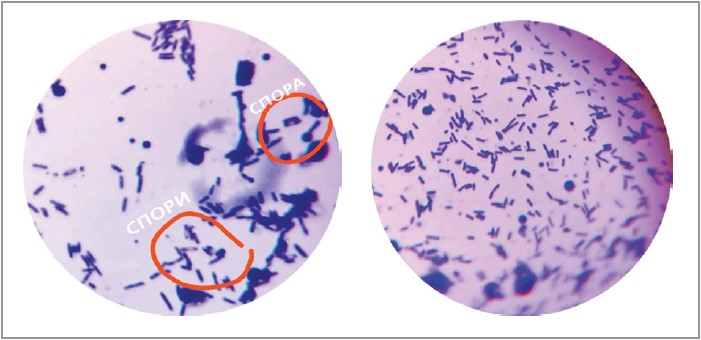
Аеробні бацили постійно потрапляють у шлунково-кишковий тракт здорових людей або з навколишнього середовища, або в результаті споживання ферментованих продуктів харчування. На слизових оболонках ротової порожнини, глотки, а потім і шлунка спори бактерій активізуються й переходять до вегетативного росту (рис. 1). Встановлена здатність цих мікроорганізмів розвиватися й залишатися в організмі господаря протягом деякого часу [4, 5]. Тривалість їх перебування в шлунково-кишковому тракті здебільшого визначається, з одного боку, генетичними особливостями штамів бацил, з іншого – патологічними процесами в організмі господаря.
Рис. 1. Процес переходу штамів Bacillus subtilis (Ремедіум, Sirion) зі спорової у вегетативну форму
Спороутворювальні бацили досліджуються також із метою застосування у виробництві та зберігання їстівної продукції впродовж тривалого часу. Наприклад, широко відомий штам B. subtilis (natto) використовується в Японії для ферментації бобів [6]. Додавання B. subtilis natto до культурального середовища з лактобацилами сприяє збільшенню кількості життєздатних клітин молочнокислих бактерій [7]. Припускають, що такий позитивний вплив бацил зумовлений продукуванням ними каталази й субтилізину. Продукт natto та його основний компонент B. subtilis схвалено Міністерством охорони здоров’я, праці та добробуту Японії як ефективний засіб для збереження здоров’я (Foods for Specified Health Use).
Актуальним науковим напрямом сучасних досліджень бактерій роду Bacillus є розроблення на їхній основі пробіотичних продуктів для ветеринарії та медицини, що мають високу профілактичну й терапевтичну ефективність.
Пробіотики – це живі мікроорганізми, які приносять користь організму господаря при введенні в адекватних кількостях [8]. Пробіотичні мікроорганізми можуть бути включені до складу різноманітної продукції, зокрема продуктів харчування, лікарських препаратів і харчових добавок.
Хоча більшість із відомих пробіотиків створено на основі бактерій родів Lactobacillus і Bifidobacterium, спороутворювальні бацили як пробіотики мають низку істотних переваг порівняно з іншими представниками мікробіоти кишечнику. Експериментально доведена їхня нешкідливість, а також вища протимікробна та ферментативна активність. Вони позитивно впливають на імунний статус організму господаря та зниження рівня холестерину в крові, проявляють антиоксидантні властивості, стійкі до кислоти та жовчі, технологічні у виробництві, стабільні при зберіганні [9, 10].
Зацікавленість до бацил як до пробіотиків істотно зросла за останні 15 років. Це пов’язано з накопиченням наукових даних, які демонструють їхню профілактичну й терапевтичну ефективність при захворюваннях шлунково-кишкового тракту, порушеннях імунного статусу й обміну речовин [3, 4, 8, 9]. Багато питань, які стосуються їхнього багатофакторного механізму дії та впливу на організм, продовжують ретельно досліджуватися.
Лікувальний ефект пробіотиків на основі бактерій роду Bacillus визначається сумою специфічних активностей, які мають ці мікроорганізми та продукти їхнього метаболізму. Механізм дії препаратів із живих мікробних культур здебільшого зумовлений наявністю в пробіотичних штамів цілої низки корисних для макроорганізму властивостей, зокрема здатності до продукування різноманітних біологічно активних сполук [4, 5]. Пробіотична активність є суто штамовою ознакою. Різні штами, в тому числі одного виду, здійснюють на організм тільки притаманний їм пробіотичний ефект.
Міжнародні організації (FAO/WHO) висувають чіткі вимоги до оцінки пробіотичних штамів і препаратів на їхній основі. Зокрема, вимагаються точна ідентифікація мікроорганізмів, комплексна характеристика біологічної активності та безпеки препарату, отримання доказової бази клінічної ефективності пробіотиків [8, 11].
Механізми, за допомогою яких спороутворювальні пробіотики можуть поліпшувати здоров’я господаря, включають стимуляцію імунної системи, синтез різних протимікробних сполук і модуляцію складу мікробіоти кишечнику.
Однією з основних біологічних властивостей бактерій роду Bacillus, які визначають їхній пробіотичний ефект, є антагоністична активність щодо широкого спектра патогенних та умовно-патогенних мікроорганізмів. Антагонізм бацил безпосередньо пов’язаний зі здатністю представників різних видів синтезувати антибіотичні речовини. На сьогодні відомо близько 800 антибактеріальних сполук, синтезованих бактеріями роду Bacillus. Антибіотики відрізняються за своєю структурою та за спектром мікроорганізмів, на які вони діють. Відомо, що більшість ідентифікованих антибіотиків, утворених бактеріями роду Bacillus, є поліпептидами [12-14]. Представники виду B. subtilis є найпродуктивнішими й утворюють близько 70 різних антибіотиків.
Штами B. subtilis і B. licheniformis мають здатність синтезувати циклічні ліпопептидні антибіотики [15, 16]. Основні компоненти цих антибіотиків – сурфактин і фенгіцин – характеризуються множинною біологічною активністю, низькою токсичністю та мають потенціал для застосування в медицині як противірусні, антибактеріальні, протипухлинні й гіпохолестеринемічні засоби [17].
Бактерії роду Bacillus синтезують не лише різноманітні протимікробні субстанції, вони також є продуцентами ферментів, полісахаридів, амінокислот і вітамінів. Нині ці бактерії посідають провідні позиції у світі як об’єкти мікробної біотехнології для отримання ферментів – протеаз, амілаз, ксиланаз, целюлаз і пектиназ [18]. Завдяки синтезу ферментів різних класів аеробні бацили можуть існувати на різних субстратах, а також брати участь у регулюванні та стимуляції травлення, чинити протиалергенну й антитоксичну дії. Серед гідролітичних ферментів особливо варто відзначити протеази, які займають ключову позицію завдяки їх важливій фізіологічній ролі в організмі [19].
Протимікробна активність бацил може бути зумовлена синтезом не лише антибіотиків, а й літичних ферментів (лізин), які викликають лізис клітин грампозитивних і грамнегативних бактерій, а також дріжджоподібних грибів. Літичні ферменти – це складний комплекс ферментів із різною субстратною специфічністю, які спільно або окремо здатні здійснювати деградацію клітинної стінки мікроорганізмів. Представники роду Bacillus продукують літичні ферменти на кшталт лізоциму, а також комплекс ферментів, зокрема глюканазу, мананазу, протеазу, ацетилгексозамінідазу, амідазу й інші ферменти, здатні руйнувати клітинні стінки грамнегативних мікроорганізмів [20].
Ще однією важливою для здоров’я організму групою біологічно активних речовин, синтезованих бацилами, є екзополісахариди. Відомо, що позаклітинні полісахариди здатні підвищувати захисний потенціал організму до бактеріальних і вірусних інфекцій, активізувати фагоцитоз, продукцію лізоциму, чинити протипухлинну, протизапальну, ранозагоювальну дії, що свідчить про широкі можливості їх застосування в медицині [21].
Аеробні спороутворювальні бактерії роду Bacillus мають здатність до синтезу вільних амінокислот, зокрема незамінних [22]. Амінокислоти виконують низку найважливіших функцій в організмі: беруть участь у білковому та вуглеводному обмінах, формують протиінфекційний захист, забезпечують киснем процес утворення нових клітин, є будівельним матеріалом для ферментів, антитіл і деяких гормонів, слугують джерелом енергії на клітинному рівні.
Крім того, бацили є продуцентами вітамінів – рибофлавіну (вітамін В2), кобаламіну (В12) та біотину (В7) [18].
Нині у світі для застосування в медицині як пробіотиків найдослідженішими є штами бацил кількох видів – B. subtilis, B. cereus, B. licheniformis, B. megaterium, B. pumilus, B. clausii, B. coagulans, B. amyloliquefaciens. На їхній основі створені препарати для профілактики та лікування порушень мікрофлори кишечнику, кишкових інфекцій, антибіотикоасоційованої діареї, синдрому подразненого кишечнику, корекції імунного статусу.
Одним із нових протимікробних продуктів є пробіотик Ремедіум (Sirion), який містить 5 видів полірезистентних до антибіотиків штамів Bacillus (B. subtilis, B. licheniformis, B. amyloliquefaciens, B. megaterium, B. pumilus), безпечність яких підтверджена висновками Управління з контролю якості продуктів харчування та лікарських засобів США (FDA). Одна доза препарату містить 1,7×109 КУО/флакон живих мікробних клітин.
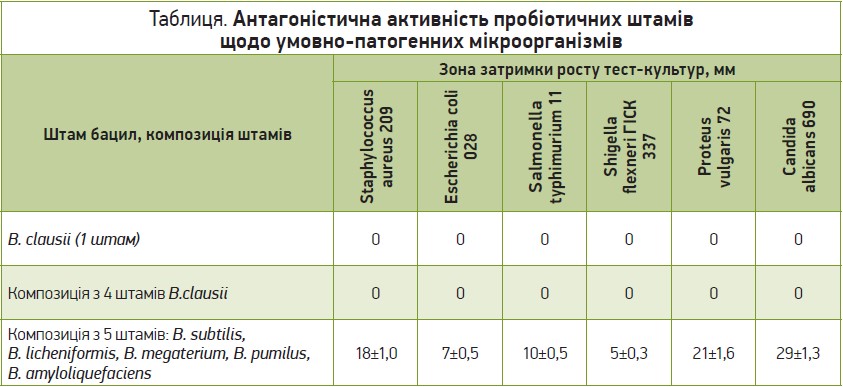
На базі Інституту мікробіології і вірусології ім. Д. К. Заболотного НАН України проведено дослідження антагоністичної активності деяких пробіотичних штамів бацил та їхніх композицій щодо представників різних родів умовно-патогенних мікроорганізмів (метод відтермінованого антагонізму) (табл.).
В умовах даного досліду лише композиція, яка включала 5 різних штамів бацил, виявила інгібувальний ефект стосовно досліджених тест-культур. Попередніми дослідженнями встановлено наявність антагоністичної активності композиції з 5 пробіотичних штамів до широкого спектра умовно-патогенних культур різних видів бактерій і дріжджоподібних грибів роду Candida (рис. 2). Найвища протимікробна активність дослідженої композиції виявлена до бактерій роду Staphylococcus, Proteus і грибів роду Candida.
Рис. 2. Пригнічення росту умовно‑патогенних мікроорганізмів під впливом пробіотичної композиції з 5 штамів (у середині чашки Петрі – бацили, цифрами позначені тест-культури:
1 – S. aureus 209,
2 – S. aureus УКМ B‑918,
3 – E. coli УКМ B‑906,
4 – E. coli 028,
5 – C. albicans УКМ У‑2681,
6 – C. albicans 690,
7 – S. flexneri ГІСК 337,
8 – S. sonnei 233169,
9 – S. typhimurium 11,
10 – S. derby 1519,
11– P. vulgaris U‑8,
12 – P. vulgaris 72)
Виражені протимікробні властивості пробіотичних штамів бактерій дають змогу розглядати можливість застосування препаратів на їхній основі як альтернативу антибіотикам, що особливо важливо в епоху стрімкого розповсюдження резистентних форм патогенних мікроорганізмів і зниження ефективності низки протимікробних засобів [23, 24].
Відомо, що при переході спорової форми пробіотиків із бацил до вегетативних клітин штами бактерій виділяють біологічно активні речовини, зокрема антибіотичні сполуки, які зумовлюють лікувально-профілактичний ефект препарату.
Отже, спороутворювальні бактерії роду Bacillus безпечні для макроорганізму (за винятком B. anthracis і B. cereus), є продуцентами комплексу біологічно активних речовин, корисних для макроорганізму, мають імуномодулювальні властивості, стійкі до низьких температур і pH, позитивно впливають на організм господаря. Це одна з найперспективніших груп мікроорганізмів для створення нових лікувально-профілактичних препаратів для людини та тварин. Отримані за останнє десятиліття результати численних клінічних досліджень щодо ефективності пробіотиків із бацил відкривають нові можливості та напрями їх використання в комплексному лікуванні різних захворювань і корекції імунітету.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 13-14 (506-507), 2021 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
Відтворення майбутнього здорової нації – один з найважливіших сенсів існування теперішнього покоління. День боротьби з ожирінням нагадує нам про поширеність цього проблемного явища і важливість попередження його наслідків. Ожиріння може мати вплив на різні аспекти здоров'я, включаючи репродуктивне....
Вивчення клініко-патогенетичних особливостей поєднаного перебігу остеоартрозу (ОА) у хворих із метаболічними розладами, які характеризують перебіг метаболічного синдрому (МС), зокрема цукровим діабетом (ЦД) 2 типу, ожирінням (ОЖ), артеріальною гіпертензією (АГ), є актуальним, оскільки це пов’язано з неухильним збільшенням розповсюдженості цього захворювання, недостатньою ефективністю лікування, особливо за коморбідності з іншими захворюваннями, які патогенетично пов’язані з порушеннями метаболічних процесів. ...
Синдром подразненого кишечнику (СПК) є одним з найпоширеніших захворювань органів травлення (до 20% серед дорослого населення). Характерними ознаками СПК є хронічний абдомінальний біль, порушення дефекації, метеоризм. Дотепер остаточно не з’ясована етіологія цього стану, проте доведено роль низки різнопланових, взаємопов’язаних між собою факторів у його розвитку. До них відносять: дисфункцію осі «мозок – кишечник», вісцеральну гіперчутливість, моторні порушення, підвищену проникність кишечнику, запалення низького ступеня, дисбіоз....
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....