Обрані питання в ендокринології: сучасний стан проблеми
«Школа ендокринолога» – один з найкращих потужних освітніх проєктів ендокринологічної галузі. Без перебільшення кожний захід – це подія. Подія за масштабом наукової програми, яка не лише охоплює топові теми, але й завжди ґрунтовно презентує проблеми рідкісних, тяжких, складних захворювань; подія за кількістю спікерів – провідних лідерів думок галузі, які діляться власним унікальним досвідом. Пандемія, звичайно, внесла свої корективи в життя медичної спільноти, але завдяки онлайн-формату «Школи ендокринолога» лікарі не втратили можливості брати участь у дискусіях, отримувати нову інформацію, ставити питання дискутувати і, головне, – мати можливість безперервного навчання. Отже, представляємо увазі читачів обрані доповіді спікерів чергового засідання «Школи ендокринолога», яке відбулося на початку цього року і на якому були висвітлені теми латентного аутоімунного діабету в дорослих, стероїд-індукованої гіперглікемії, когнітивних розладів у хворих на цукровий діабет (ЦД) і диференціальної діагностики гіперандрогеній.
Ключові слова: латентний аутоімунний діабет, LADA, стероїд-індукована гіперглікемія, стероїд-індукований цукровий діабет, деменція, діабет-асоційована деменція, гіперандрогенія, гірсутизм, СПКЯ, ДГЕА-С, 17-ОНР, вроджена дисфункція кори наднирників
 За доброю традицією з вступною промовою до учасників конференції завжди звертається науковий керівник науково-освітнього проєкту «Школа ендокринолога» – президент Української асоціації клінічних ендокринологів, директор ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), академік НАМН України, член-кореспондент НАН України, завідувач кафедри ендокринології Національного університету охорони здоров’я (НУОЗ) України ім. П.Л. Шупика МОЗ України (м. Київ), доктор медичних наук, професор Микола Дмитрович Тронько. А незмінним блискучим модератором і одним із головних організаторів заходу є керівник відділу клінічної діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук Любов Костянтинівна Соколова.
За доброю традицією з вступною промовою до учасників конференції завжди звертається науковий керівник науково-освітнього проєкту «Школа ендокринолога» – президент Української асоціації клінічних ендокринологів, директор ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» (м. Київ), академік НАМН України, член-кореспондент НАН України, завідувач кафедри ендокринології Національного університету охорони здоров’я (НУОЗ) України ім. П.Л. Шупика МОЗ України (м. Київ), доктор медичних наук, професор Микола Дмитрович Тронько. А незмінним блискучим модератором і одним із головних організаторів заходу є керівник відділу клінічної діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук Любов Костянтинівна Соколова.
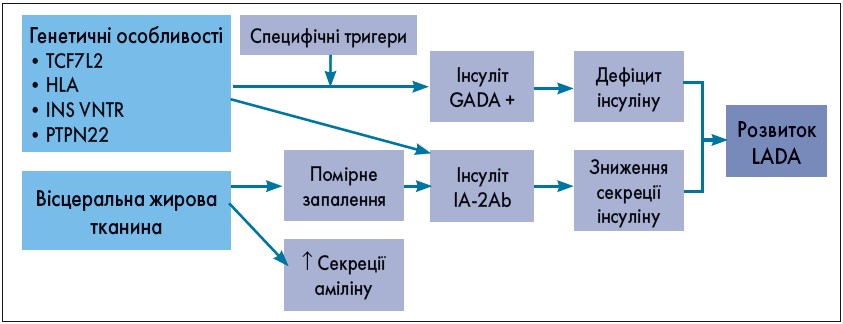
Темою виступу завідувача кафедри клінічної імунології, алергології та ендокринології Буковинського державного медичного університету (м. Чернівці), доктора медичних наук, професора Наталії Вікторівни Пашковської став латентний аутоімунний діабет у дорослих (LADA), зокрема механізм розвитку цього захворювання (рис. 1), діагностичні критерії, клінічні особливості перебігу, перспективи лікування.
Рис. 1. Потенційні патогенетичні механізми розвитку LADA
 35 років тому був відкритий незвичайний тип діабету, який не вписувався в картину ЦД ані 1, ані 2 типу. Так, L.C. Groop та співавт. в 1986 р. повідомили про групу хворих на ЦД 2 типу, в яких, незважаючи на наявність підвищення антитіл до антигенів острівцевого апарату підшлункової залози, зберігалася функція β-клітин. Автори назвали захворювання латентним діабетом 1 типу.
35 років тому був відкритий незвичайний тип діабету, який не вписувався в картину ЦД ані 1, ані 2 типу. Так, L.C. Groop та співавт. в 1986 р. повідомили про групу хворих на ЦД 2 типу, в яких, незважаючи на наявність підвищення антитіл до антигенів острівцевого апарату підшлункової залози, зберігалася функція β-клітин. Автори назвали захворювання латентним діабетом 1 типу.
Як показали інші спостереження, у приблизно 4-14% пацієнтів із ЦД 2 типу виявляють аутоімунні маркери (за результатами Британського проспективного дослідження ЦД (UKPDS) – 11,6%):
- АТ до декарбоксилази глутамінової кислоти (GADA);
- АТ до тирозинфосфокінази (АГ‑2 (ІА‑2Аb);
- АТ до острівцевих клітин (ІСА);
- АТ до транспортеру цинка 8 – ZnT8Ab.
LADA – це повільно прогресуюча форма аутоімунного діабету, що розвивається в дорослому віці і впродовж певного часу після встановлення діагнозу не потребує інсулінової терапії.
LADA вважається гетерогенним захворюванням і характеризується менш інтенсивним аутоімунним процесом і широким клінічним фенотипом, якщо порівнювати з класичним ЦД 1 типу, може мати клінічні ознаки обох типів ЦД.
У науковій літературі можна зустріти різні назви (епоніми) цього різновиду діабету, зокрема:
- Латентний діабет 1 типу.
- LADA.
- Повільно прогресуючий ЦД 1 типу.
- ЦД 1 типу з повільним початком.
- Діабет типу 1/2, або діабет 1,5.
Більшість випадків LADA діагностують в осіб віком >35 років.
Про складний і специфічний механізм розвитку LADA свідчить його виражена гетерогенність за генетичними, фенотиповими та імунологічними ознаками.
У пацієнтів із LADA можуть бути наявні генетичні ознаки ЦД як 1, так і 2 типу, із чим пов’язана велика варіабельність:
- швидкості деструкції (β)-клітин підшлункової залози (ПЗ);
- інсулінорезистентності;
- аутоімунітету;
- зниження інкретинової відповіді і недостатнього пригнічення глюкагону.
Про актуальність проблеми LADA свідчить той факт, що Американська діабетологічна асоціація (ADA) у 2021 р. вперше внесла його в класифікацію ЦД як різновид ЦД 1 типу:
- діабет 1 типу (унаслідок аутоімунного руйнування β-клітин ПЗ, що зазвичай призводить до абсолютної недостатності інсуліну, зокрема LADA);
- діабет 2 типу (через прогресуючу втрату β-клітинної секреції, часто на тлі інсулінорезистентності);
- специфічні типи діабету, спричинені іншими чинниками, наприклад моногенними синдромами діабету, захворюваннями екзокринної ПЗ, та індуковані лікарськими і хімічними речовинами;
- гестаційний ЦД.
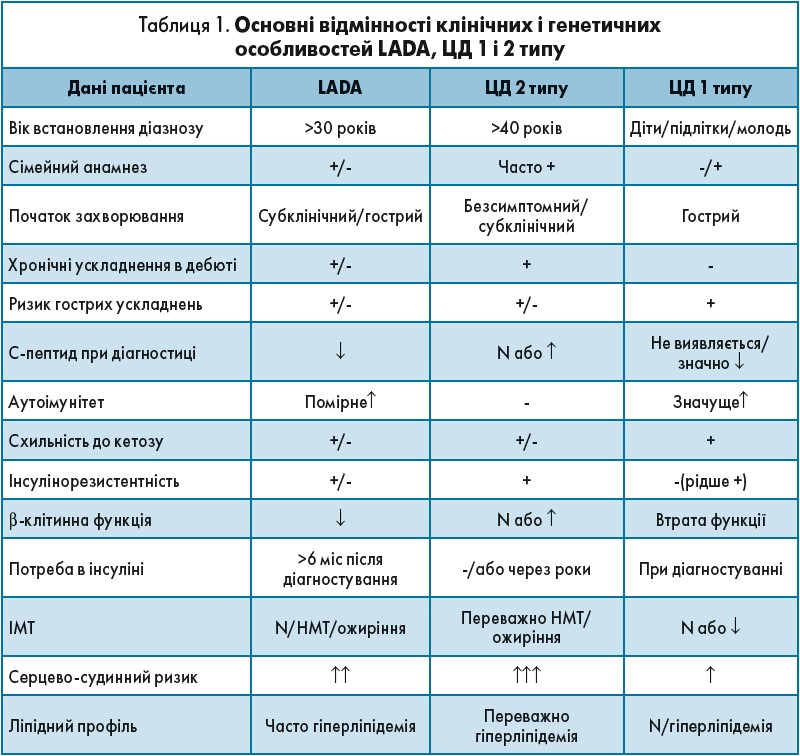
У таблиці 1 наведені основні відмінності клінічних і генетичних особливостей LADA, ЦД 1 і 2 типів.
Критерії діагностики LADA
Відповідно до рекомендацій IDS (Товариства з імунології діабету) до основних критеріїв відносять:
- дебют захворювання у віці після 30 років;
- наявність принаймні одного з таких видів антитіл: GADA, ICA, аутоантитіла до інсуліну (IAA, IA‑2Ab – незалежно від титру, числа або специфічності);
- відсутність потреби в інсуліні впродовж перших 6 міс маніфестації.
Додаткові критерії:
- низький базальний і стимульований рівень С-пептиду;
- поєднання LADA з іншими аутоімунними захворюваннями;
- наявність HLA-алелей високого ризику щодо ЦД 1 типу.
Необхідно зауважити, що питання діагностичних критеріїв LADA залишається дискусійним через генетичну, фенотипову й імунологічну гетерогенність, високу варіабельність швидкості загибелі β-клітин і різні ступені резистентності до інсуліну та вираженості аутоімунітету.
У нещодавній консесусній заяві міжнародної групи експертів (2020) зазначені оновлені діагностичні критерії LADA (автори наголошують, що жодна з цих позицій категорично не визначає LADA):
- вік >30 років (обмежені дані щодо пацієнтів старшого віку з більшою ймовірністю розвитку ЦД 1 типу в пацієнтів молодшого віку);
- сімейний/особистий анамнез аутоімунітету;
- менша, порівнюючи з ЦД 2 типу, частота метаболічного синдрому – нижчі індекс інсулінорезистентності НОМА, індекс маси тіла (IMT), рівні AT і дисліпідемія;
- серцево-судинні наслідки такі самі, як і при ЦД 2 типу;
- рівні С-пептидів знижуються повільніше, ніж при ЦД 1 типу;
- наявність GADA як найчутливіший маркер; інші АТ виявляють рідше (ICA, IA‑2Ab, ZnT8Ab і АТ до тетраспаніну‑7);
- не потребує інсуліну на початку перебігу.
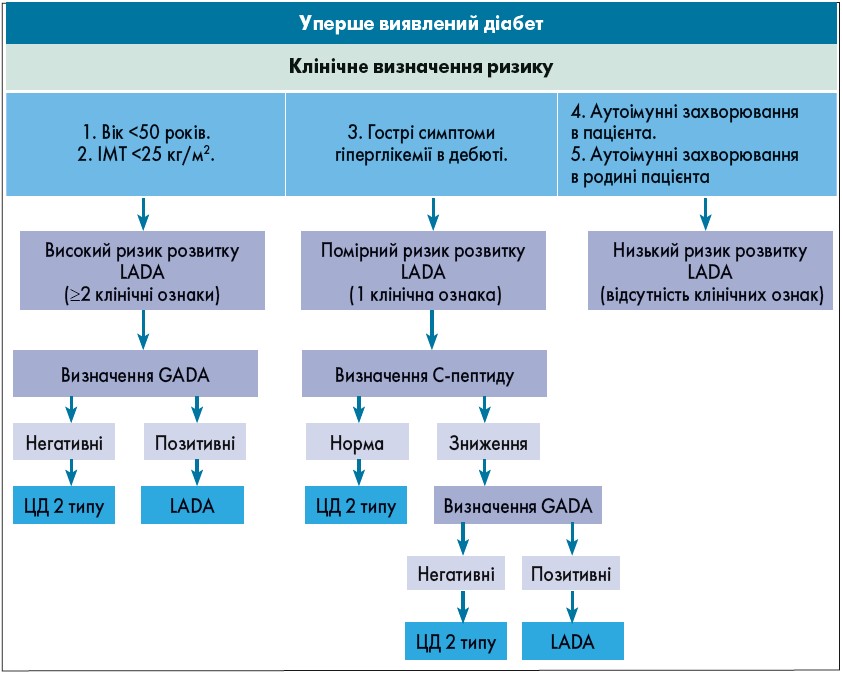
На рисунку 2 представлений схематичний алгоритм діагностики LADA, запропонований S. Pieralice і P. Pozzilli (2018).
Рис. 2. Алгоритм діагностики LADA
Відповідно до клінічно-діагностичних ознак виділяють 2 підтипи LADA:
LADA 1:
- більш схожий на ЦД 1 типу;
- високі титри АТ;
- низькі рівні С-пептиду, вищі показники HbA1с, нижчий IMT, схильність до кетозу.
LADA 2:
- переважають ознаки ЦД 2 типу;
- невисокі титри АТ;
- ознаки метаболічного синдрому;
- кращий глікемічний контроль.
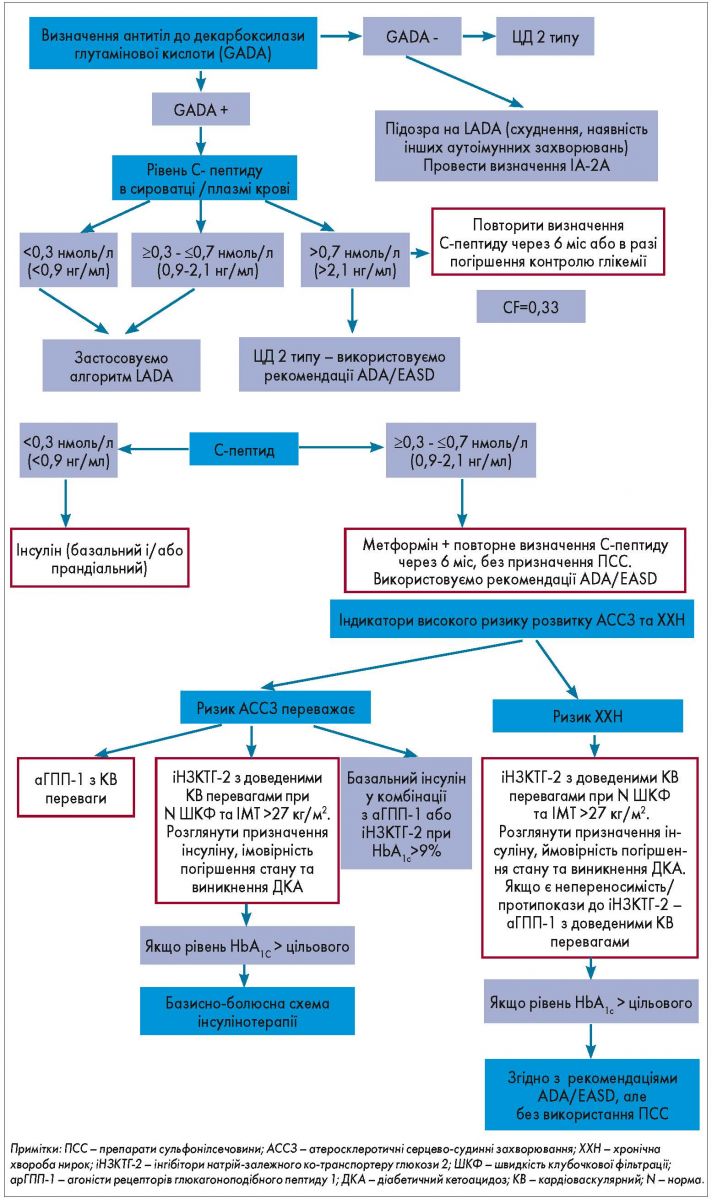
Схема терапії LADA, запропонована в нещодавній консенсусній заяві міжнародної групи експертів (2020), представлена на рисунку 3.
Рис. 3. Схема терапії LADA згідно з консенсусною заявою міжнародної групи експертів (2020)
Отже, зазначила наприкінці свого виступу спікер, можна зробити такі висновки:
- LADA становить до 14% усіх випадків діабету.
- Уперше виникає в людини у віці 35-50 років.
- Може мати фенотипові ознаки ЦД і 1, і 2 типу.
- Діагноз підтверджується визначенням АТ (GADA, IA‑2Ab тощо).
- Вибір терапії залежить від рівня інсулінової секреції, наявних хронічних ускладнень і супутніх захворювань.
Дискусійним питанням залишається невідповідність принципів ведення пацієнтів із LADA чинним рекомендаціям щодо менеджменту ЦД 1 типу.
Украй важливій проблемі стероїд-індукованої гіперглікемії присвятила свою доповідь керівник відділу клінічної діабетології ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», доктор медичних наук Любов Костянтинівна Соколова.
 На сьогодні приблизно 3% дорослого населення лікуються за допомогою глюкокортикостероїдів (ГКС). Поширеність використання ГКС у стаціонарних хворих може перевищувати 10% (Swafe et al., 2014). Частка ЦД, індукованого використанням ГКС, може сягати 30% усіх випадків діабету. У разі стаціонарного лікування ГКС-індукований ЦД спостерігають у 16% пацієнтів (NaDIA 2012). 40% випадків вживання ГКС амбулаторними хворими припадає на лікування респіраторних захворювань, решта – на терапію захворювань опорно-рухового апарату і шкіри, а також на стани, що потребують імуносупресії. Найчастіше ГКС використовують менше 5 днів, у 22% випадків – понад півроку, у 4,3% – довше 5 років (Fardet et al., 2011).
На сьогодні приблизно 3% дорослого населення лікуються за допомогою глюкокортикостероїдів (ГКС). Поширеність використання ГКС у стаціонарних хворих може перевищувати 10% (Swafe et al., 2014). Частка ЦД, індукованого використанням ГКС, може сягати 30% усіх випадків діабету. У разі стаціонарного лікування ГКС-індукований ЦД спостерігають у 16% пацієнтів (NaDIA 2012). 40% випадків вживання ГКС амбулаторними хворими припадає на лікування респіраторних захворювань, решта – на терапію захворювань опорно-рухового апарату і шкіри, а також на стани, що потребують імуносупресії. Найчастіше ГКС використовують менше 5 днів, у 22% випадків – понад півроку, у 4,3% – довше 5 років (Fardet et al., 2011).
Що може збільшити ризик розвитку гіперглікемії в разі застосування ГКС:
- уже наявний ЦД 1 або 2 типу;
- наявність чинників ризику розвитку діабету (ожиріння, сімейний анамнез діабету, попередній гестаційний діабет, приналежність до певних етнічних меншин, синдром полікістозних яєчників , СПКЯ);
- наявність порушення рівня глюкози в плазмі натще або толерантності до глюкози, рівень HbA1c 5,7-6,5%;
- раніше застосовувана стероїдна терапія, яка супроводжувалася тимчасовою гіперглікемією.
Важливо! Ризик розвитку стероїд-індукованої гіперглікемії виникає за умови прийому таких доз ГКС:
- преднізолон – >20 мг;
- гідрокортизон – >50 мг;
- дексаметазон – >4 мг.
Ключові положення щодо контролю гіперглікемії і застосування стероїдної терапії
- ГКС можна вводити за різними режимами і в змінюваних дозах.
- Найпоширеніший спосіб введення ГКС – одноразово або коротким курсом (наприклад, преднізолон) уранці. У пацієнтів із факторами ризику з пізнього ранку може виникати гіперглікемія, яка триває до вечора. Зазвичай за ніч рівень глюкози в крові знижується до базового. Отже, лікування гіперглікемії потрібно адаптувати таким чином, щоб уникати виникнення гіпоглікемії вночі і рано вранці.
- У деяких ситуаціях (зокрема, вагітним) ГКС можуть призначати коротким курсом.
- У стаціонарі здебільшого застосовують багаторазове введення добової дози ГКС.
- Рівень глюкози в більшості пацієнтів може прогнозовано підвищитися приблизно через 4-8 год після прийому оральних ГКС і швидше – після введення ГКС внутрішньовенно.
- Моніторинг рівня глюкози в капілярній крові (CBG) є першорядним втручанням.
- Рівень глюкози може нормалізуватися через 24 год після припинення внутрішньовенного введення ГКС.
- При пероральному застосуванні дози ГКС знижують поступово впродовж декількох тижнів. Відповідно, рівень глікози може знижуватися залежно від актуальної дози ГКС. Але так буває не завжди, особливо в пацієнтів із факторами ризику розвитку стероїд-індукованого діабету, а також в осіб із раніше діагностованим діабетом.
Відповідно до настанов керівництва Об’єднаної групи британських діабетичних товариств для стаціонарного лікування (Joint British Diabetes Societies, JBDS) 2016 року рекомендований цільовий рівень CBG для стаціонарних пацієнтів становить 6-10 ммоль/л (прийнятний діапазон 4-12 ммоль/л).
Однак певні групи осіб не підлягають жорсткому контролю (наприклад, ті, хто перебуває в предсмертному стані), а також пацієнти:
- із зареєстрованою гіпоглікемічною подією;
- із деменцією;
- із депресією;
- старшого віку;
- із ризиком падіння;
- зі зміненим апетитом і ті, які дотримуються дієти.
До початку прийому ГКС перевіряють рівень HbA1с у пацієнтів із високим ризиком розвитку стероїд-індукованого діабету. На початку терапії ГКС в осіб із групи ризику розвитку стероїд-індукованого діабету моніторинг рівня CBG варто розпочинати з його визначення 1 раз на день до/після обіду/вечері, коли гіперглікемічні ефекти ранкового прийому ГКС будуть найбільшими.
В осіб без попереднього діагнозу ЦД моніторинг рівня CBG потрібно проводити щонайменше 1 раз на добу – бажано перед обідом або вечерею або ж, альтернативно, через 1-2 год після обіду/вечері. Якщо початковий рівень CBG <12 ммоль/л, тестування проводять 1 раз на добу до/після обіду/вечері. Якщо виявиться, що рівень CBG перевищує 12 ммоль/л, частоту тестування треба збільшити до 4 разів на добу (перед їдою та перед сном). Якщо ж рівень CBG стабільно, тобто двічі впродовж 24 год, перевищує 12 ммоль/л, тоді пацієнту проводять навчання щодо:
- лікування діабету;
- вибору здорового способу життя;
- ризику розвитку гіпоглікемії при лікуванні пероральними цукрознижувальними препаратами (ПЦЗП) і/або інсуліном.
В осіб з уже наявним ЦД моніторинг рівня CBG необхідно проводити 4 рази на добу – до або після їди і перед сном, незалежно від фонового контролю діабету. Якщо буде виявлено, що глікемія стабільно, тобто двічі впродовж 24 год, перевищує 12 ммоль/л, пацієнту пропонують таку схему лікування стероїд-індукованої гіперглікемії.
Діабет 2 типу – неінсулінова терапія:
- якщо пацієнт отримує ПСС – максимально збільшити ранкову дозу;
- може бути корисним титрування метформіну;
- може бути корисним тимчасове додавання базального людського інсуліну.
Діабет 2 типу – інсулінотерапія:
Змішаний режим
- може бути ефективним збільшення ранкової дози інсуліну.
Базально-болюсний режим
- може бути корисним збільшення короткого обіднього і вечірнього болюсів перед прийомом їжі;
- у разі застосування базального інсуліну – перенести його введення на ранок і збільшувати дозу з кроком 2-4 Од (або на 10-20%) кожні 24-48 год відповідно до результатів моніторингу глюкози;
- у разі застосування аналога базального інсуліну – ретельно стежити за ранньою ранковою гіпоглікемією;
- якщо гіперглікемія зберігається – потрібна складніша схема інсулінотерапії.
Фармакокінетика інсуліну НПХ подібна до такої преднізолону. Пік концентрації інсуліну НПХ корегує гіперглікемію і не призводить до розвитку гіпоглікемії вночі/зранку.
При лікуванні пацієнтів за допомогою ГКС на тлі ЦД 2 типу необхідно встановити цільовий рівень CBG, наприклад 6-10 ммоль/л, збільшити частоту моніторингу до 4 разів на добу, навчити пацієнта особливостям самоконтролю діабету. Якщо епізоди гіперглікемії виникають на тлі терапії ПЦЗП, метформін титрують до 1 г двічі на добу. Якщо гіперглікемія набула неконтрольованого характеру або ГКС вводять багаторазово впродовж доби, розглядають можливість переходу на базальний аналог інсуліну і базально-болюсний режим інсулінотерапії (або альтернативний режим). Необхідно остерігатися нічної і ранкової гіпоглікемії.
У рекомендаціях JBDS 2016 надано алгоритм дій лікаря при виписці зі стаціонару пацієнтів із ризиком розвитку стероїд-індукованої гіперглікемії.
Якщо пацієнтові вже призначили ГКС:
- пацієнт, або його опікун, або особа, яка його доглядає, мають пройти стандартне навчання;
- треба визначати рівень CBG 1 раз на добу (перед обідом і/або після обіду);
- якщо показники CBG у пацієнта перевищують 12 ммоль/л упродовж 24 год, необхідно розглянути зазначений вище алгоритм лікування стероїд-індукованого діабету.
Якщо пацієнта виписують зі зменшенням дози ГКС до 5 мг на добу:
- пацієнт, або його опікун, або особа, яка його доглядає, мають пройти стандартне навчання, зокрема отримати поради щодо порядку дій у разі розвитку гіпоглікемії;
- продовжувати моніторинг глікемії доти, доки рівень CBG не нормалізується (4-7 ммоль/л);
- пацієнт має проходити в лікарні регулярний огляд узгодженою особою (наприклад, лікарем загальної практики, діабетологом, медсестрою – спеціалістом із лікування діабету тощо);
- за необхідності розглянути можливість зменшення титрування антигіперглікемічної терапії.
Якщо пацієнта виписано після припинення прийому ГКС:
- у разі збереження гіпеглікемії:
- здійснювати моніторинг глікемії до нормалізації рівня CBG або до встановлення остаточного діагнозу діабету;
- призначити остаточний тест на діабет (пероральний глюкозотолерантний тест або визначення рівня HbA1c).
На замітку лікарю
- У разі призначення ГКС контролювати глікемію після обіду і перед вечерею.
- Рекомендувати пацієнтам вживати менше вуглеводів у другій половині дня.
- Можна призначати метформін, ПСС, іДПП‑4, арГПП‑1, іНЗКТ‑2 – але це не завжди є ефективним.
- У разі застосування преднізолону – інсулін НПХ.
- У разі застосування дексаметазону призначають базально-болюсний режим інсулінотерапії (30/70%).
На проблемі когнітивних розладів (КР) у хворих на ЦД зосередила свою увагу завідувач кафедри неврології № 2 Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська.
Деменція, що в перекладі з латинської означає «слабоумство», – це тяжке захворювання людей переважно похилого віку і не менш тяжке випробування для їхніх родин (адже саме їм доводиться мати справу крім медичних, ще й з економічними і психологічними труднощами), це неабиякий фінансовий тягар для суспільства, подібний до такого, якщо йдеться про серцево-судинні захворювання (ССЗ) та онкопатологію.
Очікується, що кількість хворих на деменцію в країнах із високим, середнім і низьким рівнем доходів у період між 2010 і 2050 роками збільшиться з 35 до 115 млн осіб (Alzheimer’s Disease International, 2010; Hurd et al., 2013).
Загальна вартість лікування деменції в США у 2010 р. становила від 157 до 215 млрд доларів (Hurd et al., 2013). В Європі щорічні економічні прямі й непрямі витрати на всі захворювання мозку перевищують 790 млрд євро проти 200 млрд євро, що були витрачені на лікування ССЗ, і 150 млрд євро – на лікування злоякісних утворень (Olesen et al., 2012).
ЦД як фактор ризику зниження когнітивних здібностей
Метааналіз 14 популяційних досліджень показав, що частота «будь-якої деменції» була вища у хворих на ЦД, ніж в осіб без діабету, як для хвороби Альцгеймера (ХА), так і судинної деменції (у 8 з 13 і в 6 з 9 досліджень відповідно).
Під час метааналізу 27 досліджень було виявлено, що діабет асоційований зі статистично значущим погіршенням когнітивних показників в одній або декількох когнітивних ділянках у 13 з 29 поперечних зрізів і в 5 із 7 лонгітудинальних досліджень. Зв’язок між діабетом і КР різнився в окремих доменах, ЦД значуще впливав на швидкість обробки інформації в 63% дослідженнях, увагу – в 50%, пам’ять – в 44%.
Пацієнти з ЦД мають постійно здійснювати моніторинг рівня глюкози, дотримуватися складних схем прийому ліків, дієти і виконувати фізичні вправи. Усі ці заходи потребують планування, постійного самоконтролю, уваги, іноді – прийняття важливих рішень. Пацієнти з ЦД і КР виконують ці досить складні завдання менш ефективно, через що мають підвищений ризик розвитку серйозних серцево-судинних подій і смерті.
Ступені вираженості КР
- Легкі КР (ЛКР): легкі суб’єктивні/об’єктивні розлади в одній або кількох когнітивних сферах (КС). У хворого зберігається нормальне функціонування. Наявні дані вказують на те, що ЛКР часто, але не завжди розвиваються внаслідок меншого ступеня тих самих типів мозкових змін, які спостерігають при ХА або інших формах деменції:
- аномальні згустки бета-амілоїдного білка (бляшки) і мікроскопічні згустки тау-білка, характерні для ХА (клубки);
- тільця Леві – мікроскопічні грудочки білка, пов’язаного з хворобою Паркінсона, деменцією з тільцями Леві і деякими випадками ХА;
- лакунарні інсульти або зменшення церебрального кровотоку через судини мозку.
- Візуалізаційні методи дослідження мозку показують, що деякі зміни можуть бути пов’язані з ЛКР:
- зменшення гіпокампа – ділянки мозку, важливої для пам’яті;
- збільшення простору мозку, заповненого рідиною (шлуночки);
- скорочення споживання глюкози – цукру, що є основним джерелом енергії для клітин у ключових регіонах мозку.
- Помірні КР: об’єктивне помірне зниження когнітивних функцій (КФ) в одній або кількох КС. У хворого зберігається відносна незалежність у повсякденній активності, проте виконання звичних процедур може потребувати більше часу.
- Тяжкі КР: різке зниження КФ, поступово розвиваються рухові розлади, згасає здатність до мислення і мовного спілкування. Хворий потребує постійного догляду через безпорадність у побуті.
Скринінгові шкали для визначення КР
- MMSE (коротка оцінка КФ) – первинний скринінг, низька чутливість до судинних КР (СКР).
- MoCA (Монреальська когнітивна шкала) – оцінює виконавчі функції та увагу, тому чутливіша для виявлення ранніх стадій СКР.
- Тест малювання годинника – визначає зорово-просторові порушення при КР.
Ключовою частиною превентивних стратегій щодо КР є виявлення взаємозмінних факторів ризику. У пацієнтів із ЦД це передусім адекватний контроль вуглеводного обміну.
Діабет-асоційована деменція (ДАД) – це підгрупа деменцій без ХА або з меншою її вираженістю і без ССЗ у хворих на ЦД. Діагностують на підставі таких ознак:
- ЦД 2 типу: тривалий термін захворювання і менш контрольована глікемія, високий рівень HbA1c, похилий вік;
- деменція: порушення уваги і виконавчих функцій, повільне прогресування КР, але менше виражене порушення запам’ятовування слів;
- КТ/МРТ: немає ознак уражень судин, дифузна атрофія кори головного мозку, але менш тяжка атрофія медіальної скроневої частки;
- цереброспінальна рідина: нормальний рівень тау-білка і Ав1-42;
- носійство АроЕ 4: низька частота;
- виключення інших причин деменції – гіпотиреоз, дефіцит вітамінів В1, В12, травма голови, хронічний алкоголізм, центральний венозний застій, інші нейродегенеративні захворювання;
- на однофотонній емісійній КТ і позитронно-емісійній томографії: відсутність гіпоперфузії/гіпометаболізму в задній частині мозку, негативне або сумнівне накопичення амілоїду, зниження rCBF у невеликих ділянках лобно-скроневої і лімбічної часток мозку.
ДАД пов’язана з метаболічними розладами і гіперглікемією при ЦД. Контроль глікемії може поліпшити такі КФ, як увага і виконавчі функції, в осіб із ДАД, яку можна розглядати як контрольовану або модифіковану деменцію. На відміну від інших типів деменції виявлення ДАД може бути необхідно для вибору відповідної терапії та профілактики.
У дослідженнях встановлено, що гіпоглікемія посилює експресію мРНК, що кодує білок-попередник β-амілоїду, індукує гіперфосфорилювання тау-білка, яке може призвести до утворення нейрофібрилярних клубків. Під час гіпоглікемічних подій посилюється активність тромбоцитів і лейкоцитів, збільшується утворення фібриногену, знижується NO-опосередкована функція ендотелію, що призводить до вторинного впливу на систему кровообігу, зокрема зменшує об’єм плазми.
Гіпоглікемія шкідливо впливає на гематоенцефалічний бар’єр, запускаючи патогенез вторинних ушкоджень головного мозку.
Додаткові чинники КР при ЦД
- Дисметаболічні патологічні стани, серед яких гіпотиреоз, порушення функції печінки або нирок.
- Дефіцит вітаміну В12, фолієвої кислоти та ін.
- Підвищення рівня гомоцистеїну.
- Наявність супутніх артеріальної гіпертензії та атеросклерозу.
- Підвищення маси тіла, ожиріння.
- Ортостатична гіпотензія.
- Наявність синдрому обструктивного апное сну.
Наостанок доповіді спікер наголосила на окремих моментах. А саме:
- Хворі на ЦД мають вищий, проти іншої популяції, ризик розвитку КР. Однак і сьогодні вплив діабету на нормальні психічні функції часто ігнорується.
- Гіперглікемія на тлі ЦД асоційована зі збільшенням імовірності розвитку ХА і судинної деменції, а також ДАД, що потребує призначення ефективної і безпечної гіпоглікемічної терапії.
- Зменшення частоти мікросудинних ускладнень, гіпер- і гіпоглікемії є доведеним способом запобігання зниженню КФ.
Завершував робочу програму заходу виступ провідного наукового співробітника відділу орфанних захворювань ДУ «Інститут ендокринології та обмну речовин ім. В.П. Комісаренка НАМН України», кандидата медичних наук Лариси Андріївни Луценко, яка представила увазі слухачів доповідь «Гіперандрогенії. Диференційна діагностика». 
Синдром гіперандрогенії (ГА) – патологічний стан, зумовлений надлишковою продукцією андрогенів яєчниками і/або наднирниками або підвищенням локальної тканинної чутливості до циркулюючих андрогенів. Найпоширеніша ендокринопатія в жіночій популяції (приблизно 10-20%). Клінічними проявами ГА є акне, гірсутизм, вірилізація, репродуктивні порушення.
Стани, зумовлені ГА
- Гірсутизм: надлишковий ріст волосся, його пігментація та огрубіння.
- Себорея, акне: підвищена активність сальних залоз.
- Метаболічні порушення: інсулінорезистентність, підвищений рівень інсуліну, дисліпідемія, прогресування ожиріння.
- Ановуляція: атрезія антральних фолікулів.
Під час діагностики ГА необхідно визначити її джерело і патогенез, оцінити вплив на репродуктивну функцію. Для цього уточнюють анамнез, а саме вік початку пубертату і послідовність появи телархе, адренархе, менархе; характер менструального циклу (частота, тривалість і ознаки дисменореї); репродуктивний анамнез (хронічне невиношування, передчасні пологи, непліддя), вік початку і прогресування акне, гірсутизму, себореї, алопеції; прийом будь-яких медикаментів (зокрема, чи був ефект від лікування, якщо проводилася терапія акне і гірсутизму).
Необхідно також перевірити в сімейному анамнезі наявність проявів ГА (гірсутизм, акне, непліддя, раннє (до 35 років) облисіння в родичів чоловічої статі); метаболічні прояви (ЦД, ожиріння, ССЗ, дисліпідемія).
Об’єктивно вивчають дерматологічні прояви: акне, себорею, гірсутизм, алопецію, яку оцінюють за шкалою Людвіга:
- І ступінь: помітне стоншення волосся на маківці, обмежене спереду лінією, розташованою на відстані 1-3 см від лінії росту волосся;
- ІІ ступінь: виражене розрідження волосся на маківці в ділянці, яка вражається при І ступені;
- ІІІ ступінь: повне облисіння (повна денудація) в ділянках, які вражаються при І та ІІ ступені.
Ступінь тяжкості гірсутизму визначають за модифікованою шкалою Феррімана–Галлвея, яка оцінює поширеність термінального волосся в 9 андрогензалежних зонах за 5-бальною шкалою (від 0 до 4 балів). Загальний показник може коливатися від 0 до 36 балів.
Критерії оцінки ступеня тяжкості гірсутизму
- Легкий – 8-15 балів.
- Помірний – 16-25 балів.
- Тяжкий – >25 балів.
Основними проявами вірилізації є виражений гірсутизм (>25 балів); барифонія; атрофія молочних залоз; андрогенна алопеція; маскулінізація; гіпертрофія клітора (довжина >10 мм). У разі швидкого прогресування проявів ГА з тяжкою олігоменореєю або аменореєю є підстави запідозрити розвиток вірильного синдрому.
Патогенетичні форми ГА
- Справжня ГА:
- яєчникова: функціональна (СПКЯ) і пухлинна;
- наднирникова: функціональна (вроджена дисфункція кори наднирників – ВДКН) і пухлинна.
- Інші форми ГА:
- транспортна (причини: гіпотиреоз, гіперінсулінемія, ожиріння, гіпоестрогенія (перименопауза), патологія печінки, нефротичний синдром);
- периферична (рецепторна);
- ятрогенна;
- вторинна.
Найчастіші нозології, які супроводжуються ГА
- СПКЯ.
- Ідіопатичний гірсутизм.
- ВДКН.
- Стромальний текоматоз і стромальна гіперплазія яєчників.
- Вірилізуючі пухлини наднирників.
- Пухлини яєчників, які продукують андрогени.
Кожному лікарю під час діагностики ГА треба знати, які медикаментозні препарати мають андрогенні властивості: анаболічні стероїди, андрогени, гестагени, антигонадотропні, протитуберкульозні, протиепілептичні, седативні, глюкокортикоїди, транквілізатори, циклоспорини, інтерферони.
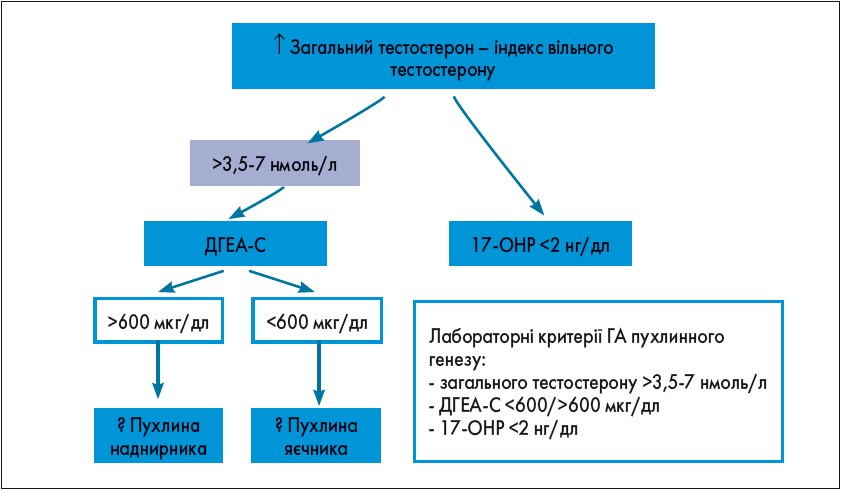
Наступним кроком у діагностичному пошуку є лабораторне обстеження (рис. 4). Діагностичний пошук і загальні діагностичні критерії ГА представлені на рисунках 5 і 6.
Рис. 4. Лабораторне обстеження за підозри на ГА
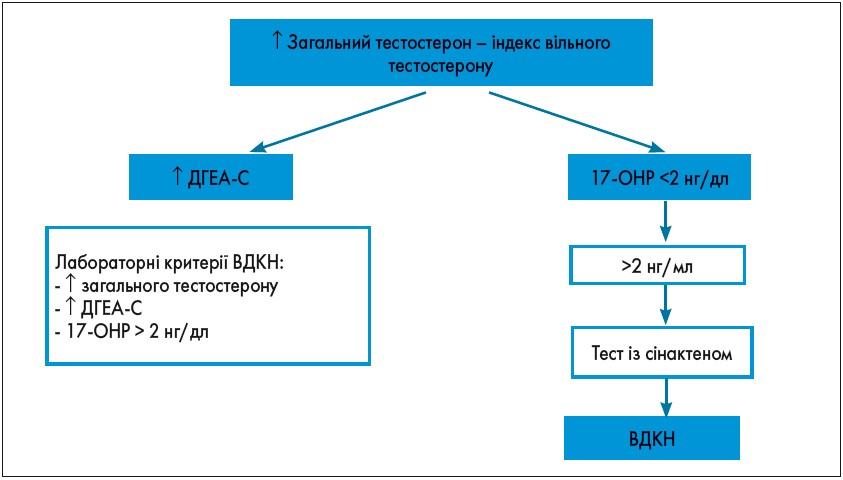
Рис. 5. Діагностичний пошук при ГА
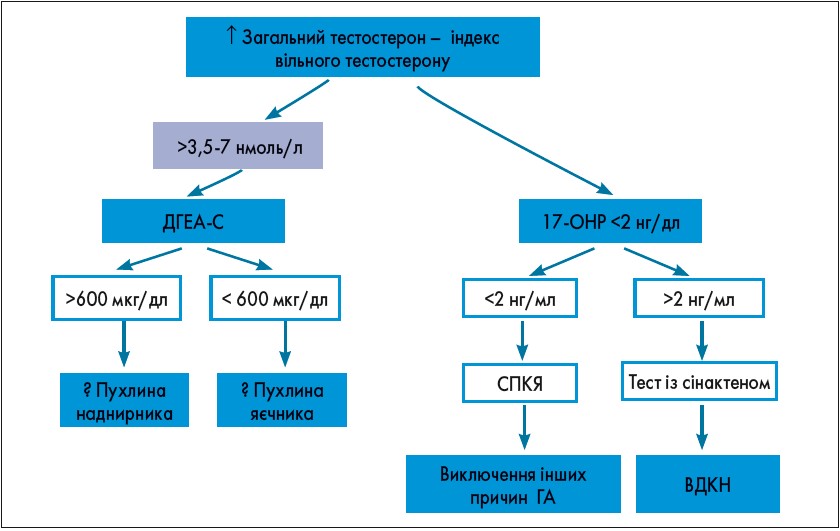
Рис. 6. Загальний діагностичний критерій ГА
Відмінність андрогенпродукуючих пухлин яєчників (АППЯ) і наднирників (АППН) полягає в раптовому початку, швидкому прогресуючому наростанні симптомів ГА, а також значному підвищенні рівня загального тестостерону (>3,5-7 нмоль/л). У разі АППЯ також спостерігатиметься змішана картина гіперкортицизму і вираженої прогресуючої ГА, рівень ДГЕА-С <600 мкг/дл, при АППН ДГЕА-С >600 мкг/дл. Для підтвердження діагнозу проводять МРТ/КТ обстеження.
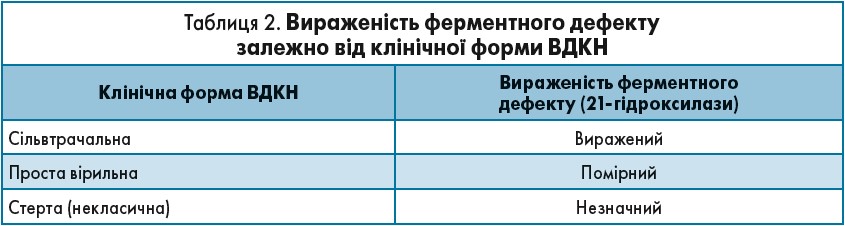
ВДКН – вроджена гіперплазія кори надниркових залоз, адрогенітальний синдром – група захворювань з аутосомно-рецесивним типом спадковості, в основі яких лежить дефект одного з ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу в корі наднирників.
У 90-95% усіх ферментних дефектів при ВДКН виявляють дефіцит 21-гідроксилази (табл. 2).
У разі некласичної форми ВДКН у 90% пацієнток спостерігають двофазний цикл, але можливе і порушення менструального циклу. Фенотипово тілобудова – за жіночим типом, гірсутизм +/-, на УЗД матка нормальних розмірів, яєчники мультикістозні. Характерне підвищення рівнів індексу вільного тестостерону, 17-ОНР, ДГЕА-С, супресія фолікулостимулюючих гормонів (ФСГ), порушення росту й дозрівання фолікула (недостатність лютеїнової фази). Репродуктивний анамнез при некласичній ВДКН може включати: пологи з наступним вторинним непліддям, невиношування вагітності, викидні з 8-го до 28-го тиж вагітності, завмерлі вагітності.
Золотим стандартом у діагностиці ВДКН є тест із сінактеном (250 мкг), який складається з таких етапів:
- визначення базального рівня 17-ОНР уранці (о 8:00 год);
- внутрішньовенне введення сінактену (250 мкг);
- визначення рівня 17-ОНР через 30-60 хв після введення сінактену.
Тест із сінактеном проводять для підтвердження діагнозу до початку лікування ГА.
Клінічні прояви ГА на тлі СПКЯ: гірсутизм – 60-90%, непліддя – 55-75%, акне – 15-35%, андрогенетична алопеція – 5%. Біохімічними ознаками є підвищення рівня вільного (до 70%) і загального тестостерону, інсулінорезистентність (55-75%), збільшення співвідношення ЛГ/ФСГ (34-60%), ↑ДГЕА-С (27-38%).
Підготувала Юлія Золотухіна
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 2 (54) 2021 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....
Метформін – протидіабетичний препарат першої лінії, який пригнічує глюконеогенез у печінці і в такий спосіб знижує рівні глюкози в крові. Крім того, він знижує ризик кардіоваскулярних подій, чинить нефропротекторний ефект і здатен подовжувати тривалість життя. Завдяки цим властивостям метформін нині розглядають як мультифункціональний препарат і дедалі частіше застосовують для лікування та профілактики різноманітних захворювань....
Сучасне лікування хворих на цукровий діабет (ЦД) 2 типу включає зміну способу життя і медикаментозну терапію для контролю глікемії та профілактики ускладнень. Проте дослідження показують, що на практиці небагато хворих досягають контролю захворювання (частково через погану прихильність до лікування). Частка пацієнтів, які дотримуються протидіабетичної терапії, коливається від 33 до 93% (упродовж 6-24 міс) [1, 2]....