Про що не скаже HbA1c: результати дослідження SWITCH PRO
Визначення глікозильованого гемоглобіну (HbA1c), який надає інформацію про середній рівень глікемії за останні 3 міс, є золотим стандартом оцінки ефективності глікемічного контролю та досягнення компенсації у хворих на цукровий діабет (ЦД). Проте рівень HbA1c, на жаль, не відображає варіативності глікемії, тобто не дає лікарю реального уявлення про відхилення рівня глюкози в крові від цільових значень протягом доби.
На сьогодні відомо, що значна добова варіативність глікемії пов’язана з ризиком розвитку ускладнень ЦД. З одного боку, навіть короткі періоди гіперглікемії підвищують ризик розвитку мікро- та макроваскулярних ускладнень, а з іншого – епізоди гіпоглікемії (особливо нічні) становлять серйозну небезпеку для здоров’я й навіть життя хворого. При цьому за наявності в пацієнта епізодів гіпер- і гіпоглікемії може бути отримане нормальне значення HbA1c, яке вводитиме клініциста в оману щодо реальної картини глікемії протягом доби. Тому останніми роками для оцінки глікемічного контролю стали використовувати два нові показники варіабельності глікемії протягом доби: час перебування значень глюкози крові в цільовому діапазоні (time in range – TIR) і час перебування значень нижче цільового діапазону (time below range – TBR). Ці показники можна визначити за допомогою таких сучасних методів обстеження, як постійний моніторінг глюкози (CGM) та флеш-моніторинг глюкози (FMG).
Саме метод FMG за допомогою пристрою Freestyle Libre Pro (Abbott Laboratories), який не потребує регулярної калібровки та дає можливість оцінити реальні коливання глюкози в умовах повсякденного життя пацієнта, використовувався з метою оцінки глікемічного контролю у відкритому перехресному багатоцентровому рандомізованому дослідженні IV фази SWITCH PRO, результати якого були вперше представлені у вересні 2020 р. R. Goldenberg і співавт. на 56-му щорічному конгресі Європейської асоціації з вивчення діабету (EASD). У ході цього дослідження за участі пацієнтів із ЦД 2 типу, які раніше отримували базальний інсулін (у поєднанні з пероральними цукрознижувальними препаратами (ПЦЗП) або без них) і мали підвищений ризик гіпоглікемії, порівнювали контроль глікемії на тлі застосування інсуліну деглюдек 100 Од/мл та інсуліну гларгін 100 Од/мл. Як первинна кінцева точка розглядався показник TIR (%), який надає достовірнішу інформацію щодо контролю глікемії, ніж визначення лише рівня HbA1c, а отже, дає змогу максимально індивідуалізувати лікування завдяки своєчасній корекції інсулінотерапії та режиму харчування.
Дизайн
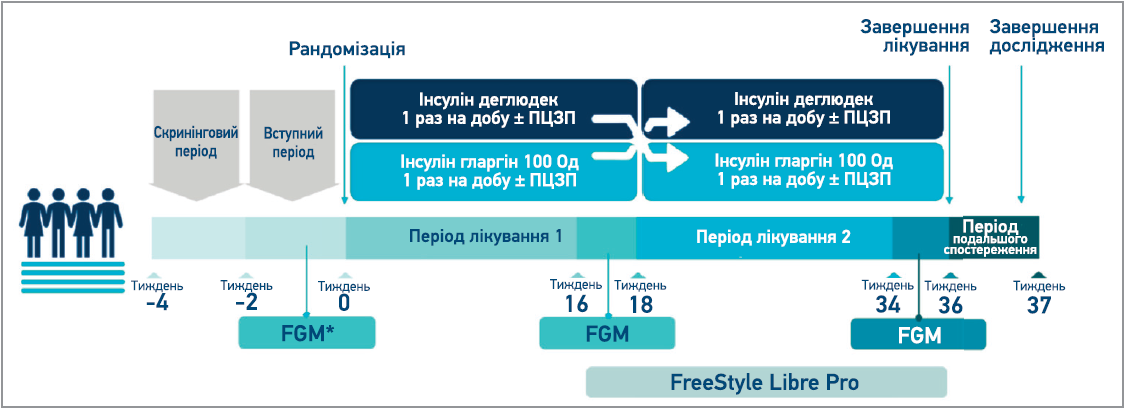
Випробування SWITCH PRO загалом тривало 41 тиж. До початку дослідження його потенційні учасники мали здійснити скринінговий візит (візит 1), після котрого проходили 2-тижневий вступний період для оцінювання прихильності до дотримання вимог застосування методу FGM. На 3-му візиті учасники були рандомізовані у співвідношенні 1:1 в один із двох періодів лікування на застосування інсуліну деглюдек або інсуліну гларгін 100 Од/мл 1 раз на день у той самий час доби (рис.). Кожен період лікування складався з 16-тижневого періоду титрування дози та наступного 2-тижневого періоду підтримувальної терапії, під час якого учасникам встановлювали сенсор FGM. Дозу інсуліну титрували 1 раз на тиждень за показниками глікемії натще (мета титрування – 3,9-5,0 ммоль/л), які визначалися пацієнтами самостійно за допомогою глюкометра; режим застосування ПЦЗП не змінювався. Після цього учасники переходили до іншої групи лікування, де їм проводили такі самі оцінки, як і в першому періоді.
Рис. Дизайн дослідження SWITCH PRO
Примітка: * вихідна оцінка комплаєнтності пацієнта щодо використання сенсора для FGM на тлі застосування
попередньо призначеного інсуліну.
Критерії включення в дослідження:
→ вік ≥18 років;
→ ЦД 2 типу ≥180 днів;
→ застосування базального інсуліну ± ПЦЗП протягом ≥90 днів;
→ HbA1c ≤9,5% (80 ммоль/моль);
→ індекс маси тіла ≤45 кг/м2;
→ наявність ≥1 фактора ризику розвитку гіпоглікемії:
- ≥1 епізод тяжкої гіпоглікемії протягом 1 року до скринінгу;
- порушення ниркової функції середнього ступеня тяжкості (розрахункова швидкість клубочкової фільтрації – 30-59 мл/хв/1,73 м2);
- відоме порушення розпізнавання гіпоглікемії (відсутність ранніх насторожувальних проявів гіпоглікемії);
- лікування інсуліном протягом >5 років;
- епізод гіпоглікемії (зі значенням рівня глюкози крові <70 мг/дл, або 3,9 ммоль/л) протягом останніх 12 тиж перед скринінговим візитом.
Критерії виключення:
- застосування інших препаратів для лікування ЦД або ожиріння протягом останніх 90 днів перед скринінгом (дозволялося інтермітуюче болюсне введення інсуліну тривалістю не довше ніж 14 днів);
- передбачуваний початок або зміна супутньої медикаментозної терапії (прийом препаратів на кшталт орлістату, тиреоїдних гормонів або кортикостероїдів, які можуть впливати на масу тіла чи метаболізм глюкози);
- неконтрольована чи потенційно нестабільна діабетична ретинопатія або макулопатія;
- інфаркт міокарда, інсульт, серцево-судинне захворювання протягом останніх 180 днів перед скринінгом;
- неадекватний контроль артеріальної гіпертензії 3 ступеня на тлі медикаментозного лікування (систолічний артеріальний тиск ≥180 мм рт. ст. або діастолічний ≥100 мм рт. ст.), порушення функції печінки (підвищення рівня аланінамінотрансферази в ≥2,5 рази чи білірубіну в >1,5 рази від верхньої межі норми на момент скринінгу), тяжке порушення ниркової функції (розрахункова швидкість клубочкової фільтрації <30 мл/хв/1,73 м2).
Загалом скринінг пройшли 613 пацієнтів. На підставі аналізу всіх вищезазначених критеріїв 498 із них були включені в дослідження. Середній вік учасників (± стандартне відхилення) становив 62,8±9,8 року; 48% із них – чоловіки. Середня тривалість ЦД дорівнювала 15,1±7,7 року, індекс маси тіла – 32,2±5,5 кг/м2, HbA1c – 7,6±1,0%.
Під час періоду лікування дозволявся прийом таких пероральних протидіабетичних препаратів (мали використовуватися щонайменше за 26 тиж до візиту 1), як метформін, інгібітори дипептидилпептидази‑4, інгібітори натрійзалежного котранспортера глюкози 2 типу, тіазолідиндіони, інгібітори α-глюкозидази. Також дозволялося пероральне застосування зареєстрованих комбінованих препаратів, які включають діючі речовини з перелічених класів. На момент включення в дослідження ПЦЗП отримували 89% пацієнтів: 56% – 1 ПЦЗП, 33% – 2 чи більше.
Лікування інсуліном деглюдек отримали 490 пацієнтів, інсуліном гларгін 100 Од/мл – 484 пацієнти. При цьому за протоколом було проаналізовано дані 448 хворих у кожній групі рандомізації, які закінчили дослідження та мали всі показники FGM та оцінки безпеки.
! Як первинна кінцева точка в дослідженні SWITCH PRO розглядався показник TIR (%) – час перебування в цільовому діапазоні глікемії (3,9-10,0 ммоль/л) під час 2-тижневого періоду підтримувальної терапії на тлі проведення FGM: між візитами 19-21 і 37-39 (тиждень 17-18 і 35-36 відповідно).
Вторинними кінцевими точками, які оцінювалися під час 2-тижневого періоду підтримувальної терапії, виступали такі показники:
- час перебування в суворому діапазоні цільових значень глюкози (3,9-7,8 ммоль/л, або 70-140 мг/дл);
- нічний час перебування значень глюкози в суворому цільовому діапазоні (3,9-7,8 ммоль/л, або 70-140 мг/дл);
- значення HbA1c;
- середні рівні глюкози за даними FGM;
- варіативність глюкози;
- середня доза інсуліну;
- час, проведений в умовах попередження про гіпоглікемію (рівень 1: 3,0-3,8 ммоль/л);
- час, проведений в умовах клінічно значущої гіпоглікемії (рівень 2: <3,0 ммоль/л);
- кількість клінічно значущих гіпоглікемічних епізодів (рівень 2) загалом і в нічні періоди.
Результати
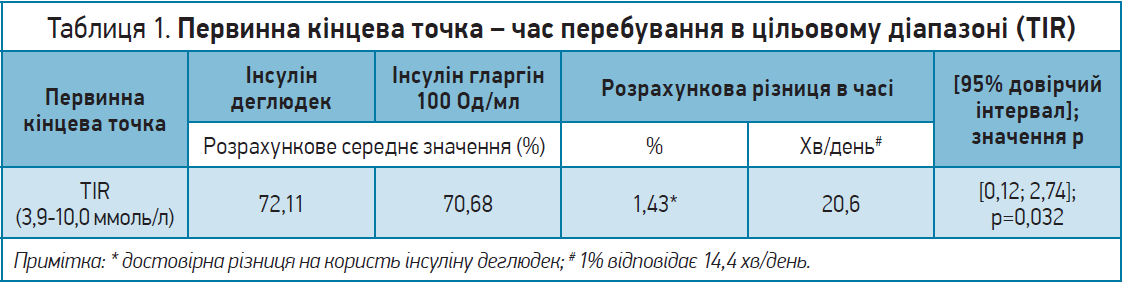
! Дані оцінки первинної кінцевої точки продемонстрували перевагу інсуліну деглюдек перед інсуліном гларгін 100 Од/мл: середнє значення TIR становило 72,11% для інсуліну деглюдек проти 70,68% для інсуліну гларгін 100 Од/мл. Це еквівалентно достовірно більшому часу (20,6 хв/день), проведеному в цільовому діапазоні, на тлі введення інсуліну деглюдек порівняно з інсуліном гларгін 100 Од/мл (табл. 1).
Ба більше, на тлі лікування інсуліном деглюдек клінічно значущого підвищення TIR (≥5%) досягли 39,5% учасників, тоді як на тлі застосування інсуліну гларгін 100 Од/мл – 28,8% учасників (відношення шансів [95% ДІ]: 1,37 [1,09; 1,72]; апостеріорний аналіз).
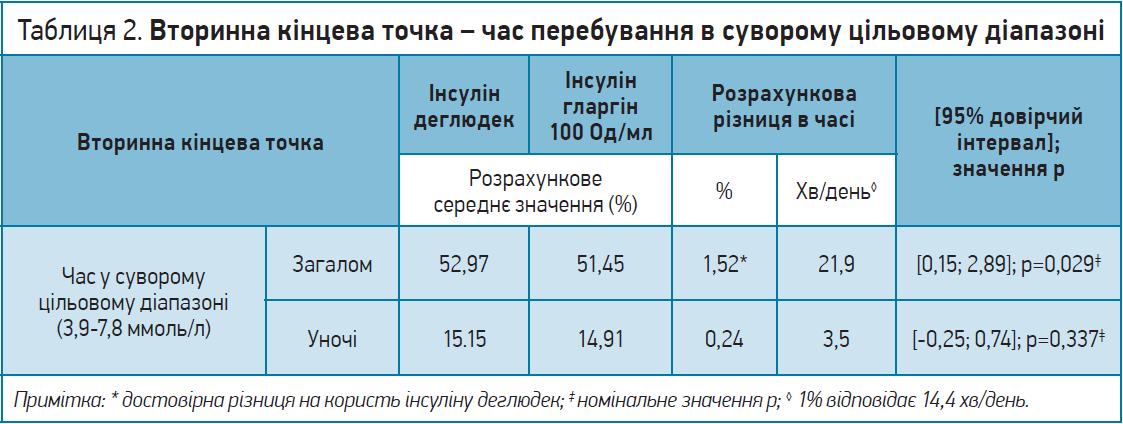
! Аналіз вторинних кінцевих точок засвідчив, що загальний час перебування значень глюкози в суворому цільовому діапазоні (3,9-7,8 ммоль/л) був тривалішим на тлі застосування інсуліну деглюдек порівняно з інсуліном гларгін 100 Од/мл (табл. 2). Розрахункова різниця між групами лікування була достовірно більша на 1,52%, або на 21,9 хв/день, на користь інсуліну деглюдек порівняно з інсуліном гларгін 100 Од/мл.
Що стосується такої вторинної кінцевої точки, як час перебування значень глюкози нижче цільового діапазону (TBR), то було продемонстровано, що терапія інсуліном деглюдек характеризувалася достовірним зменшенням TBR уночі порівняно з лікуванням інсуліном гларгін 100 Од/мл: у період застосування інсуліну деглюдек пацієнти проводили менше часу в TBR (рівні 1, 2 та 1+2) порівняно з періодом лікування інсуліном гларгін 100 Од/мл. На тлі введення інсуліну деглюдек також було зареєстровано меншу кількість нічних епізодів гіпоглікемії (31,1 на пацієнто-рік впливу – PYE) порівняно з інсуліном гларгін 100 Од/мл (40,9 PYE); відношення шансів [95% ДІ]: 0,76 [0,65; 0,90]). Однак загальний показник TBR не відрізнявся між групами лікування (табл. 3).
Середнє значення HbA1c було нижчим на тлі застосування інсуліну деглюдек (7,10%; 54,1 ммоль/моль) порівняно з інсуліном гларгін 100 Од/мл (7,16%; 54,8 ммоль/моль). Середня добова доза базального інсуліну була достовірно меншою в пацієнтів, які отримували інсулін деглюдек, порівняно з інсуліном гларгін 100 Од/мл (56,3 та 58,6 ОД відповідно).
Висновки
Результати дослідження SWITCH PRO продемонстрували, що в осіб із ЦД 2 типу, які вже отримували раніше базальний інсулін і мали підвищений ризик гіпоглікемії, інсулін деглюдек забезпечує такі переваги порівняно з інсуліном гларгін 100 Од/мл:
- більший час перебування в цільовому діапазоні глюкози (TIR);
- більший час перебування в суворому цільовому діапазоні глюкози;
- менша кількість нічних епізодів гіпоглікемії рівня 2;
- менший час перебування в діапазоні гіпоглікемії вночі (рівень 1 і 2).
На тлі застосування інсуліну деглюдек більша кількість пацієнтів досягли клінічно значущого покращення TIR (≥5%) порівняно із застосуванням інсуліну гларгін 100 Од/мл. Менша частота нічних гіпоглікемій і більший час перебування в цільовому діапазоні свідчать про нижчу варіативність глікемії, а також дають змогу сподіватися на зниження ризику віддалених ускладнень ЦД на тлі терапії інсуліном деглюдек.
КОМЕНТАР ЕКСПЕРТА
Керівник відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова:
 – На сьогодні добова варіативність глікемії, об’єктивно оцінювати яку дала змогу поява високочутливих методів постійного моніторингу глюкози (зокрема, флеш-моніторингу глюкози – FGM), перебуває в центрі уваги науковців і клініцистів, адже її аналіз надає вичерпну інформацію про реальну картину глікемічного контролю в пацієнта протягом доби. Відомо, що висока варіативність глікемії збільшує ризик серйозних серцево-судинних ускладнень ЦД, а також є предиктором виникнення тяжких гіпоглікемічних епізодів. Результати відкритого перехресного багатоцентрового рандомізованого дослідження IV фази SWITCH PRO, про які було вперше повідомлено під час минулорічного конгресу EASD, надали діабетологам можливість «зазирнути за ширму» традиційного критерію компенсації ЦД – HbA1c – та за допомогою методу FMG оцінити глікемічний контроль на тлі застосування 2 різних інсулінів тривалої дії (інсуліну деглюдек й інсуліну гларгін 100 Од/мл) саме в тих пацієнтів, які вже мали певні фактори підвищеного ризику виникнення гіпоглікемії. Первинною кінцевою точкою, яку оцінювали в ході цього дослідження, був не рівень HbA1c, а такий сучасний критерій оцінки якості глікемічного контролю протягом доби, як TIR (time-in-range) – показник часу, вираженого у відсотках, протягом якого рівень глюкози в крові в пацієнта перебуває в межах цільового діапазону. Саме TIR наразі пропонується використовувати як новий високоінформативний індикатор контролю глікемії протягом доби (ADA, 2021). Згідно з рекомендаціями Міжнародного консенсусу з оцінки показника TIR (Battelino T. et al., 2019), у дорослих пацієнтів оптимальним є значення TIR >70% при цільовому діапазоні глікемії 3,9-10,0 ммоль/л. У дослідженні SWITCH PRO на тлі інсулінотерапії цей критерій був досягнутий. При цьому результати порівняльної оцінки TIR в учасників дослідження SWITCH PRO засвідчили достовірну перевагу інсуліну деглюдек – на тлі його введення значення глікемії в пацієнтів перебували в цільовому діапазоні протягом достовірно більшого часу, ніж при застосуванні інсуліну гларгін 100 Од/мл. Нижча варіативність глікемії на тлі лікування інсуліном деглюдек, продемонстрована в цьому дослідженні, також супроводжувалася достовірним зменшенням часу перебування значень глікемії нижче цільового діапазону (TBR) вночі та меншою кількістю нічних епізодів клінічно значимої гіпоглікемії (<3,0 ммоль/л) порівняно з лікуванням інсуліном гларгін 100 Од/мл. Таким чином, отримані в дослідженні SWITCH PRO дані обґрунтовують переваги інсуліну деглюдек з точки зору балансу між утриманням значень глікемії в межах цільового діапазону та безпекою інсулінотерапії. Ширше застосування методів постійного моніторингу глюкози має підтвердити ці переваги інсуліну деглюдек у реальній клінічній практиці й у кінцевому підсумку покращити якість життя та прогноз у пацієнтів із ЦД 2 типу, які потребують інсулінотерапії, завдяки зменшенню частоти розвитку ускладнень захворювання.
– На сьогодні добова варіативність глікемії, об’єктивно оцінювати яку дала змогу поява високочутливих методів постійного моніторингу глюкози (зокрема, флеш-моніторингу глюкози – FGM), перебуває в центрі уваги науковців і клініцистів, адже її аналіз надає вичерпну інформацію про реальну картину глікемічного контролю в пацієнта протягом доби. Відомо, що висока варіативність глікемії збільшує ризик серйозних серцево-судинних ускладнень ЦД, а також є предиктором виникнення тяжких гіпоглікемічних епізодів. Результати відкритого перехресного багатоцентрового рандомізованого дослідження IV фази SWITCH PRO, про які було вперше повідомлено під час минулорічного конгресу EASD, надали діабетологам можливість «зазирнути за ширму» традиційного критерію компенсації ЦД – HbA1c – та за допомогою методу FMG оцінити глікемічний контроль на тлі застосування 2 різних інсулінів тривалої дії (інсуліну деглюдек й інсуліну гларгін 100 Од/мл) саме в тих пацієнтів, які вже мали певні фактори підвищеного ризику виникнення гіпоглікемії. Первинною кінцевою точкою, яку оцінювали в ході цього дослідження, був не рівень HbA1c, а такий сучасний критерій оцінки якості глікемічного контролю протягом доби, як TIR (time-in-range) – показник часу, вираженого у відсотках, протягом якого рівень глюкози в крові в пацієнта перебуває в межах цільового діапазону. Саме TIR наразі пропонується використовувати як новий високоінформативний індикатор контролю глікемії протягом доби (ADA, 2021). Згідно з рекомендаціями Міжнародного консенсусу з оцінки показника TIR (Battelino T. et al., 2019), у дорослих пацієнтів оптимальним є значення TIR >70% при цільовому діапазоні глікемії 3,9-10,0 ммоль/л. У дослідженні SWITCH PRO на тлі інсулінотерапії цей критерій був досягнутий. При цьому результати порівняльної оцінки TIR в учасників дослідження SWITCH PRO засвідчили достовірну перевагу інсуліну деглюдек – на тлі його введення значення глікемії в пацієнтів перебували в цільовому діапазоні протягом достовірно більшого часу, ніж при застосуванні інсуліну гларгін 100 Од/мл. Нижча варіативність глікемії на тлі лікування інсуліном деглюдек, продемонстрована в цьому дослідженні, також супроводжувалася достовірним зменшенням часу перебування значень глікемії нижче цільового діапазону (TBR) вночі та меншою кількістю нічних епізодів клінічно значимої гіпоглікемії (<3,0 ммоль/л) порівняно з лікуванням інсуліном гларгін 100 Од/мл. Таким чином, отримані в дослідженні SWITCH PRO дані обґрунтовують переваги інсуліну деглюдек з точки зору балансу між утриманням значень глікемії в межах цільового діапазону та безпекою інсулінотерапії. Ширше застосування методів постійного моніторингу глюкози має підтвердити ці переваги інсуліну деглюдек у реальній клінічній практиці й у кінцевому підсумку покращити якість життя та прогноз у пацієнтів із ЦД 2 типу, які потребують інсулінотерапії, завдяки зменшенню частоти розвитку ускладнень захворювання.
Підготувала Вікторія Новікова
Медична газета «Здоров’я України 21 сторіччя» № 15 (508), 2021 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
21 березня в рамках II Міжнародної школи «Сучасний лікар: від теорії до практики» професор кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, лікар-ендокринолог вищої категорії, доктор медичних наук Вікторія Олександрівна Сергієнко представила доповідь, присвячену хронічним ускладненням цукрового діабету (ЦД). Зокрема, було акцентовано увагу на причинах розвитку діабетичної полінейропатії (ДП), розглянуто клінічні варіанти цього ускладнення, діагностичні підходи та основні принципи лікування. Пропонуємо огляд цієї доповіді у форматі «запитання – відповідь»....
Останніми десятиліттями в усьому світі спостерігалося значне зростання поширеності цукрового діабету (ЦД), що зумовило серйозні наслідки стосовно якості життя населення, а також спричинило певний тягар для системи охорони здоров’я та економічні витрати [1]. За даними Діабетичного атласу Міжнародної діабетичної федерації (International Diabetes Federation Diabetes Atlas), у 2021 р. ≈537 млн людей мали ЦД і, за прогнозами, до 2045 р. цей показник досягне 783 млн [2]. Значна захворюваність і підвищена смертність асоційовані з пов’язаними із ЦД макросудинними (інфаркт міокарда, інсульт) і мікросудинними (сліпота, ниркова недостатність, ампутації) ускладненнями [3]....
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....