Особливості антигіпертензивної терапії у пацієнтів із гіпертонією та ішемічною хворобою серця: місце комбінації телмісартану з амлодипіном
 Поєднання артеріальної гіпертензії (АГ) та ішемічної хвороби серця (ІХС) є доволі частою коморбідністю. Приблизно 60% осіб з ІХС мають підвищений артеріальний тиск (АТ), що за відсутності його ефективного контролю значно погіршує перебіг ІХС та серцево-судинний (СС) прогноз хворого. Сучасні настанови з діагностики та лікування АГ виокремлюють групу пацієнтів з АГ й ІХС, зважаючи на особливі підходи до ініціювання та вибору антигіпертензивної терапії.
Поєднання артеріальної гіпертензії (АГ) та ішемічної хвороби серця (ІХС) є доволі частою коморбідністю. Приблизно 60% осіб з ІХС мають підвищений артеріальний тиск (АТ), що за відсутності його ефективного контролю значно погіршує перебіг ІХС та серцево-судинний (СС) прогноз хворого. Сучасні настанови з діагностики та лікування АГ виокремлюють групу пацієнтів з АГ й ІХС, зважаючи на особливі підходи до ініціювання та вибору антигіпертензивної терапії.
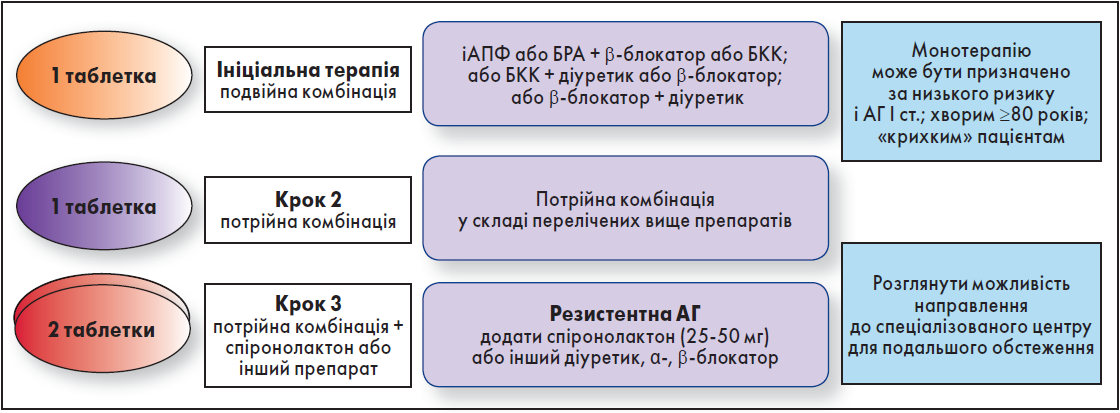
У рекомендаціях Європейського товариства кардіологів / Європейського товариства з гіпертензії (ESC/ESH, 2018) вказано, що у пацієнтів з ІХС варто розглянути призначення медикаментозного лікування вже на етапі передгіпертензії (Williams, 2018). Тактика антигіпертензивної терапії докорінно не відрізняється від застосовуваної у загалу хворих на АГ. Проте в осіб із АГ та ІХС є особливості щодо вибору антигіпертензивних засобів, які водночас можуть бути й антиангінальними (рис. 1).
Пріоритетною є комбінація, яка містить блокатор ренін-ангіотензин-альдостеронової системи (РААС) – інгібітори ангіотензинперетворювального ферменту (іАПФ) або блокатори рецепторів ангіотензину ІІ (БРА) з додаванням β-блокатора або блокатора кальцієвих каналів (БКК) залежно від клінічного варіанта ІХС. Вибір на користь β-блокаторів буде однозначним у пацієнтів із перенесеним інфарктом міокарда (ІМ) принаймні протягом першого року, за наявності серцевої недостатності зі зниженою фракцією викиду лівого шлуночка (ЛШ) та у разі стенокардії для зменшення потреби міокарда в кисні за рахунок зниження частоти серцевих скорочень. БКК чинять антиангінальну дію іншим способом – шляхом вазодилатації коронарних артерій, і також використовуються при стенокардії.
Рис. 1. Стратегія фармакотерапії при коморбідних АГ та ІХС
Примітки: іАПФ – інгібітор ангіотензинперетворювального ферменту, БРА – блокатор рецепторів ангіотензину ІІ,
БКК – блокатор кальцієвих каналів.
Блокада РААС має ключове значення не лише в лікуванні АГ. Вона є одним з ефективних засобів зниження ризику СС-катастроф та подовження тривалості життя пацієнтів з ІХС. Наразі два препарати групи іАПФ – раміприл і периндоприл – доведено покращують СС-прогноз осіб з ІХС.
Периндоприл у дослідженні EUROPA сприяв зниженню відносного ризику розвитку первинної кінцевої точки (як-то СС-смерть, ІМ, зупинка серця) на 20% у пацієнтів з ІХС, більшість яких мали в анамнезі ІМ та реваскуляризацію коронарних артерій (Fox, 2003). Раміприл довів свою здатність покращувати прогноз у хворих високого СС-ризику, зокрема з ІХС, у дослідженні НОРЕ. Зменшення ймовірності розвитку первинної кінцевої точки (як-от СС-смерть, ІМ, інсульт) становило 22%; окремо ризик інсульту знизився на 32%, ІМ – на 20%, СС-смерті – на 26% і летальних випадків від усіх причин – на 16% (Sleght, 2000).
Щодо впливу БРА на прогноз пацієнтів з ІХС, телмісартан – єдиний представник цієї групи, прогностичну ефективність якого було вивчено порівняно з іАПФ раміприлом у проспективному прямому порівняльному дослідженні ОNТАRGЕТ у пацієнтів високого ризику. За його результатами встановлено рівнозначний вплив телмісартану та раміприлу на ризик розвитку СС-патологій і смерті від них – 16,7 і 16,5% відповідно для БРА та іАПФ.
У пацієнтів з АГ та ІХС, як і загалом при АГ, пріоритетними єфіксовані комбінації (ФК). Проте широке використання ФК в осіб з ІХС обмежене їх доступністю. Натепер у терапевтичному арсеналі є поодинокі фіксовані комбінації β-блокаторів з іАПФ, БКК та діуретиком. Однак із кожним роком збільшується кількість ФК блокаторів РААС із БКК. Однією з новацій у нашій країні є ФК БРА телмісартану із БКК амлодипіном.
Як зазначалося вище, телмісартан має доведені прогностичні переваги у пацієнтів з ІХС. Окрім того, за даними інших досліджень, телмісартан покращував пізні результати стентування коронарних артерій (покриті та непокриті стенти) в осіб із гострим ІМ, АГ та АГ у поєднанні з цукровим діабетом (Hasegawa et al., 2011; Yamaguchi et al., 2014; Terashima et al., 2012).
На стадії асимптомного гіпертензивного ураження серця телмісартан ефективніший щодо регресу гіпертрофії ЛШ (ГЛШ), аніж карведилол та гідрохлоротіазид (ГХТЗ). За даними дослідження TRANSCEND, ризик виникнення нових випадків ГЛШ виявився нижчим на 37% (р<0,001) у групі телмісартану порівняно із плацебо (Подзолков, Тарзиманова, 2017).
Слід зауважити, що на тлі регресу ГЛШ під впливом телмісартану також відбувалося:
- зменшення порожнин серця – ЛШ та передсердь;
- поліпшення систолічної та діастолічної функції ЛШ;
- зменшення ознак порушення діастолічного розслаблення ЛШ у хворих на ранню діабетичну кардіоміопатію.
Зменшення ремоделювання серця, зокрема передсердь, може бути однією з передумов зниження ризику виникнення порушень серцевого ритму, зокрема фібриляції/тріпотіння передсердь. У низці досліджень було встановлено здатність телмісартану запобігати виникненню рецидивів фібриляції передсердь (Mizuguchi 2009; Pan, 2014; Fogary, 2012).
Що стосується другого компонента комбінації амлодипіну, механізм його дії пов’язаний із вазодилатацією за рахунок модуляції кальцієвих каналів L-типу. Вазодилатувальний вплив амлодипіну реалізується не лише на рівні периферичних, але й коронарних і ниркових артерій – його ефекти охоплюють практично всі судинні басейни. Головним аргументом на користь вибору ББК, зокрема амлодипіну як другого компонента для стартової терапії в пацієнтів з АГ і ІХС, є доведені органопротекторні властивості, доказова база щодо поліпшення прогнозу в осіб з АГ та його антиангінальна дія (Jamerson, 2008).
Амлодипін – антиангінальний препарат, який застосовують для лікування стенокардії, зокрема вазоспастичної. За даними дослідження САРЕ, у пацієнтів з епізодами ішемії міокарда приймання амлодипіну сприяло:
- зменшенню кількості нападів стенокардії та вживання нітрогліцерину;
- зниженню частоти епізодів ішемії міокарда й загального часу ішемії за даними 48-годинного моніторування ЕКГ.
На сьогодні в Україні представлено лише одну фіксовану комбінацію телмісартану/амлодипіну – препарат Телдіпін. Досвід її застосування у різних категорій пацієнтів з АГ підтверджує високу антигіпертензивну ефективність препарату і тривалий ефект упродовж доби завдяки фармакокінетичним властивостям компонентів. Телмісартан та амлодипін характеризуються чи не найдовшим серед антигіпертензивних засобів періодом напіввиведення – 24 і 35‑52 год відповідно. За даними F.H. Leenen, навіть через два дні від застосування амлодипіну АТ утримується на досягнутому рівні.
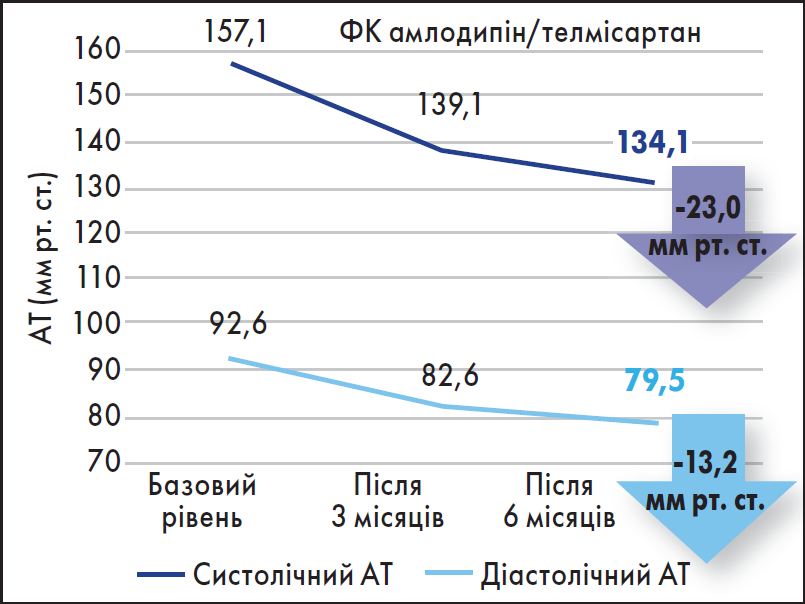
Високу антигіпертензивну ефективність та сприятливий профіль переносимості генеричної ФК телмісартан/амлодипін (Телдіпін) було продемонстровано в дослідженні Telmistar у різних категорій хворих на АГ: з ІХС, ожирінням, цукровим діабетом, хронічною хворобою нирок. Лікування цією ФК протягом шести місяців сприяло зниженню САТ і ДАТ на 23 і 13,2 мм рт. ст. відповідно і досягненню ефективного контролю АТ у 70 та 90% для САТ і ДАТ відповідно (рис. 2).
Рис. 2. Результати лікування ФК телмісартан/амлодипін протягом шести місяців
Важливо зазначити, що на тлі терапії рівень сечової кислоти, сечовини, креатиніну та основних електролітів (калію, натрію, хлору) не зазнав змін, а в осіб із вихідною гіперурикемією навіть спостерігалося зниження сироваткового вмісту сечової кислоти на 39,4 мкмоль/л. Окрім того, Телдіпін сприяв поліпшенню вуглеводного та ліпідного метаболізму. Про це свідчить зниження рівнів загального холестерину (ХС) на 5,7% за рахунок ХС ліпопротеїнів низької щільності (ЛПНЩ) на 9,2% та глюкози на 11,5%, що, ймовірно, є наслідком стимуляції РРАR-γ рецепторів (Сaprnda et al. 2020).
Далі наведено клінічний випадок як ілюстрацію індивідуальної антигіпертензивної ефективності ФК телмісартан/амлодипін (Телдіпін) й обміну досвідом її призначення у пацієнта з АГ та ІХС.
Клінічний випадок
Пацієнт К., 63 роки.
Скарги. Звернувся зі скаргами на погіршення самопочуття після перенесеного в листопаді COVID‑19: періодичний головний біль, дискомфорт у ділянці серця при підвищенні АТ >160/100 мм рт. ст., фізичних навантажень уникає, відзначає слабкість і поганий сон.
Анамнез. Має АГ впродовж 14 років. Діагноз ІХС: стенокардію напруги функціонального класу ІІ встановлено 2 роки тому. Сімейний анамнез не обтяжений, курить близько 15 цигарок на добу, веде малорухомий спосіб життя.
Терапія на момент огляду. Бісопролол у дозі 5 мг вранці, ФК лізиноприл/ГХТЗ по 10/12,5 мг вранці, клопідогрель по 75 мг/добу. Приймання симвастатину припинив у період хвороби на COVID‑19. Додатково отримує 750 мг/добу мельдонію та 500 мг/добу фенібуту.
Обстеження. Офісний АТ – 168/95 мм рт. ст., пульс ритмічний – 62 уд./хв., індекс маси тіла – 31,2 кг/м2, окружність талії – 112 см. Із боку внутрішніх органів і систем – без клінічно значущих змін. Набряків немає.
За даними амбулаторного добового моніторування АТ має місце підвищений рівень середньоденного (141/90 мм рт. ст.) і середньонічного АТ (129/82 мм рт. ст.); порушення добового ритму АТ у вигляді недостатнього зниження АТ у нічні години (добовий індекс САТ/ДАТ – 8,5/8,9%); висока варіабельність САТ у денний і нічний період – 17,5/15,4 мм рт. ст. відповідно.
ЕКГ: ритм синусовий, регулярний, частота серцевих скорочень – 60‑62/хв, переважання біопотенціалів ЛШ. За даними оцінки стану органів-мішеней, наявні ГЛШ (індекс маси міокарда ЛШ – 119 г/м2) та атеросклеротичне ураження сонних артерій (а саме бляшки у правій та лівій внутрішній сонній артерії: стенози за NASCET – від 35 до 45%), функція нирок збережена (швидкість клубочкової фільтрації – 101 мл/хв/1,73 м2).
Із боку лабораторних показників привертає увагу комбінована дисліпідемія зі значно підвищеним рівнем загального ХС 7,1 ммоль/л за рахунок ХС ЛПНЩ 4,2 ммоль/л і гіпертригліцеридемія до 2,4 ммоль/л.
Лікування. Підсумовуючи результати огляду та обстеження пацієнта з АГ та ІХС, варто закцентувати увагу на необхідності поновлення статинотерапії та інтенсифікації антигіпертензивного лікування з метою досягнення цільових значень ХС ЛПНЩ і АТ. Хворому рекомендовано високоінтенсивну статинотерапію розувастатином у дозі 40 мг/добу, враховуючи високий вихідний рівень ХС ЛПНЩ.
Для покращання контролю АТ ФК лізиноприл/ГХТЗ було замінено на ФК телмісартан/ амлодипін (Телдіпін) по 80/10 мг/добу. Вибір на користь даної подвійної комбінації був зумовлений кількома факторами. Попередня подвійна комбінація містила іАПФ і ГХТЗ у мінімальних дозах, тому доцільним було призначення подвійної комбінації в максимальній дозі.
У пацієнтів з АГ та ІХС із точки зору органопротекторних та антиангінальних властивостей раціональним є вибір амлодипіну, а не ГХТЗ. Принциповим аргументом на користь обраної комбінації є також доказова база телмісартану й амлодипіну щодо поліпшення прогнозу в осіб з АГ та ІХС.
Окрім того, поєднання двох препаратів із тривалим періодом напіввиведення має забезпечити стабільний та ефективний контроль АТ протягом доби, знижуючи також високий ранковий приріст АТ. Вкрай важливим також є доведена відмінна переносимість терапії комбінацією телмісартану й амлодипіну, а також позитивний вплив на вуглеводний і ліпідний метаболізм.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (77) 2021 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Інколи саме з цього перерізу вдається візуалізувати тромбоемболи в основних гілках легеневої артерії або вегетації на стулках легеневого клапана (що трапляється надзвичайно рідко). Нахиливши датчик до самої верхівки серця, можна отримати її переріз по короткій осі, на якому, знову ж таки, порожнина лівого шлуночка має круглясту форму, а правого шлуночка – близьку до трикутника із виразною трабекулярністю (рис. 22.9). Розглядаючи зображення, також звертають увагу на те, що в нормі всі сегменти ЛШ скорочуються синхронно, не випереджаючи інші і не відстаючи. ...
Застосування статинів середньої інтенсивності в комбінації з езетимібом порівняно зі статинами високої інтенсивності окремо може забезпечити більше зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ішемічним інсультом. Пропонуємо до вашої уваги огляд статті Keun-Sik Hong et al. «Moderate-Intensity Rosuvastatin Plus Ezetimibe Versus High-Intensity Rosuvastatin for Target Low-Density Lipoprotein Cholesterol Goal Achievement in Patients With Recent Ischemic Stroke: A Randomized Controlled Trial», опублікованої у виданні Journal of Stroke (2023; 25(2): 242‑250). ...
Артеріальна гіпертензія (АГ) сьогодні є одним із найпоширеніших серцево-судинних захворювань (ССЗ), що асоціюється з високим кардіоваскулярним ризиком, особливо в коморбідних пацієнтів. Навіть помірне підвищення артеріального тиску (АТ) пов’язане зі зменшенням очікуваної тривалості життя. До 40% хворих на АГ не підозрюють у себе недугу, бо це захворювання на початку може мати безсимптомний перебіг. Оптимальний контроль АТ є вагомим чинником профілактики фатальних серцево-судинних подій (ССП) для забезпечення якісного та повноцінного життя таких хворих. ...