Якість життя, пов’язана зі здоров’ям, у жінок у пременопаузі з поширеним HR+/HER2- РМЗ: результати лікування рибоциклібом у поєднанні з ендокринною терапією
Дані рандомізованого клінічного дослідження III фази MONALEESA-7
У своїй клінічній практиці онкологи неодноразово стикаються з певними труднощами у лікуванні раку молочної залози (РМЗ). Ці труднощі пов’язані не тільки з появою резистентності до лікування, а й із потребою забезпечення підтримки належної якості життя (ЯЖ) у молодих пацієнток.
Згідно з рекомендаціями Національної онкологічної мережі США (National Comprehensive Cancer Network, 2019) та останніми даними консенсусу Європейської школи онкології і Європейського товариства медичної онкології (2018) як терапію першої лінії у жінок у пременопаузі з гормон-рецепторпозитивним (HR+), негативним за експресією рецептора епідермального фактора росту людини 2 (HER2-) поширеним РМЗ рекомендовано призначати інгібітор циклінзалежної кінази 4/6 (CDK4/6) у поєднанні з ендокринною терапією (ЕТ) [1, 2]. Ефективність такого режиму терапії порівнювали з плацебо у поєднанні з гозереліном і нестероїдним інгібітором ароматази (НІА) летрозолом або анастрозолом чи тамоксифеном у пацієнток у пременопаузі з HR+/HER2- РМЗ у клінічному дослідженні III фази MONALEESA‑7 [4].
У рамках цього клінічного дослідження було показано, що медіана виживаності без прогресування (ВБП) була більшою та складала 23,8 міс у групі рибоциклібу, тоді як у групі плацебо – 13,0 міс (відношення ризиків – ВР – 0,55; 95% довірчий інтервал – ДІ – 0,44-0,69; p <0,0001). Додавання рибоциклібу до ЕТ також сприяло зростанню загальної виживаності (ЗВ) зі зниженням відносного ризику смерті на 29% порівняно з плацебо (ВР 0,71; 95% ДІ 0,54-0,95; p=0,00973). ЗВ через 42 міс спостереження складала 70,2% (95% ДІ 63,5-76,0) у групі рибоциклібу та 46,0% (95% ДІ 32,0-58,9) у групі плацебо [5].
Як правило, профіль безпеки можна було контролювати шляхом модифікації дози та схеми лікування [4].
Вторинним завданням дослідження MONALEESA‑7 було оцінювання повідомлених пацієнтками результатів (Patient-reported Outcomes, PRO) щодо їх ЯЖ, пов’язаної зі здоров’ям (Health-related Quality of Life, HRQoL).
Матеріали та методи
Повідомлені пацієнтками результати
PRO оцінювали на основі затверджених Європейською організацією з вивчення і лікування онкологічних захворювань (EORTC) анкет ЯЖ (QLQ-C30) з модулем специфічних для РМЗ запитань (QLQ-BR23). Анкету EQ‑5D‑5L використовували для оцінювання показників PRO щодо ЯЖ пацієнток, їх працездатності, симптомів захворювання та побічних ефектів, пов’язаних із лікуванням.
Час до настання погіршення (TTD) ≥10% за шкалою загального стану/ЯЖ та вторинні результати PRO за анкетою EORTC QLQ-C30 були проаналізовані на основі 10-бального порога, який вважається еталоном клінічної значущості [6, 7]. Погіршення стану на 10% трактувалося як зниження показника ЯЖ ≥10% порівняно з початковим за умови відсутності подальшого покращення ЯЖ вище цього порога протягом усього періоду лікування або смерті внаслідок будь-якої з причин.
Результати
Розподіл учасників
Як повідомлялося раніше, на момент закінчення збору даних 30 листопада 2018 р. 116 (34,6%) пацієнток групи рибоциклібу та 57 (16,9%) хворих групи плацебо продовжили лікування [5]. На час закінчення збору даних 219 (65,4%) пацієнток, які приймали рибоцикліб, та 280 (83,1%) хворих, яким призначали плацебо, припинили терапію. Головною причиною припинення лікування стало прогресування захворювання, яке спостерігалося у 51,6% учасників групи рибоциклібу та у 68,2% групи плацебо відповідно.
ЯЖ
ЯЖ оцінювали на початку дослідження та протягом усього лікування. 90 та 83% хворих груп рибоциклібу та плацебо відповідно заповнювали анкету EORTC QLQ-C30 на початку дослідження та через ≥1 період від його початку. Медіана TTD ≥10% HRQoL значно зменшилася при застосуванні рибоциклібу порівняно з плацебо (35,8 проти 23,3 міс відповідно; ВР 0,67; 95% ДІ 0,52-0,86; рис.).
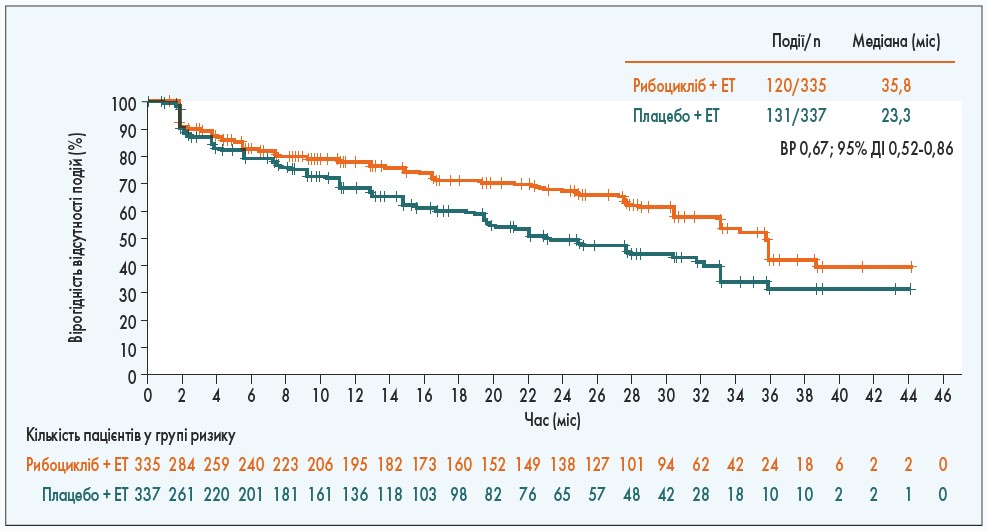 Рис. Час до настання погіршення ≥10% загальної HRQoL у пацієнток, які отримували рибоцикліб, порівняно з плацебо
Рис. Час до настання погіршення ≥10% загальної HRQoL у пацієнток, які отримували рибоцикліб, порівняно з плацебо
Зіставні результати були отримані при визначенні TTD ≥5% (медіана у групі рибоциклібу складала 35,8 міс проти 23,3 у групі плацебо; ВР 0,65; 95% ДІ 0,51-0,84) та TTD ≥15% (медіана становила 38,7 та 33,1 міс у групі рибоциклібу та плацебо відповідно; ВР 0,69; 95% ДІ 0,52-0,92). У пацієнток, які отримували рибоцикліб і в яких не відмічалося прогресування захворювання, спостерігалося відстрочення TTD ≥10% HRQoL порівняно з учасниками, в яких захворювання прогресувало (медіана не досягнута – НД – проти 24,0 міс відповідно; ВР 0,31; 95% ДІ 0,21-0,48).
Загальний стан здоров’я оцінювали як зміну від початкового рівня у лінійній моделі зі змішаними ефектами, в якій враховували дані лікування, фактори стратифікації та початкові показники стану здоров’я. Початкові показники загального стану здоров’я складали 64,7 у групі рибоциклібу та 65,1 у групі плацебо та були порівнянними зі значенням, характерним для великої загальної (неспецифічної для раку) популяції жінок віком 40‑49 років у Північній Америці та Європі, в якій даний показник становив 62,9 [8]. Після 25 циклів, що відповідає середній тривалості лікування 2 роки в групі рибоциклібу [5], зміна середнього бала від початкового рівня в групі рибоциклібу (n=164) та в групі плацебо (n=92) становила +3,9 і +2,2 бала відповідно. Наприкінці лікування зміна середнього бала від початкового рівня в групі рибоциклібу (n=182) та у групі плацебо (n=236) дорівнювала -4,0 та -3,2 бала відповідно.
Лікування рибоциклібом при порівнянні з плацебо також супроводжувалося тривалішим покращенням ключових субдоменів опитувальника EORTC QLQ-C30, включаючи біль і втому. У групі рибоциклібу медіана TTD ≥10% больового синдрому не була досягнута порівняно з групою плацебо (ВР 0,65; 95% ДІ 0,45-0,92). Результати оцінювання TTD ≥10% втоми не були настільки значущими, як загальної ЯЖ чи болю (ВР 0,76; 95% ДІ 0,56-1,02). Порівнянні дані щодо переваг лікування рибоциклібом з результатами оцінювання загального стану здоров’я були отримані при оцінюванні TTD ≥10% фізичного, емоційного та соціального показників.
Рибоцикліб схвалений до застосування у комбінації з НІА у пацієнток у пременопаузі, тому було проведено аналіз загального стану здоров’я та субдоменів EORTC QLQ-C30 опитувальника у когорті пацієнток, які приймали НІА (група рибоциклібу, n=248; плацебо, n=247). Результати в когорті НІА були загалом порівнянними з тими, що спостерігалися в загальній популяції пацієнток. Медіана TTD ≥10% загального стану здоров’я становила 34,2 міс у групі рибоциклібу та 23,3 міс у групі плацебо (ВР 0,69; 95% ДІ 0,52-0,91). У ключовому субдомені болю середня TTD ≥10% не була досягнута у жодній з груп, проте ВР було вищим у групі рибоциклібу (ВР 0,64; 95% ДІ 0,43-0,96). Крім того, відмічалася дещо більша медіана TTD ≥10% у групі рибоциклібу порівняно з плацебо (ВР 0,78; 95% ДІ 0,56-1,10).
Обговорення
Таким чином, у дослідженні MONALEESA‑7 було продемонстровано статистично значущі переваги щодо ВБП і ЗВ та керований профіль безпеки при застосуванні рибоциклібу у поєднанні з ЕТ порівняно з призначенням плацебо та ЕТ [4, 5]. Іншим ключовим аспектом клінічної користі комбінації рибоциклібу з ЕТ, продемонстрованої у клінічному дослідженні, є HRQoL, що особливо актуально для жінок у пременопаузі, оскільки молоді пацієнтки можуть зіткнутися з істотним неспокоєм щодо впливу РМЗ на їх здатність піклуватися про сім’ю та кар’єру [9]. У цьому дослідженні HRQoL зберігалася протягом усього лікування, а TTD загального стану здоров’я, ключових субдоменів болю та втоми був відстрочений при застосуванні рибоциклібу порівняно з плацебо. Схожі результати було отримано при застосуванні рибоциклібу порівняно з плацебо у когорті пацієнток, які приймали НІА.
У MONALEESA‑7 подовження ВБП у групі рибоциклібу супроводжувалося покращенням загального стану порівняно з плацебо. Тобто у пацієнток, які отримували рибоцикліб, відмічався вищий рівень ЯЖ та довший період без прогресування захворювання, що, ймовірно, є ключовими факторами, які сприяють збільшенню тривалості TTD ≥10% загального стану здоров’я у групі рибоциклібу.
Оцінка клінічної ефективності лікарського засобу базується на даних про ефективність, безпеку та HRQoL. Переваги щодо ВБП у групі рибоциклібу відмічалися у всіх трьох дослідженнях MONALEESA [4, 10-12]. У дослідженнях MONALEESA‑3 та MONALEESA‑7 у пацієнток, які приймали рибоцикліб, також було продемонстровано статистично значущі переваги щодо ЗВ [5, 13]. Профіль безпеки рибоциклібу чітко визначений і добре піддається контролю. Відповідно до підтримання рівня ЯЖ у групі рибоциклібу у дослідженні MONALEESA‑7 окремі аналізи PRO показали, що рівень ЯЖ також залишався стабільним протягом усього лікування при додаванні рибоциклібу до летрозолу у дослідженні MONALEESA‑2 та при поєднанні рибоциклібу з фулвестрантом у дослідженні MONALEESA‑3 [14, 15].
Слід зазначити, що переваги додавання інгібіторів CDK4/6 до ЕТ у плані HRQoL були менш значущими в інших дослідженнях III фази, хоча порівняння у перехресних дослідженнях слід проводити з обережністю. У дослідженні MONARCH‑3 було показано, що додавання абемациклібу до НІА не призвело до статистично та клінічно значущих відмінностей у загальному стані здоров’я, про яке повідомляли пацієнтки. Однак слід враховувати той факт, що результати TTD в балах EORTC на момент написання цієї статті не були повідомлені [17]. У дослідженні PALOMA‑2 оцінювання ЯЖ для палбоциклібу та летрозолу не проводилося за шкалою глобального стану здоров’я QLQ-EORTC C30, однак результати аналізу TTD за шкалою функціональної оцінки протипухлинної терапії РМЗ (FACT-B) були зіставними у групах палбоциклібу та плацебо (ВР 0,88; 95% ДІ 0,67-1,16) [18]. Результати досліджень MONARCH‑3 і PALOMA‑2 особливо актуальні, у них також вивчали ефективність поєднання інгібітору CDK4/6 з НІА у першій лінії терапії, хоча переважно у пацієнток у постменопаузі.
Таким чином, враховуючи значну клінічну користь в аспекті ВБП і ЗВ, що спостерігається в дослідженні MONALEESA‑7, варто відзначити, що рибоцикліб у поєднанні з ЕТ покращує ЯЖ у цій популяції пацієнток. Це підтверджує загальні клінічні переваги комбінованої терапії на основі інгібіторів CDK4/6 у лікуванні пацієнток у пре- та перименопаузі з HR+/HER2- РМЗ.
Стаття друкується у скороченні.
Список літератури знаходиться в редакції.
Harbeck N. et al. Health-related quality of life in premenopausal women with hormonereceptor-positive, HER2-negative advanced breast cancer treated with ribociclib plus endocrine therapy: results from a phase III randomized clinical trial (MONALEESA‑7). Ther Adv Med Oncol. 2020; 12: 1-8. DOI: 10.1177/1758835920943065.
Переклала з англ. Ірина Неміш
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (71) 2021 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




