ACROSTUDY: понад 10 років досвіду використання пегвісоманту в лікуванні акромегалії
Акромегалія (АМ) – рідкісне захворювання ендокринної системи – виникає в людини внаслідок вироблення гіпофізом у дорослому віці надлишкової кількості гормону росту (ГР) і найчастіше зумовлена аденомою гіпофіза, що секретує цей гормон [1]. Циркулюючий ГР стимулює продукцію інсуліноподібного фактора росту‑1 (IФР‑1), який так само стимулює ріст хрящів, м’яких тканин, органів, що призводить до їх збільшення і деформації [1, 2]. Результатом прямого впливу ГР є розвиток інсулінорезистентності [3]. За відсутності належного лікування АМ може призвести до серйозних супутніх захворювань і становити загрозу життю. Причинами підвищеної смертності при АМ часто є супутні серцево-судинні, метаболічні і респіраторні захворюваннями [2, 4].
Ключові слова: акромегалія, гормон росту, інсуліноподібний фактор росту‑1, ACROSTUDY, пегвісомант, трансфеноїдальне втручання, аденома гіпофіза, безпека, ефективність, реальна клінічна практика.
Мультидисциплінарний підхід до лікування АМ складається з оперативної, променевої та медикаментозної терапії [5, 6]. Трансфеноїдальне втручання дає можливість швидко знизити рівень ГР і рекомендується як первинне лікування, коли можна повністю або частково видалити пухлину [1]. Променева терапія, яка характеризується повільною відповіддю на лікування і високим ризиком розвитку гіпопітуїтаризму [4], показана пацієнтам із залишковою післяопераційною пухлинною масою за неефективності медикаментозного лікування [1, 7]. Є також медикаментозне лікування: ліганди рецепторів соматостатину (ЛРС), агоністи дофаміну (АД) і антагоніст рецептора ГР – пегвісомант (PEGV). Зазвичай для пригнічення секреції ГР, рівня ІФР-1 в пацієнтів з АМ використовують такі ЛРС, як октреотид тривалої дії і ланреотид [8, 9]. Пасиреотид – це новіший ЛРС, він може забезпечити біохімічний контроль у тих пацієнтів, які не реагують на лікування октреотидом або ланреотидом [10]. АД, зокрема каберголін, характеризуються обмеженою ефективністю, тому їх часто використовують як засоби допоміжної терапії [1, 11].
PEGV – це рекомбінантний білок, який за структурою нагадує людський ГР дикого типу і його рекомбінантні варіанти [12]. Він зв’язується з рецептором ГР людини з вищою спорідненістю, ніж нативний ГР, і блокує передачу сигналу, зменшуючи таким чином концентрацію циркулюючого ІФР‑1. Завдяки пегілюванню препарату збільшується період його напіввиведення. PEGV, який вводять підшкірно, в основному використовують у вигляді монотерапії, але його також можна поєднувати з ЛСР або АД. Основним біохімічним маркером для моніторингу ефективності PEGV є рівень IФР‑1 у сироватці крові [4, 13].
Початкові базові дослідження показали, що PEGV зазвичай добре переносили пацієнти з АМ, якщо термін їх лікування не перевищував 18 міс; нормалізації рівня ІФР‑1 у сироватці крові вдалося досягти в 97% пацієнтів, які отримували PEGV ≥12 міс [14, 15]. PEGV був затверджений в Європі у 2002 р. [16], у США – у 2003 р. [17] для лікування хворих на АМ, яку неможливо адекватно контролювати за допомогою оперативного втручання, і/або променевої терапії, і/або прийому ліків. Пізніше препарат було схвалено у США для первинного медикаментозного лікування, якщо не вдалося досягти контролю захворювання після операції і/або променевої терапії або коли ці методи лікування визнані недоцільними [17].
Глобальне багатоцентрове неінтервенційне дослідження ACROSTUDY було розпочато 2004 року як постреєстраційне дослідження безпеки (ПРДБ) після запиту Європейського агентства з лікарських засобів (EMA) з метою оцінки довгострокової безпеки й ефективності PEGV. Попередні звіти показали позитивні результати щодо безпеки при моно- і комбінованій терапії [18-26]. У звіті представлені кінцеві результати стосовно безпеки й ефективності PEGV усієї когорти з 2221 пацієнта, за даними спостереження тривалістю до 14 років.
Методи
Дизайн дослідження
Пацієнтів залучали в дослідження ACROSTUDY безперервно; мінімальний термін спостереження становив 5 років. Вимога ПРДБ щодо оцінки безпеки 5-річного лікування PEGV принаймні серед 1 тис пацієнтів з АМ була виконана у 2013 р. [19, 20]. Дослідження було добровільно продовжено заявником для оцінки показників безпеки (передусім зміни рівня глюкози) та якості життя, що дало можливість приблизно 400 пацієнтам, уже залученим для участі в ACROSTUDY, продовжити лікування за допомогою PEGV. Додатково було залучено 100 нових пацієнтів з АМ, які раніше не отримували лікування або були напівнаївними (тобто не отримували PEGV протягом 6 міс до включення в дослідження). Випробування проводили в 15 країнах, де PEGV був зареєстрований для лікування АМ. Дозу і режим застосування препарату визначали дослідники, які проводили лікування. Стан пацієнтів оцінювали під час звичайних консультацій і контрольних оглядів, які проводили до грудня 2017 року, коли ACROSTUDY завершилось.
Пацієнти
Звіт спрямовано на аналіз даних загальної популяції, представленої всіма пацієнтами, які були залучені до ACROSTUDY з 2004 по грудень 2017 року і отримали принаймні 1 дозу PEGV. Також були включені пацієнти з АМ, які отримували або тільки починали отримувати лікування PEGV перед залученням в ACROSTUDY. Деякі європейські дослідницькі центри змогли залучити для участі в дослідженні педіатричних пацієнтів (<18 років). Усім учасникам дослідження було рекомендовано провести візуалізацію гіпофіза впродовж 6 міс до включення в дослідження. Під час добровільного продовження участі в ACROSTUDY мали право залучати лише дорослих пацієнтів (≥18 років). Критеріями виключення були участь у будь-якому іншому клінічному дослідженні АМ протягом останніх 6 міс, потреба в оперативній декомпресії пухлини або немедикаментозній терапії через звуження полів зору, параліч черепно-мозкових нервів або внутрішньочерепна гіпертензія чи алергія до PEGV або його складових. Вагітні й жінки, які годували груддю, участі в дослідженні також не брали.
Безпека
Перед початком лікування PEGV визначали вихідні показники. Дані щодо безпеки охоплювали частоту небажаних реакцій (НР), результати печінкових тестів і дані візуалізації пухлини гіпофіза. Проводили оцінку всіх зареєстрованих НР, серйозних НР (СНР), НР, які становили особливий інтерес (наприклад, реакції в місці введення препарату, гепатобіліарні НР та зміни розміру пухлини) і випадків смерті. Усі НР кодували за допомогою Медичного словника термінології регуляторної діяльності (версія MedDRA 20.1). Дані стосовно супутнього лікування і супутніх захворювань збирали в лікуючих лікарів за допомогою стандартизованого опитувальника. Як НР реєстрували будь-які розлади, що виникли після включення в дослідження.
Первинними кінцевими точками щодо безпеки, пов’язаними з печінковими тестами, були відсоток пацієнтів із рівнем трансаміназ (АЛТ і АСТ), що в ≥3 рази перевищував верхню межу норми (ВМН), і відсоток пацієнтів із підвищенням будь-яких показників печінкових тестів (лужна фосфатаза, білірубін, гамма-глутамілтрансфераза).
Візуалізацію пухлини гіпофіза та її оцінку проводили перед початком прийому PEGV, через 6 і 12 міс після початку лікування, а потім щороку. Достовірна зміна розміру пухлини визначалася як зміна найбільшого діаметра мікроаденоми гіпофіза >3 мм або як зміна обсягу макроаденоми >20% (>10 мм).
Ефективність
У місцевих і центральних лабораторіях вимірювали сироваткові рівні IФР‑1, який є одним з основних лабораторних маркерів ефективності лікування АМ за допомогою PEGV. Для оцінки ефективності аналізували розподіл пацієнтів за рівнем IФР‑1 (<нижньої межі норми (НМН), норма, >ВМН відповідно до референтних лабораторних значень) і відсоток пацієнтів, які досягли нормального рівня ІФР‑1, що залишався стабільним.
Статус «із контрольованим рівнем ІФР‑1» був присвоєний тим учасникам випробування, у кого вміст ІФР‑1 залишався в діапазоні референтних значень із моменту останнього вимірювання. Статус «із неконтрольованим рівнем ІФР‑1» отримали ті, у кого вміст ІФР‑1 був >ВМН або <НМН. Рівні глюкози в крові натще і рівень глікованого гемоглобіну (HbA1c) визначали під час звичайної консультації, а відсотки пацієнтів зі значеннями, що виходили за межі норми, узагальнювали.
Результати
Демографічні дані
Загалом до участі в дослідження ACROSTUDY і вибірки для аналізу був залучений 2221 пацієнт із 14 країн Європи, а також зі США. Із них 434 пацієнти були переведені з первинного дослідження і 110 пацієнтів, які раніше не отримували лікування або були напівнаївними, були залучені під час добровільного продовження ПРДБ. Більшість пацієнтів були європеоїдної раси (92,4%); співвідношення чоловіків і жінок було практично однаковим. Середній вік пацієнтів на момент встановлення діагнозу АМ становив 41,1 року, на момент початку лікування PEGV – 49,7 року, на момент залучення в дослідження – 51,5 року. Максимальна тривалість лікування PEGV становила 20,8 року (із медіаною 9,3 року). Спостереження в дослідженні ACROSTUDY тривало до 13,9 року (медіана 7,4 року). Усього в дослідженні взяли участь 11 (0,5%) педіатричних пацієнтів; 5 – віком від 2 до 11 років, 6 – віком від 12 до 18 років.
До початку терапії PEGV більшість пацієнтів (87,2%) мали хоча б одне супутнє захворювання (табл.). Найпоширенішими з них були АГ (51,3%), ЦД (32,2%), остеоартрит (21,3%) та апное уві сні (20,8%). Між початком прийому PEGV і залученням в ACROSTUDY 30,1% із 1586 пацієнтів повідомили про нові супутні захворювання, причому найчастіше це були АГ (12,3%), остеоартроз (10,7%) і ЦД (10,5%). На початку дослідження в 38,8% пацієнтів були зареєстровані неоплазії (доброякісні або злоякісні), найчастіше – у щитоподібній залозі (17,6%) і товстому кишечнику (14,8%).
Лікування АМ
До початку лікування PEGV майже половина (48,1%) пацієнтів отримували як медикаментозне, так і оперативне лікування; 21,6% пацієнтів – хірургічне, променеве і медикаментозне; 18,8% – лише медикаментозна терапія. До початку терапії PEGV 65,7% пацієнтів отримували лише ЛРС, 31,2% – ЛРС у поєднанні з АД, а 3,0% використовували лише АД. На початку PEGV найчастіше призначали у вигляді монотерапії (55,1%) і в поєднанні з ЛРС (34,3%). Згодом схема лікування дещо змінювалася: частота монотерапії PEGV зросла із 47,0% до 55,1%, тоді як використання PEGV/ЛРС з роками зменшилося з 34,3 до 24,4%. Більшість пацієнтів (80,8%) розпочинали лікування з щоденного застосування PEGV, при цьому найпоширенішою була доза 10-15 мг (67,0%). Деякі пацієнти отримували дозу PEGV <10 мг 2-6 разів на тиждень (7,7%) або раз на тиждень (7,1%). Найпоширеніші дози PEGV протягом 1-го року: 10-15 мг (31,1%), 15-20 мг (20,4%) і 20-25 мг (18,5%). Загалом дози PEGV у подальшому збільшувалися. Кількість пацієнтів, які щодня використовували ≥30 мг PEGV, зросла із 7,1% на 1-му до 22,4% на 14-му році дослідження.
Безпека
Побічні явища
Серед 2221 учасника ACROSTUDY в 1255 (56,5%) було зареєстровано 5567 НР. Найчастішими були підвищення рівня ІФР‑1 (10,4%), головний біль (5,1%), дефіцит вітаміну D (4,9%), артралгія (4,6%), остеоартрит (3,6%), депресія (2,6%), ЦД (2,3%), ЖКХ (2,3%) і поліп товстої кишки (2,2%). Лише 613 НР (були зареєстровані в 16,5% пацієнтів) вважалися пов’язаними з лікуванням. Найпоширенішими пов’язаними з лікуванням НР (≥1%) були підвищення рівня ІФР‑1 (1,9%), підвищення рівня трансаміназ (1,5%), ліпогіпертрофія (1,2%) та зниження рівня ІФР‑1 (1,1%).
СНР були зареєстровані в 523 (23,5%) пацієнтів, вважалися пов’язаними з лікуванням – у 53 (2,4%). Найчастіше повідомлялося про такі пов’язані з лікуванням СНР: рецидиви (0,4%; n=8) або доброякісні (0,3%; n=6) пухлини гіпофіза, підвищення показників печінкових проб (0,6%; n=14) і гепатобіліарні порушення (0,3%; n=6). Лікарський засіб відміняли (тимчасово, остаточно або відстрочено) через НР 256 (11,5%) пацієнтам, а через СНР – 167 (7,5%). З усіх випадків припинення лікування лише незначна частина була зумовлена пов’язаними з лікуванням НР (1,3%) або СНР (1,3%).
НР, які становлять особливий інтерес і пов’язані з симптомами в місці введення препарату, були зареєстровані в 3,5% пацієнтів, більшість із них була спричинена застосуванням PEGV (3,2%). Найпоширенішими пов’язаними з лікуванням НР були ліпогіпертрофія в 1,2% (n=27) пацієнтів і реакції в місці ін’єкції в 0,8% (n=18). НР в місці введення призвели до відміни (або зменшення дози) PEGV в 1,1% пацієнтів, причому причиною 13 випадків відмін стала ліподистрофія/ліпогіпертрофія.
Загалом було зареєстровано 87 смертей, жодна з яких не була пов’язана з лікуванням. Поширеними причинами смерті були серцева недостатність (n=6), цереброваскулярнї події (n=3), інфаркт міокарда (n=3), дихальна недостатність (n=3) і зупинка серця / раптова серцева смерть (n=4).
Результати візуалізації пухлини гіпофіза
Відсоток пацієнтів, яким проводили магнітно-резонансну томографію (МРТ) гіпофіза, становив 40,3% на 1-му і 45,2% на 2-му році і згодом зменшився до 31,0% на 5-му і до 4,4% на 15-му році дослідження. Усього 1795 пацієнтів після початку терапії PEGV мали ≥1 результат візуалізації гіпофіза, із них у 1276 (71,1%) не спостерігали змін розмірів пухлини гіпофіза за даними локального аналізу результатів МРТ. Зміни розмірів пухлини гіпофіза проти вихідних або результатів візуалізації, отриманих під час останнього обстеження, були виявлені принаймні один раз під час локальної оцінки в 519 пацієнтів, у тому числі у 128 (7,1%) – лише збільшення, у 310 (17,3%) – лише зменшення та у 81 (4,5%) – збільшення і зменшення (у різні моменти часу). Відповідно до протоколу дослідників попросили надсилати МРТ для центрального аналізу, якщо місцеві рентгенологи визначали виражені зміни (не потребували на етапі добровільного продовження дослідження). У 264 із 519 пацієнтів результати МРТ повторно оцінювали за допомогою центральної оцінки, яка виявила збільшення обсягу пухлини в 54 (3,0%) пацієнтів, зменшення – у 84 (4,7%), як збільшення, так і зменшення – у 12 (0,7%), відсутність змін – у 74 (4,1%), недостатні дані – у 40 (2,2%). Зміни розмірів пухлини гіпофіза були зареєстровані як НР, що становлять особливий інтерес, у 4,3% пацієнтів, і стали причиною відміни лікування PEGV в 1,4% пацієнтів.
Печінкові тести
Загалом в рамках дослідження з 2221 пацієнта у 71 (3,2%) під час лікування PEGV у будь-якій точці дослідження рівні АЛТ/АСТ більш як утричі перевищували ВМН, а з 1327 пацієнтів із нормальними вихідними рівнями АЛТ/АСТ у 42 осіб, що також становило 3,2%, під час лікування показники теж більш як утричі перевищували ВМН. Підвищення рівня АЛТ/АСТ/трансаміназ, що призвело до припинення лікування PEGV (або зниження дози), спостерігали 19 разів. Загалом у 10,1% пацієнтів повідомляли про гепатобіліарні НР, що стало причиною відміни PEGV в 1,7% пацієнтів.
У дослідженні не повідомлялося про випадки розвитку печінкової недостатності.
Ефективність
Нормалізація рівня IФР‑1
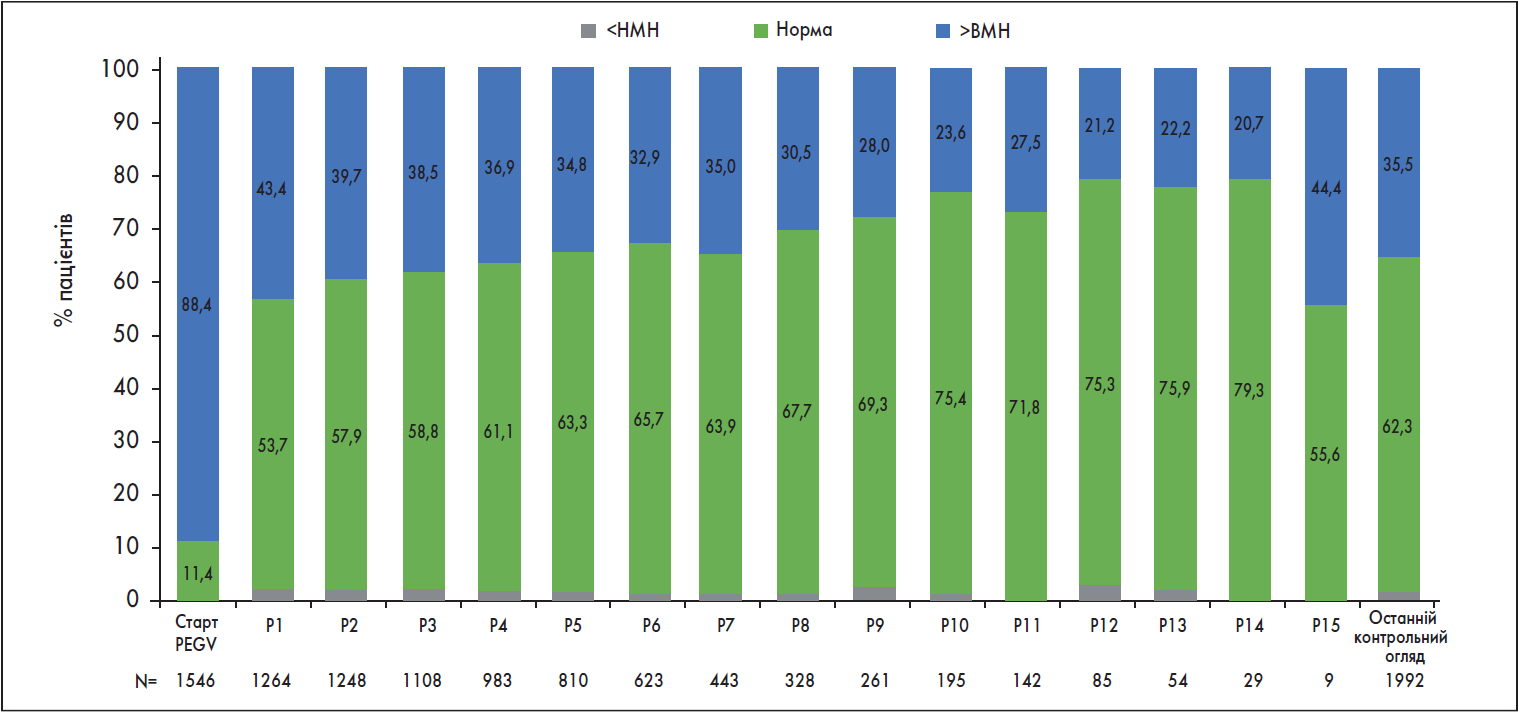
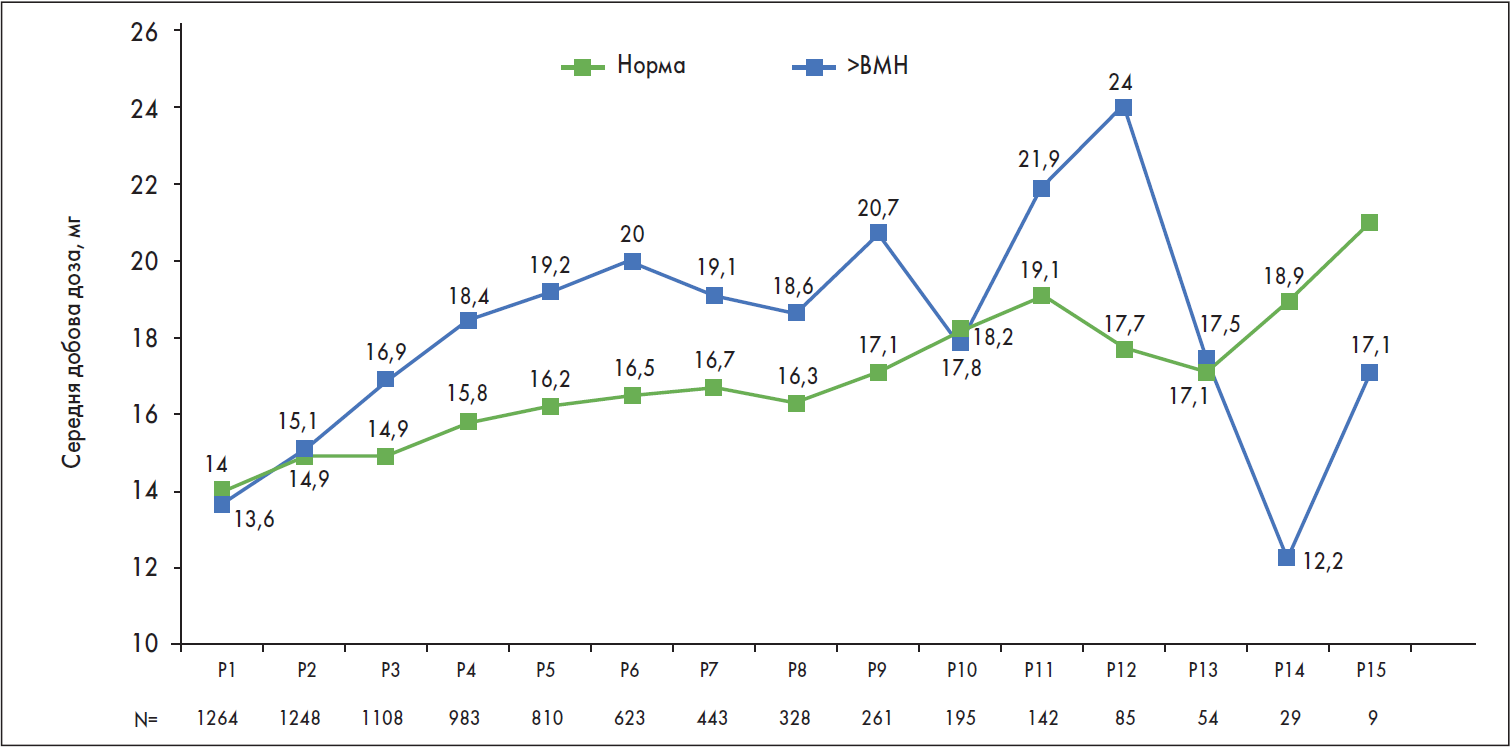
На початку терапії PEGV в 11,4% пацієнтів (n=1546) концентрація ІФР‑1 перебувала в межах референтного діапазону, тоді як у 88,4% рівень ІФР‑1 перевищував ВМН. Відсоток пацієнтів із нормальним рівнем IФР‑1 збільшився з 53,7% після першого року лікування до 63,3% на 5-му році і залишався >60% (63,3-79,3%) протягом більшої частини дослідження (рис. 1). Загалом у 62,3% пацієнтів вдалося досягти нормалізації рівня IФР‑1 на момент останнього контрольного огляду. Нормалізація рівня IФР‑1 супроводжувалася збільшенням дози PEGV; таким чином, середні добові дози PEGV у пацієнтів, в яких відбулася нормалізація рівня IФР‑1, зросли з 14,0 мг на 1-му до 18,2 мг на 10-му році дослідження (рис. 2). Дози PEGV у пацієнтів з активною АМ також згодом зростали і були більшими проти таких у пацієнтів, які досягли контролю, упродовж більшості років.
Рис. 1. Рівень ІФР‑1 у пацієнтів, залучених у дослідження ACROSTUDY
Рис. 2. Кореляція рівня ІФР‑1 із дозою PEGV у пацієнтів, залучених у дослідження ACROSTUDY
Обговорення
Загалом результати дослідження ACROSTUDY показали, що PEGV у разі середньої тривалості використання 9,3 року переноситься пацієнтами добре.
Основний висновок наведеного дослідження: PEGV має сприятливий профіль безпеки в умовах реальної клінічної практики, особливо стосовно розмірів пухлини гіпофіза і результатів печінкових проб.
Також варто зазначити, що фармакокінетичні і фармакодинамічні властивості PEGV не суттєво відрізняються в мешканців Заходу й Азійського регіону, тому очікується відсутність впливу походження на безпеку й ефективність PEGV [27-30].
В інструкції для медичного застосування PEGV [17] і настановах Міжнародного товариства ендокринологів під час лікування PEGV рекомендується контролювати розмір пухлини і функціональні печінкові проби [1]. У загальній когорті центральна оцінка результатів МРТ виявила збільшення розмірів пухлини на 3,7% (окремо або в поєднанні зі зменшенням). Схожі результати були отримані в Німецькому обсерваційному дослідженні PEGV (3,1%) [31] та інших звітах ACROSTUDY (2,2-3,2%) [19, 22, 25]. Така низька частота свідчить про те, що PEGV не сприяє збільшенню розмірів пухлини. Виявлені випадки можуть бути наслідком рецидиву/збільшення пухлини внаслідок відміни ЛРС або просто відображати природний агресивний перебіг захворювання [32, 33].
Виявлена низька частота підвищення рівня ферментів печінки під час лікування PEGV, яка не відрізняється від попередніх повідомлень [18-20, 22, 26]. Лише в 3,2% пацієнтів із нормальними вихідними рівнями АЛТ/АСТ під час спостереження в будь-який момент часу виявляли рівень
АЛТ/АСТ, що більш ніж утричі перевищував ВМН. Крім того, вважалося, що більшість НР із боку гепатобіліарної системи були зумовлені іншими причинами. Лише 1,7% пацієнтів припинили використання PEGV через гепатобіліарні НР.
Терапія PEGV може призвести до ліподистрофії та деформації жирової тканини в місці ін’єкції [37, 38]. Більшість НР у місці введення (повідомляється про 2,0% пацієнтів) в ACROSTUDY вважали пов’язаними із застосуванням PEGV.
Оскільки ліподистрофія може бути пов’язана зі зменшенням чутливості до PEGV (втратою біохімічного контролю в пацієнтів із раніше контрольованим захворюванням) [38], місця ін’єкції треба перевіряти на предмет ліподистрофії і час від часу змінювати місця введення [25].
Було помічено, що нормалізація рівня ІФР‑1 на тлі лікування PEGV згодом була досягнута у більш ніж половини (53,7%) пацієнтів протягом 1-го року з максимальною нормалізацією на рівні 79,3% в подальшому.
Майже у двох третин пацієнтів із відомим вихідним рівнем ІФР‑1 (62,3%) під час останнього спостереження зазначали нормалізацію його рівня, що узгоджується з попередніми результатами на рівні 63-73% у двох проміжних звітах ACROSTUDY, опублікованих у 2012 [19] і 2018 роках [20].
Хоча ступінь нормалізації IФР-1 тут був нижчим за такий у базових клінічних випробуваннях, на основі яких була здійснена реєстрація PEGV [14, 15], висновки авторів наведеного дослідження узгоджуються з такими реальної клінічної практики, у тому числі німецьким обсерваційним дослідженням PEGV, ретроспективними бразильським і аргентинським, японським постмаркетинговим обсерваційним дослідженнями [28-31]. Будь-яку невідповідність можна пояснити відсутністю потрібного титрування дози, неадекватним дотриманням рекомендацій пацієнтами і різними способами визначення рівня IФР‑1 або відсутністю критеріїв титрування/нормалізації ІФР-1, що використовують в умовах реальної клінічної практики, якщо порівняти з клінічними випробуваннями, де дотримуються жорсткішіх критеріїв [18, 20, 31].
Результати ACROSTUDY також узгоджуються із систематичним оглядом і метааналізом 45 досліджень ефективності PEGV, у рамках якого було продемонстровано загальний контроль над захворюванням у 60,9% (95% ДІ 51,8-69,3) пацієнтів, які отримували комбіновану терапію, а в пацієнтів на монотерапії PEGV контроль над захворюванням був кращій і становив 71,7% (95% ДІ 64,0-78,4) [40].
Ефективність PEGV може залежати від індивідуальних особливостей пацієнта. Оглядове ретроспективне дослідження показало, що резистентність до PEGV пов’язана з вищим індексом маси тіла (ІМТ) і частіше спостерігається за ІМТ >30 кг/м2 [45]. Нижчі вихідні рівні ГР, рівню ІФР‑1 і IФР‑1 x ВМН асоціювалися з частішим контролем захворювання, що частіше спостерігали, якщо вихідний рівень ІФР‑1 перевищував ВМН менш ніж у 2,7 раза [45].
Тому пацієнтам з ожирінням і рівнем IФР‑1, який перевищує ВМН більш ніж у 2,7 раза, можуть знадобитися вищі початкові дози PEGV і швидше титрування [45]. Нещодавні рекомендації Товариства з дослідження гіпофіза свідчать, що пацієнти з ЦД і вищим ІМТ потребують вищих доз PEGV і швидшого титрування для нормалізації рівня IФР‑1 [46].
У пацієнтів з АМ, якщо їх належним чином не лікувати, спостерігається значущий розвиток коморбідних станів, прогресування супутніх захворювань і підвищена смертність [2]. У цьому дослідженні оцінювали ускладнення, асоційовані з АМ, у великій когорті пацієнтів в умовах реальної клінічної практики.
Понад 90% пацієнтів на момент початку дослідження мали більш ніж одну супутню патологію, причому найчастішими були гіпертонія, АГ, ЦД і остеоартрит.
Повідомлялось, що в багатьох пацієнтів були виявлені пухлини товстої кишки і щитоподібної залози, а це підкреслює необхідність скринінгу цих станів.
Висновки
Довгострокове глобальне неінтервенційне дослідження ACROSTUDY стало найбільшим і найтривалішим випробуванням із вивчення безпеки й ефективності PEGV у пацієнтів з АМ. Цей фінальний огляд загальної когорти учасників дослідження підтверджує, що PEGV покращує контроль захворювання. Обнадійливими можна вважати результати безпеки застосування препарату, які демонструють низьку частоту прогресування пухлин. Загалом PEGV у цьому дослідженні продемонстрував сприятливе співвідношення користь-ризик для лікування АМ як у вигляді моно-, так і в складі комбінованої терапії. Отримані результати аналогічні дослідженням, проведеним у Японії, Аргентині й Бразилії.
За матеріалами M. Fleseriu et al. More than a decade of real-world experience of pegvisomant for acromegaly: ACROSTUDY.
European Society of Endocrinology.
Список літератури – у редакції.
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 3 (55) 2021 р.
СТАТТІ ЗА ТЕМОЮ Ендокринологія
21 березня в рамках II Міжнародної школи «Сучасний лікар: від теорії до практики» професор кафедри ендокринології Львівського національного медичного університету ім. Данила Галицького, лікар-ендокринолог вищої категорії, доктор медичних наук Вікторія Олександрівна Сергієнко представила доповідь, присвячену хронічним ускладненням цукрового діабету (ЦД). Зокрема, було акцентовано увагу на причинах розвитку діабетичної полінейропатії (ДП), розглянуто клінічні варіанти цього ускладнення, діагностичні підходи та основні принципи лікування. Пропонуємо огляд цієї доповіді у форматі «запитання – відповідь»....
Останніми десятиліттями в усьому світі спостерігалося значне зростання поширеності цукрового діабету (ЦД), що зумовило серйозні наслідки стосовно якості життя населення, а також спричинило певний тягар для системи охорони здоров’я та економічні витрати [1]. За даними Діабетичного атласу Міжнародної діабетичної федерації (International Diabetes Federation Diabetes Atlas), у 2021 р. ≈537 млн людей мали ЦД і, за прогнозами, до 2045 р. цей показник досягне 783 млн [2]. Значна захворюваність і підвищена смертність асоційовані з пов’язаними із ЦД макросудинними (інфаркт міокарда, інсульт) і мікросудинними (сліпота, ниркова недостатність, ампутації) ускладненнями [3]....
За визначенням Всесвітньої організації охорони здоров’я, цукровий діабет (ЦД) – це група метаболічних розладів, що характеризуються гіперглікемією, яка є наслідком дефектів секреції інсуліну, дії інсуліну або обох цих чинників. За останні 15 років поширеність діабету зросла в усьому світі (Guariguata et al., 2014). Згідно з даними Diabetes Atlas (IDF), глобальна поширеність діабету серед осіб віком 20-79 років становила 10,5% (536,6 млн у 2021 році; очікується, що вона зросте до 12,2% (783,2 млн у 2045 році (Sun et al., 2022). Наразі триває Програма профілактики діабету (ППД), метою якої є визначити, які підходи до зниження інсулінорезистентності (ІР) можуть допомогти в створенні профілактичних заходів ЦД 2 типу (The Diabetes Prevention Program (DPP), 2002). У цьому світлі визначення впливу вітаміну D на розвиток ЦД є актуальним питанням....
Внутрішній біологічний годинник людини тісно та двоспрямовано пов’язаний зі стресовою системою. Критична втрата гармонійного часового порядку на різних рівнях організації може вплинути на фундаментальні властивості нейроендокринної, імунної та вегетативної систем, що спричиняє порушення біоповедінкових адаптаційних механізмів із підвищеною чутливістю до стресу й уразливості. Поєднання декількох хвороб зумовлює двоспрямованість патофізіологічних змін....