Клініко-фармакологічні аспекти лікування пацієнтів з артеріальною гіпертензією та гіперліпідемією
За матеріалами І Національного конгресу «Серце та судини» (4‑7 листопада 2021 року, м. Одеса)
 Артеріальна гіпертензія (АГ) залишається суттєвою медико-соціальною проблемою в Україні. Ця патологія спричиняє розвиток значних ускладнень та зростання смертності від серцево-судинних захворювань (ССЗ). Найчастіше АГ та гіперліпідемія – два фактори, які «йдуть» пліч-о-пліч і знижують якість життя пацієнта. Проблемі вибору оптимального лікування присвятив свою доповідь завідувач кафедри клінічної фармакології та клінічної фармації Національного медичного університету імені О.О. Богомольця (м. Київ), д. мед. н., професор Микола Валентинович Хайтович.
Артеріальна гіпертензія (АГ) залишається суттєвою медико-соціальною проблемою в Україні. Ця патологія спричиняє розвиток значних ускладнень та зростання смертності від серцево-судинних захворювань (ССЗ). Найчастіше АГ та гіперліпідемія – два фактори, які «йдуть» пліч-о-пліч і знижують якість життя пацієнта. Проблемі вибору оптимального лікування присвятив свою доповідь завідувач кафедри клінічної фармакології та клінічної фармації Національного медичного університету імені О.О. Богомольця (м. Київ), д. мед. н., професор Микола Валентинович Хайтович.
Патогенетичний механізм розвитку та фактори ризику ССЗ
За наявними даними, в Україні 67% летальних випадків спричинені ССЗ (УУН, 2014). Водночас у європейських країнах зі сталим економічним розвитком ситуація у цьому напряму покращується. Так, у трьох країнах східної Європи (Україна, Білорусь, Російська Федерація) ризик смерті від ішемічної хвороби серця серед чоловіків віком 50‑54 роки був вищий, ніж у французів 75‑79 років (Nichols еt al., 2014).
Професор Хайтович звернув увагу слухачів на патогенетичний механізм розвитку судинного ремоделювання, а саме імунологічного запалення як фактора, що спричиняє патологічні зміни у судинах. Серед них слід відзначити порушення прохідності судин, що спричиняє:
- розвиток атеросклерозу;
- прогресування АГ;
- виникнення серцево-судинних (СС) ускладнень.
До модифікованих факторів СС-ризику за шкалою SCORE доцільно віднести соціальну депривацію як першопричину багатьох ССЗ, ожиріння (зокрема центральне) за даними вимірювання індексу маси тіла та окружності талії, гіподинамію, психосоціальний стрес. Також значення мають сімейний анамнез передчасного ССЗ (чоловіки <50 років, жінки <55 років), автоімунні та інші запальні захворювання, основні психічні розлади, лікування ВІЛ-інфекції, фібриляція передсердь, гіпертрофія лівого шлуночка, хронічне захворювання нирок, синдром обструктивного апное сну тощо.
Поєднання підвищеного АТ і гіперліпідемії
Особливу увагу варто приділити поєднанню підвищеного АТ та гіперліпідемічних порушень, а саме збільшенню вмісту ліпопротеїнів низької щільності (ЛПНЩ), гіпертригліцеридемії. Така коморбідність асоційована із вищими ризиками, особливо за умови зростання рівнів так званих малих щільних ЛПНЩ.
Чим же небезпечні малі щільні ЛПНЩ? Вони не зв’язуються з рецепторами печінки, через що не можуть виводитись із кровотоку, за рахунок малих розмірів агресивно проникають до судинної стінки та затримуються в ній, більш схильні до ліпопероксидації, підвищують синтез тромбоксану й активність тромбоцитів, спричиняють розвиток дисфункції ендотелію. Таким чином, зростання рівня малих щільних ЛПНЩ зумовлює не лише атерогенні зміни, але й подальше прогресування АГ.
Підходи до лікування
Сьогодні активно вивчаються мішені антигіпертензивної, протизапальної терапії як нового напряму контролю АГ. Доведено, що агоністичний вплив на рецептори активації проліферації пероксисом (PPARα) знижує активність молекул адгезії та блокує синтез фібрину, що зменшує функцію згортання і покращує реологічні властивості крові, а також фактор росту судин, що зупиняє проліферацію клітин гладеньких м’язів і ріст нових неповноцінних судин. Окрім того, відбуваються зменшення набряку судинної стінки за рахунок блокади ферменту альдозоредуктази та збільшення просвіту судин шляхом усунення вазоспазму. На додаток, агоністичний вплив на PPARα чинить протизапальну дію шляхом зменшення вироблення медіаторів запалення (фактора некрозу пухлин α, інтерлейкінів тощо) (Lefebvre et al., 2006).
Також спікер підкреслив окремі положення настанов Європейського товариства кардіологів та Європейського товариства з гіпертензії (ESC/ЕSH, 2018), що передбачають призначення інгібіторів ангіотензинперетворювального ферменту (іАПФ), блокаторів рецепторів ангіотензину ІІ (БРА) у комбінації з блокаторами кальцієвих каналів (БКК) та тіазидними або тіазидоподібними діуретиками. Дотримання цих рекомендацій обов’язкове для зменшення ускладнень та ураження органів-мішеней.
Серед нефармакологічних втручань важливими є зміни способу життя для підвищення ефективності лікування, такі як (Williams et al., 2018):
- зниження надлишкової ваги;
- збільшення фізичної активності;
- зменшення надходження в організм солі;
- включення у раціон більше овочів та фруктів;
- повноцінний нічний сон;
- відмова від куріння;
- обмеження вживання алкоголю;
- контроль стресу.
Загалом натепер розроблено чіткі алгоритми щодо лікування АГ. Терапія має включати комбінацію двох антигіпертензивних засобів, а якщо контролю АТ не досягнуто – додають третій препарат (Whelton et al., 2017). Однак 72,1% пацієнтів з АГ не вдається досягти цільового рівня АТ через три місяці регулярної подвійної антигіпертензивної терапії гіпотензивними препаратами основних груп (Gradmanet et al., 2013). Це диктує необхідність перегляду антигіпертензивного лікування та пошуку нових підходів.
За словами доповідача, існує етапність призначення гіпотензивних ліків. Якщо на тлі застосування 3‑4 препаратів АТ достатньою мірою не контролюється, необхідно переконатися, що пацієнт ретельно виконує призначення лікаря. Крім того, слід з’ясувати, чи приймає хворий нестероїдні протизапальні препарати (НПЗП), психостимулятори, фітопепарати на основі звіробою, які нівелюють антигіпертензивний ефект гіпотензивних засобів. Якщо ж усі перелічені фактори виключені, є підстави констатувати резистентну АГ та змінити стратегію лікування.
У цьому контексті доцільно звернути увагу на препарат центральної дії моксонідин, що впливає на симпатичну активність, а саме на імідазолінові рецептори, і частково блокує утворення норадреналіну. Моксонідин забезпечує виразний ваготропний ефект та характеризується незначною кількістю побічних явищ за рахунок низької афінності до α2-адренорецепторів.
Дослідження ефективності моксонідину довели, що препарат чинить кардіо- та васкулопротективну дію, сприяє зниженню кетохоламінів у крові, має нефропротекторні властивості. У пацієнтів із метаболічним синдромом препарат продемонстрував найбільшу ефективність завдяки додатковому впливу на метаболічні порушення, а саме зменшення інсулінорезистентності, вмісту лептину в сироватці крові, поліпшення ліпідних параметрів та зниження ваги (Fenton et al., 2006; Sharma et al., 2004).
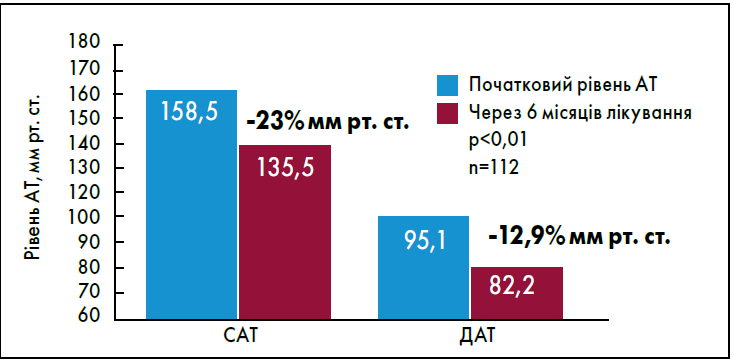
Моксонідин добре поєднується з іншими гіпотензивними засобами, що підвищує якість антигіпертензивної терапії. Так, в обсерваційному проспективному дослідженні Abellan et al. (2005) застосовували оригінальний препарат моксонідину Фізіотенс® у дозі 0,4 мг у комбінації зі стандартними антигіпертензивними ліками протягом шести місяців. Така схема лікування забезпечила зниження систолічного (САТ) і діастолічного АТ (ДАТ) у середньому на 23 і 12,9 мм рт. ст. відповідно (рисунок).
Рисунок. Середнє зниження САТ і ДАТ при застосуванні моксонідину додатково до стандартної антигіпертензивної терапії
Важливі фармакокінетичні особливості препарату Фізіотенс®:
- Біодоступність при пероральному прийманні (90%).
- Швидкий початок дії (Tmax – 1 год).
- Швидко врівноважувана концентрація у крові: Т1/2 – 2,5 год (5 год).
- Відсутній ефект першого проходження через печінку.
- Вживання їжі суттєво не впливає на біодоступність.
Якому ж варіанту слід віддавати перевагу: генерику чи оригінальному препарату? У дослідженні В.В. Руксін та співавт. (2015) порівнювали ефективність препарату Фізіотенс® як оригінального моксонідину із генеричними молекулами при гіпертонічному кризі (АТ – 200/110 мм рт. ст.). Під наглядом перебували 179 пацієнтів, середній вік яких становив 68 років, із тривалим анамнезом АГ (близько 22 років). Було показано, що терапевтичний ефект препарату Фізіотенс® відрізнявся від генериків. Після прийому препарату Фізіотенс® на 25% більше пацієнтів досягали нормального АТ впродовж 30 хв, ніж після застосування генеричних моксонідинів.
Ще одним важливим аспектом є хронічне запалення в судинах, яке часто пов’язують із дисліпідемією. Включення у лікувальну тактику не лише статинів, але й фібратів як додаткової терапії сприяє зниженню СС-ризику, зменшенню загальної смертності на 32% та запобіганню розвитку ішемічної хвороби серця на 34% (Zhu et al., 2020).
В актуальній європейській настанові ведення пацієнтів із гіперхолестеринемією з’явилися рекомендації щодо застосування фібратів у комбінації зі статинами (ESC/EAS, 2019). Так, використання цієї стратегії є доцільним у пацієнтів групи високого ризику із концентрацією тригліцеридів (ТГ) >2,3 ммоль/л (>200 мг/дл) незважаючи на статинотерапію (ІІb, С). Також фенофібрат можна застосовувати в комбінації зі статинами з метою первинної профілактики у пацієнтів із цільовим рівнем холестерину ЛПНЩ і вмістом ТГ >2,3 ммоль/л (>200 мг/дл) (IIb, B).
На додаток, М.В. Хайтович наголосив на необхідності контролю вегетативної регуляції, зокрема зниження надлишкової симпатичної активності. У цьому контексті моксонідин (Фізіотенс®) має низку переваг:
- чинить центральну дію, зменшуючи периферичну симпатичну активність, знижує загальний периферичний судинний опір;
- сприятливу переносимість;
- низький потенціал для медикаментозних взаємодій;
- відрізняється від генериків за фармакодинамікою;
- може застосовуватися як допоміжний засіб при лікуванні АГ і неускладненому гіпертензивному кризі;
- покращує метаболічний профіль у пацієнтів з АГ та ЦД, метаболічним синдромом;
- може використовуватися у пацієнтів з АГ і супутніми бронхіальною астмою та/або хронічним обструктивним захворюванням легень.
Протизапальна терапія – дуже важливий напрям у лікуванні пацієнтів із ССЗ, зокрема з дисліпідемією. Як було зазначено вище, для профілактики кардіальних подій слід звернути увагу на комплексне застосування статинів із фібратами для корекції обміну ліпідів. Окрім впливу на рівень ТГ, препарати цього типу активують фермент ліпопротеїнліпазу, який відповідає за регуляцію ліпопротеїнів низької та дуже низької щільності. Саме комплексне застосування даних ліків максимально знижує ризик розвитку атеросклерозу і його ускладнень.
Фенофібрат (Трайкор®) є ефективним щодо покращення ліпідного профілю і зменшення ймовірності розвитку великих кардіальних подій. Також слід відзначити його помірний вплив на CYP2C9, тож пацієнтам із ЦД, які приймають похідні сульфонілсечовини, потрібно ретельніше контролювати рівень глюкози.
Трайкор® відрізняється високою біодоступністю та має хороший профіль безпеки. Оскільки препарат метаболізується лише у ІІ фазі, його можна призначати літнім хворим і навіть пацієнтам із помірними порушеннями функції печінки.
Підготувала Мар’яна Гнатів
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (79) 2021 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Як відомо, кальцій бере участь у низці життєво важливих функцій. Хоча більшість досліджень добавок кальцію фокусувалися переважно на стані кісткової тканини та профілактиці остеопорозу, сприятливий вплив цього мінералу є значно ширшим і включає протидію артеріальній гіпертензії (передусім у осіб молодого віку, вагітних та потомства матерів, які приймали достатню кількість кальцію під час вагітності), профілактику колоректальних аденом, зниження вмісту холестерину тощо (Cormick G., Belizan J.M., 2019)....
Торакалгія – симптом, пов’язаний із захворюваннями хребта. Проте біль у грудній клітці може зустрічатися за багатьох інших захворювань, тому лікарям загальної практики важливо проводити ретельну диференційну діагностику цього патологічного стану та своєчасно визначати, в яких випадках торакалгії необхідна консультація невролога. В березні відбувся семінар «Академія сімейного лікаря. Біль у грудній клітці. Алгоритм дій сімейного лікаря та перенаправлення до профільного спеціаліста». Слово мала завідувачка кафедри неврології Харківського національного медичного університету, доктор медичних наук, професор Олена Леонідівна Товажнянська з доповіддю «Торакалгія. Коли потрібен невролог»....
Рівень ліпопротеїну (a) >50 мг/дл спостерігається в ≈20-25% населення і пов’язаний із підвищеним ризиком серцево-судинних захворювань (ССЗ) [1]. Ліпопротеїн (a) задіяний в атерогенезі та судинному запаленні, а також може відігравати певну роль у тромбозі через антифібринолітичну дію і взаємодію із тромбоцитами [2, 3]. Дієта та фізична активність не впливають на рівень ліпопротеїну (a); специфічної терапії для його зниження також не існує. Підвищений ризик ССЗ, пов’язаний з ліпопротеїном (а), залишається навіть у пацієнтів, які приймають статини [4]. Саме тому існує критична потреба в терапії для зниження цього ризику, особливо в первинній профілактиці. ...
Запалення відіграє важливу роль у розвитку багатьох хронічних захворювань, зокрема атеросклерозу. Нещодавно було встановлено, що гіперурикемія спричиняє запалення ендотеліальних клітин судин, ендотеліальну дисфункцію та, зрештою, атеросклероз. Експериментальна робота Mizuno та співавт. (2019), у якій було продемонстровано здатність фебуксостату пригнічувати запальні цитокіни, привернула увагу дослідників до протизапальних ефектів уратзнижувальних препаратів. Кількість лейкоцитів – надійний маркер запалення, пов’язаний із різними кардіоваскулярними захворюваннями, як-от ішемічна хвороба серця; у багатьох попередніх дослідженнях його використовували для оцінки протизапального ефекту терапевтичного втручання. Мета нового аналізу дослідження PRIZE – вивчити вплив фебуксостату на кількість лейкоцитів у пацієнтів із безсимптомною гіперурикемією....