Застосування троксерутину/карбазохрому в комплексному лікуванні ускладнень COVID‑19
 Відомо, що з коронавірусною хворобою (COVID‑19) асоціюються дихальна недостатність (ДН), цитокіновий шторм, серцево-судинні розлади, а також коагулопатія / прокоагулянтний стан. Хоча більшість випадків обумовлених SARS-CoV‑2 інфекцій є самообмежувальними, в 20% пацієнтів з’являються симптоми, які нерідко спричиняють потребу в госпіталізації (Magro C. M. et al., 2021).
Відомо, що з коронавірусною хворобою (COVID‑19) асоціюються дихальна недостатність (ДН), цитокіновий шторм, серцево-судинні розлади, а також коагулопатія / прокоагулянтний стан. Хоча більшість випадків обумовлених SARS-CoV‑2 інфекцій є самообмежувальними, в 20% пацієнтів з’являються симптоми, які нерідко спричиняють потребу в госпіталізації (Magro C. M. et al., 2021).
Тяжкі прояви COVID‑19 зазвичай розвиваються через 1-2 тиж після появи симптомів і характеризуються утрудненням дихання та ускладненнями, асоційованими з вираженим прокоагулянтним станом (Magro C. et al., 2020; Levi M. et al., 2020; Klok F. et al., 2020). У пацієнтів із тяжким перебігом COVID‑19 спостерігаються поширена мікроангіопатія та підвищений ризик тромбозу великих судин, тому вважається, що тяжкий COVID‑19 є своєрідною (спричиненою вірусом) васкулопатією з потенціалом ураження багатьох органів і систем.
C. M. Magro та співавт. (2021) проаналізували зразки тканин осіб, померлих від COVID‑19, віком від 28 до 95 років; у зразках легень було виявлено макро- та мікротромби як артеріального, так і венозного русла, руйнування капілярної стінки, відсутність життєздатного ендотелію, подвоєння базальної мембрани, периваскулярний набряк. Мікроваскулярні тромби спостерігалися також у тканинах нирок, мозку, серця, печінки; патерн тромбозу в різних пацієнтів відрізнявся. Імуногістохімічний аналіз виявив, що більше половини ендотеліальних клітин мікроваскулатури легень експресували рецептор ангіотензинперетворювального ферменту 2 типу (АПФ‑2); високий рівень експресії цього рецептора спостерігався також у клітинах шкіри та ендотелії мікросудин мозку. Отримані авторами дані свідчать, що спайк-білок SARS-CoV‑2 уражає мікроваскулярне русло всіх органів і систем, клітини яких здатні експресувати рецептор АПФ‑2.
Механізм прокоагулянтного стану при COVID‑19, який спричиняє мультиорганні тромбози, розпочинається з майже повного руйнування АПФ‑2-позитивного ендотелію легень. У подальшому баланс ренін-ангіотензинової системи зміщується в бік реалізації ефектів ангіотензину ІІ, а також підвищується активність ендотеліальної НАДФН2-оксидази. Остання зміна сприяє некротичному відмиранню клітин і вазоконстрикції, яка в умовах некрозу та деструкції ендотелію спричиняє утворення тромбіну. Гіпоксія внаслідок ушкодження ендотелію додатково підсилює гіперкоагуляцію, а прозапальні цитокіни (ІЛ‑6, ІЛ‑8, ІЛ‑1β, фактор некрозу пухлини) сприяють агрегації тромбоцитів.
За даними патологоанатомічного атласу М. В. Самсонової та співавт. (2020), присвяченого змінам унаслідок COVID‑19, основною морфологічною зміною в легенях є дифузне ушкодження альвеол у поєднанні з патологічними змінами судинного ложа легень і геморагічним синдромом в альвеолах. На думку авторів, терміни «інтерстиційна пневмонія» та «шокова легеня» не повною мірою відображають зміни при COVID‑19, оскільки не характеризують притаманного коронавірусній хворобі васкуліту. Було запропоновано включати у висновок патологічні зміни легеневих судин, переважно мікроциркуляторної ланки (мікроангіопатія з тромбозом, тромбоваскуліт), а також тромбоемболії великих судин із геморагічними інфарктами. Автори атласу також наголошують на васкулітоподібних і мікроангіопатичних змінах у міокарді, нирках та шкірі.
Отже, роль ураження судинного русла в патогенезі COVID‑19 не викликає сумнівів. Цей факт критично важливо враховувати під час обрання лікування для таких хворих.
Оскільки препаратів, призначених винятково і прицільно для лікування COVID‑19, наразі не існує, лікування різних стадій та варіантів перебігу цієї хвороби ґрунтується на застосуванні препаратів з іншими показаннями, які можуть відповідати терапевтичним цілям при коронавірусній хворобі за своєю хімічною природою, а також механізмом дії.
M. Smith та J. Smith (2020) за допомогою суперкомп’ютера SUMMIT провели пошук малих молекул, які можуть стати потенційними засобами-кандидатами для лікування COVID‑19 у зв’язку зі здатністю зв’язуватися з S-білком SARS-CoV‑2 або з ліганд-зв’язувальним комплексом рецептора АПФ‑2. Таке зв’язування порушує взаємодію між вірусом та організмом-господарем, отже, різко зменшується вірусний тягар і полегшується перебіг захворювання. Однією з речовин із найвищим показником зв’язування інтерфейсу S-білок / рецептор АПФ‑2 є карбазохром – продукт окиснення адреналіну, який зазвичай використовують у комплексі з троксерутином.
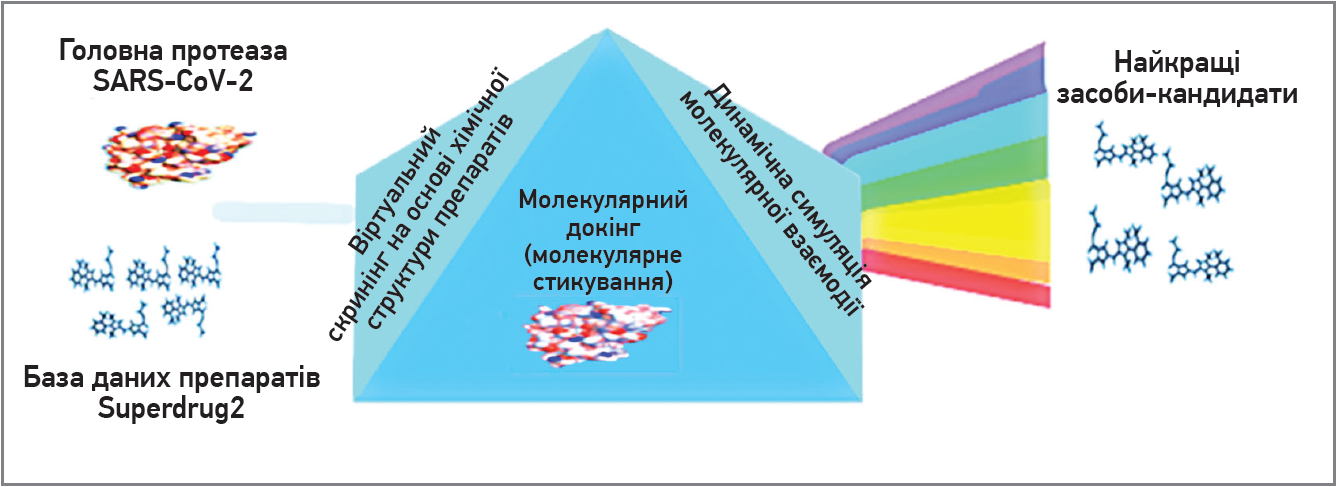
Троксерутин також запропоновано як молекулу-кандидата для лікування COVID‑19. N. Farhat та A. U. Khan (2021) провели віртуальний скринінг і симуляцію молекулярної взаємодії різних препаратів із головною протеазою вірусу SARS-CoV‑2 (рис. 1) з метою пошуку засобу, здатного пригнічувати цю протеазу, яка бере участь у перебудові поліпептидів у функціональний вірусний білок. Для цього автори застосували молекулярний докінг (молекулярне стикування) – метод моделювання на основі тривимірних структур білка та ліганду, який дозволяє визначити найвигіднішу для утворення стійкого комплексу орієнтацію однієї молекули відносно іншої. Під час аналізу була доведена здатність троксерутину зв’язуватися із залишками субстрат-зв’язувальних кишень головної протеази вірусу, а також формувати низку нековалентних зв’язків. На думку авторів, троксерутин та інші засоби зі схожими молекулярними властивостями доцільно використовувати для лікування COVID‑19 після експериментального підтвердження ефективності та безпеки в клінічних дослідженнях.
Рис. 1. Схема пошуку засобів-кандидатів для лікування COVID‑19
На фармацевтичному ринку України комплекс троксерутин/карбазохром представлено препаратом Карбарутин (компанія World Medicine). Карбарутин являє собою розчин для ін’єкцій, у 3 мл якого міститься 150 мг троксерутину, а також 1,5 мг карбазохрому. Карбарутин призначений для лікування судинних захворювань та геморагічних синдромів при підвищеній слабкості стінок капілярів. Цей препарат чинить протизапальну й антиоксидантну дію, пригнічує гіалуронідазу, запобігає окисненню гіалуронової / аскорбінової кислоти, а також адреналіну, пригнічує перекисне окислення ліпідів.
Троксерутин (вітамін Р4) є біофлавоноїдом, який зменшує підвищену проникність і ламкість капілярів, а також запобігає ушкодженню базальної мембрани ендотеліальних клітин, чинить антиоксидантну, мембраностабілізувальну, антигеморагічну, протизапальну та венотонізувальну дію. Завдяки зазначеним ефектам троксерутин зменшує набряк, покращує трофіку тканин, мікроциркуляцію та мікросудинну перфузію, зменшуючи вираженість симптоматики, пов’язаної з венозною недостатністю або порушенням відтоку лімфатичної рідини. Крім того, троксерутин підсилює ангіопротекторну дію вітаміну С, виконує і активує синтез гіалуронової кислоти, яка відповідає за міцність стінок судин, зменшує вивільнення гістаміну – потужного пронабрякового агента.
Своєю чергою, карбазохром за своєю хімічною природою є ортохіноном і являє собою продукт окислення адреналіну без симпатоміметичної активності. Карбазохром чинить локальну судинозвужувальну дію на дрібні судини без системного впливу на серцево-судинну діяльність, а також зменшує проникність і підвищує міцність капілярів. При застосуванні комбінації троксерутину та карбазохрому спостерігається взаємопідсилення фармакологічних і терапевтичних ефектів діючих речовин в аспекті гемостазу, а також вазопротекції.
Класичними показаннями до застосування Карбарутину є симптоми венозної недостатності та підвищена ламкість капілярів, але вищезазначені факти обумовлюють доцільність використання цього вазопротекторного препарату як засобу для лікування COVID‑19. Режим застосування препарату передбачає внутрішньом’язове введення в дозі 1-3 ампули/добу; тривалість лікування та дозовий режим визначають індивідуально.
На теренах України вже є випадки успішного застосування Карбарутину в лікуванні COVID‑19, три з яких наведено далі.
Представляємо випадки з реальної клінічної практики, де в комплексному лікуванні пацієнтів із СOVID‑19 застосовували Карбарутин.
Клінічний випадок 1
Хвора П., 63 роки, надійшла до інфекційного відділення лікарні швидкої медичної допомоги (ЛШМД) м. Маріуполя 04.11.2021 р. із діагнозом «Позагоспітальна двобічна вірусна пневмонія, спричинена SARS-CoV‑2 (?), тяжкий перебіг. ДН ІІ-ІІІ ступеня. COVID‑19 (?)».
Супутня патологія: ішемічна хвороба серця (ІХС). Атеросклеротичний кардіосклероз. Серцева недостатність (СН) ІІА ст. Гіпертонічна хвороба ІІ ступеня, 2 стадії, ризик 3. Цукровий діабет 2 типу.
Скарги при надходженні: загальна слабкість, задишка при мінімальному фізичному навантаженні, головний біль, запаморочення, біль у м’язах, діарея.
Анамнез хвороби: хворіє із 28.10.2021 р., коли вперше з’явилися загальна слабкість, головний біль, підвищення температури до 38,5 °C, запаморочення, задишка. Самостійно приймала німесулід. 02.11.2021 р. звернулася до сімейного лікаря. Було проведено тест на антиген СOVID‑19 (позитивний) та призначено лікування (інфузійна терапія, аскорбінова кислота, інозин, левофлоксацин, цефоперазон, дексаметазон, сульфокамфокаїн). Цього ж дня проведено рентгенографію органів грудної клітки (ОГК) та виявлено правобічну нижньочасткову пневмонію. 04.11.2021 р. стан пацієнтки погіршився: зросла задишка, яка стала турбувати її у спокої, кашель став болісним, нападоподібним, посилилися слабкість та млявість, з’явилися діарея, нудота, зменшився апетит, порушився сон. Хвора викликала швидку допомогу та з діагнозом COVID‑19 її було госпіталізовано до інфекційного відділення ЛШМД м. Маріуполя.
Об’єктивний статус при надходженні: стан хворої ближче до тяжкого, активна; свідомість ясна. Температура тіла – 37,8 °C. Шкіра бліда, акроціаноз. Слизова ротоглотки фізіологічного кольору, язик вологий з білим нальотом. Мигдалики за дужками, нальоти відсутні. В легенях дихання з обох боків значно ослаблене, особливо нижче лопаток; вислуховуються рясні вологі дрібнопухирчасті хрипи з обох боків, SрO2 – 88-87%. Після інгаляції О2 протягом 20 хв SрO2 відновилася до 94-95%. Діяльність серця ритмічна, частота серцевих скорочень (ЧСС) 82 уд./хв, артеріальний тиск (АТ) – 130/80 мм рт. ст. Живіт м’який, при пальпації неболючий; печінка біля краю реберної дуги, селезінка не пальпується; симптом Пастернацького негативний з обох боків, фізіологічні відправлення без особливостей. Менінгеальні ознаки відсутні.
Було призначено таке лікування: цефаперазон, левофлоксацин, еноксапарин, дексаметазон, молочнокислі бактерії, пантопразол, бромгексин, карбоцистеїн, сульфокамфокаїн, ацетилсаліцилова кислота, анальгін, дифенгідрамін, флуконазол, ентеросорбент на основі діоксиду кремнію, ремдесивір, фізіологічний розчин, едаравон, комплекс кверцетину з повідоном, метилпреднізолон, панкреатин, діосмектит, інфузійний розчин (натрію хлорид, калію хлорид, натрію гідрокарбонат).
05.11.2021 р. у назофарингеальному мазку було виявлено РНК вірусу SARS-CoV‑2; з огляду на клінічний перебіг захворювання встановлено діагноз «Негоспітальна двобічна вірусна пневмонія, що є проявом COVID‑19, підтверджена лабораторно, тяжкий перебіг, ДН ІІ-ІІІ ст.». Рентгенологічне обстеження ОГК від 06.11.2021 р. виявило двобічну, ймовірно, вірусну, пневмонію з негативною динамікою порівняно з 02.11.2021 р.
Інші обстеження: ЕКГ (21.11.2021 р.): синусовий регулярний ритм, ЧСС 61 уд./хв, вертикальне положення електричної осі серця, дифузні зміни міокарда, посилена біоелектрична активність лівого шлуночка. Загальний аналіз крові (ЗАК, 29.11.2021 р.): гемоглобін 118 г/л, еритроцити 3,7×1012/л, кольоровий показник 0,9, тромбоцити 360×109/л, лейкоцити 10,7×109/л, швидкість осідання еритроцитів (ШОЕ) 16 мм/год, паличкоядерні нейтрофіли 2%, сегментоядерні нейтрофіли 78%, токсична зернистість нейтрофілів +, еозинофіли 1%, лімфоцити 11%, моноцити 8%. Коагулограма (29.11.2021 р.): міжнародне нормалізоване відношення 1,1, протромбіновий індекс 90,9, активований частковий тромбопластиновий час 41,2 с, фібриноген 3,3 г/л. Біохімічний аналіз крові (29.11.2021 р.): сечовина 5,9 ммоль/л, креатинін 72,8 мкмоль/л, лужна фосфатаза 160,7 ммоль/л, аспартатамінотрансфераза (АСТ) 63,5 од, аланінамінотрансфераза (АЛТ) 56,3 од.
На тлі лікування стан пацієнтки стабілізувався: рівень SpO2 збільшився до 90-92% без кисню та до 95-97% на невеликому потоці О2, зникла діарея, зменшився кашель, нормалізувалися апетит та сон. Однак з’явилися кровотечі з місць ін’єкцій. З огляду на перебіг хвороби та результати лабораторних обстежень зменшувати дозу антикоагулянтів / антиагрегантів було небажано. До лікування хворої було додано Карбарутин у дозі 3,0 мл 2 р/добу внутрішньом’язово. На 3-тю добу використання Карбарутину кровотечі з місць ін’єкцій припинилися, що дозволило залишити без змін дозу антикоагулянтів та антиагрегантів.
02.12.2021 р. пацієнтку було виписано зі стаціонару з поліпшенням.
Клінічний випадок 2
Хворий О., 66 років, надійшов до інфекційного відділення ЛШМД м. Маріуполя 24.11.2021 р. із діагнозом «Негоспітальна двобічна вірусна пневмонія, що є проявом COVID‑19, підтверджено лабораторно (тест ПЛР на РНК вірусу SARS-CoV‑2 позитивний від 20.11.2021 р. за № 85), перебіг середньої тяжкості, ДН І-ІІ ст.».
Супутня патологія: ІХС, атеросклеротичний кардіосклероз. СН ІІА. Гіпертонічна хвороба ІІ ступеня, 2 стадії, ризик 3. Цукровий діабет 2 типу з нейропатією.
Скарги при надходженні: загальна слабкість, задишка при мінімальному фізичному навантаженні, головний біль.
Анамнез хвороби: хворіє з 11.11.2021 р., коли вперше з’явилися кашель та слабкість. Лікувався самостійно (цефаперазин, моксифлоксацин, ривароксабан, омепразол, аскорбінова кислота + рутин, бромгексин). 13.11.2021 р. при рентгенографії ОГК змін виявлено не було. 20.11.2021 р. проведено ПЛР на вірус COVID‑19 у назофарингеальному мазку й отримано позитивний результат. 23.11.2021 р. стан хворого погіршився, посилилася задишка, через що хворий був госпіталізований до інфекційного відділення ЛШМД.
Об’єктивний статус при надходженні: стан хворого середньої тяжкості, активний, свідомість ясна. Температура тіла – 37,5 °C. Шкіра помірно бліда. Слизова ротоглотки фізіологічного кольору. Язик вологий з білим нальотом. Мигдалики за дужками, нальоти відсутні. В легенях дихання з обох боків ослаблене в нижніх ділянках, вислуховуються вологі дрібнопухирчасті хрипи з обох боків, SрO2 – 89‑92%. Була розпочата інгаляція О2, після чого SрO2 відновилася протягом 20 хв (у позиції пронації на рівні 95-96%). Діяльність серця ритмічна, ЧСС 94 уд./хв, АТ 120/85 мм рт. ст. Живіт м’який, при пальпації неболючий. Печінка біля краю реберної дуги; селезінка не пальпується; симптом Пастернацького негативний з обох боків. Фізіологічні відправлення без особливостей. Менінгеальні ознаки відсутні.
Було призначено таке лікування: ердостеїн, парацетамол, метамізол, дифенгідрамін, цефепім, еноксапарин, омепразол, ацетилсаліцилова кислота, клопідогрель, дексаметазон, сульфокамфокаїн, дибазол, папаверин, раміприл, багатокомпонентна інфузійна терапія, комплекс кверцетину з повідоном, аргініну глутамат, альфа-ліпоєва кислота. Також проводили інгаляцію О2.
Рентгенологічне обстеження ОГК від 26.11.2021 р. виявило двобічну, ймовірно, вірусну, пневмонію.
Інші обстеження: ЗАК (02.12.2021 р.): гемоглобін 152 г/л, еритроцити 4,6×1012/л, кольоровий показник 0,99, тромбоцити 460×109/л, лейкоцити 8,0×109/л, ШОЕ 48 мм/год, паличкоядерні нейтрофіли 2%, сегментоядерні нейтрофіли 54%, еозинофіли 4%, лімфоцити 28%, моноцити 12%. Коагулограма (02.12.2021 р.): міжнародне нормалізоване відношення 1,26, протромбіновий індекс 78,9, активований частковий тромбопластиновий час 25,0 с, фібриноген 4,4 г/л. Біохімічний аналіз крові (02.12.2021 р.): сечовина 4,4 ммоль/л, креатинін 100,0 мкмоль/л, лужна фосфатаза 313,8 ммоль/л, АСТ 25,3 од, АЛТ 23,5 од.
На тлі лікування стан пацієнта стабілізувався, рівень SpO2 збільшився до 95‑96% без кисню. Однак у хворого з’явилися кровотечі з місць ін’єкцій та прожилки крові в мокротинні (ймовірно, внаслідок надсадного кашлю). З огляду на перебіг хвороби та результати лабораторних обстежень зменшувати дозу антикоагулянтів / антиагрегантів було небажано. До лікування пацієнта було додано Карбарутин у дозі 3,0 мл 2 р/добу внутрішньом’язово. На 2-гу добу лікування Карбарутином у мокротинні зникли прожилки крові, а на 3-тю добу припинилися кровотечі з місць ін’єкцій, що дозволило залишити без змін дозу антикоагулянтів та антиагрегантів.
07.12.2021 р. пацієнта було виписано зі стаціонару з поліпшенням.
Клінічний випадок 3
Хвору С., 66 років, було госпіталізовано до місцевої лікарні м. Харкова з попереднім діагнозом двобічної пневмонії, пов’язаної з COVID‑19.
Об’єктивний статус при надходженні: стан середньої тяжкості, свідомість ясна. Скарги на загальну слабкість, кашель, підвищення температури до 38,6 °C, задишку при ходьбі, біль у грудній клітці, який посилюється при кашлі. При аускультації дихання ослаблене, жорстке, вислуховуються сухі хрипи, шум тертя плеври відсутній, частота дихання 24/хв, SpO2 89%. Тони серця чисті, ритмічні, ЧСС 88 уд./хв, АТ 130/80 мм рт. ст.
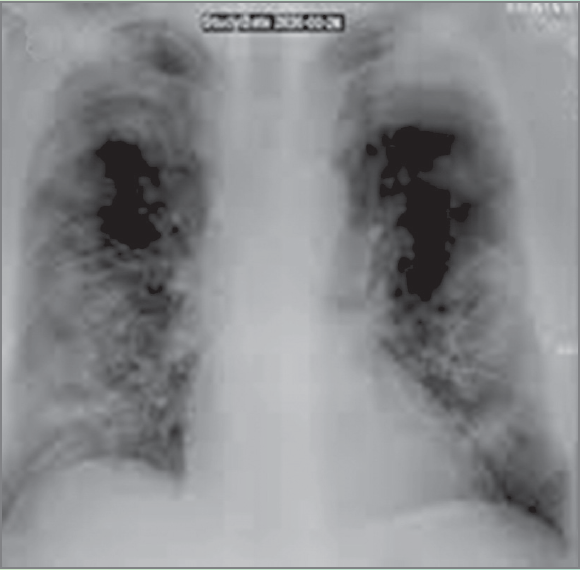
На оглядовій рентгенограмі ОГК у прямій проєкції від 02.12.2021 р. визначаються вогнищево-зливні тіні латеральних відділів обох легень низької інтенсивності на тлі пневмофіброзу. Корені легень малоструктурні, нерозширені. Контури куполів діафрагми рівні, чіткі, синуси вільні. Серце звичного положення, аортальної форми, розширене вліво (рис. 2). ПЛР (назофарингеальний мазок) виявила РНК SARS-CoV‑2.
Рис. 2. Рентгенограма пацієнтки
Інші обстеження: ЗАК: гемоглобін 130 г/л, еритроцити 4,48×1012/л, тромбоцити 158×109/л, лейкоцити 3,9×109/л, ШОЕ 31 мм/год, паличкоядерні нейтрофіли 2%, сегментоядерні нейтрофіли 54%, еозинофіли 4%, лімфоцити 28%, моноцити 12%. Коагулограма: фібриноген 3,9 г/л, час рекальцифікації плазми крові 116 с, протромбіновий індекс 96%, D-димери 1,9 мг/л, С-реактивний білок 55 мг/л.
Було встановлено діагноз двобічної пневмонії (супутні захворювання – аортосклероз, гіпертонічна хвороба), а також призначено лікування (оксигенотерапія, цефтріаксон, левофлоксацин, еноксапарин, дексаметазон, мельдоній, пантопразол, Карбарутин (3,0 мл внутрішньом’язово 2 р/добу 5 днів, потім 3,0 мл внутрішньом’язово 1 р/добу 10 днів), ацетилцистеїн, аргініну гідрохлорид).
На тлі проведеної терапії стан хворої покращився з позитивною динамікою (частота дихання знизилася до 18/хв, SpO2 зросла до 96%). На контрольній рентгенограмі ОГК від 21.12.2021 р. було виявлено позитивну динаміку – двобічну пневмонію в стадії розсмоктування. На 16-ту добу пацієнтка була виписана з відділення в задовільному стані для подальшого лікування під наглядом сімейного лікаря.
Отже, до складу комплексної терапії COVID‑19 з метою покращення мікроциркуляції у легенях та зменшення місцевої інфільтрації та набряку доцільно включати парентеральний венотонізувальний препарат Карбарутин, який чинить протинабрякову, антигеморагічну та протизапальну дію. Карбарутин запобігає ушкодженню базальної мембрани ендотеліальних клітин та покращує обмінні процеси в легенях. На тлі терапії Карбарутином (порівняно з пацієнтами, які не отримували цього препарату) спостерігали швидше розсмоктування осередків інфільтрації, що підтверджувалося рентгенологічними даними, клінічною картиною перебігу хвороби та загальним станом пацієнтів.
Медична газета «Здоров’я України 21 сторіччя» № 23-24 (516-517), 2021 р.
СТАТТІ ЗА ТЕМОЮ Терапія та сімейна медицина
Тіамін (вітамін В1) – важливий вітамін, який відіграє вирішальну роль в енергетичному обміні та метаболічних процесах організму загалом. Він необхідний для функціонування нервової системи, серця і м’язів. Дефіцит тіаміну (ДТ) спричиняє різноманітні розлади, зумовлені ураженням нервів периферичної та центральної нервової системи (ЦНС). Для компенсації ДТ розроблено попередники тіаміну з високою біодоступністю, представником яких є бенфотіамін. Пропонуємо до вашої уваги огляд досліджень щодо корисних терапевтичних ефектів тіаміну та бенфотіаміну, продемонстрованих у доклінічних і клінічних дослідженнях....
Актуальність проблеми порушень моторної функції шлунково-кишкового тракту (ШКТ) за останні десятиліття значно зросла, що пов’язано з великою поширеністю в світі та в Україні цієї патології. Удосконалення фармакотерапії порушень моторики ШКТ та широке впровадження сучасних лікарських засобів у клінічну практику є на сьогодні важливим завданням внутрішньої медицини....
Дисліпідемія та атеросклеротичні серцево-судинні захворювання (АСССЗ) є провідною причиною передчасної смерті в усьому світі (Bianconi V. et al., 2021). Гіперхолестеринемія – третій за поширеністю (після артеріальної гіпертензії та дієтологічних порушень) фактор кардіоваскулярного ризику в світі (Roth G.A. et al., 2020), а в низці європейських країн і, зокрема, в Польщі вона посідає перше місце. Актуальні дані свідчать, що 70% дорослого населення Польщі страждають на гіперхолестеринемію (Banach M. et al., 2023). Загалом дані Польщі як сусідньої східноєвропейської країни можна екстраполювати і на Україну....
Однією із найвагоміших знахідок із часу відкриття дигіталісу Нобелівський комітет назвав синтез і дослідження β-блокаторів, які зараз мають провідні стабільні позиції у лікуванні більшості серцево-судинних хвороб (ішемічна хвороба серця – стенокардія, гострий коронарний синдром, інфаркт міокарда, артеріальна гіпертензія, серцева недостатність, тахіаритмії) (Радченко О.М., 2010). Це епохальне відкриття зроблено під керівництвом британського фармаколога Джеймса Блека (James Whyte Black), який отримав за нього Нобелівську премію в 1988 році. ...