Нові можливості лікування раку підшлункової залози
20 листопада за підтримки компанії «Серв’є» відбулася ІІІ Всеукраїнська науково-практична конференція «Нові можливості лікування гастроінтестинального раку». У рамках заходу були представлені сучасні досягнення у лікуванні раку підшлункової залози (РПЗ).
 На початку з вітальним словом виступив генеральний директор ТОВ «Серв’є Україна» Фредерік Фуйю (Frederic Fouilloux), який зазначив, що продуктове портфоліо компанії в Україні представлене 19 оригінальними брендами. Це забезпечує доступ українських пацієнтів до високоякісного ефективного та безпечного лікування у ключових терапевтичних напрямах: онкологія, кардіометаболізм, неврологія, імунозапальні захворювання.
На початку з вітальним словом виступив генеральний директор ТОВ «Серв’є Україна» Фредерік Фуйю (Frederic Fouilloux), який зазначив, що продуктове портфоліо компанії в Україні представлене 19 оригінальними брендами. Це забезпечує доступ українських пацієнтів до високоякісного ефективного та безпечного лікування у ключових терапевтичних напрямах: онкологія, кардіометаболізм, неврологія, імунозапальні захворювання.
Одним із напрямів, який активно розвиває компанія, є розроблення ефективних підходів до терапії злоякісних новоутворень шлунково-кишкового тракту, зокрема й РПЗ. З цією метою компанією запроваджено програми підтримки пацієнтів та пацієнторієнтовані проєкти, розроблено освітні матеріали з рекомендаціями, створено бібліотеки та школи для пацієнтів з гастроінтестинальним раком, а також сформовано виважену цінову політику щодо препаратів.
 Модератор заходу, завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов, окреслив актуальність проблеми РПЗ.
Модератор заходу, завідувач кафедри онкології ДЗ «Запорізька медична академія післядипломної освіти МОЗ України», доктор медичних наук, професор Олексій Олексійович Ковальов, окреслив актуальність проблеми РПЗ.
– Підшлункова залоза разом з легенею, передміхуровою залозою, печінкою, яєчником належить до 5 основних локалізацій раку, при яких смертність підвищувалася протягом останніх 20 років. Проте з 2015 р. РПЗ – єдине онкологічне захворювання, при якому вона продовжує зростати і найближчим часом посідатиме друге місце після раку легені. У світі щорічно виявляють приблизно 460 000 нових випадків РПЗ, а понад 430 000 хворих помирають.
Причинами зростання захворюваності у ХХІ ст. є демографічний перехід (збільшення тривалості життя населення) та зміна способу життя. До факторів ризику розвитку РПЗ належать вік старше 70 років, наявність цукрового діабету, ожиріння, вживання алкогольних напоїв, тютюну, червоного м’яса, низький вміст фруктів і фолатів у раціоні, хронічний панкреатит.
Приблизно 10% пацієнтів із РПЗ мають рак у сімейному анамнезі. До спадкових захворювань, пов’язаних із підвищеним ризиком виникнення РПЗ, належать спадковий рак грудної залози та яєчника (HBOCS), сімейна атипова множинна меланома (FAMMM), сімейний аденоматозний поліпоз (FAP-синдром), синдроми Лінча, атаксії-телеангіктазії, Пейтца – Єгерса, спадкового панкреатиту. Немає переконливих доказів того, що скринінг знижує захворюваність і смертність.
На час встановлення первинного діагнозу РПЗ уже є системним захворюванням. Лише у 9% пацієнтів процес локальний, у решти наявні віддалені метастази або локорегіонарне поширення захворювання.
Хірургічне втручання є основним методом, при якому можна збільшити загальну виживаність, проте термін «одужання» щодо РПЗ майже ніколи не застосовується, оскільки 5-річна виживаність при ньому не перевищує 7%. Особливістю хірургічного лікування цієї форми раку (операція Віппла) є низька частота резектабельності, великий об’єм резекції, висока частота резекції R1, а також ускладнень і смерті.
На жаль, стандартні методи візуалізації не дають змоги виявити мінімальну залишкову пухлину, і у 80% хворих рецидив настає незважаючи на проведення ад’ювантної терапії, причому у 60% – протягом перших 6 міс після перенесеної R0-резекції. Саме тому 95% пацієнтів з РПЗ, незалежно від стадії захворювання, потребуватимуть паліативної терапії.
Основними проблемами терапії метастатичного РПЗ є резистентність пухлини, токсичність комбінованих схем хіміотерапії, недоведена ефективність таргетних та імунних препаратів, агресивне прогресування пухлини, коротка очікувана тривалість життя.
При цій локалізації раку немає ефективних методів паліативної хірургії (як, наприклад, резекція або радіочастотна термоабляція метастазів печінки, що збільшують виживаність хворих при поширеному колоректальному раку). Проведенню паліативної хіміотерапії заважають ускладнення, що супроводжують пухлинний процес: анорексія/кахексія, мальнутриція, порушення травлення, венозний тромбоз, больовий синдром.
Щороку Національні інститути здоров’я США виділяють близько 6 млрд доларів на дослідження раку, з них на вивчення РПЗ – лише 100 млн доларів. За 20 років на вивчення РПЗ витрачено 2 млрд доларів. Відповідно до закону про дослідження агресивних і резистентних онкологічних захворювань, у 2013 р. фінансування було збільшено до 200 млн доларів на рік, але це становить лише 3% від фінансування інших досліджень.
У 2011 р. організація PanCAN проголосила «бачення прогресу» і поставила за мету подвоїти виживаність пацієнтів з РПЗ до 2020 р., проте досягти цього поки що не вдалося. Слід визнати, що у напрямі лікування РПЗ немає інновацій і досягнуто межі виживаності. Імовірність радикальної зміни терапевтичної парадигми протягом наступних 5 років досить низька.
Нині з-поміж 430 активних клінічних досліджень лише у 14 тестують нові лікарські засоби; здебільшого вивчають не нові молекули, а методи ескалації комбінованої терапії вже відомими препаратами. У 23 дослідженнях III фази вивчають нові способи доставки вже схвалених Управлінням з контролю якості харчових продуктів і лікарських препаратів препаратів США. Остаточні результати очікуються приблизно через 8-10 років, проте оцінювана імовірність успіху становить близько 3%.
Безумовним кроком уперед у подоланні РПЗ можна вважати створення ліпосомальної форми іринотекану. Завдяки пегілюванню препарат не поглинається ретикуло-ендотеліальними клітинами печінки та селезінки і тому довго (понад 2 доби) циркулює у крові. Ліпосоми не проникають із просвіту судин у тканини із щільним з’єднанням епітелію та капілярів (наприклад, міокард), проте можуть легко надходити у тканини з нещільним з’єднанням клітин, такими як пухлини. Після проникнення у строму ліпосоми поглинаються макрофагами, й іринотекан перетворюється на активний метаболіт SN-38, тривалий вплив якого на клітини (168 год) призводить до значного пригнічення їх росту. При цьому для забезпечення терапевтичного ефекту необхідна у 5 разів нижча доза препарату – лише 10 мг/кг маси тіла.
Доказова база пегільованого ліпосомального іринотекану (далі – препарат Онівайд®*) дуже переконлива. Комбінація препарату з 5-фторурацилом і лейковорином у 2-й лінії терапії метастатичного РПЗ забезпечила пацієнтам медіану загальної виживаності 9,4 міс і 6-місячну загальну виживаність у 65% хворих (р=0,012), а медіану виживаності без прогресування – 3,5 міс (р=0,0001). Слід врахувати, що йдеться про вкрай агресивну резистентну прогресуючу пухлину.
У настановах Національної онкологічної мережі США (NCCN) рекомендоване призначення комбінації ліпосомального іринотекану з 5-фторурацилом і лейковорином після терапії на основі гемцитабіну за умови стабільного стану хворого.
Таким чином, із реєстрацією препарату Онівайд® онкологи України отримали ще одну можливість покращити лікування хворих на метастатичний РПЗ.
 Наукова секція конференції розпочалася доповіддю «Континуум лікування метастатичної аденокарциноми підшлункової залози згідно із сучасними рекомендаціями», представленою провідним науковим співробітником відділення пухлин органів черевної порожнини Національного інституту раку (м. Київ), доктором медичних наук Костянтином Володимировичем Копчаком.
Наукова секція конференції розпочалася доповіддю «Континуум лікування метастатичної аденокарциноми підшлункової залози згідно із сучасними рекомендаціями», представленою провідним науковим співробітником відділення пухлин органів черевної порожнини Національного інституту раку (м. Київ), доктором медичних наук Костянтином Володимировичем Копчаком.
– РПЗ посідає 4-те місце серед причин смерті від онкологічних захворювань у США, 6-те місце у Європі, а за даними Національного канцер-реєстру України – 6-те місце у структурі смертності від злоякісних новоутворень у чоловіків та 9-те місце у жінок. У 2019 р. в Україні (без урахування тимчасово окупованих територій) загальна кількість випадків РПЗ склала 4527, а випадків смерті від цього захворювання – 3430. При цьому 70,2% пацієнтів із вперше виявлених не прожили 1 року. Лише 26,9% хворих були охоплені спеціальним лікуванням, у тому числі 8,0% – хірургічним та 3,8% – комплексним і комбінованим.
Факторами ризику розвитку РПЗ є куріння, цукровий діабет, ожиріння, висококалорійна дієта, зловживання алкоголем. Близько 10% пацієнтів з РПЗ мають обтяжений сімейний анамнез щодо РПЗ. Також вивчається зв’язок між розвитком РПЗ й інфікуванням H. pylori, І групою крові, вживанням кави тощо. У 85% пацієнтів РПЗ представлений протоковою аденокарциномою. Близько 10% займають інші форми екзокринного раку та близько 5% – нейроендокринні пухлини. Більше 80% пацієнтів на момент діагностики РПЗ не підлягають хірургічному лікуванню у зв’язку із місцево-поширеною чи метастатичною хворобою. За рівнем виживаності онкологічних хворих РПЗ посідає останнє місце. Так, 5-річна виживаність пацієнтів з РПЗ не перевищує 10%.
За прогнозами GLOBOCAN 2020, з 2020 по 2040 р. кількість нових випадків РПЗ зросте на 70,2%, а летальність – на 72,0%. Відсутність ранніх характерних симптомів призводить до пізнього виявлення РПЗ, наявності метастазів на момент діагностики та високого рівня смертності.
Важливе значення при лікуванні РПЗ має з’ясування резектабельності пухлини. NCCN прийняла критерії резектабельності РПЗ, схожі до таких Європейського товариства медичної онкології (ESMO).
Підходи до лікування РПЗ. Вибір тактики лікування залежить від стадії захворювання та поширення пухлини. Сьогодні застосовують хірургічне (радикальне, паліативне), хіміотерапевтичне (неоад’ювантне, ад’ювантне, паліативне) та хіміопроменеве лікування.
Єдиним радикальним методом лікування РПЗ є хірургічне втручання, основною метою якого є досягнення R0 статусу. Для зменшення розміру, стадії пухлини та досягнення її резектабельності перед хірургічним втручанням проводиться неоад’ювантна хіміотерапія (ХТ). Основною метою ад’ювантної ХТ є контроль мікрометастазів і збільшення загальної виживаності (ЗВ) пацієнтів з РПЗ.
Паліативна ХТ має на меті подовження ЗВ, покращення якості життя та зменшення симптомів. Паліативну терапію проводять пацієнтам із IV стадією РПЗ та рецидивом хвороби після оперативного втручання.
Через обмежені дані щодо ефективності променева терапія рекомендована лише у рамках клінічних досліджень.
Згідно з настановами NCCN, як 1-ша лінія лікування пацієнтів з метастатичним або місцево-поширеним неоперабельним РПЗ, статусом за ECOG 0-1 рекомендоване застосування режиму FOLFIRINOX (іринотекан + лейковорин + оксаліплатин + 5-фторурацил) або модифікованого FOLFIRINOX, гемцитабін + наб-паклітаксел (в Україні не зареєстрований) чи інші комбінації з гемцитабіном. Пацієнтам зі статусом 2 за ECOG гемцитабін можна призначати у монотерапії або в комбінації з капецитабіном чи ерлотинібом, а зі статусом 3 – лише підтримуючу терапію. Якщо пацієнти отримували лікування на основі гемцитабіну у 1-й лінії, то комбінацію пегільований ліпосомальний іринотекан (препарат Онівайд®) + 5-фторурацил (5-ФУ) + лейковорин (ЛВ) можна застосовувати у 2-й лінії.
Безпеку й ефективність препарату Онівайд® вивчали у багатоцентровому рандомізованому відкритому контрольованому клінічному дослідженні NAPOLI-1. У ньому досліджували два режими терапії пацієнтів з метастатичною аденокарциномою ПЗ із задокументованим прогресуванням захворювання після терапії гемцитабіном. Встановлено покращення ЗВ хворих на метастатичний РПЗ, які приймали комбінацію Онівайд® + 5-ФУ + ЛВ, порівняно з тими, хто отримував терапію без препарату Онівайд® (6,1 та 4,2 міс відповідно; р=0,012; відношення ризиків 0,67; A. Wang-Gillam et al., 2016).
 Доповідь «Новий підхід терапії пацієнтів із метастатичною аденокарциномою ПЗ в рамках лікувального континууму» представив завідувач відділення малоінвазивної хірургії, ендоскопії та інтервенційної радіології Національного інституту раку (м. Київ), доктор медичних наук Андрій Володимирович Лукашенко.
Доповідь «Новий підхід терапії пацієнтів із метастатичною аденокарциномою ПЗ в рамках лікувального континууму» представив завідувач відділення малоінвазивної хірургії, ендоскопії та інтервенційної радіології Національного інституту раку (м. Київ), доктор медичних наук Андрій Володимирович Лукашенко.
– Радикальне оперативне втручання сьогодні залишається основним методом лікування локальної резектабельної форми РПЗ. Операцією вибору при протоковій аденокарциномі головки ПЗ є панкреатодуоденектомія. Проте ЗВ пацієнтів при цьому методі втручання не перевищує 24,8 міс навіть у провідних клініках світу (V.P. Groot et al., 2018). Слід зазначити, що розширена лімфодисекція не продемонструвала впливу на віддалені результати лікування пацієнтів із протоковою аденокарциномою.
У дослідженні III фази PRODIGE 24/CCTG PA6 порівнювали ефективність і безпеку ад’ювантних режимів FOLFIRINOX і гемцитабіну після хірургічного лікування пацієнтів із протоковою аденокарциномою ПЗ. Медіана ЗВ склала 54,4 міс у разі використання схеми FOLFIRINOX проти 35,0 міс – гемцитабіну. При цьому 3-річної ЗВ вдалося досягти у 63,4 та 48,6% пацієнтів відповідно.
Обнадійливі результати демонструють дослідження, у яких вивчається застосування неоад’ювантної терапії при РПЗ, що особливо актуально для пацієнтів із гранично резектабельною аденокарциномою. Вже отримані дані про збільшення медіани безрецидивного періоду до 14,7 міс, 2-річної безрецидивної виживаності – до 43% та ЗВ – до 37,7 міс у разі використання схеми FOLFIRINOX у неоад’ювантному режимі при гранично резектабельному РПЗ (J.E. Murphy et al., 2018).
Що стосується метастатичного РПЗ, то згідно із рекомендаціями NCCN, найкращим варіантом лікування таких хворих є участь у клінічних дослідженнях. Варто зауважити, що за останні 5 років 19 досліджень щодо лікування РПЗ виявились неуспішними. Зокрема, було продемонстровано, що таргетна й імунотерапія не забезпечують значних переваг для хворих на протокову аденокарциному ПЗ. Натомість деякий прогрес у лікуванні таких пацієнтів пов’язаний із застосуванням різних схем поліхіміотерапії (H.A. Burris et al., 1997; M.J. Moore et al., 2005; T. Conroy et al., 2011; D.D. Von Hoff et al., 2013).
Таким чином, РПЗ дуже важко піддається лікуванню. Складна біологія ПЗ, зокрема наявність щільного стромального шару, імуносупресивних пухлинасоційованих макрофагів, низька щільність мікросудин і підвищена проникність судинної стінки зумовлює неефективність доставки лікарських засобів, недостатній вплив на пухлину й обмежену ефективність сучасних методів лікування. Інноваційним препаратом для лікування метастатичного РПЗ є Онівайд®, при застосуванні якого доведене покращення виживаності (р=0,012) та якості життя пацієнтів із РПЗ (A. Wang-Gillam et al., 2016; R.A. Hubner et al., 2019).
 Про міжнародний досвід лікування метастатичної аденокарциноми ПЗ розповів завідувач відділення хіміотерапії КНП ЛОР «Львівський онкологічний регіональний лікувально-діагностичний центр», кандидат медичних наук Ярослав Васильович Шпарик.
Про міжнародний досвід лікування метастатичної аденокарциноми ПЗ розповів завідувач відділення хіміотерапії КНП ЛОР «Львівський онкологічний регіональний лікувально-діагностичний центр», кандидат медичних наук Ярослав Васильович Шпарик.
– РПЗ асоціюється із найнижчим рівнем виживаності серед інших видів раку. При цьому смертність від РПЗ упродовж останніх 20 років продовжує зростати. Очікується, що протягом десятиліття у США РПЗ стане другою провідною причиною смертності від злоякісних новоутворень (L. Rahib et al., 2014).
Одним із важливих факторів, що впливають на виживаність пацієнтів з РПЗ, є стадія хвороби на момент встановлення діагнозу. Так, за даними Американського товариства клінічної онкології (ASCO), 5-річна виживаність хворих на РПЗ локальної резектабельної стадії (І, ІІ) становить близько 37%, а пацієнтів із місцево-поширеним (стадія ІІ/ІІІ) та поширеним (стадія IV) РПЗ не перевищує 12 та 3% відповідно. Однак лише у 10-15% випадків РПЗ виявляють на локальній стадії, коли ще можливо виконати радикальне втручання. У 35-40% пацієнтів РПЗ діагностуються на стадії регіонарних метастазів, а у 45-55% – віддалених метастазів.
Сьогодні пропонується проведення скринінгу серед пацієнтів високого ризику, особливо носіїв мутації генів, асоційованих з РПЗ. Виявлено зв’язок між розвитком РПЗ й такими спадковими синдромами, як синдром Лінча, спадковий рак молочної залози, пов’язаний з мутацією гена BRCA, синдроми Пейтца – Єгерса, атаксії-телеангіектазії, сімейної атипової множинної меланоми та спадковий панкреатит. Важливу роль відіграють сімейні фактори і фактори довкілля. Відомо, що зі збільшенням кількості хворих родичів першого ступеня спорідненості ризик захворіти на РПЗ зростає.
Сучасні варіанти терапії поширеного/метастатичного РПЗ. Першим препаратом, який дозволив дещо збільшити виживаність хворих на метастатичний РПЗ, став гемцитабін у монорежимі та в комбінації з іншими препаратами (V. Heinemann et al., 2006; C. Louvet et al., 2005; M.J. Moore et al., 2007; D.D. Von Hoff et al., 2013). У дослідженні T. Conroy та співавт. (2011) порівнювали ефективність монотерапії гемцитабіном та схеми FOLFIRINOX. Медіана виживаності у групах гемцитабіну та FOLFIRINOX склала 6,8 та 11,1 міс відповідно, а виживаність без прогресування (ВБП) – 3,3 та 6,4 міс відповідно. Недоліком схеми FOLFIRINOX є її токсичність. Так, серед побічних реакцій 3-4 ступеня тяжкості найчастіше виникали нейтропенія (у 45,7% пацієнтів групи FOLFIRINOX проти 21% у групі гемцитабіну), гарячка (у 23,6 проти 17,8%), нудота (14,5 проти 8,3%) та діарея (12,7 проти 1,8% відповідно; T. Conroy et al., 2011).
Наступним стало рандомізоване дослідження фази II PRODIGE 35-PANOPTIMOX. У ньому порівнювали три схеми лікування: 12 циклів FOLFIRINOX (група А), 8 циклів FOLFIRINOX із подальшою підтримуючою терапією 5-фторурацилом і лейковорином до прогресування та реіндукцією FOLFIRINOX після прогресування (група В), альтернуючі режими FOLFIRI 3 і гемцитабін у монорежимі по 2 міс кожен (режим FIRGEM, група С). Альтернуючий режим FIRGEM продемонстрував найгірші результати, а ефективність лікування у групах А і В виявилася зіставною.
У дослідженні V. Hoff та співавт. (2013) медіана виживаності хворих при застосуванні комбінації гемцитабіну з наб-паклітакселом (в Україні не зареєстрований) склала 8,5 міс порівняно з 6,7 міс при лікуванні лише гемцитабіном. Ретроспективні дані, отримані з клінічної практики, вказують на зіставну ефективність щодо ЗВ схеми FOLFIRINOX і комбінації гемцитабіну з наб-паклітакселом у 1-й лінії терапії метастатичного РПЗ. Так, медіана ЗВ склала 13,8 міс у хворих, які отримували FOLFIRINOX, та 12,1 міс – гемцитабін із наб-паклітакселом.
Вибір схеми ХТ 1-ї лінії при РПЗ здійснюється з урахуванням віку та загального стану хворого. Так, схему FOLFIRINOX у 1-й лінії можна призначати пацієнтам віком ≤75 років за умови статусу 0-1 за ECOG. Особам похилого віку (>75 років) FOLFIRINOX не рекомендована, а гемцитабін з наб-паклітакселом призначається лише при статусі 0-2 за ECOG.
Історично близько 50% пацієнтів є кандидатами на лікування після прогресування (D. Schrag et al., 2007). Донедавна стандартів терапії для пацієнтів із прогресуванням після 1-ї лінії лікування не було. Після гемцитабіну схемою вибору була FOLFOX, яка, втім, не демонструвала хороших результатів (H. Oettle et al., 2014; S. Gill et al., 2016).
Перспективною терапевтичною опцією для клініцистів став пегільований ліпосомальний іринотекан (препарат Онівайд®). У комбінації з 5-ФУ і ЛВ Онівайд® схвалений Управлінням з контролю якості харчових продуктів і лікарських препаратів США та Європейським агентством з лікарських засобів за централізованою процедурою в Європі для лікування пацієнтів з метастатичним РПЗ, що прогресує після терапії гемцитабіном. Спеціально розроблена ліпосомальна форма дозволяє покращити доставку іринотекану при одночасному зменшенні токсичності. Ліпосомальна композиція, що містить близько 80 тис. молекул іринотекану у ліпосомі, сприяє переважно підвищеному впливу іринотекану на пухлину, подовжує його циркуляцію більш ніж у 3 рази й обмежує розподіл порівняно з неліпосомальними формами іринотекану. 95% іринотекану залишається інкапсульованим у ліпосомі під час циркуляції.
Онівайд® забезпечує вищу протипухлинну активність, ефективніше та стійке пригнічення росту пухлини, ніж стандартний іринотекан. Ліпосома довше циркулює у крові з поступовим розподілом препарату. Завдяки ефекту підвищення проникності та утримання ліпосома потрапляє переважно у середовище пухлини, де після її поглинання пухлиноасоційованими макрофагами іринотекан під впливом карбоксилестераз перетворюється на активний метаболіт SN-38, активність якого приблизно в 1000 разів перевищує таку неліпосомального іринотекану. Тривалий вплив SN-38 на пухлину зумовлює значне пригнічення її росту (рис. 1).
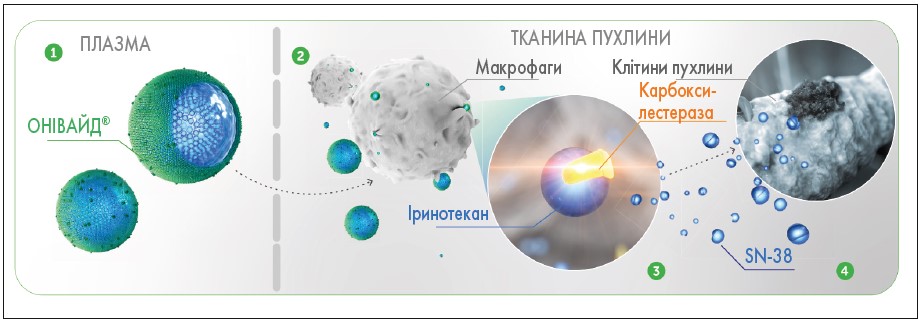 Рис. 1. Протипухлинна активність препарату Онівайд®
Рис. 1. Протипухлинна активність препарату Онівайд®
У рандомізованому контрольованому клінічному дослідженні NAPOLI-1 застосування препарату Онівайд® сприяло покращенню загальної та безрецидивної виживаності. Так, ЗВ склала 6,1 міс у групі хворих, які отримували препарат Онівайд® + 5-ФУ + ЛВ, проти 4,2 міс у групі пацієнтів, котрі отримували терапію без препарату Онівайд® (рис. 2). Медіана ВБП сягала 3,1 та 1,5 міс відповідно (р=0,0001). Крім цього, комбінація Онівайд® + 5-ФУ + ЛВ забезпечувала вищу об’єктивну відповідь і частоту відповіді пухлинного маркера CA19-9 (р=0,0006).
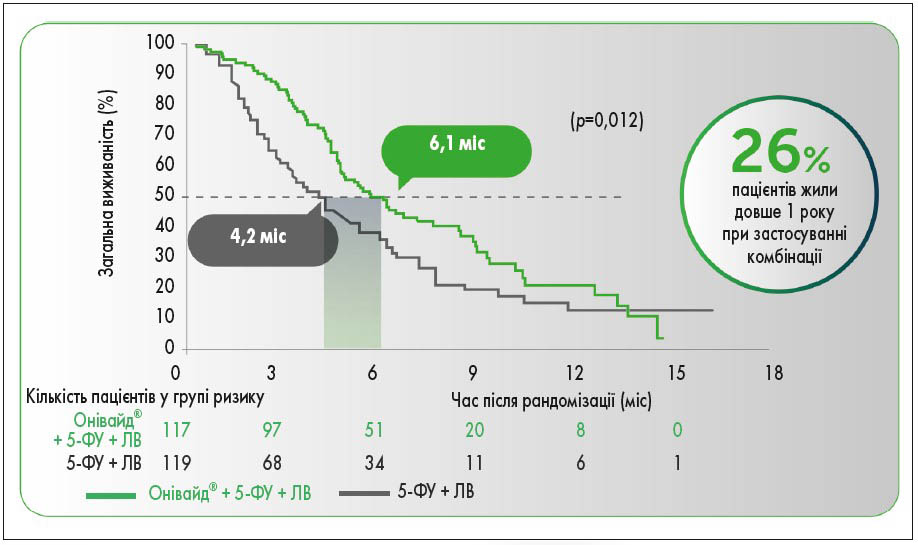 Рис. 2. Загальна виживаність при застосуванні комбінації Онівайд® + 5-ФУ + ЛВ (дослідження NAPOLI-1)
Рис. 2. Загальна виживаність при застосуванні комбінації Онівайд® + 5-ФУ + ЛВ (дослідження NAPOLI-1)
При аналізі даних підгрупи пацієнтів, які прожили більше 1 року, виділено такі можливі позитивні прогностичні фактори, як вік <65 років, хороший загальний стан, співвідношення нейтрофіли/лімфоцити ≤5, СА19-9 ≤59 верхньої межі норми та відсутність метастазів у печінці.
Ефективність препарату Онівайд® підтверджена і в клінічній практиці. Так, Онівайд® + 5-ФУ + ЛВ забезпечували медіану ЗВ 9,4 міс та медіану ВБП 3,5 міс. При цьому 6-місячна ЗВ склала 65,1%, а 6-місячна ВБП – 37,5% (C. Yoo et al., 2019).
Відкритими залишаються питання щодо порівняння ефективності схеми Онівайд® + 5-ФУ + ЛВ з іншими схемами на основі фторпіримідину в умовах 2-ї лінії, клінічної активності препарату Онівайд® у пацієнтів, які попередньо отримували схему FOLFIRINOX, та можливість використання пегільованого ліпосомального іринотекану у 1-й лінії терапії прогресуючого/метастатичного РПЗ.
* В Україні пегільований ліпосомальний іринотекан зареєстрований за торговою назвою ОНІВАЙД® пегільований ліпосомальний (далі – ОНІВАЙД®; Р/П № UA/18775/01/01, наказ МОЗ України № 1768 від 20.08.2021).
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (73) 2021 р.
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




