Тромбоз глибоких вен і легенева емболія: схожі, але різні. Специфічність проявів за COVID‑19
Тромбоз глибоких вен (ТГВ) і легенева емболія (ЛЕ) є проявами одного захворювання під назвою венозна тромбоемболія (ВТЕ), яка становить серйозну проблему для охорони здоров’я й залишається предметом обговорення в клінічній медицині, що зачіпає лікарів усіх спеціальностей. Щорічна частота венозних тромбозів становить 0,1-0,3% на рік, у європейській популяції вони трапляються в 1-2 осіб на 1000 випадків [1-6].
Симптоматичну тромбоемболію легеневої артерії (ТЕЛА) має приблизно третина пацієнтів із венозним тромбозом [7].
ЛЕ – найсерйозніший прояв ТГВ, адже є тяжким і потенційно смертельним захворюванням. Виживання через 3 міс після випадку ЛЕ становить лише 62,8%, що набагато нижче, ніж після ТГВ (91,9%) [8]. Летальність протягом 30 днів у пацієнтів із ЛЕ вища за таку в пацієнтів із ТГВ (9,7% проти 4,6% відповідно). Найчастіше ЛЕ виникає як ускладнення вираженого клінічного прояву чи «тихого» ТГВ нижніх кінцівок. Епідеміологію ЛЕ важко визначити, бо вона може залишатися безсимптомною й бути діагностованою випадково.
Історичні аспекти
Давно було відомо, що кров людини може утворювати згустки, виходячи з кровоносного русла. На це звертали увагу у своїх працях давньогрецький лікар і філософ Гіппократ (близько 460-377 рр. до н. е.) та давньоримський медик Клавдій Гален (130-200 рр. н. е.). У трактаті «Про частини тварин» геніальний давньогрецький філософ Аристотель (384-322 рр. до н. е.) вказує на елементи, з яких складаються тварини, зокрема на волокна, під якими мається на увазі фібрин, що утворюється при зсіданні крові. Основоположник патологічної анатомії Джованні Баттіста Морганьї (1682-1771) у класичній праці «Про місцезнаходження та причини хвороб, виявлених анатомом» першим описав згустки крові, утворені всередині судини та припустив, що існує взаємозв’язок між легеневою патологією й ураженням. Подібні дослідження проводили шотландський хірург Джон Гантер (1728-1793), французький патологоанатом Жан Крювельє (1791-1874) й австрійський лікар Карл фон Рокитанський (1804-1878). У роботі видатного французького медика Рене Лаеннека (1781-1826) було описано геморагічний інфаркт легені та висловлено припущення, що тромби нижніх кінцівок є джерелом тромбоемболії в легеневій артерії. Це експериментально довів німецький учений Рудольф Вірхов (1821-1902). Тріадою Вірхова описуються чинники ризику ВТЕ. Припускають, що венозний тромбоз є результатом принаймні одного з трьох етіологічних чинників: гіперкоагуляції, гемодинамічних змін (застій, турбулентність), пошкодження/дисфункція ендотелію. Від 75 до 96% пацієнтів із ВТЕ мають хоча б один із цих чинників.
Захворюваність і смертність
Захворюваність на ВТЕ у світі становить близько 10 млн випадків на рік. Є дані, які показують: щорічно понад пів мільйона смертей у Європі та понад 300 тис. у США пов’язані з венозним тромбозом. Але є підстави вважати, що рівень захворюваності та загальна кількість випадків можуть бути значно вищими. ТГВ сам собою не часто призводить до смерті, що підтверджують звіти Національного центру статистики охорони здоров’я США, тоді як ЛЕ відповідальна за набагато більше смертей [9, 10]. ЛЕ часто не діагностується й тому справжня смертність, очевидно, суттєво вища. Дані епідеміологічних досліджень на рівні угруповань показують, що приблизно кожна п’ята людина помирає від ЛЕ практично відразу, а 40% – протягом 3 міс [11, 12]. Багато хто з пацієнтів, які вижили, страждатимуть усе життя з ризиком виникнення ще одного епізоду. У 30% тих, у кого було зафіксовано ТГВ, є ймовірність повторення епізоду в найближчі 10 років із найбільшим ризиком у перші 2 роки [13, 14]. Рецидив імовірніший, якщо початковий епізод був «спонтанним», тобто не спровокованим (часто разові події). Пацієнти із симптоматичною ЛЕ схильні до вищого ризику рецидиву ВТЕ порівняно з пацієнтами із симптомами лише ТГВ [15]. Із досі незрозумілих причин ризик рецидиву ВТЕ вищий у чоловіків, аніж у жінок.
Визначення понять
ТГВ передбачає утворення одного або кількох згустків крові (тромбів), що утворюються в одній із великих вен, найчастіше в нижніх кінцівках [16]. Згустки можуть спричинити часткове або повне припинення циркуляції у вені, що призводить до набряку, болю в ногах, зміни кольору або почервоніння ураженої ділянки, виразок [17-20]. Найсерйознішим ускладненням, яке виникає внаслідок ТГВ, є ТЕЛА, що трапляється більш ніж у третини пацієнтів [21].
Ембол – це будь-який сторонній матеріал у судинній системі, який може застрягти в судині та блокувати її просвіт. До них належать атероматозні бляшки, розростання на серцевих клапанах, фрагменти пухлини, навколоплідні води, повітря та жир. Понад 90% великих емболів походять із тромбів. Емболія виникає, коли ембол блокує кровообіг. Симптоми тромбозу й емболії можуть відрізнятися залежно від локалізації та типу закупорювання тромбом глибоких вен.
Утворення тромбів
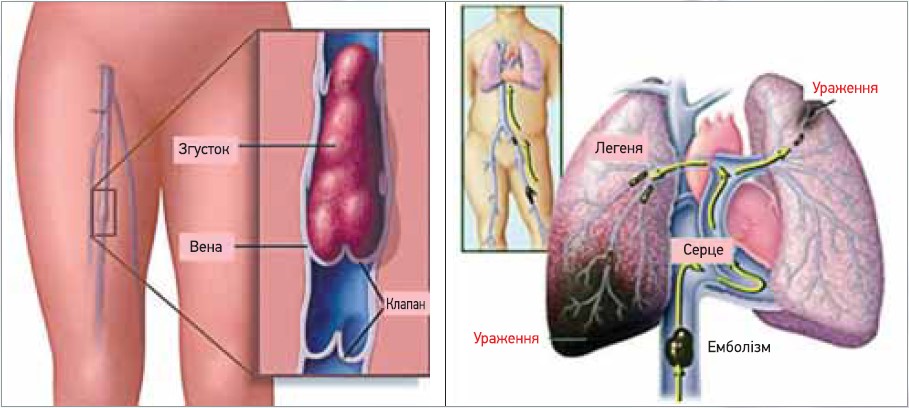
Згусток крові утворюється тоді, коли клітини накопичуються на стінці пошкодженої кровоносної судини, щоб захистити її та зупинити кровотечу. У фізіологічних умовах після загоєння рани тромб розчиняється. В іншому випадку згусток може відірватися й порушити прохідність судини. Подеколи тромби утворюються випадково. Сформований тромб може відокремлюватися від місця свого утворення й переноситися током крові спочатку в нижню порожнисту вену, потім у праве передсердя, правий шлуночок і, нарешті, обтурувати структури артеріального русла легень. Основним джерелом тромбів є система нижньої порожнистої вени (близько 85%). Значно рідше тромби утворюються в системі верхньої порожнистої вени (1,3-1,7%). Найчастіше місцем утворення тромбу служать вени гомілки. Найбільшу небезпеку становлять так звані флотувальні (англ. floating – плавальні) тромби (рис. 1).
Рис. 1. Утворення тромбу у вені та його переміщення в серце та легені
Поінформованість громадськості про ВТЕ залишається досить низькою. Деякі мають лише базові знання про її симптоми та чинники ризику порівняно з іншими основними судинними захворюваннями, як-от інфаркт міокарда й інсульт. Знання чинників, що спричиняють виникнення ВТЕ, дасть можливість надалі здійснювати цілеспрямовану профілактику та призначати адекватне лікування.
Чинники ризику ТГВ
- Тромбоз і тромбоемболія в анамнезі, тромбофілія: люди із сімейним анамнезом тромбоутворення можуть мати вищий ризик їх розвитку. Крім того, наявність одного тромбу збільшує ймовірність розвитку іншого.
- Травми: серйозне ушкодження глибокої кровоносної судини. Наприклад, після перелому кістки або автомобільної аварії.
- Іммобілізація (у зв’язку з госпіталізацією, відновленням після травми, тривалого постільного режиму або паралічу): люди, які протягом довгого часу ведуть малорухливий спосіб життя, мають вищий ризик.
- Вагітність: вагітні вразливіші до утворення тромбів. Окрім того, дуже рідко може розвинутися такий небезпечний для життя стан, як емболія навколоплідними водами. Ризик найвищий у III триместрі вагітності та через 6 тиж після пологів (у 60 разів вище через 3 міс після пологів, якщо порівнювати з невагітними). Екстракорпоральне запліднення збільшує ризик розвитку ВТЕ.
- Гормональна замісна терапія: в жінок у постменопаузі, які отримують замісну гормональну терапію.
- Рак: є добре відомим чинником ризику ВТЕ. Найвища ймовірність ВТЕ для онкогематології, раку легень, шлунково-кишкового тракту та підшлункової залози, а також головного мозку. Загальний ризик ВТЕ в пацієнтів зі злоякісними новоутвореннями в 4 рази вищий, аніж у популяції. Пацієнти, які отримують хіміотерапію, мають у 6 разів вищий ризик ВТЕ порівняно зі здоровою популяцією.
- Хірургія та пов’язані з нею стани: хірургічні процедури, особливо операції на стегні, тазі чи коліні, підвищують ризик утворення тромбу.
- Деякі лікарські препарати (протизаплідні пігулки, замісна гормональна терапія, тамоксифен, еритропоетин).
- Літній вік: особливо особи віком понад 65 років.
- Нефротичний синдром.
- Серцева недостатність.
- Попередні ТГВ чи ЛЕ.
- Ожиріння.
- Куріння.
Чинники ризику ЛЕ
- Повітря у вені: потрапляння повітря в кровоносну судину може спричинити утворення емболу.
- Сторонні предмети в організмі: будь-який сторонній предмет, наприклад уламок або куля, потенційно може потрапити в кровоносні судини та спричинити закупорювання.
- Інфекція: деякі інфекції можуть зумовлювати проникнення шкідливих патогенів і призводити до обтурації кровоносних судин.
- Септична емболія: септична емболія легеневого русла зазвичай пов’язана з ендокардитом у правих відділах серця. Чинники ризику включають внутрішньовенне введення препаратів та інфіковані катетери або електроди кардіостимуляторів. Інші причини включають септичні тромби з мигдалин, а також яремної, зубної й тазової ділянок.
- Жирова емболія: емболізація жировою тканиною відбувається практично в усіх пацієнтів із переломами таза чи трубчастих кісток. Окрім того, емболія може бути зумовлена інфузією ліпідних препаратів, жировою хворобою печінки, панкреатитом, ліпосакцією.
- Повітряна емболія: найчастіше це ускладнення маніпуляцій із центральними венозними та гемодіалізними катетерами.
- Емболія амніотичної рідини: амніотична емболія – рідкісне, але дуже небезпечне ускладнення, унікальне для вагітності. Найімовірніший механізм полягає в тому, що при пологах амніотична рідина потрапляє у вени матки під тиском або коли плацента відшарована чи травмована втручанням. Наслідком цього є те, що легеневі судини закриваються клітинами й меконієм, спричиняючи запальну реакцію та виділяючи активні метаболіти. У більшості пацієнток розвиваються судоми. Відзначається висока смертність (близько 21%).
- Емболія тканиною пухлини: легеневі внутрішньосудинні пухлинні емболи виявляються у 26% автопсій пацієнтів із солідними новоутвореннями (діагноз рідко встановлюється прижиттєво). Найчастіші причини – рак простати, травневої системи, печінки та молочної залози. Хоча більшість ЛЕ відбувається у хворих на рак товстої кишки, легень і простати, найвищий відносний ризик ВТЕ при мієломній хворобі, раку головного мозку, підшлункової залози. У поодиноких випадках емболії створюються штучно, щоби зменшити приплив крові до ракової пухлини.
- Нетромботична ЛЕ: різні типи клітин, як-от адипоцити, гемопоетичні та пухлинні клітини, трофобласт, бактерії, гриби, паразити, чужорідні матеріали, газ.
Наслідки ЛЕ
- Масивна ЛЕ (зниження кровотоку >60%) – швидко призводить до смерті (раптова смерть). Зазвичай це довгі тромби, що потрапляють із вен ніг.
- Велика ЛЕ – ураження судин середнього розміру. Пацієнти із задишкою, кашлем, мокротинням із плямами крові, болем у грудях, запамороченням, непритомністю, шоком, колапсом.
- Мала ЛЕ – закупорювання дрібних периферичних легеневих артерій. Безсимптомна чи незначна задишка. Рецидивні незначні ЛЕ призводять до легеневої гіпертензії. Можуть залишитися непоміченими.
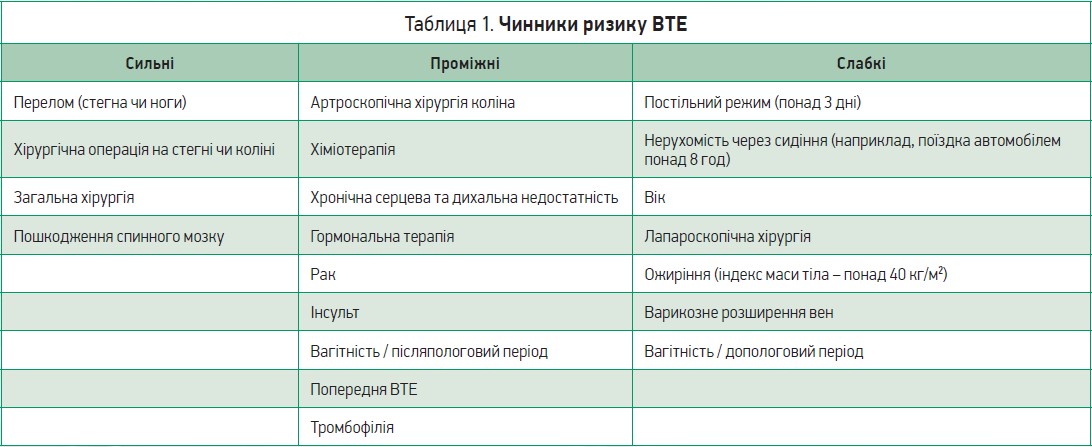
Чинники ризику ВТЕ диференціюють на сильні, проміжні та слабкі [22] (табл. 1).
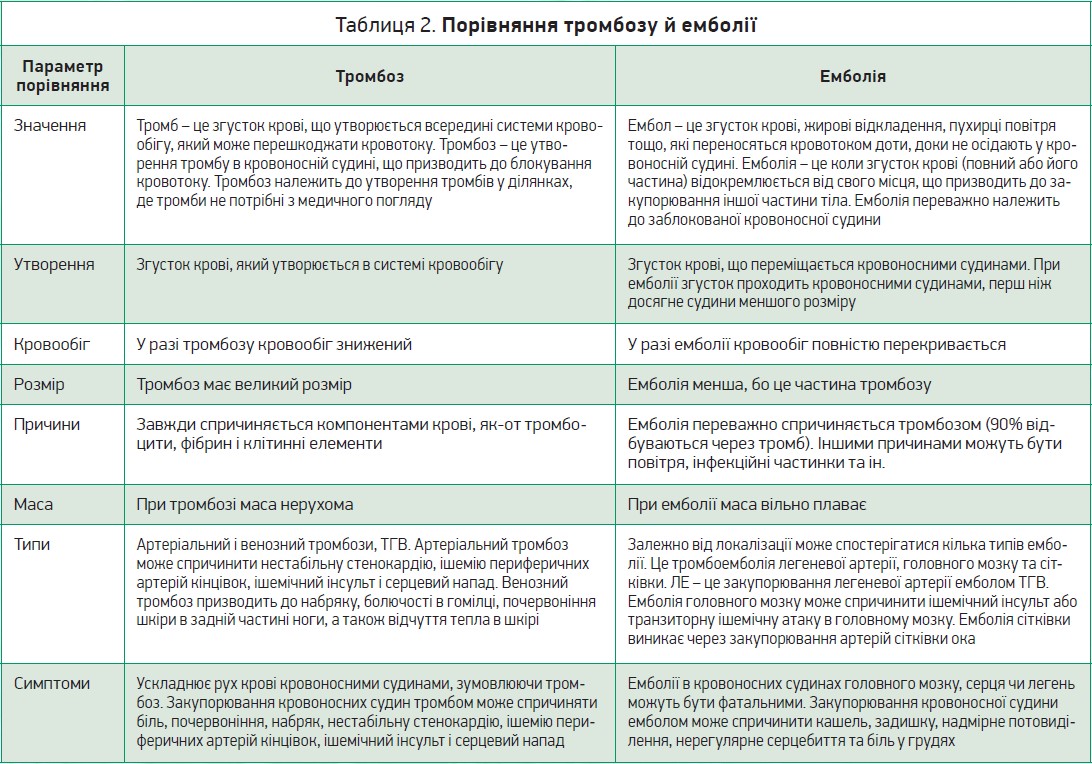
Основні відмінності тромбозу й емболії представлено в таблиці 2.
Тромбоемболія та COVID‑19
Коронавірусна хвороба (COVID‑19) залишається глобальною пандемією з 2019 року зі зростанням показників смертності та захворюваності. Кількість виявлених у світі осіб, інфікованих вірусом SARS-CoV‑2, за даними американського Університету Джонса Гопкінса, на середину січня 2022 року становила 335 424 530. При цьому зафіксовано 5 573 790 летальних випадків [23].
На початку пандемії пацієнти з COVID‑19 (особливо у відділенні інтенсивної терапії) мали збільшення часу зсідання крові або тромбоз. Це проявлялось як ТГВ чи ТЕЛА. Крім венозних тромбів також було виявлено: в пацієнтів із COVID‑19 відзначається тромбоз артерій головного мозку, що спричиняє інсульт й утворення тромбів у кровоносних судинах, які живлять серцевий м’яз. Тромбоемболічні ускладнення (ТГВ, ТЕЛА, тромбоз підшкірних вен) у період пандемії COVID‑19 набули особливої актуальності не тільки як одні з ключових чинників тяжкого перебігу та несприятливого прогнозу у хворих, але і як новий чинник ризику ВТЕ після одужання. ВТЕ є найчастішим ускладненням COVID-асоційованої коагулопатії [24-27].
Механізми розвитку гіперкоагуляції при COVID‑19
Виділяють два основні фенотипи пацієнтів із тромботичними ускладненнями при COVID‑19:
1) пацієнти зі «звичайною» ВТЕ;
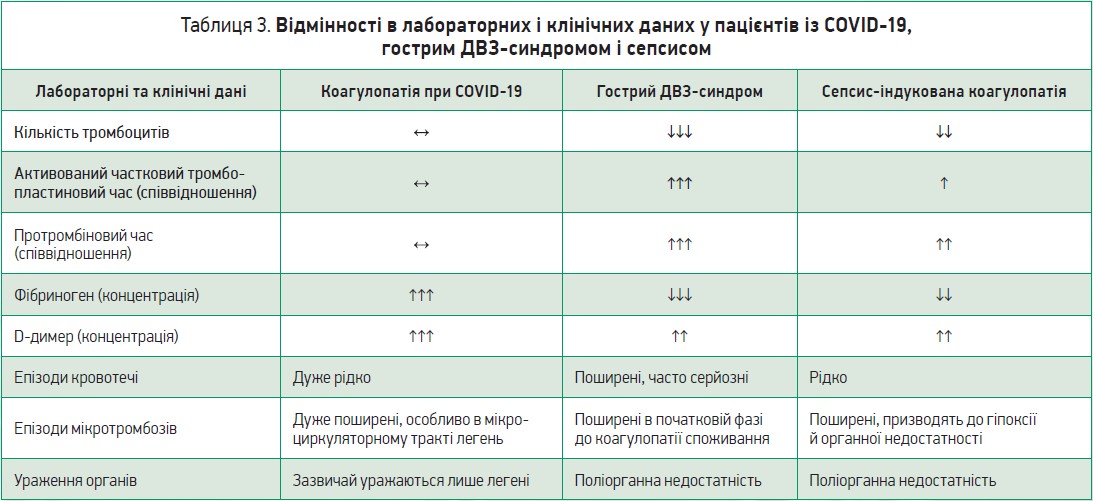
2) пацієнти з легеневим мікротромбозом, який може бути результатом локальної гіперкоагуляції. Механізми, що лежать в основі коагулопатії, індукованої COVID‑19, можуть відрізнятися від тих, що спостерігаються в пацієнтів із гострим синдромом дисемінованого внутрішньосудинного зсідання (ДВЗ) крові та сепсисом (табл. 3).
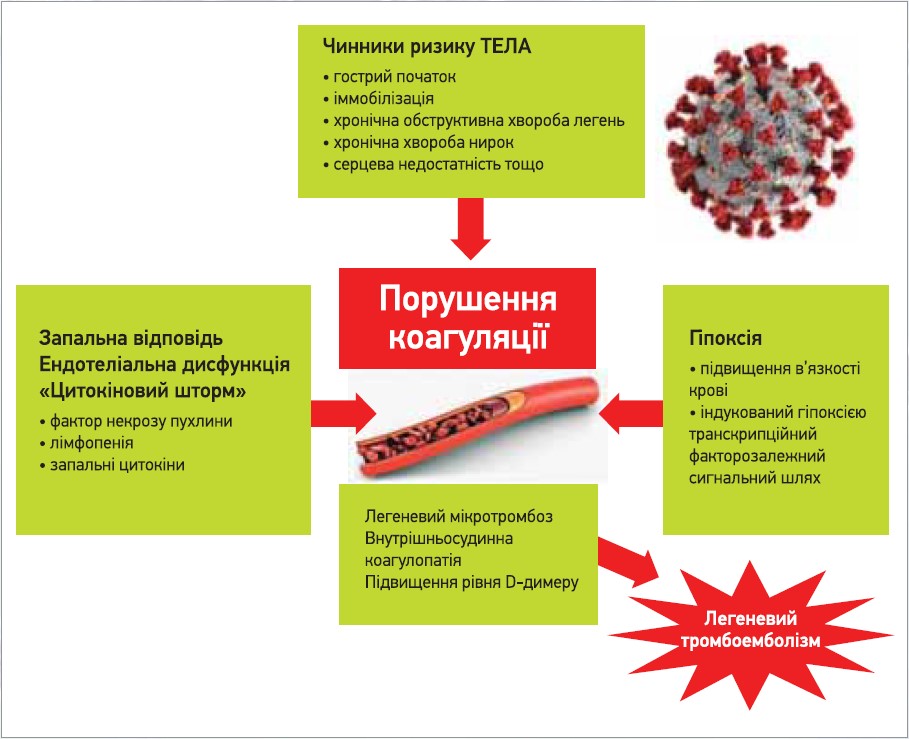
Прямі та непрямі патологічні наслідки COVID‑19, як-от тяжка гіпоксія, супутні захворювання та пов’язана з ними органна дисфункція, спричиняють порушення гемостазу [28]:
1) гіпоксія (збільшення в’язкості крові);
2) ендотеліальна дисфункція (підвищення рівня фактора фон Віллебранда, активація Toll-подібних рецепторів, тканинного фактора, комплементу, вивільнення цитокінів);
3) «цитокіновий шторм» зумовлює активацію зсідання крові, підвищуючи ризик внутрішньосудинного мікротромбозу та вторинної коагулопатії, що спричиняють виникнення тромбоемболій (рис. 2).
Рис. 2. Можливі патофізіологічні механізми, що лежать в основі порушення гемостазу в пацієнтів із COVID‑19
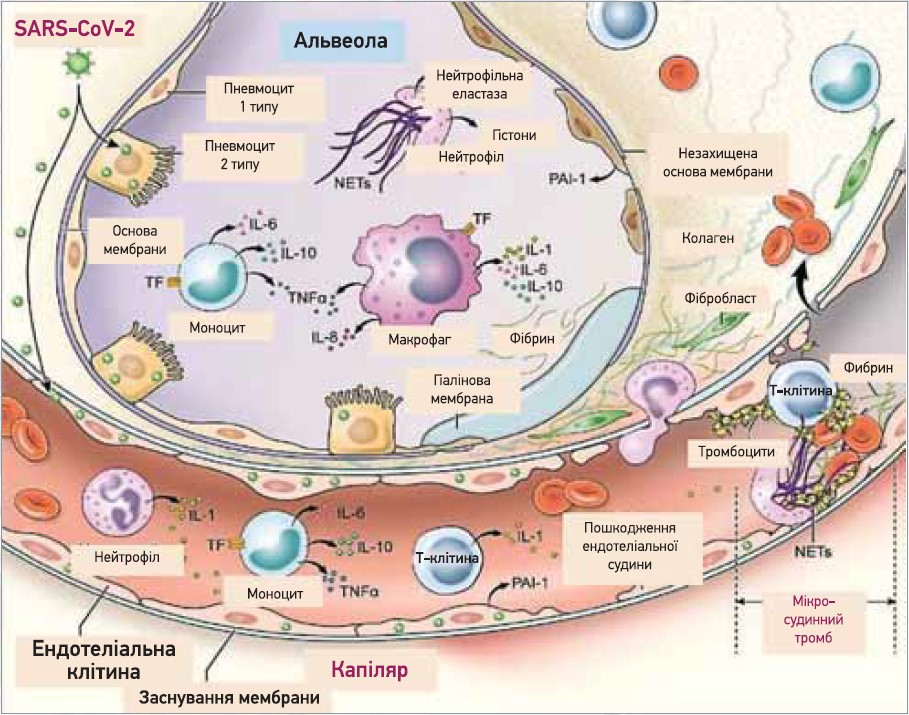
Існує кілька механізмів, за допомогою яких вірус SARS-CoV‑2 може спричиняти тромбоз мікро- та макросудин, включаючи цитокіновий шторм з активацією лейкоцитів, ендотелію та тромбоцитів. Унаслідок цього відбуваються активація тканинного фактора, утворення тромбіну та фібрину, порушення коагуляції з дисбалансом PAI‑1, інгібітора шляху тканинного фактора й активованого протеїну С, які стимулюють утворення фібрину й обмежують фібриноліз (рис. 3) [29].
Рис. 3. Механізми коагулопатії й імунної активації при COVID‑19
Висновки
Схожість між тромбом та емболом:
1) належать до згустків крові;
2) виникають усередині кровоносної системи;
3) можуть блокувати просвіт кровоносних судин.
Основні відмінності між тромбозом та емболією:
- при тромбозі тромб утворюється в кровоносній судині, котра блокує кровообіг, тоді як у разі емболії або весь згусток крові, або його частина відокремлюється від фактичного місця, що призводить до закупорювання іншої частини тіла;
- тромбоз триває кілька днів, емболія триває кілька хвилин;
- симптоми тромбозу менш серйозні на відміну від емболії;
- при тромбозі кровообіг зменшується, натомість у разі емболії кровообіг повністю припиняється;
- тромбоз більший за розміром порівняно з емболією;
- при тромбозі тромб утворюється всередині системи кровообігу, тоді як у разі емболії згусток крові проходить кровоносними судинами.
COVID‑19 супроводжується серйозними порушеннями зсідання крові, що реалізуються тромботичними епізодами в різних відділах судинного русла. Тромботичні ускладнення COVID‑19 включають ВТЕ, мікроваскулярні тромбози. Потенційний механізм полягає в пошкодженні ендотелію, гіперкоагуляції та запаленні. Тяжкий перебіг COVID‑19 істотно збільшує ризик тромбозів порівняно з іншою патологією.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 3 (520), 2022 р.
СТАТТІ ЗА ТЕМОЮ Діагностика
Еритроцити, або червоні кров’яні тільця, є найпоширенішим компонентом клітин крові, які становлять 40-45% їхнього обсягу. Плазматична мембрана еритроцитів має унікальну будову, що надає їм біологічних і механічних властивостей, необхідних для виконання специфічних функцій. Основна функція еритроцитів в організмі – це транспорт кисню, опосередкований гемоглобіном. Вони активно беруть участь як в артеріальних, так і у венозних тромбозах [1]. Гемоглобін – висококонсервативний білок, який завдяки своїй здатності зворотно зв’язувати кисень бере участь у процесах, що лежать в основі аеробного життя на планеті Земля. Головна роль цього білка полягає у підтримці клітинного гомеостазу. Однак завдяки майже 200-річним дослідженням гемоглобіну тепер відомо, що цей білок також відіграє важливу роль в інших метаболічних процесах, як-от передача сигналів у клітинах, модуляція запальної реакції, за тромбозу при гемолізі еритроцитів тощо [2-4]....
У сучасному світі онкологічні захворювання становлять чи не найбільшу загрозу життю людини, поступаючись тільки серцево-судинній патології [1]. Більшість неінфекційних хвороб людини, зокрема й онкологічні захворювання, є багатофакторними, і їх розвиток пов’язаний у тому числі з генетичними чинниками. Це, з одного боку, підвищує з віком ризик виникнення хронічних захворювань, а з іншого – дає змогу разом з лікарем розробити заходи з їх профілактики, раннього виявлення й ефективного лікування [2]....
Власна патоморфологічна лабораторія – необхідність для всіх клінік ендоскопічного, хірургічного й онкологічного профілю. Одним із видів діяльності такої лабораторії є проведення інтраопераційних досліджень. Ці дослідження виконують для визначення тактики подальшого оперативного втручання під час операції. Тому створення лабораторії на колесах, що може надавати результати патоморфологічного дослідження в будь-якому місці та ще під час операційного втручання, стало логічним рішенням для Медичної лабораторії CSD LAB, найбільшої патоморфологічної лабораторії України та Східної Європи....
Нефракціоновані (НФГ) і низькомолекулярні гепарини (НМГ) є препаратами, що широко використовуються та запобігають артеріальним і венозним тромбозам. Однак їхнє застосування також пов’язано з парадоксальною реакцією, що зумовлює потенційно небезпечний для життя протромботичний стан, результатом чого є серйозні ускладнення (гангрена, ампутація кінцівок) або фатальні наслідки. Гепарин-індукована тромбоцитопенія (ГІТ) – це імуноопосередкована відповідь на введення гепарину, який спричиняє небезпечний для життя тромбоз і є клінічно значущим негеморагічним ускладненням. ГІТ вважається потенційно загрозливим для життя станом за терапії гепарином, що спричиняє утворення нових згустків крові, а не сприяє запобіганню утворення нових тромбів. Хоча при введенні гепарину імунна реакція зустрічається досить часто (від 8 до 50%), клінічні ускладнення у разі ГІТ виникають у ≈0,2-3% пацієнтів, які приймають гепарин протягом >4 дні; частіше спостерігаються в жінок [1-3]. У цьому стані тромбоцити різко знижуються до рівня ≥20×109/л. Смертність становить 10-20%....