10 серпня, 2022
Комбінована ліпідознижувальна терапія як стратегія першої лінії у пацієнтів із дуже високим ризиком
На сьогодні доведено причинно-наслідковий зв’язок між підвищеною частотою серцево-судинних (СС) ускладнень і більшою концентрацією холестерину (ХС) ліпопротеїнів низької щільності (ЛПНЩ). Зменшення вмісту ХС ЛПНЩ стало наріжним каменем профілактики атеросклеротичних серцево-судинних захворювань (АССЗ). Якщо спеціального режиму харчування та корекції способу життя недостатньо для зниження ризику розвитку АССЗ, обов’язковим є застосування фармакологічного лікування. Зокрема, потрібний глобальний підхід із врахуванням множинних факторів ризику, як-то контроль рівня артеріального тиску та ХС ЛПНЩ. Президент EAS, професор Kausik Ray разом з іншими провідними спеціалістами* висловили свою точку зору із приводу застосування комбінованої ліпідознижувальної терапії (ЛЗТ) як стратегії першої лінії у пацієнтів із дуже високим ризиком. Пропонуємо до вашої уваги огляд роботи, опублікованої у виданні European Heart Journal (2021; 00: 1‑4).
Докази на підтвердження необхідності призначення фармакотерапії для зниження ХС ЛПНЩ
Статини вже давно зарекомендували себе як препарати першої лінії для зменшення вмісту ХС ЛПНЩ. Згідно із даними рандомізованих клінічних досліджень, в яких оцінювали статини та їх комбінацію з езетимібом або моноклональними антитілами до PCSK9, найважливішим є те, наскільки, коли і як довго досягається зниження рівня ХС ЛПНЩ, а не яким чином (Ference et al., 2017; Gencer et al., 2020). Метааналіз рандомізованих клінічних випробувань продемонстрував, що зменшення ХС ЛПНЩ на 1 ммоль/л знижує серцево-судинний (СС) ризик на 21%.
Цей висновок було підтверджено у дослідженнях із використанням менделівської рандомізації, у яких особи з мутаціями в генах, що кодують мішені ЛЗТ, мали нижчі ХС ЛПНЩ і ймовірність розвитку ССЗ (Ference et al., 2012, 2015). Отримані результати демонструють суттєвіше зниження СС-ризику (50‑55%) на 1 ммоль/л зменшення ХС ЛПНЩ, що пов’язано із кумулятивним зниженням впливу ХС ЛПНЩ протягом усього життя.
До настанови Європейського товариства кардіологів (ESC) та Європейського товариства з атеросклерозу (EAS) 2019 р. із лікування дисліпідемій увійшла рекомендація щодо необхідності подальшого зменшення ХС ЛПНЩ у хворих груп високого та дуже високого ризику на основі отриманих висновків про те, що нижчі рівні ХС ЛПНЩ є кращими за вищі та не викликають жодних небажаних ефектів (Mach et al., 2020). Для осіб із дуже високим ризиком цільове значення ХС ЛПНЩ було зменшене із 1,8 до 1,4 ммоль/л або зниження значення ХС ЛПНЩ на ≥50% від вихідного рівня.
До хворих дуже високого СС-ризику належать такі групи пацієнтів:
- із документованим атеросклерозом будь-якої локалізації (за даними коронарографії, мультиспектральної комп’ютерної томографії та інших методів досліджень);
- що перенесли інфаркт міокарда або мають в анамнезі коронарну та інші артеріальні реваскуляризації, ішемічний інсульт, захворювання периферичних артерій;
- із цукровим діабетом 2-го типу з ураженням органів-мішеней або із щонайменше трьома основними чинниками ризику або ЦД 1-го типу при ранній маніфестації та тривалістю > 20 років;
- пацієнти з тяжкою ХХН (ШКФ <30 мл/хв/1,73 м2 );
- із СС-ризиком за шкалою SCORE ≥10%;
- із сімейною гіперхолестеринемією та з АССЗ або з іншим головним ФР.
Саме для цієї когорти хворих вкрай важливим є досягнення цільових рівнів ХС ЛПНЩ, що у реальній клінічній практиці можливе лише за використання інтенсивної гіполіпідемічної терапії (Annemans et al., 2018).
Відмінності між цільовими рівнями ХС ЛПНЩ у рекомендаціях та поточній клінічній практиці
Незважаючи на те, що арсенал препаратів для зниження рівня ХС ЛПНЩ продовжує збільшуватися, досі існують значні розбіжності між цільовими показниками, зазначеними у настановах, і тими, що досягаються у реальних умовах. У дослідженні DA VINCI було показано, що більшість європейських пацієнтів з АССЗ отримували монотерапію статинами помірної (43,5%) або високої інтенсивності (37,5%). При цьому лише 9% хворих застосовували поєднання статинів з езетимібом і 1% – комбінацію, яка включала моноклональне антитіло до PCSK9 (Ray et al., 2021).
Тому й недивно, що досягнення у хворих із дуже високим ризиком цільового рівня ХС ЛПНЩ 1,4 ммоль/л, вказаного у європейських рекомендаціях 2019 р., було недостатнім. Так, цільового значення вдалося досягти лише у 22% осіб на високоінтенсивній монотерапії статинами. Отже, необхідність зміни підходів до ведення пацієнтів із гіперхолестеринемією групи дуже високого ризику для поліпшення ефективності лікування та збільшення відсотка хворих, що досягають мети терапії, є очевидною.
Дані з реєстрів, подібні до наведених вище, найдостовірніше відображають клінічні сценарії, оскільки вони взяті з рутинної практики. Таким чином, цілком імовірно, що отримані у реальних умовах результати стосовно частки пацієнтів, які досягають цільового рівня ХС ЛПНЩ, є значно гіршими за показники, наведені у поточних настановах. Дійсно, аналізи на основі бази даних виписаних рецептів у Німеччині та даних рутинної практики у Польщі продемонстрували, що лише 20% пацієнтів групи дуже високого ризику досягли цільового значення ХС ЛПНЩ <1,8 ммоль/л, зазначеного в європейських рекомендаціях 2016 р. (Fox et al., 2018; Dyrbus et al., 2019).
Серед причин недотримання рекомендацій варто виділити такі, як:
- потенційний розвиток побічних ефектів;
- недостатня інформованість пацієнтів;
- призначення складних схем терапії;
- недоступність медикаментів тощо.
Все це здатне спричинити зниження прихильності хворих до лікування (Fletcher et al., 2005).
У нещодавно проведеному дослідженні науковці порівнювали два різні цільові показники ХС ЛПНЩ (2,6 і 1,8 ммоль/л) у пацієнтів, які використовували ЛЗТ як вторинну профілактику внаслідок перенесеного ішемічного інсульту (Amarenco et al., 2020). Після медіани спостереження 3,5 років були отримані такі результати, що демонструють зниження ступеня ризику в цієї когорти хворих: серйозні СС-події спостерігалися у 8,5% хворих, котрі досягли нижчого цільового рівня ХС ЛПНЩ; серйозні СС-події мали місце у 10,9% тих, хто досяг вищого цільового значення ХС ЛПНЩ.
Таким чином, ці дані відображають зниження ризику на 22% при міжгруповій різниці середніх рівнів ХС ЛПНЩ 0,8 ммоль/л. Також вони підтверджують той факт, що у пацієнтів із дуже високим ризиком досягнення нижчого цільового ХС ЛПНЩ забезпечує суттєвіше зменшення ризику.
У цьому контексті цікавими є результати дослідження DA VINCI (Wilson et al., 2012). Із-поміж 2974 пацієнтів з АССЗ 82% мали >20% 10-річний ризик фатальних і нефатальних СС-подій за алгоритмом REACH та отримували вторинну профілактику. Середній рівень ХС ЛПНЩ в учасників становив 2,1 ммоль/л. Зменшення ХС ЛПНЩ із 2,1 ммоль/л до рекомендованого 1,4 ммоль/л у цій групі хворих дуже високого ризику привело до зниження відносного ризику на 14,7%, згідно із пропорційним зниженням ризику на 21%, пов’язаного зі зменшенням ХС ЛПНЩ на 1 ммоль/л.
Якщо припустити, що середній абсолютний СС-ризик становив 20 чи 40%, досягнення цільового показника ХС ЛПНЩ 1,4 ммоль/л сприяло запобіганню 2,9 та 5,9 СС-подій на 1 тис. осіб за рік відповідно.
Згідно з результатами обсерваційних досліджень та робіт із використанням менделівської рандомізації, можна досягти потенційно вищого ефекту, якщо тривалість ЛЗТ буде збільшено порівняно з такою у раніше проведених рандомізованих контрольованих випробуваннях.
Інтенсивна комбінована ЛЗТ як стратегія першої лінії
Наразі доступний великий вибір методів лікування, що знижують рівень ХС ЛПНЩ, проте їх впровадження досі залишається недостатнім.
Як зазначено вище, монотерапії статинами, навіть високоінтенсивної, для більшості пацієнтів із метою досягнення цільових показників ХС ЛПНЩ відповідно до рекомендацій недостатньо. Користь для СС-системи залежить лише від ступеня зниження ХС ЛПНЩ, незалежно від того, за допомогою яких лікарських засобів досягаються цільові рівні.
Тому наявний підхід до лікування потребує кардинальних змін у рутинній практиці та прагматичному мисленні. Отже, варто розглянути зміну парадигми для пацієнтів із дуже високим ризиком із підходу «стартове інтенсивне лікування статинами» на підхід «інтенсивна гіполіпідемічна терапія». Це означає, що у хворих із дуже високим ризиком рівень ХС ЛПНЩ слід знижувати ефективно, прагматично та максимально швидко.
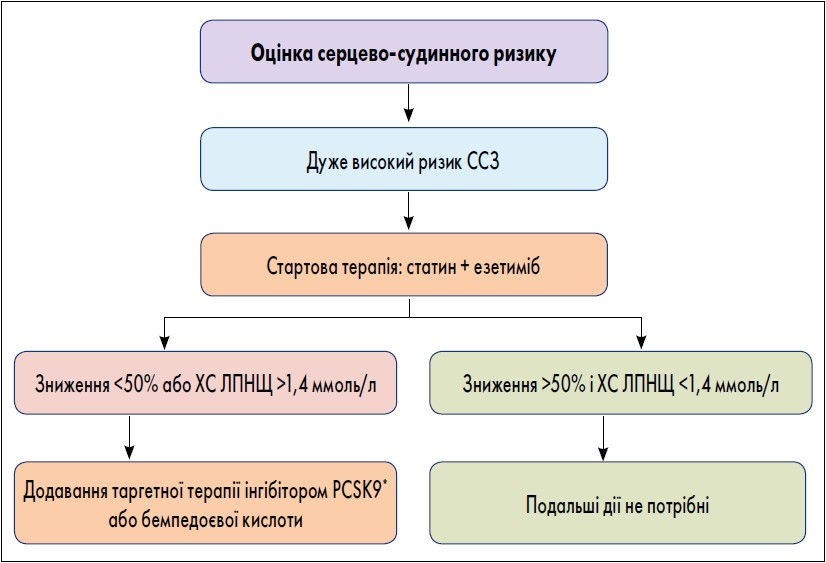
Завдяки дослідженням ЛЗТ, проведеним за останнє десятиліття, вдалося виконувати точну кількісну оцінку очікуваного середнього зниження ХС ЛПНЩ. Так, статинотерапія середньої інтенсивності дає змогу в середньому знизити рівень ХС ЛПНЩ на 30%, високої інтенсивності – на 50%, статинотерапія високої інтенсивності плюс інгібітор абсорбції холестерину (езетиміб) на 65%. Це дозволяє надійно прогнозувати контроль ХС ЛПНЩ за допомогою спрощеного алгоритму лікування пацієнтів із дуже високим ризиком (рисунок).
Рисунок. Спрощений алгоритм комбінованої ЛЗТ у хворих на АССЗ із дуже високим ризиком
Примітка. * Таргетна терапія інгібітором PCSK9 = моноклональні антитіла до PCSK9 (алірокумаб чи еволокумаб) або терапія малою інтерферувальною РНК (siRNA), що пригнічує експресію гена, який кодує PCSK9 (інклізиран). Доступність терапії бемпедоєвою кислотою та siRNA PCSK9 може варіювати в різних країнах.
Першим кроком для хворих із дуже високим ризиком може бути стартова комбінована терапія статинами та езетимібом з метою досягнення цільових рівнів ХС ЛПНЩ на ранній стадії як практичний стандарт лікування. Якщо пацієнти не досягають зазначеного у європейських рекомендаціях 2019 р. цільового показника ХС ЛПНЩ (<1,4 ммоль/л або зменшення ≥50%), доцільно додати третій компонент ЛЗТ.
Оскільки відносна користь від додаткового зниження рівня ХС ЛПНЩ становить половину впродовж першого року лікування порівняно з наступними, логічно, що з метою отримання більших переваг для СС-системи протягом першого року після інфаркту міокарда потрібно досягти суттєвішого абсолютного зменшення вмісту ХС ЛПНЩ.
Висновки
Здобутки у пошуку стратегій лікування для зниження рівня ХС ЛПНЩ дозволяють клініцистам досягати цільових значень ХС ЛПНЩ у пацієнтів навіть із дуже високим ризиком, не обмежуючись певним класом лікарських засобів. Дійсно, зменшення ХС ЛПНЩ, а не дія препарату, що приводить до цього, є основним фактором зниження СС-ризику.
Тож слід відійти від тактики «високоінтенсивної статинотерапії» та «парадигми очікування і спостереження» і замість цього одразу призначати всім пацієнтам із дуже високим та надзвичайно високим ризиком комбіновану терапію статин + езетиміб як основний стандарт лікування. Це може сприяти значному поліпшенню здоров’я населення у Європі.
Довідка «ЗУ»
Комбіноване застосування статинів та езетимібу – яскравий приклад синергічної дії двох препаратів, що впливають на різні ланки розвитку гіперхолестеринемії. Відомо, що на тлі приймання статинів відбувається пригнічення активності ГМГ-КоА-редуктази, що зумовлює низку послідовних реакцій, внаслідок яких спостерігаються зниження внутрішньоклітинного вмісту ХС, компенсаторне підвищення активності ЛПНЩ-рецепторів і, відповідно, прискорення катаболізму ХС ЛПНЩ.
За принципом зворотного зв’язку, якщо у клітинах знижується концентрація ХС, компенсаторно може зрости абсорбція ХС у кишечнику, який поступає з їжею або жовчними кислотами. Езетиміб накопичується в епітелії тонкого кишечника, де селективно пригнічує інтестинальну абсорбцію ХС та відповідних рослинних стеролів.
Молекулярною мішенню езетимібу є переносник стеролів – білок Niemann-Pick Cl-Like 1, що відповідає за всмоктування ХС та фітостеролів у кишечнику. Препарат розповсюджується на щітковій смужці тонкої кишки, пригнічує абсорбцію ХС і таким чином зменшує доставку інтестинального ХС до печінки. Як наслідок, комбінація статинів та езетимібу дозволяє знизити рівень ХС ЛПНЩ на 65% від початкового.
На даний час на вітчизняному фармацевтичному ринку представлений комбінований препарат Розуліп® Плюс, який випускається у двох комбінаціях – 10 мг розувастатину / 10 мг езетимібу та 20 мг розувастатину / 10 мг езетимібу. Застосування цього лікарського засобу дозволяє не тільки оптимізувати рівень ХС ЛНПЩ у крові, але й забезпечити кращу прихильність до лікування та поліпшити прогноз у пацієнтів груп високого і дуже високого СС-ризику.
* K.K. Ray1, L.F. Reeskamp2, U. Laufs3, M. Banach4, F. Mach5, L.S. Tokgozoglu6, D.L. Connolly7, A.J. Gerrits8, E.S.G. Stroes2, L. Masana9, J.J.P. Kastelein2; 1 Імперський центр профілактики серцево-судинних захворювань, Відділення первинної медичної допомоги та громадського здоров’я, Школа громадського здоров’я, Імперський коледж Лондона, Велика Британія; 2 Кафедра судинної медицини, Медичні центри Амстердамського університету, Нідерланди; 3 Університетська лікарня Лейпцига, Німеччина; 4 Кафедра артеріальної гіпертензії, Лодзинський медичний університет, Польща; 5 Відділення кардіології, Женевська університетська лікарня, Швейцарія; 6 Відділення кардіології, Медичний факультет Університету Хаджеттепе, Анкара, Туреччина; 7 Відділення кардіології, Лікарні Сендвела й Західного Бірмінгема NHS Trust, Інститут серцево-судинних наук, Бірмінгемський Університет, Велика Британія; 8 MEDCON International, Нідерланди; 9 Відділення судинної медицини та метаболізму, Відділення дослідження ліпідів та атеросклерозу, Університетська клініка Сант Жоан, Університет Ровіра та Віргілі, Іспанія.
Підготувала Олена Коробка