17 жовтня, 2022
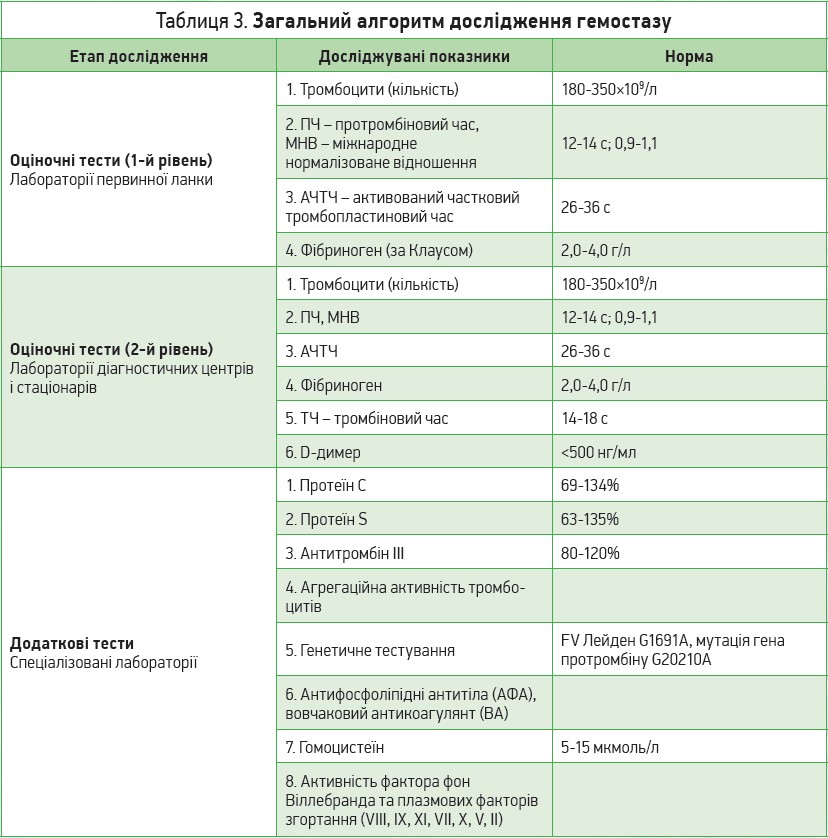
Алгоритми лабораторної діагностики порушень у системі гемостазу
Продовження. Початок у № 9 (526), 2022 р. >>
Вовчаковий антикоагулянт
Використовують 2 різні за принципом фосфоліпід-залежні тести:
1) dRVVT (час згортання з отрутою гадюки Рассела);
2) чутливий АЧТЧ‑тест (час зсідання з кремнієвим активатором). Вовчаковий антикоагулянт слід розглядати як позитивний, якщо щонайменше 1 із 2 тестів надає позитивний результат. Каолін не рекомендовано для використання як активатор через наявність інтерференції з фотооптичними аналізаторами, а елагову кислоту не застосовують через низьку чутливість до вовчакового антикоагулянту.
Антифосфоліпідні антитіла
1. Наявність антитіл до кардіоліпіну IgG та/або IgM ізотипу в сироватці в середньому чи високому титрі в ≥2 вимірах з інтервалом не менше 12 тиж.
2. Наявність антитіл до β2-глікопротеїну I ізотипів IgG та/або IgM ізотипу в сироватці у високому титрі ≥2 вимірах з інтервалом не менше 12 тиж.
Ізольоване подовження протромбінового часу (дефіцит фактора VII)
Протромбіновий час є способом оцінки дефіциту факторів протромбінового комплексу чи зовнішнього згортання. Результати тесту залежать від змісту факторів II, V, VII та X.
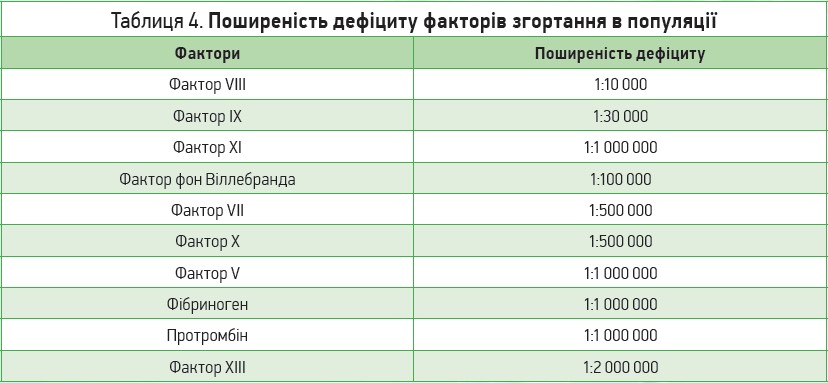
У деяких випадках спостерігається ізольована недостатність фактора VII, яка може бути набутою або вродженою, що зумовлює збільшення протромбінового часу. Набутий дефіцит фактора VII є досить рідкісною патологією і здебільшого пов’язаний зі злоякісними пухлинами, сепсисом та/або трансплантацією кісткового мозку. В деяких випадках лабораторні дані підтверджують вироблення автоантитіл, які можуть нейтралізувати активність фактора VII або прискорити його кліренс. Вроджений дефіцит фактора VII має встановлену поширеність 1:500 000 і часто його можна знайти випадково. Пацієнти можуть не відчувати симптомів і не мати спонтанних суглобових та церебральних крововиливів. Ускладнені кровотечі зазвичай з’являються в гомозиготних та гетерозиготних індивідуумів на відміну від дефіциту факторів VIII та IX. Ступінь дефіциту фактора VII погано корелює зі схильністю до кровотеч.
Діагностика тромбоемболічних станів
Складнішим і комплексним завданням є визначення причин венозного та артеріального тромбозу чи невиношування вагітності. Наразі перше місце серед причин смертності посідають захворювання, в патогенезі яких велику роль відіграє стан гіперкоагуляції; у >50% пацієнтів у світі безпосередньою причиною смерті є тромбоз (гострий інфаркт міокарда, ішемічний інсульт, тромбоемболія легеневої артерії, онкотромбоз тощо) На жаль, у цьому випадку скринінгові тести не є інформативними, при цьому результати коагуляційних тестів, що рутинно використовуються, для визначення АЧТЧ і ПЧ найчастіше залишаються незмінними навіть за розвитку тромбозу.
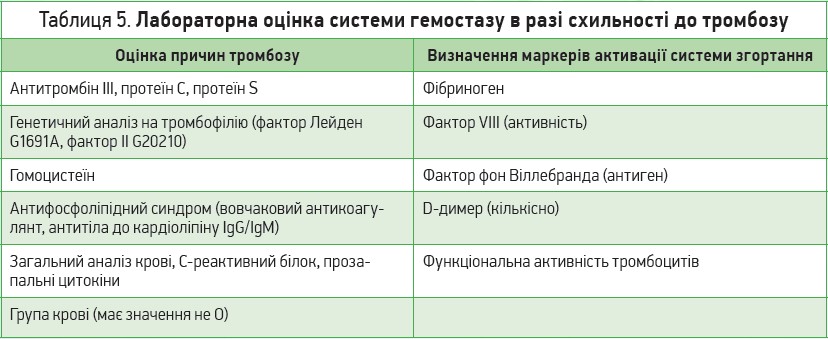
Відповідно до клінічної ситуації мають бути зроблені кроки з дослідження маркерів активації згортання, гіперактивності тромбоцитів, спрямованого пошуку спадкової тромбофілії, антифосфоліпідного синдрому, визначення гомоцистеїну (табл. 5). Якщо тромбоемболічних ускладнень немає, але передбачається їх високий ризик, рівень ризику оцінюється здебільшого клінічно відповідно до діагнозу, за сімейним та індивідуальним анамнезом і може бути доповнений лабораторними даними.
Клінічні предиктори схильності до тромбоутворення:
→ повторні епізоди тромбозу глибоких вен, ТЕЛА, гострий інфаркт міокарда тощо;
→ венозний стаз (вагітність, іммобілізація, варикоз, хвороба вен тощо);
→ васкуліти, рак, мієлопроліферативні захворювання;
→ прийом оральних контрацептивів, тривале введення гепарину.
Лабораторні предиктори тромбозу:
• тромбоцитоз (>600×109/л);
• виражена гіперфібриногенемія (6-8 г/л);
• наявність вовчакового антикоагулянту й антитіл до кардіоліпіну;
• дефіцит АТ III, протеїну С, протеїну S;
• збільшення активності фактора VIII;
• тромбогенні мутації G1691A, G20210A.
Важливо зазначити те, що дослідження окремих факторів, як-от концентрація фібриногену, активності фактора VIII і фактора фон Віллебранда, а також активності природних антикоагулянтів (АТ III, протеїнів С і S) може виявити відхилення від референтного інтервалу, але не дозволить судити про наявність гіперкоагуляції загалом. Пояснюється це тим, що зміни окремих компонентів системи згортання крові можуть бути нівельовані в організмі включенням компенсаторних механізмів; саме тому дослідження окремих маркерів коагуляції може надати лише непряму оцінку тромбінемії. Наразі в світі широко застосовують нові методи дослідження системи гемостазу (глобальні тести), як-от тромбоеластографія, тест тромбодинаміки, тест генерації тромбіну.
Висновки
Значимість лабораторної оцінки стану системи гемостазу в сучасній клінічній практиці складно переоцінити. Основна причина цього полягає у найважливішій патофізіологічній ролі, яку відіграє гемостатичний баланс у розвитку ускладнень різних захворювань. Лабораторні дані дослідження системи згортання необхідні насамперед пацієнтам, які перенесли травму, крововтрату, котрі готуються до стаціонарних і амбулаторних хірургічних втручань, приймають антикоагулянти, замісну терапію, страждають на серцево-судинні захворювання, вагітним, із вродженими чи набутими порушеннями згортання. На підставі отриманих результатів у пацієнтів із геморагічним епізодом в анамнезі чи з ризиком розвитку тромбозу лікар-клініцист приймає подальші важливі рішення від установлення діагнозу до обрання характеру терапії.
Медична газета «Здоров’я України 21 сторіччя» № 10 (527), 2022 р.