В последние годы методы лечения больных с метастатической меланомой претерпели изменения в связи с внедрением ингибиторов иммунных чекпоинтов и разработкой терапии, направленной на MAP-киназный сигнальный путь (MAPK). Ингибиторы чекпоинтов блокируют протеины CTLA‑4 и PD‑1 на цитотоксических Т-клетках или раковых клетках, тем самым реактивируя системный иммунный ответ, направленный против опухолевых клеток. Ипилимумаб, антитело против CTLA‑4, был первым ингибитором чекпоинтов, одобренным для применения в терапии пациентов с меланомой. В контролируемых исследованиях ипилимумаб продемонстрировал стабильную активность против меланомы как у пациентов после проведенной химиотерапии (ХТ), так и у больных, ранее не получавших лечения. На основании рандомизированных исследований, показавших улучшение результатов по сравнению с монотерапией ипилимумабом, недавно были одобрены два новых направленных на PD‑1 ингибитора иммунных чекпоинтов – пембролизумаб и ниволумаб.
Дисрегуляция, ассоциированная с мутацией BRAF в сигнальном пути MAPK, является ключевым фактором при метастатической меланоме. Два ингибитора белка BRAF, вемурафениб и дабрафениб, были одобрены для лечения пациентов с неоперабельной меланомой IIIC или IV стадии и мутацией BRAF. Результатами рандомизированных контролируемых исследований BRIM‑3 и BREAK‑3 было подтверждено, что, по сравнению с дакарбазином, в первой линии терапии эти препараты продемонстрировали лучшие результаты у пациентов с неоперабельной или метастатической меланомой при наличии мутации BRAF V600. Траметиниб является сильнодействующим и селективным мелкомолекулярным ингибитором MEK-киназы, которая активируется геном BRAF в сигнальном пути MAPK. Траметиниб эффективен как у пациентов с неоперабельной или метастатической меланомой при наличии мутации BRAF V600 после проведения ХТ, так и у тех, кто ранее не получал лечения. Эти результаты позволили лучше понять механизмы резистентности к таргетной терапии и изучить комбинированные подходы к лечению.
Эффективность и безопасность комбинированной терапии дабрафенибом и траметинибом оценивались в двух исследованиях ІІІ фазы – COMBI-d и COMBI-v, а также ІІ фазы – BRF113220. Результаты этих исследований продемонстрировали, что применение дабрафениба в сочетании с траметинибом увеличивает выживаемость без прогрессирования (ВБП) и общую выживаемость (ОВ) по сравнению с монотерапией дабрафенибом или монотерапией вемурафенибом у ранее не леченных пациентов с неоперабельной или метастатической меланомой и мутацией BRAF V600.
Был проведен сетевой метаанализ отношения рисков (ОР) для ВБП и ОВ, о которых сообщалось в рандомизированных контролируемых исследованиях по применению первой линии терапии у пациентов с распространенной или метастатической меланомой при наличии мутации BRAF. Метаанализ был ограничен препаратами и их комбинациями, которые были одобрены Министерством здравоохранения Канады по состоянию на февраль 2015 г. для применения в терапии первой линии у пациентов с метастатической меланомой, а именно: дабрафениб в сочетании с траметинибом, дабрафениб, вемурафениб, траметиниб, ипилимумаб и дакарбазин. Ниволумаб, пембролизумаб и кобиметиниб в сочетании с вемурафенибом в анализ не включались, поскольку не были одобрены на момент его проведения.
Данные включенных в анализ исследований были взяты из двух систематических обзоров литературы. Первый обзор проводился для оценки эффективности, безопасности и переносимости монотерапии дабрафенибом и траметинибом по сравнению с другими препаратами первой линии терапии пациентов с неоперабельной распространенной или метастатической меланомой. Первый обзор включал данные рандомизированных и нерандомизированных исследований по применению дабрафениба, траметиниба, дакарбазина, ипилимумаба, вемурафениба, фотемустина и темозоломида, опубликованные до октября 2012 г. Было выявлено 123 исследования, соответствовавших всем критериям включения, из которых 24 – рандомизированные исследования пациентов, ранее не получавших лечение.
Во втором обзоре оценивалась эффективность и безопасность комбинированного лечения дабрафенибом и траметинибом по сравнению с другими препаратами первой или второй линии терапии (вемурафениб + кобиметиниб, монотерапия дабрафенибом, траметинибом, вемурафенибом, ипилимумабом, ниволумабом и пембролизумабом) у пациентов с неоперабельной или метастатической меланомой. Все проанализированные данные были опубликованы до октября 2015 г., в общей сложности отобрано 12 рандомизированных контролируемых исследований по применению одного или нескольких видов лечения.
Объединенные результаты этих двух обзоров и данные семи исследований с участием ранее не леченных пациентов, получавших любой из одобренных на момент анализа препаратов (COMBI-d, BRF113220, COMBI-v, BREAK‑3, BRIM‑3, METRIC и CA184-024), позволили сравнить ВБП и ОВ на фоне терапии дабрафенибом и траметинибом и другими препаратами. Данные об ОР для ВБП и ОВ были основаны на анализе самых последних доступных данных.
Оценка ОР проводилась при помощи байесовского сетевого метаанализа с использованием WinBUGS1.4.3 с входными данными в виде логарифмически преобразованного ОР из каждого исследования и соответствующих стандартных ошибок. При каждом сравнении логарифмы ОР для ВБП и ОВ оценивались с использованием многомерного и одномерного сетевого метаанализа.
Многомерный сетевой метаанализ включал одновременно корреляцию ОР для ВБП и ОВ. Использование этого подхода является разумным с учетом высокой корреляции между лечебным эффектом и ВБП и ОВ при метастатической меланоме.
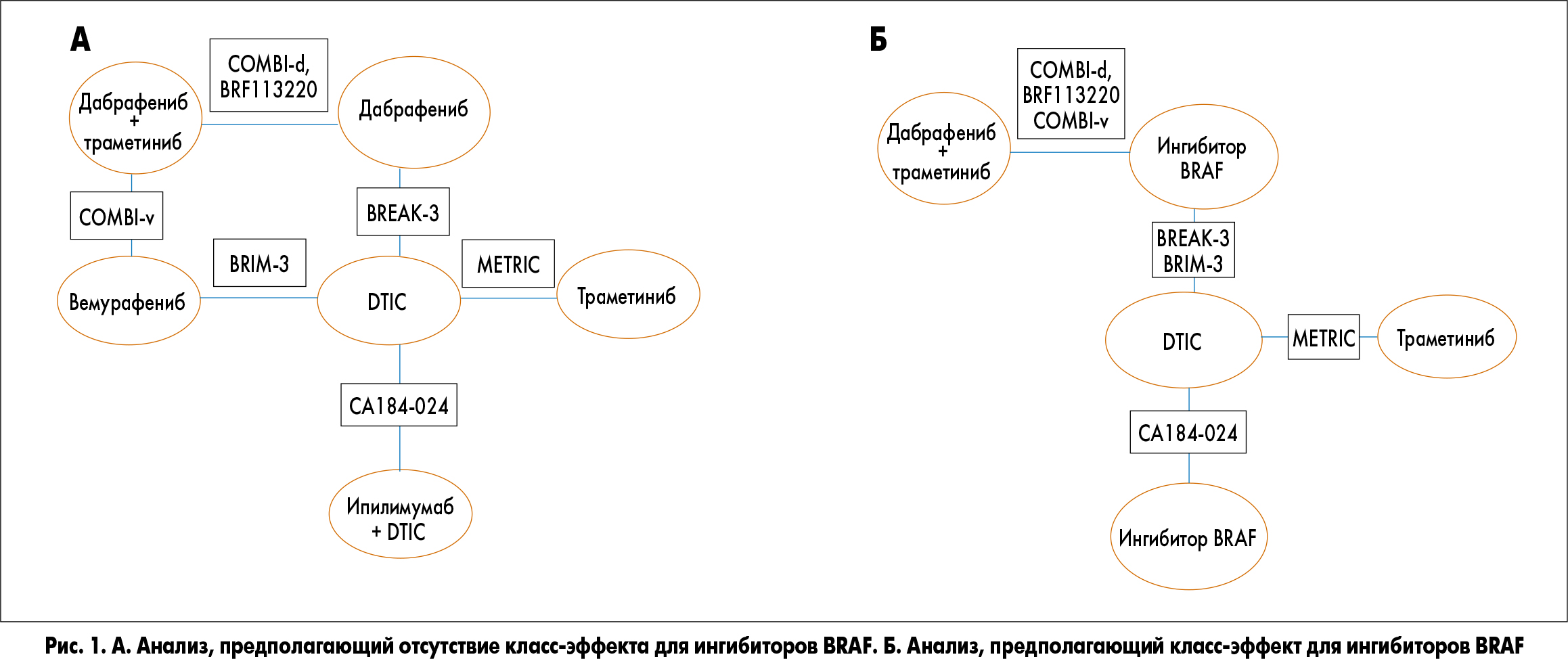
Были выполнены две серии анализов. В одной из них предполагалось отсутствие класс-эффекта, т.е. возможность разного влияния дабрафениба и вемурафениба на ВБП и ОВ, а показатели ОР для дабрафениба и вемурафениба оценивались отдельно. В другой серии предполагалось наличие класс-эффекта, т.е. отсутствие разницы между дабрафенибом и вемурафенибом в воздействии на ВБП и ОВ. В этом анализе рассчитывались ОР для других препаратов в сравнении с монотерапией ингибитором BRAF. Он позволил объединить данные о ВБП и ОВ, полученные в ходе исследований COMBI-d, COMBI-v и BRF113220, что значительно повысило точность сравнений. Оба анализа проводились с поочередным включением и исключением исследования BRF113220. Многомерный сетевой метаанализ (показатель ОР для ВБП и ОВ оценивался одновременно с учетом корреляции) проводился с поочередным включением в анализ и исключением из него траметиниба, сочетания ипилимумаба и дакарбазина, что позволило определить вероятность того, что корреляция между воздействием на ОВ и ВБП зависит от класса препарата.
Диаграммы анализа ВБП и ОВ, предполагающего отсутствие класс-эффекта для ингибиторов BRAF, и анализа, предполагающего класс-эффект для ингибитора BRAF, показаны соответственно на рис. 1А и 1Б. В последнем анализе объединены данные относительно ОР для ВБП и OВ при сравнении дабрафениба в комбинации с траметинибом и монотерапии ингибитором BRAF в исследованиях COMB-v, COMBI-d и BRF113220, а также ОР для монотерапии ингибитором BRAF в сравнении с DTIC в исследованиях BREAK‑3 и BRIM-3.
Средний возраст пациентов составил от 49 лет (BRF113220, дабрафениб + траметиниб 1 мг) до 58 лет (BRF113220, дабрафениб + траметиниб 2 мг). Количество пациентов мужского пола варьировалось от 49% (METRIC, дакарбазин) до 63% (BRF113220, дабрафениб + траметиниб 2 мг). Количество пациентов с функциональным статусом по шкале ECOG >0 колебалось от 25% (COMBI-d, дабрафениб + траметиниб) до 37% (BRF113220, дабрафениб). Стадия M1C при постановке диагноза составила от 55% (CA184-024, дакарбазин) до 70% (BRF113220, дабрафениб + траметиниб 2 мг). Повышенный уровень лактатдегидрогеназы (ЛДГ) наблюдался в промежутке от 30% (BREAK‑3, DTIC) до 58% (BRIM‑3, DTIC) случаев.
Показатели ОР для ВБП в контрольной группе и группе исследования были статистически значимыми. Показатель ОР для ОВ для группы исследования по сравнению с контрольной группой был статистически значимым в исследованиях COMBI-v, COMBI-d, BRIM‑3 и CA184-024. Стоит отметить, что ОР для ОВ в исследованиях BREAK‑3, BRIM‑3, METRIC и BRF113220 основаны на анализе RPSFT, который необходим для перехода от контрольных исследований к активной терапии (рис. 2).
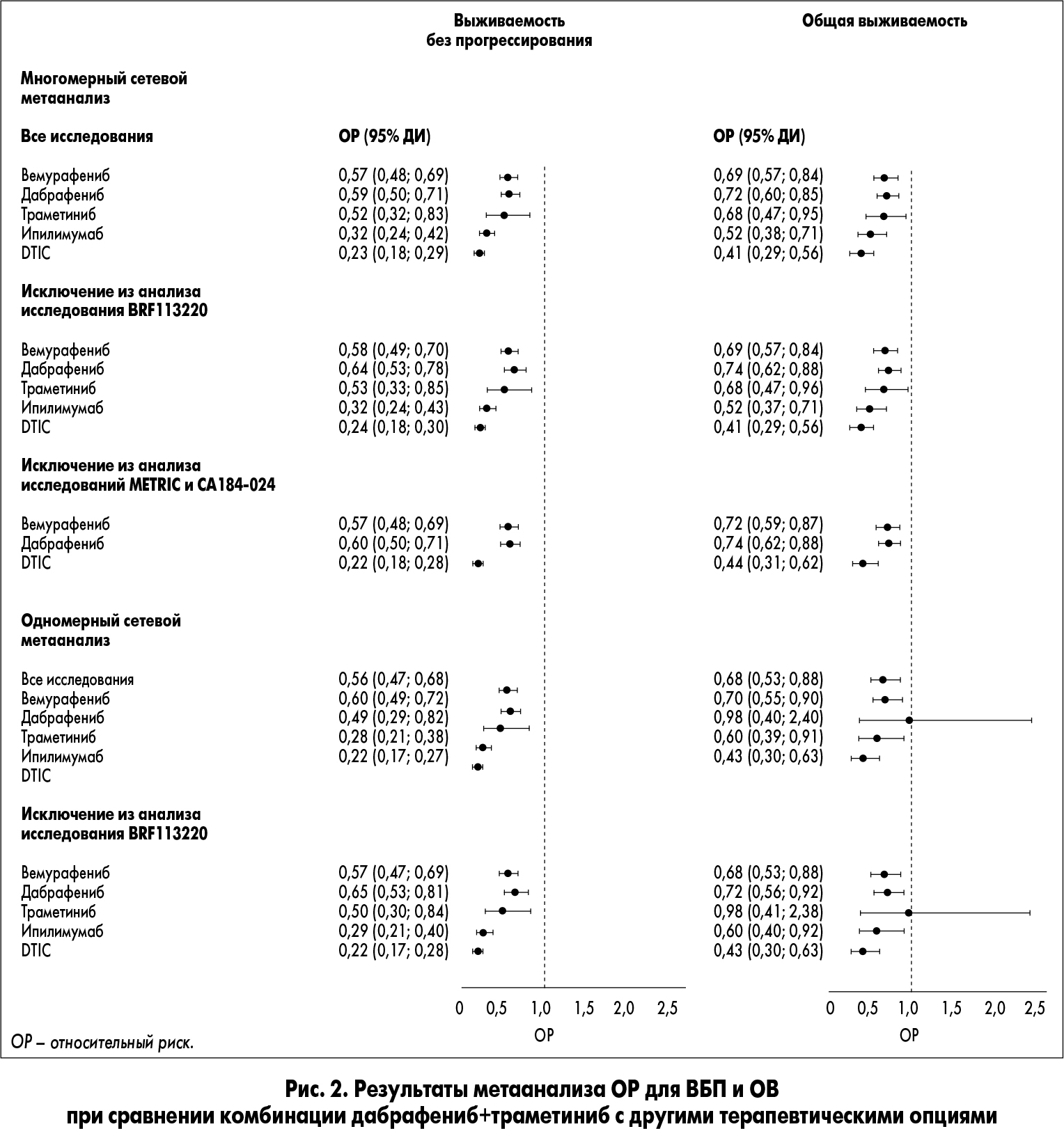
По результатам сетевого метаанализа в отношении ОР для ВБП и ОВ, предполагающего отсутствие класс-эффекта для ингибиторов BRAF, показатель ОР (95% доверительный интервал – ДИ) в различных исследованиях для ВБП подтвердил преимущество применения сочетания дабрафениб + траметиниб: 0,23 при сравнении с терапией дакарбазином, 0,32 – ипилимумабом + дакарбазином, 0,52 – траметинибом, 0,57 – вемурафенибом и 0,59 – дабрафенибом. Показатель ОР (95% ДИ) для OВ также был в пользу применения сочетания дабрафениб + траметиниб: 0,41 при сравнении с терапией дакарбазином, 0,52 – ипилимумабом + дакарбазином, 0,68 – траметинибом, 0,69 – вемурафенибом и 0,72 – дабрафенибом.
Результаты были аналогичными, когда из анализа исключили исследование II фазы BRF113220. Исключение сочетания ипилимумаба с дакарбазином и траметиниба из анализа незначительно повлияло на ОР. Когда оценка ОР для ВБП и ОВ проводилась отдельно, с использованием одномерного анализа, благоприятное воздействие на ОВ дабрафениба и траметиниба было меньше по сравнению с оценкой при многомерном анализе, в котором одновременно оценивались ОР для ВБП и ОВ.
Результаты сетевого метаанализа ОР для ВБП и ОВ при анализе, предполагающем класс-эффект для ингибиторов BRAF, в целом аналогичны результатам анализа, в котором оценивались отдельные данные относительно ОР для монотерапии дабрафенибом и вемурафенибом. Когда в метаанализ были включены все исследования и методы лечения, показатели ОР для ВБП и ОВ при комбинированной терапии дабрафенибом и траметинибом оказались значительно <1 по сравнению с другими терапевтическими режимами.
Отсутствие гетерогенности в отношении показателя ОВ выявлено во всех исследованиях – показатель I2 был равен 0%. Для ВБП значительная гетерогенность эффектов лечения наблюдалась только при сравнении комбинированной терапии препаратами дабрафениб + траметиниб с монотерапией дабрафенибом в исследованиях COMBI-d и BRF113220 – I2 = 74,2%. При включении в анализ данных COMBI-V гетерогенность остается повышенной, но падает ниже порога значимости – I2 = 53,9%. Не было выявлено гетерогенности при сравнении монотерапии ингибиторами BRAF и дакарбазином на основе исследований BREAK‑3 и BRIM‑3 – I2 = 0%.
Сетевой метаанализ ОР дал возможность оценить показатели ВБП и ОВ на фоне комбинированного лечения дабрафенибом + траметинибом по сравнению с другими препаратами первой линии терапии у пациентов с метастатической меланомой при наличии мутации BRAF, а также провести экономическую оценку применения данного сочетания в качестве терапии первой линии при метастатической меланоме. Результаты этого анализа позволяют предположить, что сочетание дабрафениб + траметиниб демонстрирует улучшенную ВБП и ОВ по сравнению с другими препаратами первой линии терапии. Кроме того, результаты данной комбинированной терапии были лучше по сравнению с траметинибом и сочетанием ипилимумаба с дакарбазином при многомерном анализе, который позволяет учесть корреляционную связь между проведенной терапией и одновременно ОР для показателей ВБП и ОВ по сравнению с традиционным одномерным анализом, когда ОР для показателей ВБП и ОВ оценивается отдельно. Результаты были в целом сходны в случаях, когда предполагался класс-эффект для ВБП и ОВ при монотерапии ингибитором BRAF и когда предполагалось его отсутствие. Результаты также были сходными при включении в анализ исследования BRF113220 и его исключении из анализа.
Прицельный поиск выявил несколько сетевых метаанализов, посвященных эффективности методов лечения пациентов с метастатической меланомой. В двух из них сравнивалась эффективность ХТ и интерферона. В одном из исследований проводилось сравнение эффективности ипилимумаба и иммунотерапии, ХТ и биохимиотерапии, но не рассматривались ингибиторы BRAF или MEK.
К. Srivastava и соавт. провели системный обзор и косвенное сравнение дабрафениба или траметиниба в качестве монотерапии с другими методами лечения у ранее не леченных пациентов с метастатической меланомой, однако это исследование не включало комбинированную терапию BRAF + MEK. Найдено только одно исследование, в котором изучалась эффективность дабрафениба в сочетании с траметинибом. В этом исследовании R. Mai и соавт. сравнили комбинацию ингибиторов BRAF+MEK с монотерапией ингибитором BRAF, монотерапией ингибитором MEK, ингибиторы BRAF + ХТ и ингибиторы MEK + ХТ, в исследовании не учитывался ипилимумаб. Авторы сообщили, что комбинированное ингибирование BRAF + MEK значительно увеличивает ВБП по сравнению с ингибированием только BRAF (ОР 0,58; ДИ 95%) и только MEK (ОР 0,29; ДИ 95%). Аналогичные результаты были получены для ОВ, комбинированное ингибирование BRAF и MEK показало лучшие результаты в сравнении с ингибированием только BRAF (ОР 0,67; 95% ДИ 0,56-0,81; p=0,0001) и в сравнении с ингибированием MEK (ОР 0,48; 95% ДИ 0,36-0,65; p=0,0001).
Следует отметить ограничения этого исследования. Возможно, самое главное – в данном анализе не были рассмотрены новые иммунотерапевтические препараты, такие как ниволумаб и пембролизумаб, или сочетание вемурафениба с ингибитором МЕК кобиметинибом, так как на момент исследования они не были одобрены к применению. В дальнейшем метаанализ следует проводить с учетом этих новых методов лечения.
Неоднородность в группах пациентов, дизайне исследований и продолжительности наблюдения могла повлиять на эффект от терапии и привести к искажению результатов во время сравнения. Например, исследования COMBI-d и CA184-024 были двойными слепыми, тогда как другие исследования были открытыми. В исследование CA184-024 вошли пациенты как с мутацией BRAF, так и с диким типом BRAF. Учитывая небольшое количество исследований, оценить влияние этих различий на результаты не представляется возможным.
В данном анализе показатель ОР был использован как мера эффективности лечения. Использование ОР требует предположения о соотношении рисков, которое может не соблюдаться во всех исследованиях, включенных в метаанализ. М. Ouwens и соавт. описали подход к проведению сетевого метаанализа по параметрическим распределениям выживаемости, который учитывает ограничения при проведении анализа на основе ОР; данная методика, хотя и требует доработки, все же является потенциально важной для будущих исследований.
В Северной Америке и Европе для ипилимумаба утверждена доза 3 мг/кг 1 раз в 3 недели. Однако систематические обзоры литературы не выявили каких-либо контролируемых исследований монотерапии ипилимумабом и дакарбазином в подобной дозе. Соответственно, был проведен анализ ОР для ВБП и ОВ при терапии ипилимумабом 10 мг/кг и дакарбазином против монотерапии дакарбазином по данным исследования CA184-024. Использование результатов этого анализа для оценки относительной эффективности монотерапии ипилимумабом в дозировке 3 мг/кг в сравнении с другими препаратами требует предположений, что влияние на ВБП и ОВ при использовании дозировок 10 и 3 мг/кг отсутствует, а также что включение дакарбазина в схему лечения ипилимумабом не влияет на его исход. Данные о влиянии добавления дакарбазина к терапии ипилимумабом на ее эффективность ограниченны и неубедительны. В открытом исследовании II фазы MDX010-08 ипилимумаб в дозировке 3 мг/кг в сочетании с дакарбазином демонстрирует лучший ответ на терапию, а также увеличение ВБП и ОВ по сравнению с монотерапией ипилимумабом (3 мг/кг) среди 76 пациентов с метастатической меланомой, ранее получавших лечение. Однако эти результаты неубедительны, учитывая небольшую выборку. Медиана ВБП составляла 99 и 85 дней, а медиана ОВ – 14,3 и 11,4 мес в группах моно- и комбинированной терапии соответственно.
Предположение о том, что эффективность ипилимумаба в дозе 10 мг/кг эквивалентна 3 мг/кг, было рассмотрено в исследовании CA184-004 с участием 101 пациента с ранее не леченной меланомой. В одной группе пациенты получали ипилимумаб в дозировке 3 мг/кг, в другой – 10 мг/кг. При увеличении дозы препарата преимуществ в ВБП и ОВ не наблюдалось. Напротив, в исследовании CA184-022 отмечался статистически значимый дозозависимый эффект. Ранее леченные пациенты (214 человек) были разделены на три группы и получали ипилимумаб в дозировке 0,3, 3 и 10 мг/кг. Медиана ОВ и 1‑ и 2-летняя выживаемость значительно увеличились в группе пациентов, получавших 10 мг/кг ипилимумаба, по сравнению с группами пациентов, получавших 3 и 0,3 мг/кг препарата. Эти результаты указывают на то, что добавление дакарбазина к терапии ипилимумабом может принести определенную пользу и что применение дозировки 10 мг/кг способно улучшить результаты лечения.
Соответственно, использование результатов исследования CA184-024 для оценки относительной эффективности ипилимумаба (3 мг/кг) в сравнении с дакарбазином может сместить относительную эффективность в сторону ипилимумаба против ингибиторов BRAF и MEK.
Исследования эффективности ингибиторов BRAF и MEK были сосредоточены на пациентах с мутациями BRAF, тогда как исследование CA184-024 фокусировалось на смешанной популяции пациентов с мутацией и диким типом BRAF. Для включения в исследование не требовалось определение BRAF-статуса, не сообщалось также о ВБП и ОВ в подгруппах пациентов с мутацией BRAF и без таковой.
Данные свидетельствуют о том, что меланома при наличии мутации BRAF отличается от меланомы с диким типом BRAF. Кроме того, многочисленные исследования показали, что меланома с мутацией BRAF ассоциирована с более агрессивным течением и худшими исходами. Поскольку данные об эффективности терапии ипилимумабом в сравнении с дакарбазином в зависимости от BRAF-статуса недоступны, невозможно оценить влияние этого фактора на эффективность терапии.
Это первое исследование, в котором использовался как одномерный, так и многомерный сетевой метаанализ для оценки показателя ОР для ВБР и ОВ. Многомерный сетевой метаанализ ОР позволяет одновременно определить корреляцию между проведенной терапией и показателями как ВБП, так и ОВ.
В исследованиях COMBI-d, COMBI-v, BREAK‑3 и BRIM‑3 влияние лечения на ВБП было выше, чем на показатель ОВ. В исследовании METRIC эффект от терапии траметинибом на ОВ был равен таковому для ВБП (ОР 0,44 для обоих). В исследовании CA184-024 предполагаемый эффект терапии ипилимумабом в сочетании с дакарбазином на ОВ был выше, чем на ВБП (ОР 0,76 для ВБП и 0,72 для ОВ). Как следствие, многомерный метаанализ продемонстрировал смягчение влияния терапии траметинибом и ипилимумабом в сочетании с дакарбазином на ОВ. Например, ОР для ОВ при сравнении терапии траметинибом и дакарбазином в исследовании METRIC составил 0,44 (95% ДИ 0,2-1,0), тогда как показатель, полученный из многомерного метаанализа, был равен 0,6 (95% ДИ 0,41‑0,83). Точно так же ОР для ОВ для ипилимумаба в сочетании с дакарбазином по сравнению с монотерапией дакарбазином в исследовании CA184-024 составил 0,72 (95% ДИ 0,59-0,87), тогда как в многомерном метаанализе он равнялся 0,78 (95% ДИ 0,67-0,90). Результаты этих анализов могут быть неоднозначны, если предположить, что существуют свойства траметиниба и ипилимумаба, которые по-разному влияют на ОВ и ВБП. Для траметиниба это, скорее, связано с небольшим числом испытуемых в подгруппе первой линии терапии в исследовании METRIC и неточностью метода интерпретации результатов RPSFT. В то же время связанные с иммунной системой эффекты ипилимумаба могут проявляться позже, чем цитотоксический эффект ингибиторов BRAF и MEK, что объясняет относительно большее влияние на ОВ, чем на ВБП. Многомерный сетевой метаанализ может иметь смещенные результаты как в пользу, так и против ипилимумаба в комбинации с дакарбазином, поэтому их следует интерпретировать с осторожностью.
В заключение следует отметить, что данный сетевой метаанализ демонстрирует увеличение ВБП и OВ на фоне комбинированной терапии дабрафенибом и траметинибом по сравнению с монотерапией дабрафенибом, траметинибом, вемурафенибом, ипилимумабом и дакарбазином в первой линии у пациентов с метастатической меланомой и мутацией BRAF. В дальнейшем предполагается проведение подобного метаанализа с включением других, более новых методов лечения, результаты которого, возможно, будут основаны не на ОР, а на показателе распределения выживаемости.
Статья печатается в сокращении.
Amdahl J., Chen L., Delea T.E., Network meta-analysis of progression-free survival and overall survival in first-line therapy of BRAF mutation-positive metastatic melanoma, 2016.
Перевела с англ. Екатерина Марушко







