8 червня, 2018
Бархатный сезон в жизни женщины: как предупредить осложнения

В Киеве 8-9 декабря 2017 г. состоялась научно-практическая конференция «Репродуктивное здоровье женщины в возрасте 40+», организаторами которой выступили Национальная медицинская академия последипломного образования имени П.Л. Шупика, ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», ВОО «Ассоциация гинекологов-эндокринологов Украины». Среди многих докладов особый интерес слушателей вызвало выступление профессора Т.Ф. Татарчук и руководителя клинического направления лабороторной диагностики медицинской лаборатории «Синэво» О.В. Рыковой, представленное в формате клинического диалога.
Менеджмент здоровья женщины в возрасте 40+
В течение последних десятилетий глобальные тенденции демографических изменений состоят в уменьшении рождаемости и увеличении продолжительности жизни. Согласно прогнозам экспертов, к 2050 г. 21% населения планеты будут составлять лица старше 60 лет. Аналогичная динамика демографических показателей наблюдается и в нашей стране. Так, если в 2006 г. в структуре женского населения Украины лица старше 50 лет составляли 38%, то в 2016 г. – 47%. При этом доля женщин репродуктивного возраста (19-49 лет) значительно уменьшилась (43 против 28% соответственно).
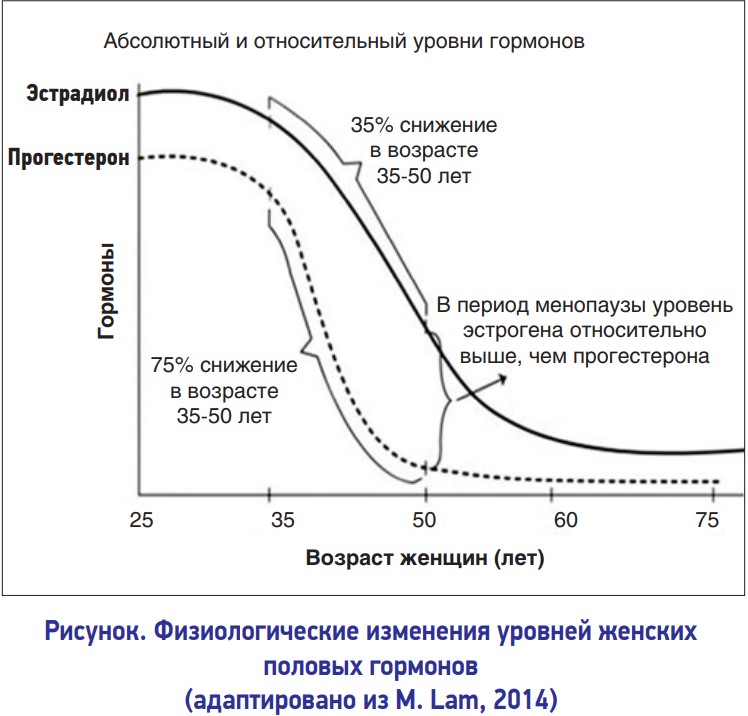 В современных условиях пик профессиональной карьеры для многих женщин приходится на 45-55 лет. Поэтому им крайне важно сохранить хорошую физическую форму, красоту, женственность, здоровье, способность к обучению, стремление к самосовершенствованию, интерес к жизни. Известно, что состояние здоровья женского организма, собственно женственность, определяется и зависит от уровней ключевых гормонов: эстрогенов, прогестерона и андрогенов. Физиологические изменения концентрации прогестерона и эстрогена у женщин начинаются с 35 лет (рисунок). Первоначально наблюдается снижение уровня прогестерона, затем эстрадиола. В возрасте 35-50 лет формируется относительная гипогестагения.
В современных условиях пик профессиональной карьеры для многих женщин приходится на 45-55 лет. Поэтому им крайне важно сохранить хорошую физическую форму, красоту, женственность, здоровье, способность к обучению, стремление к самосовершенствованию, интерес к жизни. Известно, что состояние здоровья женского организма, собственно женственность, определяется и зависит от уровней ключевых гормонов: эстрогенов, прогестерона и андрогенов. Физиологические изменения концентрации прогестерона и эстрогена у женщин начинаются с 35 лет (рисунок). Первоначально наблюдается снижение уровня прогестерона, затем эстрадиола. В возрасте 35-50 лет формируется относительная гипогестагения.
Алгоритм ведения пациенток предусматривает:
- распределение по возрасту (35-45, 45-55, 55-65, > 65 лет);
- стратификацию по статусу здоровья:
- здоровые женщины;
- здоровые с наличием факторов риска (связанными или несвязанными с гормональной дисфункцией яичников);
- клинически здоровые (с асимптомными или латентными заболеваниями, связанными или несвязанными с гормональной дисфункцией яичников);
- женщины с клиническими проявлениями заболеваний (связанными или несвязанными с гормональной дисфункцией яичников).
Одной из главных задач врача является своевременное выявление, обследование и наблюдение пациенток, имеющих факторы риска или асимптомные/латентные заболевания. Эти женщины должны получить адекватные рекомендации относительно определения функционального состояния репродуктивной системы, потенциальных рисков соматических заболеваний и онкопатологии.
Оценка состояния репродуктивного здоровья женщины в возрасте 35-45 лет включает:
- полное клиническое и гинекологическое обследование с тщательным сбором анамнеза и определением факторов риска;
- базовую маммографию (в 40 лет);
- УЗИ и пальпацию молочных желез;
- УЗИ органов малого таза;
- гистероскопию и биопсию эндометрия (по показаниям);
- определение рН вагинального отделяемого;
- цитологию вагинального мазка;
- тестирование на вирус папилломы человека;
- по показаниям – определение уровня тиреотропного гормона (ТТГ); фолликулостимулирующего гормона (ФСГ); антимюллерова гормона (АМГ).
Оценка функционального резерва яичников
На сегодняшний день для оценки функционального резерва яичников существуют две группы маркеров: УЗИ и лабораторные. Следует учитывать, что лабораторные маркеры менее субъективны, более стабильны и чувствительны. К ним относятся ФСГ, АМГ, ингибин В.
С возрастом уровень ФСГ повышается, его значение ≥ 10 МЕ/л свидетельствует о снижении овариального резерва. Наряду с этим снижается концентрация АМГ, отражая истощение фолликулярных запасов. Однако величина показателей ФСГ и ингибина В в значительной мере зависит от дня менструального цикла. Вместе с тем определение АМГ, который секретируется гранулезными клетками яичников, может быть проведено в любой день. Уровень этого гормона является более чувствительным для оценки овариального резерва. В возрасте 35-40 лет у 25% женщин наблюдается снижение уровня АМГ при нормальном ФСГ (в отсутствие патологии), в 41-44 года – АМГ снижается у 38% женщин, а ФСГ повышается у 13%. После 45 лет все женщины имеют низкие показатели АМГ, тогда как высокий ФСГ наблюдается у 28%. Таким образом, АМГ является наиболее ранним маркером снижения овариального резерва яичников, предиктором менопаузы.
Клиническое значение определения АМГ:
- оценка овариального резерва – репродуктивные планы;
- предиктор менопаузы – целесообразность и сроки старта менопаузальной гормональной терапии (МГТ);
- прогноз синдрома гиперстимуляции яичников – выбор протокола вспомогательных репродуктивных технологий;
- диагностика синдрома поликистоза яичников (СПКЯ);
- онкомаркер гранулезоклеточного рака яичников.
На основании полученного результата обследования на АМГ разрабатывается план ведения и наблюдения за пациенткой (таблица). При этом более значимой для диагностики является динамика показателей. Кроме того, следует учитывать, что в ряде исследований продемонстрирована ассоциация между низким уровнем АМГ и повышением ТТГ; недостаточностью витамина D.
Таблица. Интерпретация результатов определения уровня АМГ
Для иллюстрации принципов диагностики с учетом результатов определения лабораторных маркеров приводим несколько клинических ситуаций.
1. Пациентка М., 35 лет, обратилась по поводу появившихся нарушений менструального цикла. Уровни ФСГ, лютеинизирующего гормона (ЛГ), эстрадиола, прогестерона, ТТГ, пролактина – в пределах нормальных значений. Вопрос состоит в том, может ли снижение овариального резерва быть причиной жалоб пациентки? Результат обследования на АМГ (1,1 нг/мл) дает основания для положительного ответа.
2. Пациентка Н., 35 лет, с диагностированным СПКЯ. Уровень АМГ равен 2,8 нг/мл, что может свидетельствовать о нормальном овариальном резерве. Однако с учетом имеющегося диагноза важнее оценить динамику данного показателя.
3. Пациентка Ф., 35 лет, диагноз «бесплодие». При лабораторном обследовании обнаружено снижение уровней ФСГ, ЛГ, эстрадиола; АМГ 2,8 нг/мл (нормальный овариальный резерв). В таком случае дальнейшее обследование должно быть направлено на поиск причин гипогонадотропного гипогонадизма.
Таким образом, минимально необходимое лабораторное обследование для оценки функционального резерва яичников состоит в определении уровня АМГ. При нормальном или повышенном уровне ФСГ и наличии клиники нарушений менструального цикла в алгоритм обследования следует включить определение АМГ в динамике (снижение свидетельствует об истощении овариального резерва). Полный комплекс диагностики дополнительно содержит определение уровня ингибина В.
При высоком уровне АМГ (в ≥ 10 раз выше нормы) у женщины после 40-45 лет необходимо помнить о его значении как онкомаркера. В таких ситуациях дифференциальной диагностике помогает определение ФСГ для оценки овариального резерва и дополнительно – ингибина В.
Низкий уровень АМГ является показанием к измерению концентрации ТТГ (при его повышении рассмотреть вопрос лечения) и 25-гидроксивитамина D (коррекция дефицита при необходимости).
Репродуктивные планы после 40 лет
Следует помнить, что показатели АМГ – это оценка количества, но не качества ооцитов. Низкие уровни АМГ у женщин репродуктивного возраста свидетельствуют только о низкой вероятности беременности, в то время как высокие – не обязательно о высокой ее вероятности, а возможно о наличии патологии (СПКЯ, рак яичников).
При обращении по поводу аменореи женщины старше 40 лет, имеющей желание забеременеть, в отсутствие признаков беременности на УЗИ необходимо оценить показатель хорионического гонадотропина человека в сопоставлении с уровнем ФСГ. Наличие у пациентки в возрасте 40-55 лет хорионического гонадотропина ≥ 5 мЕд/мл при условии ФСГ ≤ 45 мЕд/мл с большей вероятностью связано с возрастным повышением.
Причины обращения к гинекологу женщин старшего репродуктивного возраста:
- оценка риска гиперплазии эндометрия;
- прибавка массы тела;
- нарушение менструального цикла;
- аномальные маточные кровотечения;
- менструальная мигрень, вазомоторные симптомы;
- предменструальный синдром;
- нарушения сна, тревога, депрессия;
- вагинальные симптомы;
- нежелательная беременность.
Контрацепция у женщин в перименопаузе
Несмотря на то что в соответствии с данными национальной статистики США наиболее высокая частота незапланированной беременности отмечается среди подростков, почти половина (48%) женщин старше 40 лет также подвержена риску таковой.
Аборты у женщин в перименопаузе характеризуются частым обострением гинекологической и экстрагенитальной патологии, более тяжелым дальнейшим протеканием климактерического синдрома. С учетом вышеизложенного у лиц в возрасте после 40-45 лет сохраняется потребность в контрацепции. При выборе контрацептивного средства целью является не только предотвращение нежелательной беременности, но и сохранение здоровья женщины, а также улучшение качества ее жизни. Согласно критериям ВОЗ, возраст женщины как единственный фактор не может быть противопоказанием для использования доступных контрацептивных методов. В соответствии с украинским национальным консенсусом по ведению пациенток в климактерии следует продолжать применять контрацепцию в течение 1 года после последней менструации, если возраст женщины составляет > 50 лет, и в течение 2 лет после последней менструации в возрасте до 50 лет.
Риск рака эндометрия снижается соответственно увеличению длительности приема комбинированных оральных контрацептивов: через 1 год использования – на 20%; через 2 года – на 40%; через ≥ 4 года – на 60%. При этом протективный эффект сохраняется спустя 15 лет после прекращения приема данных препаратов. Доказано, что наиболее выраженный антипролиферативный эффект на эндометрий оказывает диеногест.
Неконтрацептивные преимущества комбинированных оральных контрацептивов в перименопаузе:
- регуляция менструального цикла;
- сохранение минеральной плотности костей/снижение риска переломов в дальнейшем;
- лечение аномальных маточных кровотечений и/или дисменореи;
- профилактика гиперплазии эндометрия;
- профилактика рака эндометрия и рака яичников;
- купирование вазомоторных симптомов (приливы, ночная потливость, головная боль, изменения артериального давления).
В случае наличия противопоказаний к назначению эстрогенов с целью профилактики гиперплазии эндометрия возможно применение гестагенов в течение 12-14 дней (минимум 4 цикла в год). Выбор препарата должен быть персонализированным и зависеть от наличия конкретных симптомов и предпочтений пациентки. Возможными опциями являются утрожестан (предменструальный синдром), дидрогестерон (склонность к кровотечениям). Если женщина нуждается в контрацепции, средствами выбора являются внутриматочные системы Мирена, Джайдес.
Эстрогены – основа женственности
Эстрогены играют решающую роль в сохранении молодости и здоровья женского организма. Именно эти гормоны оказывают защитное влияние на все органы и системы, взаимодействуя с α- и β-эстрогенными рецепторами. Ядерные, мембранно-ассоциированные и митохондриальные эстрогенные рецепторы распределяются практически во всех отделах головного мозга и могут присутствовать как в нейронах, так и в глиальных клетках.
С целью улучшения настроения, жизненного тонуса, уменьшения выраженности приливов наряду с лечением гестагенами можно назначить препарат Климадинон, содержащий специальный стандартизированный экстракт Cimicifuga racemosa BNO 1055. Данное лекарственное средство обладает активностью фитоэстрогенного селективного модулятора эстрогенных рецепторов.
Свойства препарата Климадинон (Wuttke W. et al., 2002):
- действие на ЦНС – синтез и обмен катехоламинов в мозге (серотонин, дофамин, норадреналин, β-эндорфин, нейротензин);
- действие в системе гипоталамус/гипофиз: подавление пульсации гонадотропин-рилизинг гормона/снижение уровня ЛГ;
- действие на костную ткань: экспрессия генов, регулируемых эстрогенами; положительное влияние на маркеры костного ремоделирования;
- увеличение числа поверхностных клеток эпителия влагалища; отсутствие влияния на эндометрий;
- повышение тонуса мочевого пузыря;
- действие на матку и молочную железу: экспрессия генов, регулируемых эстрогенами, отсутствует (в высоких концентрациях угнетается эстроген-индуцированная клеточная пролиферация, снижение риска развития рака молочной железы и рака эндометрия).
В соответствии с результатами исследования, проведенного в отделении эндокринной гинекологии ГУ «Институт педиатрии, акушерства и гинекологии НАМН Украины», препарат Климадинон обладает высокой эффективностью в лечении климактерического синдрома легкой степени (Татарчук Т.Ф., Ефименко О.А. Фитотерапия ранних перименопаузальных расстройств. Репродуктивная эндокринология. 2012. № 3 (5). С. 41-44.). В исследовании приняли участие пациентки в возрасте 45-55 лет, нуждающиеся в медикаментозной коррекции симптомов менопаузы. Оценку клинических особенностей течения климактерического синдрома у исследуемого контингента проводили путем определения суммарного индекса менопаузы с использованием менопаузальной рейтинговой шкалы (MRS) до лечения, а также через 3 и 6 мес после. Пациентки были рандомизированы на две группы, сопоставимые по возрасту, индексу массы тела и степени тяжести климактерического синдрома. Женщинам I группы в дополнение к базисной терапии назначали препарат Климадинон по 1 табл/сут непрерывно в течение 3 мес.
Остальные пациентки вошли во II группу (сравнения) и получали только базисную терапию. По окончании лечения отмечалось достоверное снижение выраженности климактерических жалоб у лиц I группы. Средний менопаузальный индекс согласно шкале MRS через 3 и тем более через 6 мес в группе женщин, применявших Климадинон, был достоверно ниже, чем до начала терапии (9,3 ± 1,2; 6,3 ± 1,5; 15,3 ± 0,1 балла соответственно). Практически все женщины отметили снижение частоты приливов, улучшение настроения, нормализацию сна, повышение работоспособности, улучшение памяти.
Влияние эстрогенов на состояние кожи. До 30% коллагена теряется в первые 5 лет менопаузы. Важно знать, что толщина кожи восстанавливается после 2 лет приема заместительной гормональной терапии.
Эстрогены повышают синтез гиалуроновой кислоты и содержание воды в коже; улучшают васкуляризацию дермы и эпидермиса; повышают активность сальных желез, увеличивают пропорцию коллагена III типа по отношению к I типу на 5% в течение 6 мес; усиливают синтез эластина; стимулируют синтез коллагена; способствуют увеличению толщины и эластичности кожи, особенно дермального слоя.
Профилактика сердечно-сосудистых заболеваний. Часто гинекологи являются единственными врачами, которые консультируют относительно здоровых женщин в течение длительного периода их жизни. Поэтому именно врач-гинеколог решает задачу раннего определения индивидуальных рисков развития патологии. Кроме того, в функции специалистов данного профиля входит исключение дополнительных рисков при назначении медикаментов, имеющих потенциально неблагоприятное влияние на сердечно-сосудистую систему, при выборе гормона, а также при определении тактики лечения у женщин с миомой матки, эндометриозом, гиперплазией эндометрия.
Эстрогены оказывают благоприятное воздействие на сосуды, вызывая вазодилатацию и повышая выработку окиси азота. Долговременный эффект эстрогенов состоит в уменьшении атеросклеротического повреждения сосудистой стенки, подавлении роста гладкомышечных клеток и усилении – эндотелиальных.
Влияние эстрогенов на гемостаз зависит от их дозы. В высокой дозировке они обусловливают повышение уровней ингибитора активатора плазминогена-1, фибриногена и фактора свертывания VII, в низкой – оказывают противоположное действие.
Под действием эстрогенов происходит снижение концентрации холестерола, повышается уровень липопротеинов высокой плотности. Необходимо учитывать, что при применении пероральных форм гормональных препаратов может наблюдаться рост концентрации триглицеридов, тогда как трансдермальные формы (эстрожель) таким эффектом не обладают.
Программа здоровья женщин 35-45 лет включает:
- оценку репродуктивной функции;
- обследование состояния соматического здоровья:
- рентгенография грудной клетки;
- ЭКГ;
- уровень глюкозы сыворотки крови;
- общий анализ анализ крови + СОЭ + С-реактивный белок;
- липидный профиль;
- коагулограмма и диагностика тромбофилии (по показаниям);
- биохимический анализ крови;
- определение индекса массы тела, удельного веса жировой ткани и адекватности ее распределения;
- денситометрия;
- маркеры резорбции и формирования костной ткани.
Лабораторная диагностика в рамках программы здоровья женщин 35-45 лет
Общий анализ крови
Анемия (уровень гемоглобина ≤ 120 г/л)
Для дифференциальной диагностики анемии обязательным является определение количества эритроцитов и эритроцитарных индексов (средний объем эритроцита, среднее содержание гемоглобина в эритроците).
В ситуациях, когда уровень гемоглобина ≥ 120 г/л, следует провести оценку маркеров скрытой анемии – процент насыщения трансферрина и ферритин. Эти показатели позволяют диагностировать анемию на стадии неизмененного гемоглобина. При этом отмечается снижение ферритина и повышение трансферрина, что требует коррекции для насыщения депо железа.
Оценка СОЭ
Необходимо учитывать, что этот показатель повышается в норме с возрастом, при онкопатологии, аутоиммунных заболеваниях, анемии.
С-реактивный белок
Повышение наблюдается при воспалительных заболеваниях, а также в послеоперационном периоде. Существует две фракции С-реактивного белка: обычный (диагностика воспалительного процесса) и высокочувствительный (назначается только для выявления эндотелиального воспаления [дисфункции]).
Кардиоваскулярные риски (диагностика атеросклероза)
Основным методом является исследование липидного профиля. В половине случаев при наличии атеросклероза уровень холестерина может быть в пределах нормы. Поэтому в первую очередь определяются модифицируемые факторы риска: повышение гомоцистеина и липопротеина (а). Управление этими параметрами возможно посредством назначения фолиевой кислоты для снижения первого и препаратов с никотиновой кислотой – второго.
Инсулинорезистентность/сахарный диабет
Измерение уровня глюкозы – это нестабильный анализ, результаты которого в значительной мере зависят от наличия многих факторов (стресс, острое заболевание, уровень потребления глюкозы и др.). Для ранней диагностики сахарного диабета оптимальным методом является определение гликозилированного гемоглобина; при уровне этого показателя > 5,5% пациентка относится к группе риска, ей проводится скрининг/диагностика преддиабета и сахарного диабета независимо от клинического состояния на момент взятия крови.
С целью диагностики инсулинорезистентности рассчитывается индекс НОМА; женщина попадает в сферу особого внимания при величине > 2,5.
Тромботические риски
Исследование коагулограммы предоставляет косвенные признаки тромбозов. Для более четкой оценки тромботических рисков необходимо определение активированного частичного тромбопластинового времени (фактор, управляемый посредством антикоагулянтной терапии) и фибриногена. Прямым маркером тромбоза является повышение Д-димера.
При подозрении на антифосфолипидный синдром в комплекс обследований включается определение волчаночного антикоагулянта, антикардиолипиновых антител, антител к β2-гликопротеину (2 раза с интервалом 12 нед).
Оценив тромботические риски, можно определить вероятность развития кардиоваскулярных событий, а также осложнений МГТ до ее назначения и в ходе применения (рекомендовано 1 раз в год проводить контрольное обследование).
Спорным вопросом является целесообразность исследования параметров тромбообразования при наследственных формах нарушений свертывания крови. Наличие генетической предрасположенности дает основания для определения степени риска тромботических осложнений с учетом всех других факторов, что обусловливает выбор препарата для МГТ.
Тромбоз является одной из причин смерти пациентов от гиперкортизолемии (синдром Кушинга). Скрининг на данное эндокринное заболевание включает измерение уровня кортизола в слюне в 23.00, в суточной моче и в крови в 8.00 после введения 1 мг дексаметазона.
Онконастороженность
Идеального онкомаркера не существует, поэтому для диагностики следует выполнить два и более комплексных исследования. Необходимо учитывать, что повышение онкомаркера свидетельствует не только о наличии рака. Для диагностики важна динамика нарастания показателей. Если диагноз рака установлен, обязательно определение онкомаркера до начала лечения для последующего контроля его эффективности.
Оценка темпов старения
С этой целью определяются теломеры хромосом (счетчик клеточных делений): чем они короче, тем большее число делений прошло с момента рождения клетки-предшественницы.
Клинические аспекты менеджмента здоровья женщин в менопаузе
Возраст 46-55 лет
При консультировании женщины оцениваются клинические проявления менопаузальных нарушений. Терапией первого выбора климактерических симптомов является МГТ, которая подбирается индивидуально с учетом результатов максимального объема обследований для своевременного выявления и профилактики возможных рисков ее осложнений. При скрининговом обследовании обязательно определение клинико-лабораторных факторов риска остеопороза, сердечно-сосудистых заболеваний, болезни Альцгеймера. В случае их наличия осуществляется разработка программы длительной заместительной гормональной терапии.
Программа здоровья в этом возрасте включает:
- скрининг онкорисков:
- цитология вагинального мазка;
- УЗИ органов малого таза;
- гистероскопия и биопсия эндометрия (по показаниям);
- маммография;
- УЗИ молочной железы;
- сигмоскопия (1 paз в 3-5лет);
- колоноскопия (1 раз в 10 лет или по показаниям);
- скрининг сердечно-сосудистых рисков:
- уровень ТТГ (по показаниям);
- анализ крови + СОЭ + С-реактивный белок;
- липидный профиль;
- коагулограмма;
- биохимический анализ крови;
- нагрузочный стресс-тест;
- определение индекса массы тела, удельного веса жировой ткани и адекватности ее распределения;
- скрининг остеопороза:
- денситометрия;
- маркеры резорбции и формирования костной ткани.
Возраст 56-65 лет
Наиболее частые жалобы у пациенток этого возраста – вагинальные и урогенитальные симптомы. В качестве терапевтических опций могут быть выбраны трансдермальные формы эстрогенов, а также лубриканты.
При обращении женщин этой возрастной категории следует оценивать риск остеопороза/переломов и проводить соответствующую терапию. Согласно клиническим рекомендациям по профилактике и лечению остеопороза национального фонда остеопороза США, женщинам старше 50 лет показан прием кальция в дозе 1200 мг/сут и витамина D3 – 800-1000 МЕ/сут. Бифасфонаты являются наиболее часто назначаемыми антирезорбтивными средствами и остаются препаратами первой линии для лечения остеопороза.
При выборе параметров лабораторной диагностики необходимо учитывать следующее. Форма 25-гидроксивитамин D определяется с целью оценки уровня витамина (≤ 30 нг/мл – недостаточность, ≤ 20 нг/мл – дефицит) и контроля эффективности лечения. Измерение концентрации 1,25-дигидроксивитамина D используется для дифференциальной диагностики причин гиперкальциемии (саркоидоз, лимфомы) и как маркер почечной недостаточности (снижается).
Кроме того, тактика ведения пациенток 56-65 лет включает оценку кардиоваскулярных факторов риска и выбор мер по их снижению с акцентом на холестеролснижающие препараты (особенно статины); контроль артериальной гипертензии (модификация стиля жизни и применение антигипертензивных препаратов); менеджмент сахарного диабета (оптимизация гликемического контроля и снижение риска осложнений). Также следует определить возможность продолжения заместительной гормональной терапии либо выбрать альтернативные, негормональные методы лечения.
Таким образом, ключевые клинические аспекты ведения пациенток в возрасте 40+ таковы:
- стиль жизни оказывает решающее влияние на ее качество и продолжительность;
- первичная профилактика должна начинаться задолго до менопаузы;
- раннее начало заместительной гормональной терапии необходимо для снижения отдаленных рисков (сердечно-сосудистые заболевания, остеопороз);
- программа здоровья имеет задачу минимизировать проблемы как до, так и после прекращения месячных;
- ведение пациенток с учетом индивидуального статуса здоровья, наличия соматической патологии;
- дизайн и внедрение программы здоровья зависят от ресурсов общества.



