23 липня, 2020
Сучасне лікування спленомегалії у пацієнтів з мієлофіброзом

Мієлопроліферативні новоутворення (МПН), при яких не виявляється філадельфійська хромосома (Ph-негативні МПН), включають есенціальну тромбоцитемію, істинну поліцитемію та мієлофіброз (МФ). Ці захворювання клінічно характеризуються системними симптомами, схильністю до тромбозу та розвитком спленомегалії, яка може мати різний ступінь вираженості [1]. Спленомегалія рідко зустрічається при есенціальній тромбоцитемії, проте вона виявляється приблизно у третини пацієнтів з істинною поліцитемією та ще частіше – у хворих з МФ [2]. При цьому саме у пацієнтів з МФ особливо поширена масивна спленомегалія [3, 4].
Симптоми, вторинні щодо спленомегалії, включають відчуття тиску та біль у лівому зовнішньому квадранті живота, біль у лівому плечі та раннє насичення, спричинене стисканням шлунка. Крім того, масивна спленомегалія може призводити до портальної гіпертензії. У пацієнтів з МФ може також відзначатися тромбоз вісцеральних вен, печінковий екстрамедулярний гемопоез та облітераційна портальна венопатія [5, 6]. Масивна спленомегалія також може призводити до стискання порожнистої вени/клубових вен, внаслідок чого виникає набряк нижньої кінцівки. Крім того, типовою є клітинна секвестрація, що призводить до поглиблення наявних цитопеній і може ще більше обмежувати можливості лікування [7]. У деяких випадках за значної вираженості спленомегалії можуть утворюватися ділянки ішемії з подальшим розвитком інфарктів селезінки, що супроводжуються больовим синдромом [8]. Негативний вплив спленомегалії на загальну якість життя пацієнтів з МФ підтверджений результатами масштабного опитування, згідно з якими зменшення розміру селезінки було визначене одним із п’яти провідних завдань лікування [9].
На сьогодні основою фармакологічного лікування спленомегалії при МФ є застосування інгібіторів янус-кінази (JAK1/2), таких як руксолітиніб та нещодавно схвалений федратиніб. Ці пероральні препарати мають доведену ефективність у зменшенні розмірів селезінки, і саме вони фундаментально змінили підхід до вирішення проблеми спленомегалії при МФ [17-20]. Тим не менше приблизно 15% пацієнтів терапія інгібіторами JAK2 не може бути призначена через виражену тромбоцитопенію (<50×109/л) [21]. Крім того, у багатьох пацієнтів розвивається рефрактерність до інгібіторів JAK2. Через це наразі активно вивчаються й інші можливості симптоматичного лікування спленомегалії у пацієнтів з МФ.
У цьому огляді описані переваги та обмеження застосування інгібіторів JAK2 при спленомегалії, а також інші методи терапії та можливості оперативного лікування. Також запропонований алгоритм оптимального лікування симптомної спленомегалії у пацієнтів з МПН.
Традиційна циторедуктивна терапія
Для пацієнтів з симптомною спленомегалією доступно декілька видів лікування, які продемонстрували свою ефективність у зменшенні розмірів селезінки. До появи інгібіторів JAK2 як засоби терапії при МФ вивчали декілька препаратів. Зокрема, як перша лінія циторедуктивної терапії при істинній поліцитемії та есенціальній тромбоцитемії часто застосовується гідроксисечовина. У пацієнтів з МФ гідроксисечовина зазвичай є препаратом резерву, що використовується при гіперпроліферативних станах (включаючи спленомегалію, лейкоцитоз і системні симптоми) у разі неможливості призначення інгібіторів JAK2.
Інгібітори JAK1/2
Найбільш ефективним фармакологічним інструментом зменшення розмірів селезінки при МФ є інгібування JAK2. Механізм, що лежить в основі зменшення розмірів селезінки на тлі застосування інгібіторів JAK2, вивчений недостатньо. Він може бути пов’язаний з пригніченням опосередкованої JAK2 міграції гемопоетичних стовбурових клітин через сигнальний шлях CXCL12/CXCR4 [37]. Руксолітиніб є інгібітором JAK1/2, який у 2011 р. був схвалений Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) для лікування МФ, а пізніше отримав схвалення і для лікування істинної поліцитемії при відсутності відповіді на терапію гідроксисечовиною або при її непереносимості [45]. Схвалення застосування руксолітинібу при МФ базувалося на результатах опорних досліджень COMFORT. Ці два дослідження III фази проводилися за участі пацієнтів з МФ (захворювання проміжного або високого ризику). У дослідженні COMFORT I пацієнтів рандомізовано розподіляли у групу прийому руксолітинібу або плацебо, а у дослідженні COMFORT II руксолітиніб порівнювали з найкращою доступною терапією (НДТ). В обох дослідженнях встановили ефективність руксолітинібу у покращенні стандартизованих показників бальної оцінки симптому через 24 тижні лікування [17, 18].
У дослідженні COMFORT I застосування руксолітинібу сприяло зменшенню об’єму селезінки в середньому на 31,6% на 24‑му тижні лікування, у той час як у хворих в групі плацебо селезінка навпаки збільшилася (в середньому на 8,5%). Первинна кінцева точка – зменшення об’єму селезінки (ЗОС) на ≥35% (ЗОС 35%) – була досягнута у 41,9% пацієнтів у групі лікування руксолітинібом порівняно з 0,7% у групі плацебо [17]. Досягнуте зменшення селезінки виявилося стійким – середня тривалість відповіді склала 168,3 тижня при тривалому подальшому спостереженні [46]. Аналогічні результати спостерігалися у дослідженні COMFORT II, у якому відзначалося середнє зменшення селезінки на 29,2% через 24 тижні лікування в групі руксолітинібу порівняно з її збільшенням на 2,7% в групі НДТ. ЗОС 35% було досягнуто у 32% пацієнтів, які отримували лікування руксолітинібом, порівняно з 0% в групі НДТ [18]. Через 5 років 53,4% пацієнтів, які отримували руксолітиніб, у підсумку досягли кінцевої точки ЗОС 35% при середній тривалості спостереження 3,2 року [47]. В обох дослідженнях покращення клінічного перебігу спленомегалії спостерігалося протягом 1 місяця прийому руксолітинібу, і з часом відбувалося подальше покращення протягом 48 тижнів періоду спостереження. Важливо, що відповідь на терапію руксолітинібом з боку селезінки є дозозалежною – при застосуванні вищих доз препарату досягається більш значний ефект [48].
Апостеріорний (рost hoc) об’єднаний аналіз результатів досліджень COMFORT засвідчив, що у тих пацієнтів, у яких вдалося досягти зменшення об’єму селезінки як мінімум на 25%, відзначалася більш тривала виживаність порівняно з пацієнтами, у котрих не відбувалося зменшення органа або він збільшувався [49]. Руксолітиніб також здатний покращувати стан пацієнта при портальній гіпертензії шляхом зменшення кровотоку у селезінковій артерії та прямого вазодилатаційного впливу на внутрішньопечінкові синусоїди.
Хоча початковий рівень відповіді на терапію руксолітинібом є високим, з часом у пацієнтів розвивається його непереносимість або прогресує спленомегалія. Тривале подальше спостереження за пацієнтами у дослідженнях COMFORT I та II продемонструвало, що через 3 роки приблизно 50% хворих більше не отримували терапію руксолітинібом [23]. У пацієнтів, які припиняють терапію руксолітинібом, прогноз є невтішним: в одному дослідженні повідомлялося, що медіана загальної виживаності складала лише 14 місяців [24].
Спленектомія
До впровадження терапії інгібіторами JAK2 з метою тимчасового полегшення симптоматики, пов’язаної зі спленомегалією, зазвичай виконували спленектомію. Сьогодні спленектомія все ще залишається важливою терапевтичною стратегією для пацієнтів, які мають рефрактерність до інгібіторів JAK1/2 або їх непереносимість, а також для хворих з масивною симптомною спленомегалією. Однак ключовим фактором успіху втручання є ретельний відбір пацієнтів, яким може бути проведена ця операція.
Опромінення селезінки
У тих пацієнтів, яким не може бути виконане оперативне втручання через незадовільний функціональний статус, потенційним варіантом лікування може бути опромінення селезінки. Як відомо, селезінка є дуже радіочутливим органом, що зумовлює ефективність навіть низькодозового опромінення. Однак опромінення селезінки може призводити до багатьох ускладнень, зокрема, до виникнення значної мієлосупресії, яка часто призводить до поглиблення асоційованих із захворюванням анемії та тромбоцитопенії, а також до розвитку нейтропенії. Про тяжкі та тривалі цитопенії повідомлялося у 26% пролікованих пацієнтів; у 16% вони призвели до смертельної кровотечі або сепсису [75]. Крім того, подальше погіршення клінічної картини може виникати через значні прояви гастроінтестинальної токсичності (в тому числі нудоту та діарею).
Часткова емболізація селезінкової артерії
Часткова емболізація селезінкової артерії (ЧЕСА) виконується на тлі антибіотикопрофілактики та супроводжується значно менш вираженими ускладненнями, ніж повна емболізація. Крім того, при такому підході зберігається тканина селезінки та відповідно – її функція [79]. У рандомізованому дослідженні з оцінювання ефективності спленектомії порівняно з ЧЕСА у пацієнтів із цирозом печінки та спленомегалією ЧЕСА сприяла зменшенню тривалості госпіталізації, меншій частоті трансфузій та меншій вираженості больового синдрому після процедури, ніж у пацієнтів, яким виконували спленектомію [80].
Контрольована емболізація селезінкової артерії проводиться за допомогою мікросфер, желатинової губки, яка розсмоктується, судинних заглушок або рідких емболізуючих речовин.
На практиці основним обмеженням ЧЕСА є постемболізаційний синдром, який характеризується вираженим болем у лівому верхньому квадранті живота та часто потребує внутрішньовенного введення знеболювальних засобів, інфузійних розчинів і госпіталізації. Крім того, після ЧЕСА можуть виникати такі ускладнення, як абсцес селезінки, тромбоз портальної вени, утворення плеврального випоту та збільшення вираженості асциту.
Висновки та рекомендації
Симптомна спленомегалія залишається складним клінічним сценарієм, з яким стикаються лікарі при веденні пацієнтів з МФ. Нижче наведено клінічний алгоритм лікування симптомної спленомегалії у пацієнтів з МФ (рис.).
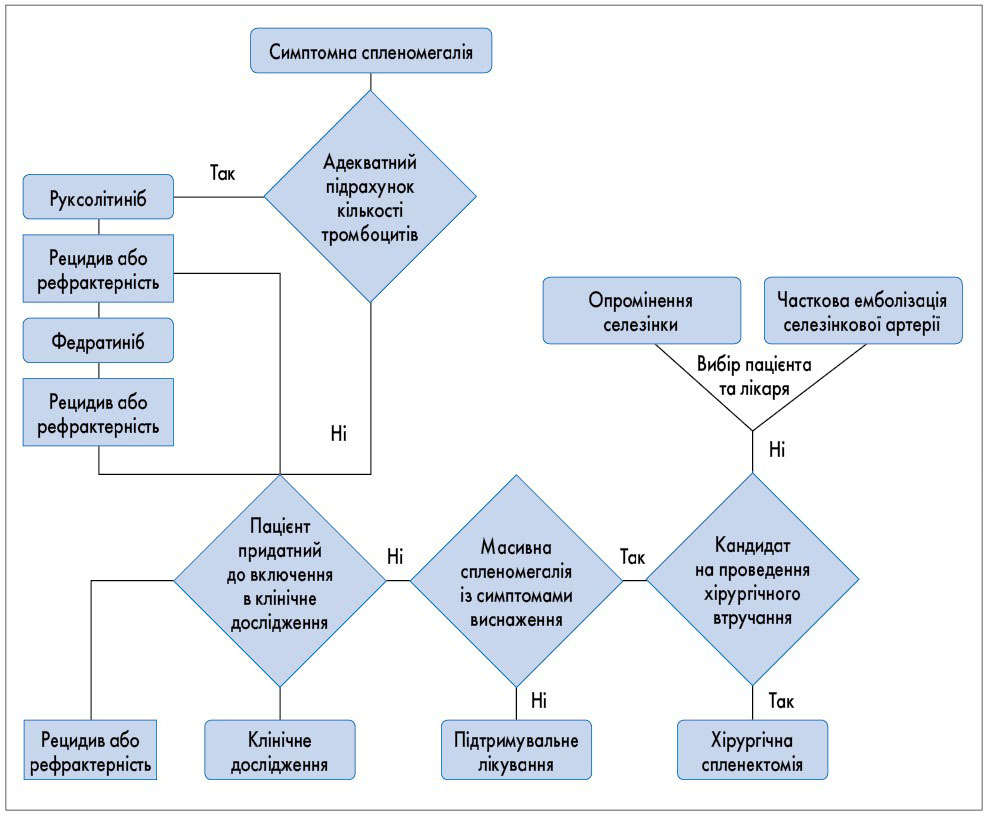 Рис. Практичний алгоритм лікування спленомегалії при МФ
Рис. Практичний алгоритм лікування спленомегалії при МФ
Пацієнти, яким може проводитися терапія інгібіторами JAK2 (тобто з адекватною кількістю тромбоцитів), мають спершу отримувати лікування доступними препаратами – руксолітинібом або федратинібом. Що стосується пацієнтів, які не розглядаються як кандидати на стартову терапію інгібіторами JAK2 або за їх неефективності, то для них має бути розглянута можливість участі у клінічних дослідженнях. У пацієнтів, які не можуть бути включені у клінічні дослідження, хірургічне видалення селезінки є лікуванням першого вибору. У пацієнтів, які не є кандидатами на хірургічне втручання (незадовільний функціональний статус або конкуруючі супутні захворювання), мають розглядатися можливості опромінення селезінки або ЧЕСА залежно від вибору фахівців та пацієнтів з урахуванням співвідношення між очікуваною користю та ризиком. Наприклад, пацієнту з високою ймовірністю розвитку постемболізаційного синдрому (похилий вік або значне виснаження) варто рекомендувати опромінення селезінки. Однак для пацієнта, який вже має вкрай виражену цитопенію, більш прийнятною може бути ЧЕСА.
Таким чином, сучасне ведення спленомегалії при МФ фундаментально змінилося протягом останнього десятиріччя та продовжує швидко еволюціонувати.
Стаття друкується у скороченні.
Повний список літератури, що включає 86 джерел, знаходиться в редакції.
Tremblay D., Schwartz M., Bakst R. et al. Modern management of splenomegaly in patients with myelofibrosis. Ann Hematol. 2020. https://doi. org/10.1007/s00277-020-04069-4.
Переклала з англ. Олена Зотова
Більше матеріалів тут: https://health-ua.com/actual-theme/hematology/41686-aktualna-tema-lkuvannya-mloprolferativnih-zahvoryuvan-nov-gorizonti?utm_source=qr-code&utm_medium=AT_hematology_41686_mloprolferativnih&utm_campaign=Novartis
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 3 (64) 2020 р.




