30 травня, 2016
Преждевременное половое развитие у девочек: возможности лабораторной диагностики
Важность своевременного выявления причин преждевременного полового развития (ППР) объясняется прежде всего возможным наличием опухолевого процесса, а также теми состояниями, которые сопровождают ускоренный пубертат. Ключевую роль в диагностике и контроле эффективности лечения ППР играют лабораторные методы исследования.
Половое развитие – генетически обусловленный процесс превращения детского организма во взрослый, способный к воспроизводству. На сроки начала пубертата влияет ряд факторов: немодифицируемые и модифицируемые (эндокринные заболевания, наличие избыточной массы тела, уровень физической нагрузки, социальные условия, экзогенное поступление гормонов). Модифицируемые факторы потенциально поддаются коррекции.
Период полового созревания – важный этап развития ребенка. Активация эндокринных механизмов регуляции полового развития у девочек происходит в возрасте 6-7 лет, но стартовое звено инициации пубертата остается неясным. Ускорение полового развития у 99,6% здоровых девочек происходит в возрасте 8-13 лет. Среди возможных причин раннего полового созревания ведущие позиции занимает гипотеза достижения «критической массы тела»: менархе наступает после того, как масса тела увеличивается до 44-47 кг. Непрерывный процесс полового созревания обычно подразделяется на дискретные стадии, предложенные в качестве критерия визуальной оценки в 1970-х гг. W. Marshall и J. Tanner; в дальнейшем эта методика была утверждена ВОЗ.
Телархе – первый признак полового созревания у девочек. Наблюдается в среднем в возрасте 10,5 лет. За 2 года грудные железы (ГЖ) достигают зрелого размера и формы, соски становятся четко выраженными. Размеры и форма ГЖ у девушек имеют выраженные индивидуальные различия. Пубархе появляется через несколько месяцев после начала роста ГЖ (у 15% девочек первым наблюдается именно этот признак). Менархе обычно наступает через 2 года после начала роста ГЖ. В течение пубертата под влиянием высокого уровня эстрогенов происходит рост костей таза в ширину, в результате чего бедра становятся шире, увеличивается количество жировой ткани с накоплением преимущественно в области ГЖ, бедер, ягодиц, плечевого пояса, лобка.
ППР считается появление вторичных половых признаков у девочек в возрасте до 8 лет. В последние годы данное патологическое состояние наблюдается все чаще. Актуальность проблемы обусловлена развитием ряда осложнений (при отсутствии лечения): низкорослости (результат преждевременного закрытия зон роста трубчатых костей); дисплазии (короткие конечности, длинное туловище, широкий таз); ранней сексуальности; навязчивых состояний; нарушения функции репродуктивной системы (пубертатные маточные кровотечения, дисфункциональные маточные кровотечения в репродуктивном возрасте, синдром поликистозных яичников, ранний климакс). Необходимость своевременной диагностики и лечения ППР очевидна и общепризнанна.
Классификация ППР (у девочек)
I. Гонадотропинзависимое ППР обусловлено преждевременной активацией гипоталамо-гипофизарно-гонадной системы при таких состояниях, как:
• гипоталамическая гамартома;
• объемные образования головного мозга (глиомы и арахноидальные кисты хиазмально-селлярной области и дна III желудочка);
• органическое поражение ЦНС;
• идиопатическое ППР.
II. Гонадотропиннезависимое ППР вызвано активацией стероидсекретирующих элементов гонад без участия гонадотропинов:
• синдром МакКьюна-Олбрайта-Брайцева;
• персистирующие фолликулярные кисты.
III. Ложное ППР спровоцировано автономной секрецией половых стероидов надпочечниками или опухолью:
• изосексуальное ППР у девочек (обусловлено увеличением секреции эстрогенов при эстрогенпродуцирующих опухолях яичников или надпочечников);
• гетеросексуальное ППР у девочек (возникает на фоне повышенной секреции андрогенов при андрогенпродуцирующих опухолях яичников или надпочечников, врожденной дисфункции коры надпочечников – дефицита 21-гидроксилазы или 11β-гидроксилазы).
IV. Изолированные формы ППР:
• изолированное преждевременное телархе;
•изолированное преждевременное адренархе.
Диагностика ППР должна проходить в 2 этапа.
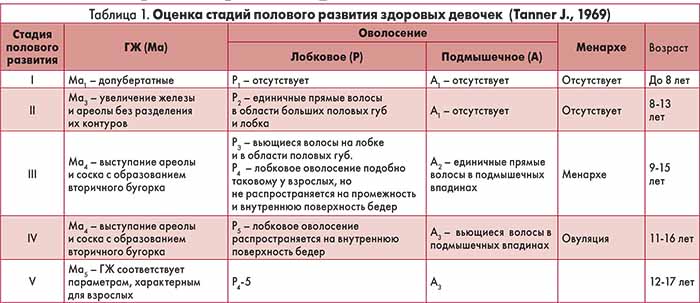
1-й этап – подтверждение ППР. Клиническая диагностика основана на оценке стадии полового развития (табл. 1).
Обязательными являются антропометрия и подсчет скорости роста ребенка за предшествующие 6-12 мес. Превышение показателей роста (относительно нормы для данного возраста) и скорости роста >2SD за предшествующий период свидетельствуют о ППР.
Исследование, позволяющее оценить костный возраст, – рентгенография кистей с лучезапястными суставами. Костный возраст, опережающий паспортный более чем на 2 года, подтверждает ППР.
2-й этап – дифференциальная диагностика форм ППР с целью определения тактики лечения. Этот этап включает проведение инструментальных и лабораторных методов исследования. При диагностическом поиске в первую очередь учитываются результаты клинического осмотра.
ППР у девочек по гетеросексуальному типу (аномальное строение наружных половых органов, появление оволосения) требует исключения патологий, обусловленных повышенной секрецией андрогенов (врожденная дисфункция коры надпочечников (ВДКН), андрогенпродуцирующие опухоли яичников или надпочечников). Акцент при обследовании делают на лабораторной диагностике. Обязательным является определение 17-ОН-прогестерона (17-ОНП), кортизола, дегидроэпиандростерона сульфата (ДГЭА-С), андростендиона и тестостерона. При выявлении повышенного содержания 17-ОНП и/или ДГЭА-С и тестостерона в крови проводится малая проба с дексаметазоном: назначают дексаметазон перорально в дозе 40 мкг/кг/сут на 2 дня. Забор венозной крови осуществляют в 8 ч утра накануне приема препарата и в 8 ч утра на 3-й день (после двух дней использования).
Критерии оценки малой пробы с дексаметазоном:
• в норме содержание 17-ОНП, ДГЭА-С и тестостерона снижается на ≥50%;
• отсутствие динамики концентрации гормонов предполагает наличие андрогенпродуцирующей опухоли.
Подозрение на андрогенпродуцирующую опухоль требует дальнейшей инструментальной диагностики – проведения ультразвукового исследования / магнитно-резонансной томографии (МРТ) органов малого таза (ОМТ), надпочечников.
При обнаружении повышенного уровня 17-ОНП, ДГЭА-С и пониженного или нормального содержания кортизола необходимо исключить неклассическую форму ВДКН. Проводится проба с синтетическим аналогом адренокортикотропного гормона короткого или пролонгированного действия (тетракозактидом): в период с 8 до 9 ч утра осуществляется забор крови для определения базальных уровней 17-ОНП и кортизола. Затем подкожно или внутривенно вводят тетракозактид в дозе 0,25-1 мг. Повторный забор крови для определения стимулированных уровней 17-ОНП и кортизола осуществляется через 30 и 60 мин (при введении препарата короткого действия) или как минимум через 9 ч (после использования препарата пролонгированного действия).
Критерии оценки пробы с тетракозактидом:
• при повышении базального значения 17-ОНП на 20-30% (у девочки с преждевременным пубархе) можно предположить неклассическую форму ВДКН;
• в норме: кортизол – 500 нмоль/л, 17-ОНП ≥36 нмоль/л (11,9 нг/мл), при дефиците 21-гидроксилазы: 17-ОНП ≥45 нмоль/л (14,9 нг/мл) [1].
Согласно рекомендациям Международного эндокринологического общества определять 17-ОНП необходимо ранним утром в фолликулярную фазу: в норме базальный 17-ОНП – 2-4 нг/мл, стимулированный 17-ОНП – <10 нг/мл [2].
Для подтверждения моногенных форм ППР (ВДКН) используются молекулярно-генетические методы исследования. Терапевтическая тактика определяется вариантом ППР. Лечение ППР направлено на регресс вторичных половых признаков, прекращение менструаций, улучшение прогноза роста путем замедления ускоренных темпов оссификации скелета.
При выявлении гормонально активных опухолей надпочечников, яичников прибегают к хирургическим методам лечения. Кроме того, оперативные вмешательства рассматриваются при необходимости коррекции строения наружных половых органов у девочек на фоне ВГКН.
Лечение гетеросексуального ППР на фоне ВГКН осуществляется путем заместительной гормонотерапии глюкокортикоидами. Контроль лечения осуществляют на основании уровней 17-ОНП (целевой уровень – верхняя граница нормы), оценивают концентрации тестостерона (1 р/год) и ренина крови.
Клинические проявления ППР по изосексуальному типу сходны с изменениями, наблюдающимися в период полового созревания: увеличение ГЖ с последующим появлением полового оволосения, феминизация фигуры.
Наиболее информативен в диагностике гонадотропинзависимого ППР лютеинизирующий гормон (ЛГ). Обязательным условием при лабораторном обследовании является использование высокочувствительных методик и наличие в лаборатории допубертатных показателей. Меньшей диагностической ценностью обладает фолликулостимулирующий гормон (ФСГ). Использование соотношения ЛГ/ФСГ помогает дифференцировать быстро прогрессирующие формы ППР (показатель выше) от не требующих лечения медленно прогрессирующих форм. Содержание эстрадиола позволяет подтвердить диагноз ППР уже при выраженной прогрессии полового развития и не является информативным на ранних стадиях.
Дополнительным показателем, позволяющим установить ППР, является антимюллеров гормон. Он практически не определяется у девочек до периода полового созревания, в то время как на фоне пубертата отмечается рост данного показателя [3].
С целью дифференциальной диагностики гонадотропинзависимых и гонадотропиннезависимых форм ППР и изолированного телархе проводится стимуляционная проба с гонадотропин-рилизинг гормоном (ГнРГ), методика которой описана в таблице 2 [4].
Критерии оценки пробы:
• повышение ЛГ >10 Ед/л свидетельствует о наличии гонадотропинзависимого ППР;
• отсутствие стимуляции ЛГ свидетельствует о наличии гонадотропиннезависимого ППР;
• соотношении ФСГ/ЛГ >1 свидетельствует о наличии изолированного телархе.
Следующий шаг в диагностическом поиске – использование инструментальных методов. Ультразвуковое исследование ОМТ не только позволяет диагностировать признаки ППР, но и является дополнительным методом дифференциальной диагностики между истинным ППР и изолированным телархе.
УЗ-признаки ППР [5]:
• увеличение длины матки >3,4 см;
• формирование угла между шейкой и телом матки;
• толщина эндометрия (М-эхо; чувствительность данного критерия невысока – 42-87%);
• увеличение размеров яичников >3 см3.
Наличие единичных фолликулов не позволяет дифференцировать ППР от изолированного телархе. Обнаружение кист яичников помогает в диагностике гонадотропиннезависимых форм ППР (синдром МакКьюна-Олбрайта-Брайцева и фолликулярных кист яичников).
Инструментальная диагностика при ППР может также включать МРТ ОМТ, МРТ головного мозга. МРТ головного мозга проводится при доказанном гонадотропинзависимом характере ППР: у девочек младше 6 лет оно обязательно, девочкам с дебютом ППР в промежутке от 6 до 8 лет назначается при наличии неврологической симптоматики и признаков гипопитуитаризма.
Для лечения истинного ППР в настоящее время применяются аналоги ГнРГ. Непременное условие терапии пролонгированными аналогами ГнРГ – непрерывность терапии, ведение календаря и строгое соблюдение режима инъекций.

Оценка эффективности терапии проводится не раньше чем через 3 мес от начала лечения, затем каждые 6 мес по совокупности клинических и лабораторных показателей. Она включает:
• осмотр пациента 1 раз в 6 мес (антропометрия, оценка полового развития);
• рентгенографию кистей 1 р/год (при высоких темпах роста и прогрессии полового развития – 1 р/6 мес);
• проведение инструментальных исследований (УЗИ ОМТ– 1 р/6 мес);
• лабораторное обследование: определение уровня ЛГ, ФСГ, эстрадиол – 1 раз/6 мес (выполняется за 1-3 дня до очередной инъекции препарата); проведение пробы с ГнРГ – через 6 мес от начала терапии и при условии прогрессии полового развития; при этом умеренно повышенный уровень ФСГ не является признаком отсутствия эффекта терапии.
В настоящее время не существует единых общепринятых схем терапии гонадотропиннезависимых форм ППР (синдром МакКьюна-Олбрайта-Брайцева). Проводятся научные исследования по лечению данного контингента больных антиэстрогенами (тамоксифен, торемифен, фулвестрант).
Список литературы находится в редакции.
| Медична газета «Здоров’я України 21 сторіччя» № 8 (381), квітень 2016 р. |