17 лютого, 2022
DUAL V: Рандомізоване Клінічне Дослідження. Вплив інсуліну гларгін (up titration) vs інсулін деглюдек/ліраглутид на рівні глікованого гемоглобіну у пацієнтів із неконтрольованим ЦД 2 типу
Для більшості пацієнтів із цукровим діабетом (ЦД) 2 типу досягнення оптимального контролю глюкози є непростим завданням; рівень глікованого гемоглобіну (HbA1c) <7,0% має третина хворих, які отримують терапію базальним інсуліном. Попри це багато пацієнтів продовжують застосовувати базальний інсулін і після інтенсифікації лікування. Остання зазвичай передбачає підвищення дози базального інсуліну чи додавання ≥1 ін’єкцій інсуліну короткої дії під час їди. Утім, в обох випадках підвищується ризик розвитку гіпоглікемії та збільшення маси тіла. Крім того, існує практичне обмеження глюкозознижувальної ефективності, якої можна досягти тільки підвищенням дози інсуліну, незалежно від застосованого режиму. Альтернативою, рекомендованою міжнародними настановами, є комбінація агоністів рецепторів глюкагоноподібного пептиду‑1 (ГПП‑1) і базального інсуліну, котра розширює наявні варіанти інтенсифікації лікування.
У дослідженні DUAL V оцінювали з практичного погляду та з погляду пацієнтів відносну ефективність і безпеку інтенсифікації дози базального інсуліну гларгін за введення 1 р/добу проти фіксованої комбінації базального інсуліну деглюдек й агоніста рецепторів ГПП‑1 ліраглутиду (максимальна доза – 50 кроків дози, що відповідає 50 ОД інсуліну деглюдек та 1,8 мг ліраглутиду) також за введення 1 р/добу.
Головною метою цього дослідження було встановити, чи є комбінація деглюдек/ліраглутид принаймні не гіршою за гларгін стосовно зміни рівня HbA1c у пацієнтів із ЦД 2 типу, неконтрольованим на тлі гларгіну й метформіну. За умови отримання позитивної відповіді визначали, чи є комбінація деглюдек/ліраглутид кращою за гларгін щодо зміни рівнів HbA1c, маси тіла та частоти підтвердженої гіпоглікемії.
Матеріали та методи
DUAL V – міжнародне багатоцентрове рандомізоване клінічне дослідження ІІІ фази, що тривало 29 тиж (2 тиж від скринінгу до рандомізації, 26 тиж лікування та 1 тиж спостереження). До участі залучали пацієнтів віком ≥18 років із ЦД 2 типу й рівнями HbA1c 7-10%, які отримували стабільні дози гларгіну (загальна добова доза – 20-50 ОД/добу) та метформіну (≥1500 мг/добу), з індексом маси тіла ≤40 кг/м2.
Пацієнтів рандомізували 1:1 на лікування комбінацією деглюдек/ліраглутид або продовження терапії гларгіном, водночас кожний препарат титрували до однаково цільового рівня глюкози натще. Пацієнти, рандомізовані на деглюдек/ліраглутид, припиняли лікування гларгіном і починали терапію комбінацією деглюдек/ліраглутид у дозі 16 кроків дози незалежно від дози гларгіну на момент рандомізації; цю дозу призначали щодня 1 р/добу в будь-який, але бажано в той самий час дня. Максимальна дозволена доза становила 50 кроків дози на добу, тобто 50 ОД деглюдеку й 1,8 мг ліраглутиду.
Пацієнти, рандомізовані на гларгін, продовжували лікування цим інсуліном у раніше застосовуваній дозі, без обмеження щодо максимальної дози під час дослідження. Препарат призначали щодня 1 р/добу.
В обох групах двічі на тиждень здійснювали титрацію дози, засновану на середньому показнику трьох попередніх самостійних вимірювань глюкози крові перед сніданком. Якщо цей показник був <4 або >5 ммоль/л, дозу інсуліну або фіксованої комбінації відповідно знижували чи підвищували на 2 кроки дози, або на 2 ОД.
Первинною кінцевою точкою була зміна HbA1c після 26 тиж лікування порівняно з вихідним рівнем. Вторинні кінцеві точки включали зміну маси тіла та кількості епізодів гіпоглікемії впродовж 26 тиж. Пошуковими заздалегідь визначеними кінцевими точками були доза інсуліну, зміна глюкози плазми натще (ГПН), профіль самостійно виміряної глюкози крові (СВГК), кількість пацієнтів, які досягли цільових рівнів HbA1c (<7 та ≤6,5%), а також комбіновані показники, що базувалися на рівні HbA1c без гіпоглікемії та/або збільшення маси тіла. Дев’ятьма точками часу для СВГК були сніданок, 90 хв після сніданку, обід, 90 хв після обіду, вечеря, 90 хв після вечері, перед сном, 4:00 ранку та сніданок наступного дня. Крім того, post hoc проаналізували середній рівень глюкози для кожної точки СВГК, а також підтверджену гіпоглікемію залежно від кінцевого рівня HbA1c. Кінцевими точками безпеки були кількість небажаних подій (НП) та нічних епізодів гіпоглікемії, зміна стандартних лабораторних показників, артеріального тиску й частоти серцевих скорочень. Для оцінки лікування з погляду пацієнтів використовували опитувальники TRIM-D та SF‑36.
Результати
Після скринінгу 767 пацієнтів у 10 країнах в клінічне дослідження рандомізували 557 хворих (середній вік – 58,8 року; жінок – 49,7%); із них 92,5% завершили дослідження та мали дані після 26 тиж терапії. За вихідними клініко-демографічними характеристиками групи були подібними. Загалом 239 із 278 пацієнтів групи комбінації деглюдек/ліраглутид (86%) та 255 із 279 хворих групи гларгіну (81%) здійснили всі заплановані візити з 0-го по 26-й тиждень.
Первинна кінцева точка
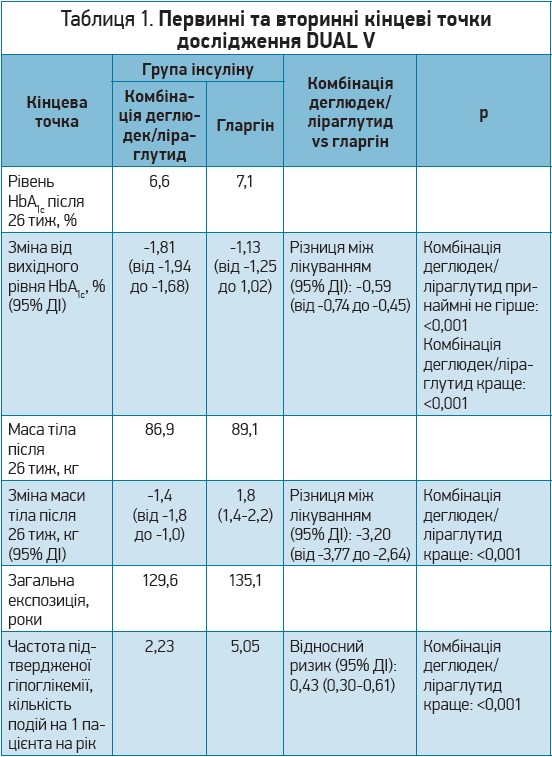
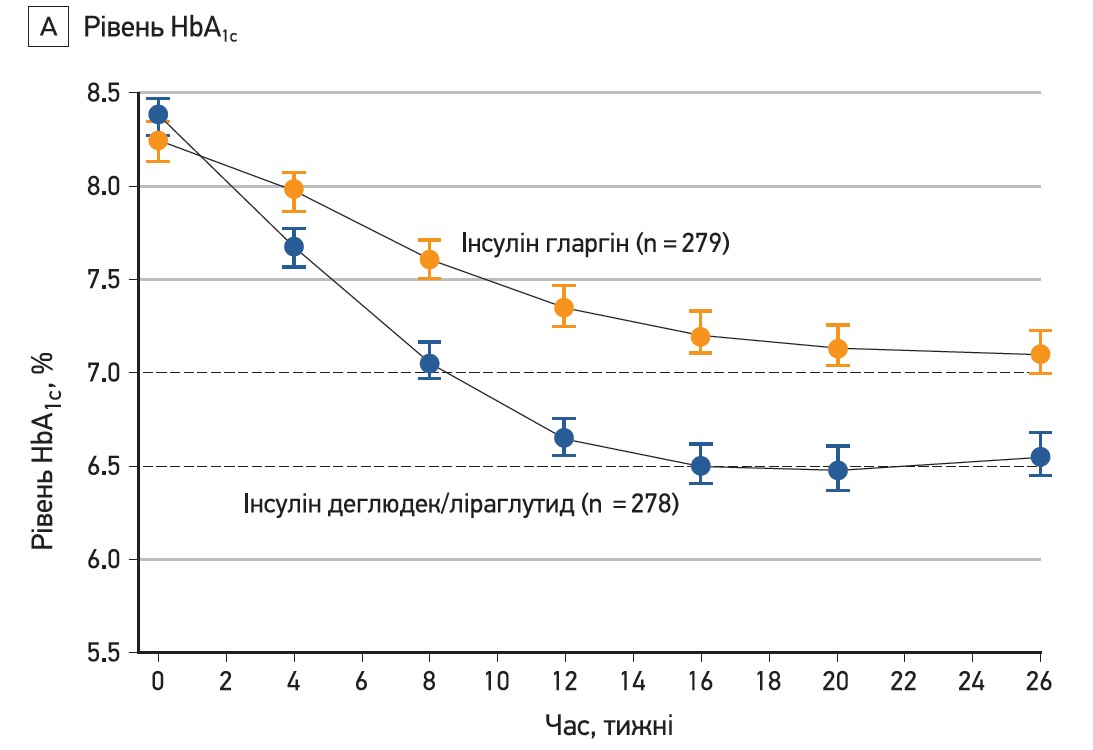
Вихідний рівень HbA1c становив 8,4% у групі комбінації деглюдек/ліраглутид та 8,2% у групі гларгіну. Цей показник знизився протягом перших 16 тиж лікування й на 26-му тижні стабілізувався до 6,6 та 7,1% відповідно. Загалом після 26 тиж терапії середній рівень HbA1c знизився на 1,81% у групі комбінації деглюдек/ліраглутид й на 1,13% у групі гларгіну, що відповідає різниці між лікуванням -0,59% (табл. 1; рис. 1А) з доведеною принаймні не гіршою ефективністю комбінації деглюдек/ліраглутид порівняно з гларгіном (р<0,001).
Вторинні кінцеві точки
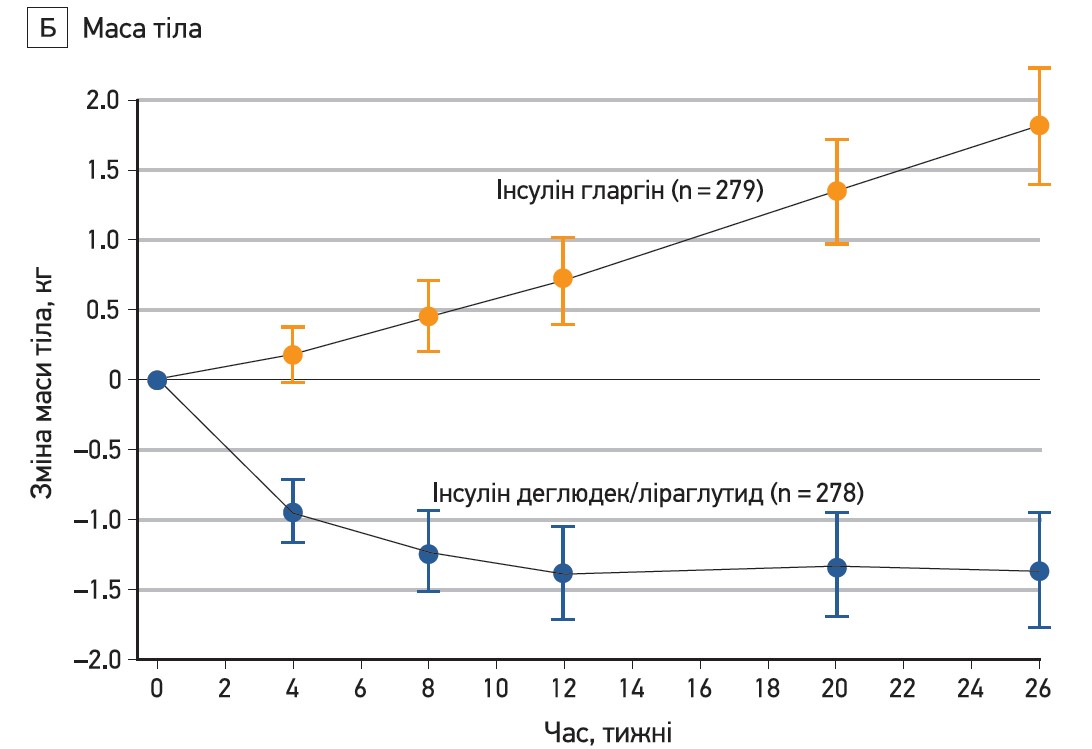
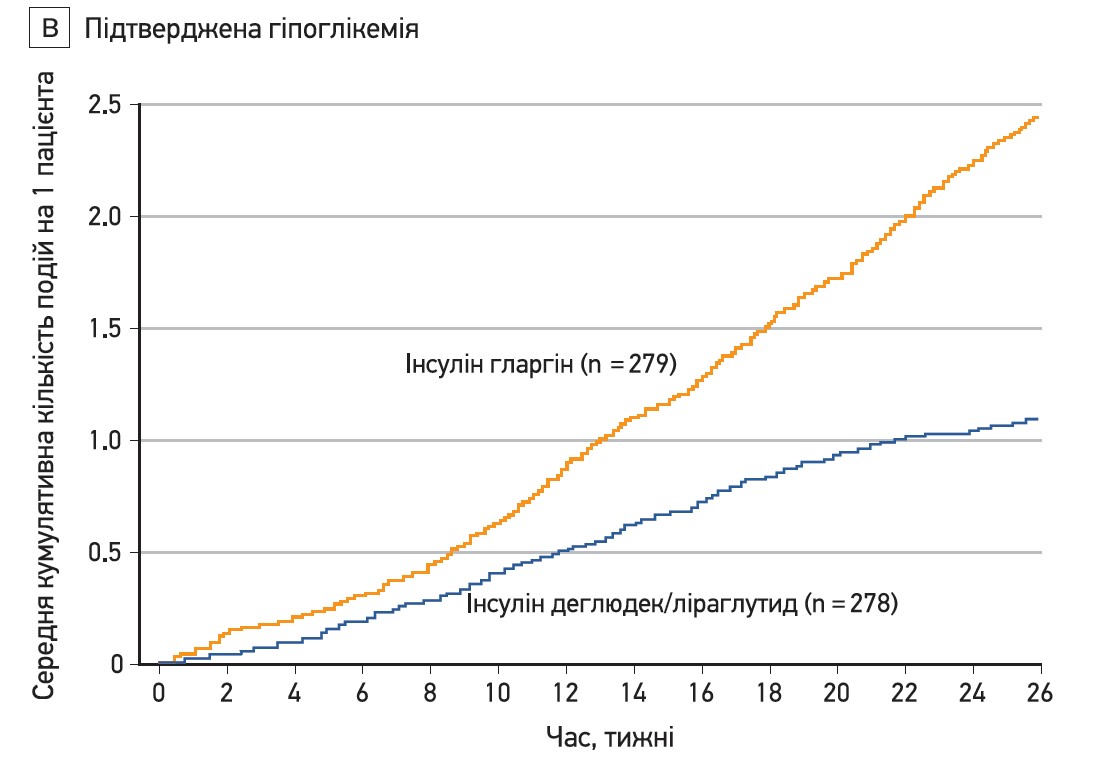
Різниця між лікуванням щодо зміни рівня HbA1c (-0,59%; р<0,001) також відповідала критерію статистично значущої переваги комбінації деглюдек/ліраглутид над гларгіном (табл. 1; рис. 1). Окрім того, в групі комбінації деглюдек/ліраглутид спостерігали зниження маси тіла на 1,4±3,5 кг (із 88,3±17,5 до 86±17,2 кг), тоді як у групі гларгіну вона зросла на 1,8±3,6 кг (із 87,3±15,8 до 89,1±15,9 кг); це відповідає різниці між лікуванням -3,20 кг (р<0,001; табл. 1, рис. 1Б). Підтверджену гіпоглікемію спостерігали в меншої кількості пацієнтів групи комбінації деглюдек/ліраглутид порівняно з хворими групи гларгіну (28,4 проти 49,1% відповідно). Так само в групі комбінації деглюдек/ліраглутид кількість епізодів гіпоглікемії на 1 пацієнта на рік була меншою, ніж у групі гларгіну (2,23 проти 5,05 епізоду відповідно), що відповідає зниженню відносного ризику гіпоглікемії на 57% у разі лікування комбінацією деглюдек/ліраглутид (р<0,001; табл. 1, рис. 1В). У дослідженні зафіксували тільки один епізод тяжкої гіпоглікемії – у групі гларгіну. Усі аналізи чутливості продемонстрували подібні результати стосовно статистичної значущості й розміру ефекту.
Рис. 1. Зміни рівня HbA1c та маси тіла, а також кумулятивна частота підтвердженої гіпоглікемії при лікуванні комбінацією деглюдек/ліраглутид проти інсуліну гларгін
Пошукові заздалегідь визначені кінцеві точки
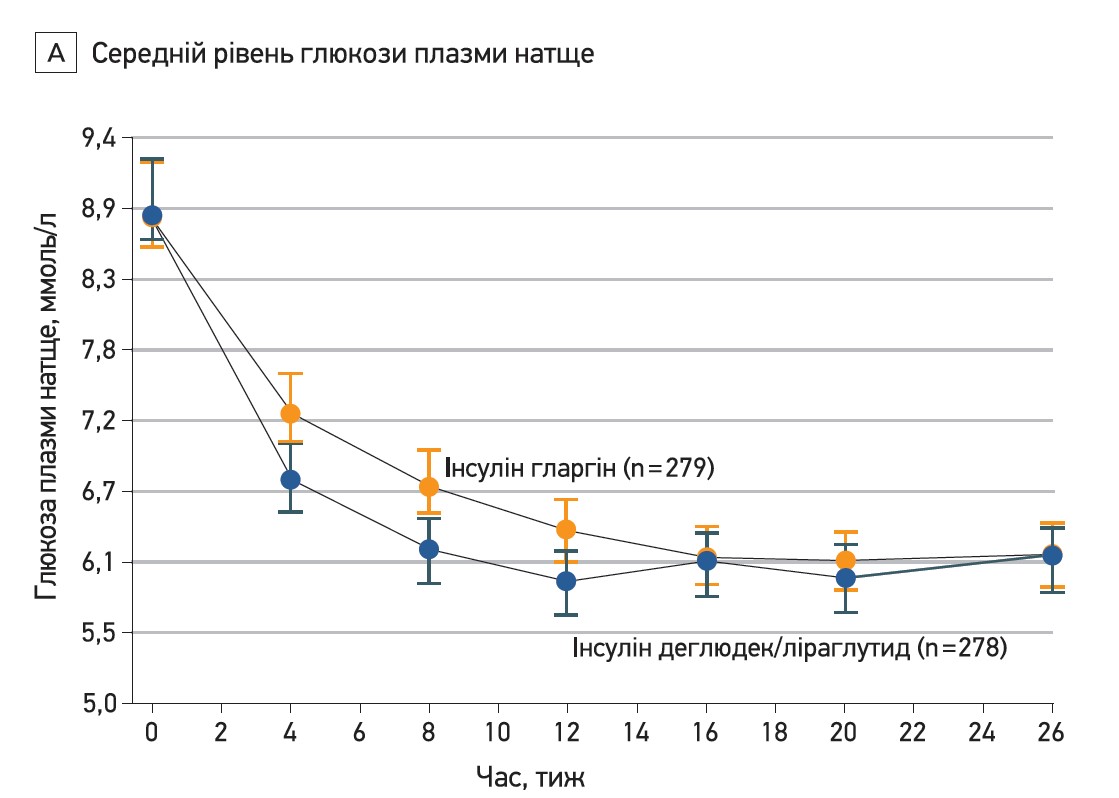
Після 26 тиж лікування рівні ГПН знизилися до 6,07±2,13 ммоль/л у групі комбінації деглюдек/ліраглутид та 6,12±2,12 ммоль/л у групі гларгіну (р=0,96; рис. 2А). Середні рівні СВГК, які вимірювали з метою титрації дози, знизилися в обох групах протягом перших 12 тиж терапії (більшою мірою в групі комбінації деглюдек/ліраглутид) та стабілізувалися до 26-го тижня на 5,87±1,44 ммоль/л у групі комбінації деглюдек/ліраглутид та 5,59±1,32 ммоль/л у групі гларгіну.
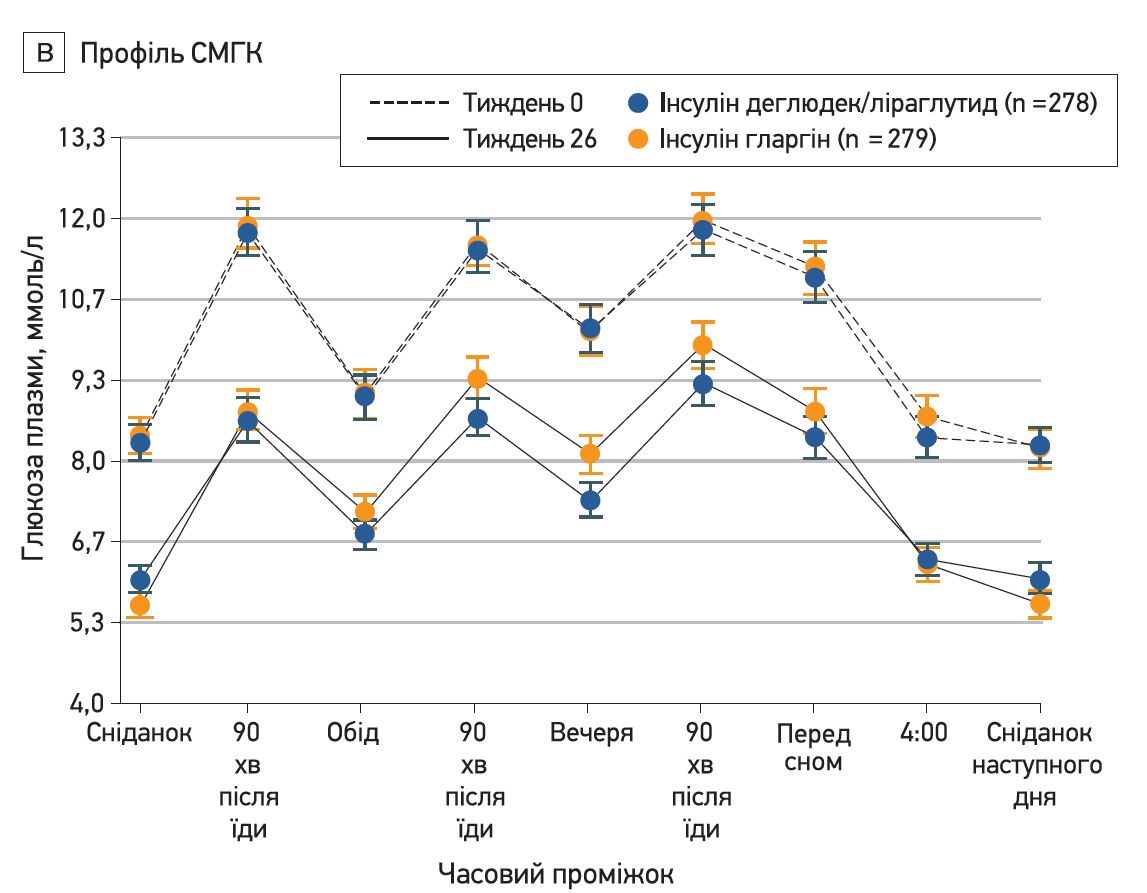
В обох групах після 26 тиж лікування також знизилися середні показники СВГК, виміряні в 9 точках часу: на 2,53±2,41 до 7,56±1,92 ммоль/л у групі комбінації деглюдек/ліраглутид та на 2,36±2,75 до 7,85±1,87 ммоль/л у групі гларгіну. Різниця між лікуванням становила -0,22 (95% довірчий інтервал (ДІ) від -0,53 до 0,09; рис. 2Б).
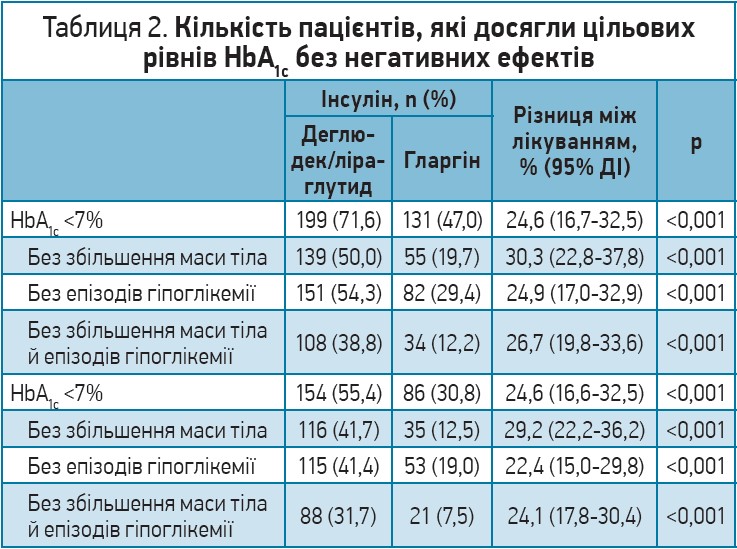
Цільові рівні HbA1c (<7,0 та ≤6,5%) зафіксували в більшої кількості пацієнтів, які отримували комбінацію деглюдек/ліраглутид, порівняно з хворими групи гларгіну, і цей результат був досягнутий без збільшення маси тіла та/або гіпоглікемії (р<0,001 для всіх показників; табл. 2).
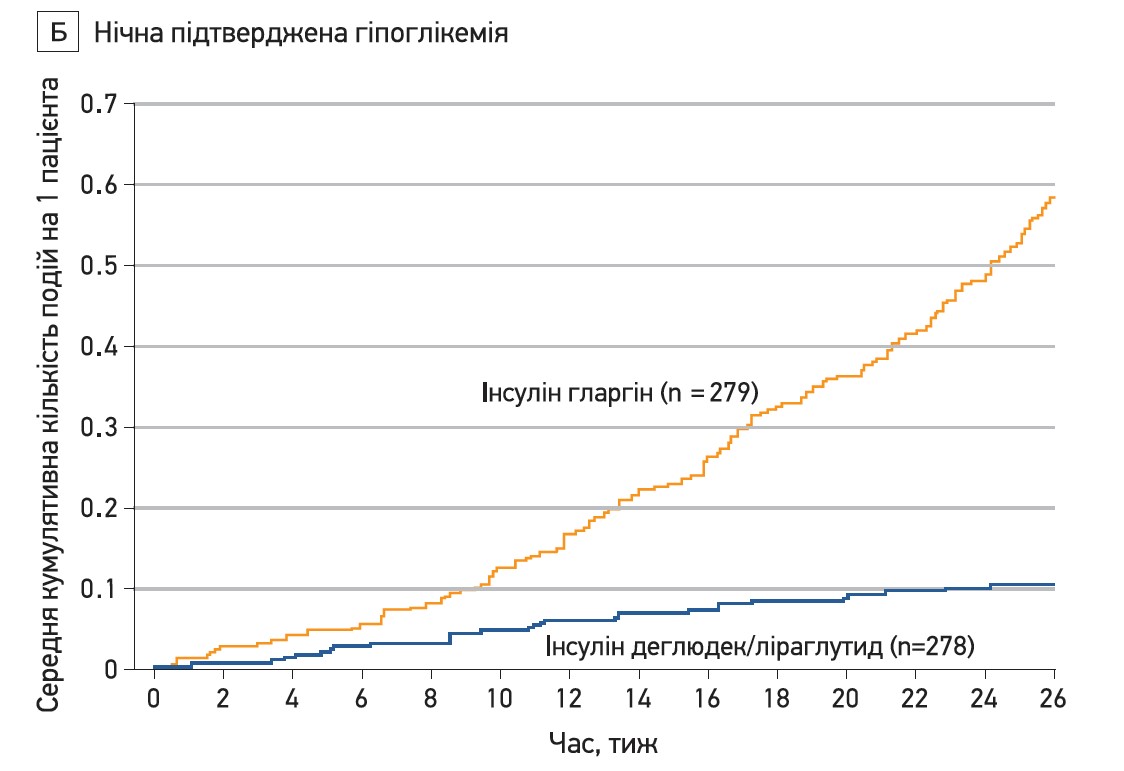
Нічні підтверджені епізоди глікемії спостерігали у 24,4% хворих групи гларгіну й тільки в 6,1% пацієнтів групи комбінації деглюдек/ліраглутид, що відповідає кількості подій на 1 пацієнта на рік 1,23 та 0,22 відповідно. Відносний ризик нічної глікемії в групі комбінації деглюдек/ліраглутид був на 83% нижчим, аніж у групі гларгіну (р<0,001; рис. 2В).
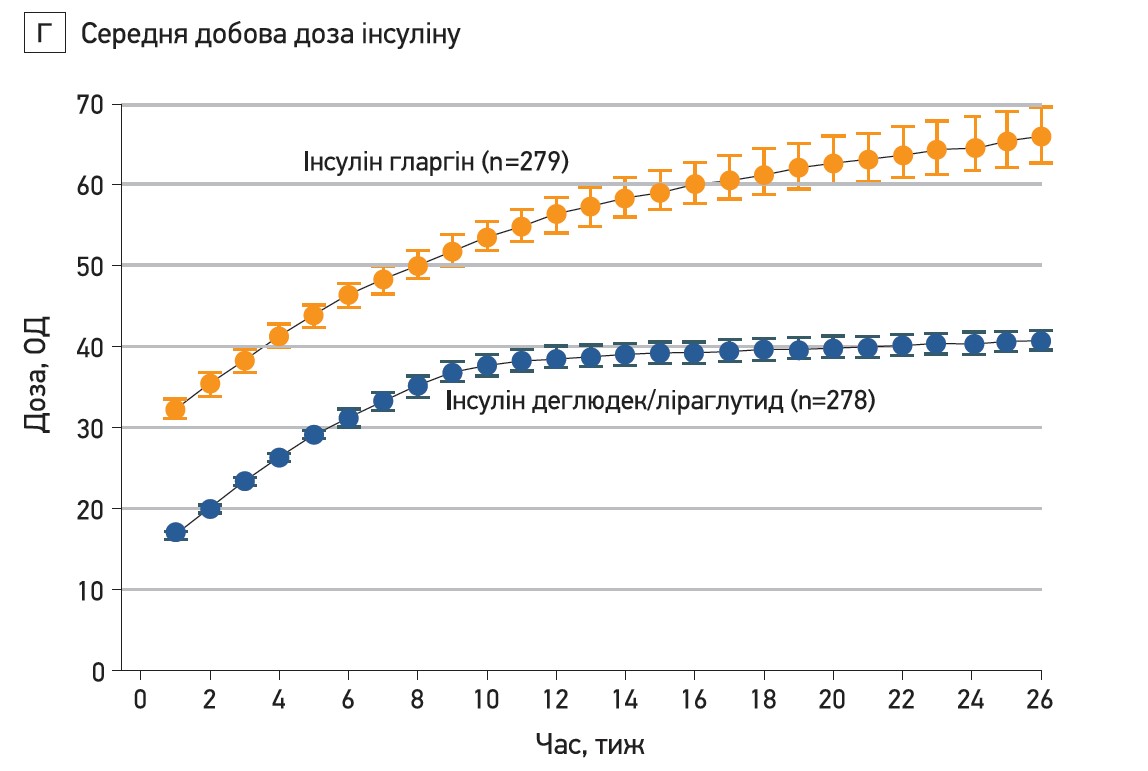
Після 26 тиж лікування середня доза комбінації деглюдек/ліраглутид становила 41 крок дози (41 ОД/1,48 мг), гларгіну – 66 ОД; різниця між лікуванням -25,47 ОД інсуліну (95% ДІ від -28,90 до -22,05; р<0,001). Приблизно 40% пацієнтів групи комбінації деглюдек/ліраглутид після 26 тиж отримали максимальні 50 кроків дози підвищення дози, з них рівня HbA1c <7% досягли 68% порівняно із 74% серед пацієнтів, які застосовували нижчу дозу комбінації деглюдек/ліраглутид.
Рис. 2. Зміни ГПН, профілю СВГК, нічної гіпоглікемії та дози інсуліну при лікуванні комбінацією деглюдек/ліраглутид проти інсуліну гларгін
Результати, повідомлені пацієнтами
Оцінка фізичного компонента опитувальника SF‑36 поліпшилася в групі комбінації деглюдек/ліраглутид (з вихідної 47,4 до 49,0 після 26 тиж) і погіршилася в групі гларгіну (із 47,7 до 46,1 відповідно); різниця між лікуванням становила 1,9 (р<0,001). Різниця між лікуванням на користь комбінації деглюдек/ліраглутид також відзначена для субдоменів «фізичне функціонування» (1,4; р=0,045), «біль у тілі» (2,0; р=0,01) та «загальне здоров’я» (1,7; р=0,008).
Оцінка за опитувальником TRIM-D – в усіх окремих субдоменах і загальна – поліпшилася в обох групах. Утім, поліпшення загальної оцінки було значно більшим для комбінації деглюдек/ліраглутид порівняно з гларгіном, переважно завдяки кращим оцінкам субдоменів «тягар лікування» та «ведення діабету» (різниця між лікуванням 3,7, р=0,02, та 7,2, р<0,001, відповідно), що свідчить про вищу задоволеність від лікування комбінацією деглюдек/ліраглутид.
Аналізи post hoc
Нижчу частоту підтвердженої гіпоглікемії для комбінації деглюдек/ліраглутид порівняно з гларгіном спостерігали незалежно від рівня HbA1c, досягнутого наприкінці дослідження. Аналіз вимірювань СВГК у 9 точках часу показав статистично значущо нижчий рівень глюкози крові через 90 хв після обіду (різниця між лікуванням -0,64 ммоль/л; р=0,006), перед вечерею (-0,69 ммоль/л; р=0,001) і після вечері (-0,57 ммоль/л; р=0,03), але вищий рівень перед сніданком наступного дня (0,40 ммоль/л; р=0,02) у групі комбінації деглюдек/ліраглутид; в 4 інших точках часу рівні глюкози крові були подібними в обох групах.
Гемодинамічні параметри
Частота серцевих скорочень після 26 тиж лікування підвищилася в групі комбінації деглюдек/ліраглутид та залишалася стабільною в групі гларгіну (різниця між лікуванням 3,71 уд./хв; р<0,001). Натомість систолічний артеріальний тиск знизився на тлі терапії комбінацією деглюдек/ліраглутид порівняно з гларгіном (-3,57 мм рт. ст.; р<0,001). Діастолічний артеріальний тиск істотно не змінився порівняно з вихідним в обох групах.
Лабораторні параметри
Після 26 тиж лікування рівні загального холестерину, холестерину ліпопротеїнів низької щільності та вільних жирних кислот були на 5, 8 і 15% нижчими порівняно з групою гларгіну (р<0,001 для всіх показників). За кінцевими рівнями холестерину ліпопротеїнів високої та дуже низької щільності, а також тригліцеридів групи не відрізнялися.
Під час терапії комбінацією деглюдек/ліраглутид спостерігали підвищення активності ліпази й амілази (+17,6 та +10,7 ОД/л відповідно); у групі гларгіну активність цих ферментів змінювалася мінімально (-2,2 та +2,2 ОД/л відповідно).
Рівні кальцитоніну були однаковими в обох групах протягом дослідження та практично не змінилися після 26 тиж лікування порівняно з початковими.
Небажані події
Загальна частота НП на 100 пацієнто-років становила 343,3 для комбінації деглюдек/ліраглутид та 286,4; частота серйозних НП на 100 пацієнто-років – 3,9 та 6,7 відповідно. Більшість НП були легкими й розцінені як такі, що малоймовірно пов’язані з лікуванням. Імовірно пов’язані з лікуванням НП, частота яких була вищою в групі комбінації деглюдек/ліраглутид, являли собою шлунково-кишкові розлади. Зокрема, про нудоту повідомляли більше пацієнтів у групі комбінації деглюдек/ліраглутид (9,4%; n=26; 26,2 події на 100 пацієнто-років), аніж у групі гларгіну (1,1%; n=3; 2,2 події на 100 пацієнто-років). Однак у будь-який тиждень під час дослідження на нудоту скаржилися не більш ніж 4% пацієнтів, які отримували комбінацію деглюдек/ліраглутид.
Із 4 підтверджених кардіоваскулярних подій 2 являли собою великі кардіоваскулярні події (визначені як нефатальний інфаркт міокарда, нефатальний інсульт або кардіоваскулярна смерть), по 1 у кожній групі. Хворий групи гларгіну помер від геморагічного інсульту, а пацієнт, який отримував комбінацію деглюдек/ліраглутид, повністю одужав після ішемічного інсульту. Обидві події були розцінені як не пов’язані з лікуванням.
Висновки
У пацієнтів із неконтрольованим ЦД 2 типу, котрі отримують гларгін і метформін, лікування комбінацією деглюдек/ліраглутид порівняно з інтенсифікацією дози гларгіну забезпечує принаймні не гірші рівні HbA1c. Вторинний аналіз свідчить про більш значуще зниження HbA1c після 26 тиж терапії комбінацією деглюдек/ліраглутид.
Коментар експерта
Завідувач відділу профілактики, лікування цукрового діабету та його ускладнень Українського науково-практично центру ендокринної хірургії, трансплантації ендокринних органів і тканин (м. Київ), експерт МОЗ України з ендокринології, доктор медичних наук, професор Володимир Іванович Паньків
 DUAL V – перше клінічне дослідження, в якому порівнювали фіксовану комбінацію деглюдек/ліраглутид (Ксалтофай) із базальним інсуліном гларгін у пацієнтів, котрі зазнали невдачі інсулінотерапії з дозволеною необмеженою титрацією. Насправді це дуже велика популяція хворих на ЦД 2 типу. Дослідження продемонструвало значно кращу здатність фіксованої комбінації досягати цільових рівнів HbA1c.
DUAL V – перше клінічне дослідження, в якому порівнювали фіксовану комбінацію деглюдек/ліраглутид (Ксалтофай) із базальним інсуліном гларгін у пацієнтів, котрі зазнали невдачі інсулінотерапії з дозволеною необмеженою титрацією. Насправді це дуже велика популяція хворих на ЦД 2 типу. Дослідження продемонструвало значно кращу здатність фіксованої комбінації досягати цільових рівнів HbA1c.
Глікемічна варіабельність (ГВ) є інтегральним компонентом гомеостазу глюкози. З’являється дедалі більше доказів, що добова ГВ корелює з підвищенням ризиків макро- та мікросудинних ускладнень діабету. У DUAL V за допомогою самостійного вимірювання глюкози крові було встановлено, що комбінація деглюдек/ліраглутид (Ксалтофай) значно краще контролює глікемію протягом доби, ніж гларгін, а отже, потенційно краще захищає від таких ускладнень. Вочевидь кращий контроль глікемії – як довгострокової, так і добової – при застосуванні комбінації деглюдек/ліраглутид (Ксалтофай) досягається комплексним впливом майже на всі центральні та периферичні складові патофізіологічного процесу ЦД 2 типу.
Важливими результатами лікування комбінацією деглюдек/ліраглутид (Ксалтофай) також є достовірне зниження ваги (тоді як гларгін її збільшував) і частоти гіпоглікемічних епізодів, а ці побічні ефекти інсулінотерапії разом із терапевтичною інертністю є головними перешкодами для ефективної інтенсифікації лікування діабету. Такі результати досягнено завдяки ліраглутиду, який має інсулінзберігальну дію та достовірно зменшує масу тіла.
Зрештою, терапія комбінацією деглюдек/ліраглутид (Ксалтофай) у дослідженні DUAL V супроводжувалася суттєвим зниженням систолічного артеріального тиску та покращенням ліпідного профілю. Супутню артеріальну гіпертензію мають три чверті пацієнтів із ЦД 2 типу, дисліпідемію – понад 90%, тому ці ефекти лікування є додатковою перевагою стосовно покращення кардіоваскулярного ризику.
У Стандартах медичної допомоги при діабеті Американської діабетичної асоціації (ADA, 2022) зазначено, що в пацієнтів із ЦД 2 типу, які потребують ін’єкційної терапії для покращення глікемічного контролю, перевагу мають агоністи рецепторів ГПП‑1, як-от ліраглутид. Водночас наголошується, що в пацієнтів, котрі перебувають на інсулінотерапії, комбінована терапія з включенням агоніста ГПП‑1 є ефективнішим і надійнішим лікуванням глікемії, ніж лише підвищення дози інсуліну. Відтак, застосування фіксованої комбінації деглюдек/ліраглутид (Ксалтофай) для інтенсифікації ін’єкційної терапії пацієнтів із ЦД 2 типу повністю узгоджується із сучасними клінічними настановами.
Список літератури знаходиться в редакції.
Стаття друкується в скороченні.
Lingvay I., Manghi F. P., García-Hernández P. et al. Effect of insulin glargine up-titration vs insulin degludec/liraglutide on glycated hemoglobin levels in patients with uncontrolled type 2 diabetes: the DUAL V randomized clinical trial. JAMA. 2016 Mar 1; 315 (9): 898-907.
Переклав з англ. Олексій Терещенко