10 листопада, 2022
Пробіотик Bacillus clausii: сьогодення та перспективи застосування в клінічній практиці
 Останніми роками отримано безліч переконливих доказів величезного потенціалу дії мікробіому на різні процеси функціонування організму людини. Фактично на наших з вами очах сталася значна трансформація. Якщо на початку XXI століття мікробіоту називали забутим органом (існувало навіть таке медичне кліше: кишкова мікробіота – це наш забутий орган), то 2022 року питання, так чи інакше пов’язані з кишковою мікробіотою, належать до числа п’яти найактуальніших медичних тем.
Останніми роками отримано безліч переконливих доказів величезного потенціалу дії мікробіому на різні процеси функціонування організму людини. Фактично на наших з вами очах сталася значна трансформація. Якщо на початку XXI століття мікробіоту називали забутим органом (існувало навіть таке медичне кліше: кишкова мікробіота – це наш забутий орган), то 2022 року питання, так чи інакше пов’язані з кишковою мікробіотою, належать до числа п’яти найактуальніших медичних тем.
І така цікавість до мікробіому є виправданою та зрозумілою. Вже доведено, що зміни в мікробіоті кишечнику сприяють розвитку і прогресуванню таких неінфекційних захворювань, як астма, ожиріння, некротичний ентероколіт, діабет 1 типу, аутизм і багато інших тяжких алергічних й автоімунних захворювань. Таким чином, крім зовнішніх факторів, таких як спосіб життя, гігієна, фізична активність і застосування антибіотиків, вирішальну роль у розвитку низки серйозних патологій відіграє і мікробіом. Величезний внесок в наше розуміння значення мікробіому вніс проєкт Human Microbiome, який стартував у 2007 році і являв собою програму з вивчення ролі мікробіому в підтриманні здоров’я людини, яка була реалізована Національним інститутом охорони здоров’я США. Результати цього проєкту переконливо продемонстрували доцільність включення пробіотичних мікроорганізмів у комплексне лікування соматичної патології. Одним із найвивченіших пробіотиків, котрий має підтверджену пробіотичну активність, високу ефективність і безпеку, є Bacillus clausii.
На сьогодні відомо, що нормальна мікрофлора кишечнику людини складається з трильйонів мікроорганізмів, включаючи 180-200 найпоширеніших і близько 1000 рідкісних штамів. Число клітин бактерій на порядок перевищує кількість клітин людини, а число генів у метагеномі становить приблизно 106, тобто на два порядки більше, ніж генів людини. Однією з найбільш вивчених пробіотичних бактерій є Bacillus clausii.
Bacillus – рід непатогенних спороутворювальних бактерій, які зустрічаються в повітрі, воді, ґрунті, а також є постійним членом мікробіоценозу кишечнику тварин і людини. У несприятливих умовах навколишнього середовища спороутворювальні бактерії проходять складний процес розвитку, впродовж якого бактеріальна клітина диференціюється у спору, здатну необмежено довго виживати за відсутності води й нутрієнтів, за екстремальних значень температури і рН, під ультрафіолетовим випромінюванням чи під дією шкідливих хімікатів. Після відновлення сприятливих умов середовища спори проростають у вегетативні клітини, здатні рости та розмножуватися. Спори Bacillus є метаболічно неактивними і можуть переносити жовчні солі, виживати в кислому середовищі шлунка; водночас вони є стабільнішими за вегетативні бактерії під час обробки та зберігання у вигляді пробіотичних лікарських препаратів або дієтичних добавок.
На сьогодні було ізольовано вже декілька штамів B. clausii. За допомогою найсучасніших молекулярно-генетичних методів дослідження, а саме методів геномного секвенування було встановлено, що штами O/C, N/R, SIN та T є тісно пов’язаними зі штамом B106, який, своєю чергою, є подібним до штаму UBBC‑07.
Фізіологічні властивості Bacillus clausii
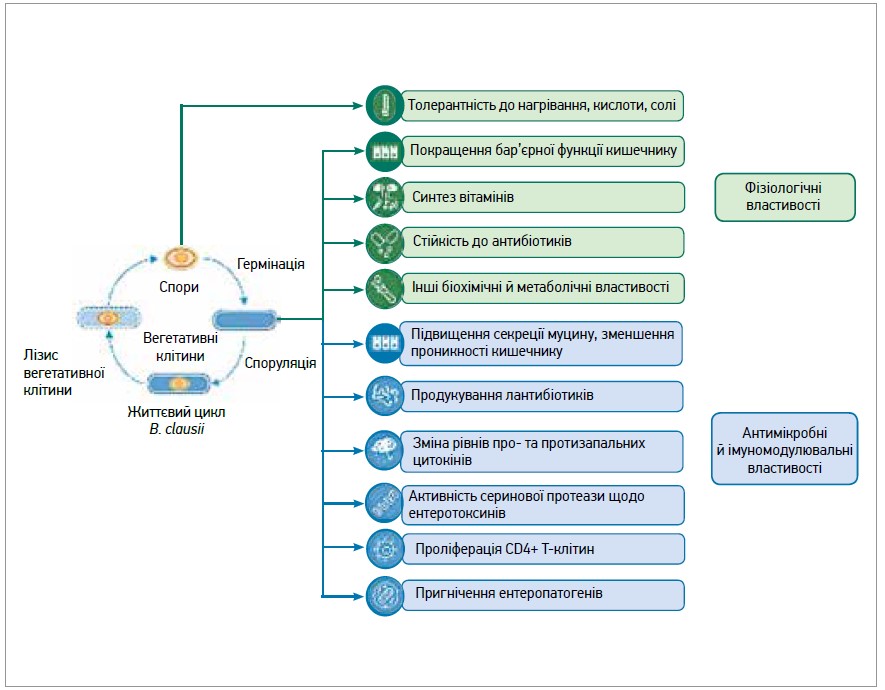
Безперечно, що організація будь-якого мікробіологічного синтезу практично важливих речовин починається з вивчення фізіології штаму. Стосовно B. clausii у численних дослідженнях були продемонстровані корисні фізіологічні властивості її штамів, наприклад, стійкість до жовчних солей і кислоти шлунка; покращення бар’єрної функції кишечнику; широкий спектр резистентності до антибіотиків, яка не може генетично передаватися іншим видам бактерій; синтез вітамінів тощо (рис.).
Рис. Фізіологічні, протимікробні й імуномодулювальні властивості Bacillus clausii (адаптовано за Ghelardi E. і співавт., 2022)
Стійкість до агресивних середовищ травного тракту
Зрозуміло, що для того щоб повною мірою виявити свої корисні ефекти, пробіотики повинні виживати в агресивних середовищах шлунково-кишкового тракту, мати здатність розмножуватися й колонізувати кишечник. У нещодавньому дослідженні вивчали здатність різних пробіотиків переносити середовище шлунка і тонкої кишки. Було встановлено, що штами B. clausii здатні виживати в симульованій шлунковій рідині принаймні 120 хв, натомість життєздатність більшості інших пробіотиків знижувалася після 30 хв. Крім того, штами B. clausii були єдиними, котрі показали здатність виживати й розмножуватися після 240 хв експозиції симульованого середовища тонкої кишки.
Синтез вітамінів
Здатність синтезувати різні вітаміни, наприклад, вітаміни групи B, і тим самим, до речі, сприяти корекції порушень, викликаних застосуванням антибіотиків, є невід’ємною складовою умов, які ми висуваємо до пробіотичних штамів. Крім того, на жаль, людина, як і тварини, не здатна продукувати рибофлавін (вітамін В2), необхідний для належного функціонування та росту клітин. Бактерії, котрі виробляють і секретують рибофлавін, більш перспективні для використання як пробіотики, оскільки можуть компенсувати дефіцит цього вітаміну. Встановлено, що вегетативні клітини B. clausii продукують достатню кількість рибофлавіну для підтримання власного росту в рибофлавін-дефіцитному середовищі, а також секретують високі рівні рибофлавіну, що дозволяє рости іншим корисним бактеріям.
Стійкість до антибіотиків
Після багатьох років і навіть десятиріч використання пробіотичних штамів з’ясувалося, що значна частина пробіотиків є чутливою до більшості антибіотиків. Дані сучасної літератури свідчать про те, що переважна більшість лактобацил, ентерококів, біфідобактерій не є резистентною до таких широко застосовуваних антибіотиків, як амоксицилін, доксициклін, фторхінолони і цефалоспорини. Це є суттєвим недоліком бактеріальних препаратів, що значно обмежує їх використання, адже їх поєднання з антибіотикотерапією або застосування безпосередньо після неї неминуче супроводжується інактивацією штамів таких пробіотиків. Тому стійкість до антибіотиків у поєднанні з доведеною нездатністю передавати цю стійкість іншим бактеріям є важливою рисою безпечного пробіотика. Це дозволяє використовувати пробіотик одночасно з лікуванням антибіотиками в ситуації, коли кишечник зазвичай позбавляється своєї природної мікрофлори та потребує повторного заселення корисними бактеріями. Вегетативні клітини B. clausii є стійкими до широко застосовуваних антибіотиків, зокрема до пеніцилінів, цефалоспоринів, макролідів, кліндаміцину, лінкоміцину, хлорамфеніколу, метронідазолу тощо.
Водночас повногеномний аналіз штаму B. clausii показав, що гени резистентності до антибіотиків знаходяться в хромосомній ДНК, тож це унеможливлює її передачу іншим видам мікроорганізмів, що також є суттєвою перевагою даного штаму.
Доклінічні дослідження
Доклінічне вивчення окремих штамів, які в майбутньому будуть використовуватися як медичні препарати, безперечно, є невід’ємною частиною процесу створення лікарського засобу. Встановлені за результатами доклінічного вивчення характеристики специфічної фармакологічної активності та нешкідливості під час застосування і щодо його ймовірних віддалених наслідків є принциповими факторами, які визначають можливість промислового випуску лікарського засобу та доцільність його медичного використання. Такі дослідження проводилися і при вивченні B. clausii. З’ясувалося, що в геномі B. clausii присутня низка пробіотичних генів, які відповідають за стійкість до кислого середовища й жовчних солей, продукування фібронектин-зв’язувальних білків, енолази, бактеріоцинів і вітамінів, а також за стійкість до антибіотиків. Штам UBBC‑07 має виражені антимікробні властивості завдяки виробленню речовин, які вбивають або попереджують ріст інших мікроорганізмів. Продукування глікозилгідролази (ферменту, котрий розщеплює глікопротеїни і є важливим компонентом лізоциму) також допомагає B. clausii стримувати ріст потенційно патогенних бактерій.
Вплив на імунну функцію кишечнику
Напевно, однією з найголовніших переваг використання бактерії B. clausii є її імуномодулюючий вплив на організм людини: B. clausii модулюють функціонування механізмів неспецифічного протиінфекційного захисту; в дослідженнях in vitro були виявлені властивості B. clausii, які допомагають підтримувати бар’єрну функцію кишечнику. На моделі ротавірусної інфекції з використанням людських ентероцитів було встановлено, що вегетативні клітини B. clausii індукують синтез муцину й антимікробних пептидів дефензину‑2 і кателіцидину; підтримують нормальну проліферацію ентероцитів, захищають їх від некрозу й апоптозу; пригнічують продукування кисневих радикалів ротавірусом та інгібують вивільнення прозапальних цитокінів. Ці механізми дії пояснюють клінічну ефективність B. clausii при гострому вірусному гастроентериті в дітей.
В іншому дослідженні на моделі травного тракту синбіотичний препарат, який містив спори B. clausii, підвищував вироблення бутирату мікробіомом, а також збільшував різноманіття мікробіоти, особливо рівні Faecalibacterium prausnitzii, Bifidobacterium spp. та Lactobacillus spp.; це свідчить про здатність B. clausii сприяти відновленню кишкового гомеостазу.
За експериментальної уремії (високих рівнів сечової кислоти в крові, що характерно для хронічної хвороби нирок) призначення спор B. clausii UBBC‑07 зменшувало сироваткові рівні сечовини, креатиніну та малонового діальдегіду, імовірно, завдяки антиоксидантним ефектам.
Вегетативні клітини деяких штамів В. clausii, зокрема UBBC‑07, можуть продукувати лантибіотик клаузин, який має антимікробну активність проти грампозитивних бактерій і зменшує цитотоксичні ефекти Clostridioides difficile.
Імуномодулюючі ефекти
Антимікробна активність пробіотиків чинить безпосередній вплив на інші кишкові мікроорганізми; натомість імуномодулююча дія пробіотиків відновлює баланс імунної системи з довготривалими корисними ефектами для здоров’я макроорганізму. Штамам B. clausii притаманні потужні імуномодулюючі механізми на гуморальному й клітинному рівнях. Під час розробки показань для клінічного застосування Bacillus повинні враховуватися унікальні імуномодулюючі властивості кожного штаму пробіотичної бактерії.
На моделі гастроентериту вегетативні клітини B. clausii індукували контрольовану запальну відповідь шляхом підвищення синтезу прозапальних цитокінів на ранній стадії інфекції та протизапальних цитокінів на більш пізніх стадіях, а також захищали макрофаги від S. typhimurium-індукованої цитотоксичності. Імуномодулюючі ефекти B. clausii також продемонстровані на моделях запалення верхніх дихальних шляхів, виразкового коліту, інфекції C. difficile та ентеропатогенної E. coli O127: H21, глистних інвазій тощо.
Клінічні дослідження
Добре відомо, що ефективність і безпека пробіотичних препаратів B. clausii підтверджені багаторічним досвідом використання і численними клінічними дослідженнями в пацієнтів із різноманітними шлунково-кишковими розладами, алергічним ринітом й інфекціями верхніх дихальних шляхів (ІВДШ).
Наприклад, у проспективному дослідженні Sudha та співавт. (2013) штам B. clausii UBBC‑07 продемонстрував клінічну ефективність у зменшенні симптомів діареї в пацієнтів дорослого віку, не спричинивши жодних побічних ефектів. У 2019 році ці науковці вивчали безпеку та ефективність суспензії спор B. clausii UBBC‑07 у лікуванні дітей віком від 6 міс до 5 років із гострою діареєю і встановили, що пробіотик скорочує тривалість діареї, зменшує частоту та покращує консистенцію випорожнень.
Одне з останніх клінічних досліджень B. clausii опубліковано Madempudi і співавт. цього року в серпні. Метою випробування було вивчити ефекти застосування штаму B. clausii UBBC‑07 у симптоматичному веденні ІВДШ у дітей. У подвійне сліпе рандомізоване плацебо-контрольоване дослідження включили 90 дітей віком від 4 до 7 років, яких розподілили на дві рівні групи – пробіотика та плацебо. Діти приймали суспензію спор B. clausii UBBC‑07 (2×109 у флаконі 5 мл) або плацебо 2 р/день протягом 3 міс. Загальна тривалість дослідження склала 6 міс – 3 міс лікування і 3 міс спостереження. Наприкінці лікування було відзначено значне зниження кількості, тривалості й тяжкості ІВДШ у групі B. clausii UBBC‑07 порівняно з вихідними показниками та групою плацебо. Крім того, в дітей групи пробіотика значно знизилися рівні IgA та IgE у слині, що свідчить про відновлення Th1/Th2 імунного гомеостазу.
Надмірне вживання енергетично щільних високооброблених харчових продуктів спричиняє дистрес кишкового мікробіому та підвищення проникності шлунково-кишкового тракту. Таке порушення, відоме як дієтична (метаболічна) ендотоксемія, призводить до транзиторного підвищення системного запалення, яке, своєю чергою, наражає людину на ризик розвитку метаболічних і кардіоваскулярних захворювань.
У дослідженні McFarlin і співавт. (2017) призначення суміші спороутворювальних пробіотичних штамів включно з B. clausii асоціювалося зі зниженням ендотоксемії на 42% через 5 год після вживання їжі; натомість вживання плацебо (рисового борошна) супроводжувалося підвищенням рівнів ендотоксинів у сироватці на 36%. Крім того, пробіотик забезпечував зменшення рівнів тригліцеридів сироватки через 3 год після вживання їжі на 24%, а також зниження прозапальних біомаркерів IL‑12p70, IL‑1β та греліну. Цікаво, що зіставний вплив на прозапальні маркери за допомогою заходів зі зниження маси тіла потребував учетверо більше часу (>12 тиж). Отже, використання пробіотика B. clausii є перспективною терапевтичною стратегією для зменшення системного запалення в пацієнтів із ризиком метаболічної ендотоксемії та пов’язаних кардіоваскулярних захворювань.
Одним із поширених захворювань слизової оболонки рота є рецидивуючий афтозний стоматит, який характеризується появою виразок, болем, порушенням жування та ковтання і може значно погіршувати якість життя пацієнтів. Порушення оральної мікробіоти, зумовлене застосуванням імуносупресивних препаратів або антибіотиків широкого спектра, може призводити до надмірного росту Candida albicans із розвитком орального кандидозу. Симптомами останнього є білі вогнища на слизовій оболонці, кровотеча, неприємний смак у роті, біль і відчуття печіння, що ускладнює вживання їжі. У пацієнтів із рецидивуючим афтозним стоматитом і кандидозом порожнини рота локальна аплікація B. clausii в комбінації з тріамцинолоном зменшувала еритему, біль і відчуття печіння порівняно з лікуванням лише тріамцинолоном. Терапевтичний ефект B. clausii, ймовірно, досягався завдяки формуванню в ротовій порожнині біоплівки, яка запобігала росту інших мікроорганізмів і захищала слизову оболонку. Нещодавні систематичні огляди і метааналізи підтвердили здатність пробіотиків зменшувати біль унаслідок афтозного стоматиту та знижувати кількість Candida spp. у ротовій порожнині.
Отже, пробіотики на основі B. clausii є перспективними в різних клінічних ситуаціях, окрім їхньої добре відомої ролі в підтриманні здоров’я кишечнику та відновленні дисбіотичної кишкової мікробіоти.
Резюмуючи, потрібно підкреслити, що активність багатьох представників роду B. clausii завжди яскраво виражена і проявляється щодо широкого спектра патогенних і умовно патогенних мікроорганізмів. Завдяки синтезу різноманітних ферментів та інших речовин вони регулюють і стимулюють травлення, надають протиалергенну та антитоксичну дію. Загалом B. clausii можна вважати одним із найперспективніших сучасних пробіотиків. Антимікробні й імуномодулюючі властивості штамів B. clausii підтримують їхнє використання для лікування та профілактики широкого спектра захворювань. Найбільша доказова база клінічної ефективності B. clausii отримана в пацієнтів із розладами кишкової мікрофлори, особливо за гострої діареї. Крім того, накопичено успішний досвід застосування B. clausii в профілактиці інфекцій у недоношених новонароджених, лікуванні алергічного риніту, ІВДШ, хронічної діареї, синдрому надмірного бактеріального росту, корекції побічних ефектів і підвищенні дієвості антихелікобактерної терапії.
Довідка «ЗУ»
На вітчизняному фармацевтичному ринку суспензія штаму B. clausii UBBC‑07 представлена дієтичними добавками Лактіалє® Жерміна та Лактіалє® Жерміна Форте (2×109 або 4×109 спор B. clausii UBBC‑07 в одному флаконі 5 мл відповідно).
Лактіалє® Жерміна / Жерміна Форте може бути рекомендована лікарем з метою:
- підтримання нормального балансу шлунково-кишкової мікрофлори при кишкових інфекціях, інтоксикаціях, порушенні травлення, незбалансованій дієті;
- попередження небажаних ефектів антибіотикотерапії;
- зменшення газоутворення та полегшення болю в животі;
- полегшення перебігу діареї;
- корекції дисвітамінозу, спричиненого застосуванням антибіотиків або хіміотерапевтичних препаратів;
- неспецифічного антитоксичного ефекту.
Лактіалє® Жерміна можна застосовувати дітям віком від 28 днів і дорослим, Лактіалє® Жерміна Форте – дітям віком від 4 років і дорослим. Лактіалє® Жерміна рекомендовано споживати натще, в разі призначення під час антибіотикотерапії – між прийомами антибіотика. Накопичена доказова база та успішний досвід застосування B. clausii створюють перспективні передумови застосування пробіотика Лактіалє® Жерміна в багатьох клінічних ситуаціях, пов’язаних із лікуванням шлунково-кишкових розладів, алергічного риніту та ІВДШ у педіатричній практиці.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 12 (529), 2022 р.