24 січня, 2023
Чинники, що впливають на дозування левотироксину в разі замісної гормональної терапії первинного гіпотиреозу в дорослих
Левотироксин (L-тироксин) вважають безпечним і ефективним препаратом для замісної гормональної терапії гіпотиреозу, спричиненого автоімунним тиреоїдитом, частковою або тотальною тиреоїдектомією, лікуванням радіоактивним йодом або побічними діями препаратів [1-5]. Хронічний характер і висока поширеність гіпотиреозу (~4% дорослих у країнах Заходу), на додачу до незміненої тривалості життя пацієнтів, що пройшли лікування, пояснює, чому L-тироксин є одним із найчастіше призначуваних препаратів [6-9].
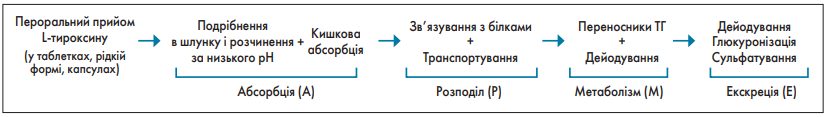
Клінічна ефективність будь-якого препарату залежить від фармацевтичних, патофізіологічних (внутрішніх) і поведінкових (зовнішніх) факторів. Більшість із цих факторів впливають на абсорбцію, розподіл, метаболізм та екскрецію (АРМЕ). Увесь цей процес наведено на рисунку 1.
Рис 1. Огляд процесів АРМЕ при пероральному прийомі L-тироксину пацієнтами з гіпотиреозом
Орально прийнятий L-тироксин (зазвичай у вигляді натрієвої солі) розчиняється в шлунку за низького pH, але абсорбується переважно в тонкому кишечнику (порожній, клубовій кишці) впродовж 3 год травлення [14-15]. Біодоступність прийнятого натще L-тироксину в осіб з еутиреозом і гіпотиреозом становить 65-80% [16, 17]. Після всмоктування епітелієм кишечнику і потрапляння в кровоносне русло препарат майже повністю (~99,9%) зв’язується з білками плазми крові (переважно з альбуміном, тироксин-зв’язувальним глобуліном (TЗГ), транстиретином, ЛПВЩ).
Середній об’єм розподілу L-тироксину в пацієнтів з еутиреозом становить 11-12 л, у пацієнтів із гіпотиреозом – до 15 л (через затримку рідини) [18, 19]. T4 метаболізується в деяких органах, залозах і ділянках мозку (переважно в печінці, а також у щитоподібній залозі (ЩЗ), передній частці гіпофіза і нирках) і в периферичних тканинах (наприклад, у м’язах) [20].
Приблизно 20% прийнятої дози L-тироксину виводиться з калом; сюди входять T4 і T3, що виділяються з жовчю після глюкуронізації або сульфатування в ході ентерогепатичного циклу [20]. Решта 80% виводиться із сечею [20]. Встановлено, що період напіврозпаду T4 становить 6-7 днів у пацієнтів з еутиреозом і 7-8 днів у пацієнтів із гіпотиреозом [22]. Однак зв’язок між рівнями ТТГ, вільного T4 і вільного T3 у пацієнтів, які отримували L-тироксин, не є таким самим, як у здорових осіб з еутиреозом, а розподіл, метаболізм і екскреція екзогенного L-тироксину відрізняються від таких ендогенного T4 [23].
Коли лікар стикається з проблемою недостатньої початкової ефективності L-тироксину або її втрати в раніше стабільних пацієнтів, він зазвичай розглядає можливість збільшення щоденної дози препарату. Однак у цій ситуації лікар має запитати себе, чи пов’язана недостатня ефективність L-тироксину з факторами, що впливають на АРМЕ препарату.
Проте потрібно завжди проводити диференційну діагностику між справжньою мальабсорбцією і псевдомальабсорбцією; остання зазвичай розвивається в результаті низького комплаєнсу (недотримання правил прийому L-тироксину). Тест на абсорбцію L-тироксину тривалістю 4-6 год (моніторинг рівнів T4 в крові після контрольованого введення дози L-тироксину, підібраної з урахуванням ваги) є головним для диференціації [24]. Тест на абсорбцію парацетамолу використовують як контроль; враховуючи те що парацетамол і L-тироксин мають різні фізико-хімічні властивості та механізми абсорбції, єдиною причиною мальабсорбції обох препаратів є тяжкі порушення з боку шлунково-кишкового тракту (ШКТ), а порушення абсорбції L-тироксину в разі нормальної абсорбції парацетамолу вказує на недотримання правил прийому L-тироксину під час лікувального процесу [25].
Отже, основною метою цього огляду було скласти повний перелік фармацевтичних, патофізіологічних (внутрішніх) і поведінкових (зовнішніх) факторів, які впливають на АРМЕ L-тироксину і, зрештою, можуть визначати ефективність, безпеку та необхідну дозу препарату. Інша ціль полягала в наданні практичної підтримки під час прийняття рішень лікарями, які ведуть пацієнтів із «резистентним до лікування» гіпотиреозом, з несподівано низькою ефективністю L-тироксину або з підозрою на його мальабсорбцію.
Методи
Літературний пошук та аналіз
Було здійснено пошук у базі даних PubMed із 1 січня 2000 р. по 30 квітня 2021 р., з використанням логічних комбінацій термінів (лише англійською мовою).
Тези були перевірені на відповідність. У разі визнання анотації актуальною повний її вміст корегувався та рецензувався. Звіти про випадки, огляди та редакторські статті були виключені. Ми довільно класифікували фактори, що впливають на зв’язок між призначеною пероральною дозою L-тироксину і клінічною ефективністю препарату, на три великі категорії: фармацевтичні (режим дозування, час прийому препарату, шлях введення, фармацевтична форма), патофізіологічні (етіологія, тип гіпотиреозу, статус захворювання, супутні хвороби або коморбідні стани, антропометричні дані, генетична складова тощо) і поведінкові (супутнє лікування лікарськими засобами, продукти харчування, дотримання режиму, досвід лікаря, який призначає препарат тощо) (табл. 1).
Фактори, що перешкоджають абсорбції L-тироксину
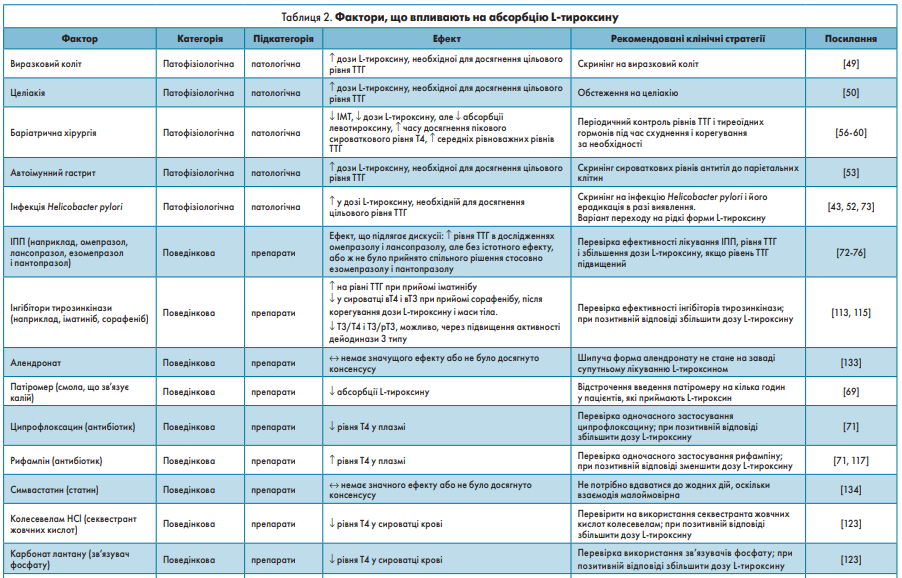
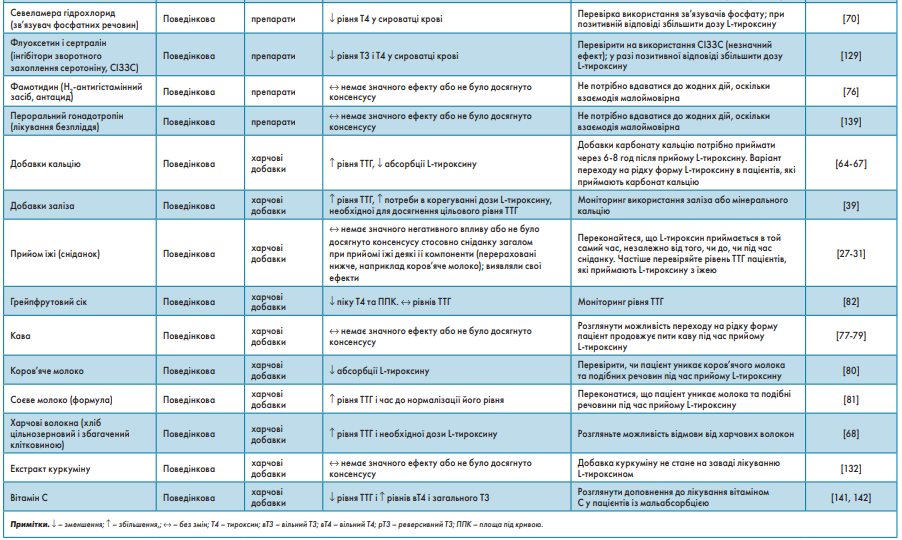
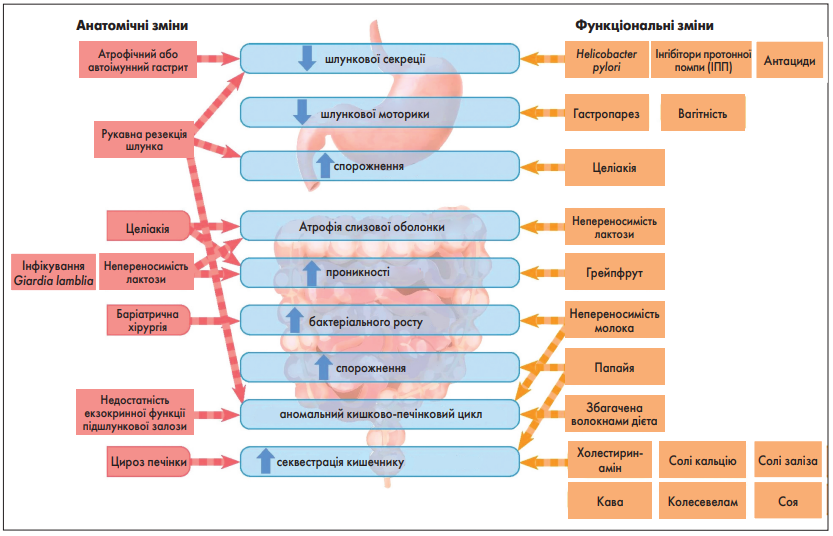
Фактори, що знижують або уповільнюють абсорбцію L-тироксину, наведені в таблиці 2 і узагальнені на рисунку 2.
Рис. 2. Анатомічні і функціональні зміни, які можуть зменшувати або сповільнювати всмоктування L-тироксину в ШКТ
Фактори, що впливають на розподіл, метаболізм і екскрецію L-тироксину
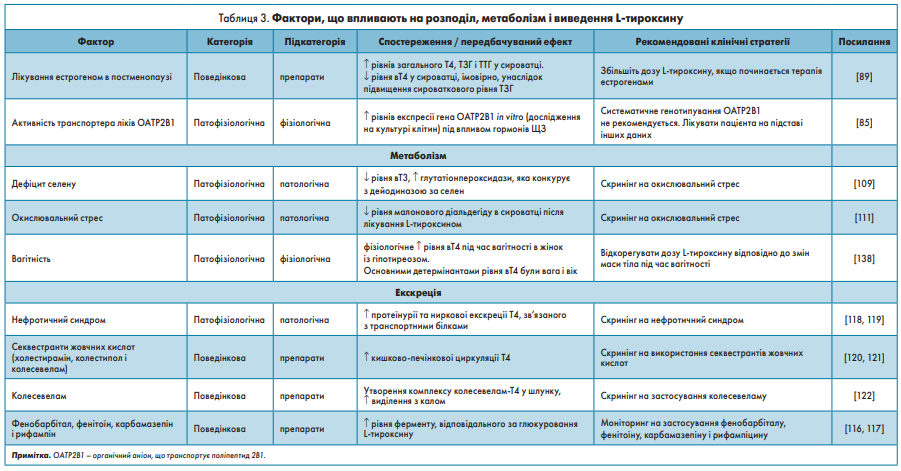
Фактори, що модулюють розподіл, метаболізм і виведення L-тироксину, наведені в таблиці 3.
Фактори, що модулюють ефективність L-тироксину, проте з невивченими механізмами, наведені в таблиці 4 [124].
Обговорення
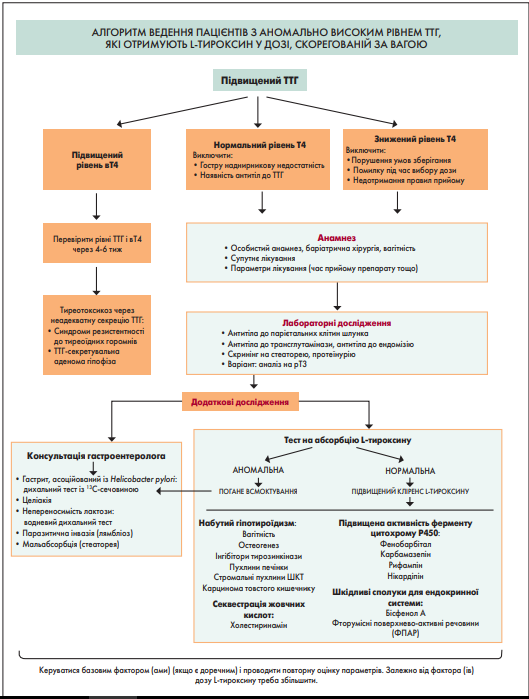
Проведений огляд літератури дав можливість скласти широкий перелік фармацевтичних, патофізіологічних і поведінкових факторів, які впливають на абсорбцію, розподіл, метаболізм і виведення L-тироксину. Переважна більшість цих факторів впливала на абсорбцію або (меншою мірою) на метаболізм (рис. 4). Якщо лікар стикається з аномально високим рівнем ТТГ у пацієнта, який приймає рекомендовану дозу L-тироксину з урахуванням ваги (>2 мкг/кг/добу або високі дози для досягнення та підтримання нормальної концентрації ТТГ), ми рекомендуємо розглянути аспекти, узагальнені на рисунку 4. Перш за все необхідно визначити рівень вТ4 у сироватці крові. Підвищений рівень вT4 у сироватці може свідчити про нещодавнє відновлення (на попередньому тижні) лікування L-тироксином, збільшення його дози або введення Т4 за 60-90 хв до забору крові. Зазвичай лікар знає про вищесказане і тому перевірить рівні ТТГ і вT4 пацієнта через 4-6 тижнів.
Рис. 4. Алгоритм ведення пацієнтів з аномально високим рівнем ТТГ, які отримують L-тироксин у дозі, скорегованій за вагою
Синдроми резистентності до гормонів ЩЗ спостерігають рідко, але їх наявність можна запідозрити після детально задокументованого ендокринного профілю пацієнта для отримання повнішої клінічної картини і виключення спадкових факторів. Можливо, варто визначити рівні ТТГ і вT4 у членів родини пацієнта [143].
Також не варто забувати про автономну секрецію ТТГ ТТГ-секретувальною аденомою гіпофіза [144]. Наостанок, у пацієнтів із вродженим гіпотиреозом (через мутації GLIS3, наприклад) може розвинутися резистентність до дії тиреоїдних гормонів [145]. Нормальний рівень вT4 у сироватці крові має навести лікаря на думку про необхідність перевірки на наявність гострої надниркової недостатності (особливо в пацієнтів, які лікуються від хронічного та первинного захворювання надниркових залоз) або гетерофільних антитіл до ТТГ.
Зрештою, низький рівень вT4 у сироватці крові може бути пов’язаний із помилкою у виборі дози, проблемою зберігання L-тироксину, мальабсорбцією L-тироксину або псевдомальабсорбцією (тобто недотримання правил прийому L-тироксину).
У пацієнтів із нормальним або низьким рівнем вT4 у сироватці крові та підвищеним рівнем ТТГ наступним кроком є детальний збір анамнезу, під час якого пацієнта опитують про його та сімейну історію хвороби (наприклад, будь-які попередні хірургічні операції, пов’язані з травним трактом), вагітність і прийом медикаментів. Зокрема, пацієнтів треба опитувати як саме і коли він/вона приймає L-тироксин (час прийому, до/під час/після їди, з напоями, окрім води тощо) та будь-які інші варіабельні чинники. Огляд медикаментів (тобто систематична оцінка всіх аспектів лікування пацієнта лікарськими засобами з метою оптимізації і досягнення кращих результатів) може бути корисним, особливо в людей похилого віку, які можуть не згадати повний список ліків під час збору анамнезу [146]. Варто також ураховувати можливе зниження функції залишкової частини ЩЗ (у пацієнтів з автоімунним тиреоїдитом).
Якщо під час опитування пацієнта не виявлено очевидного фактора нормальної або низької концентрації L-тироксину, можна призначити кілька лабораторних досліджень. Серед них скринінг на наявність антитіл проти компонентів шлунка (наприклад, циркулюючих IgG проти парієтальних клітин і кишкових антитіл проти ендомізіуму або тканинної трансглутамінази 2 як специфічного маркера целіакії) та на інфекцію Helicobacter pylori [54, 147]. Аномально високий рівень реверсивного T3 (reverse T3, rT3) свідчить про те, що перетворення T4 на rT3 за допомогою фермента дейодинази типу 3 є більш сприятливим у порівнянні з продукуванням T3 у контексті набутого гіпотиреозу [148]. Для перевірки наявності стеатореї як ознаки захворювання тонкої кишки і можливого порушення всмоктування використовують для дослідження калові маси (рідко в пацієнтів із гіпотиреозом). Смужки для аналізу сечі можна використовувати для скринінгу нефротичного синдрому з протеїнурією.
Якщо клінічна проблема не була виявлена під час опитування пацієнта і/або проведення лабораторних досліджень, наступним кроком є проведення фармакодинамічного тесту на абсорбцію L-тироксину (LAT). Хоч і було використано багато різних протоколів, LAT зазвичай передбачає пероральний прийом (під наглядом лікаря) L-тироксину з водою вранці через щонайменше 8 год після останнього прийому їжі. Зразки венозної крові беруть через 1; 2; 3; 4; 5 і 6 год після прийому L-тироксину і аналізують рівень T4. Проте відсутність стандартизації означає, що параметри LAT в різних центрах відрізняються: гостра пероральна доза L-тироксину (фіксована доза 1000 мкг проти звичайної добової дози пацієнта), визначення рівня загального T4 або вT4, рівнів, що використовують для розрахунку абсорбції, порогу нормального результату (зазвичай 60% або 65% введеної дози через 3 год) і перелік протипоказань (переважно ішемічна хвороба серця) [24, 149-152].
Позитивний результат тесту на абсорбцію L-тироксину (тобто нормальне поглинання) свідчить про вищезгадані проблеми: неправильний вибір дози, порушення зберігання і/або недотримання режиму прийому препарату. Однак є й інші можливі пояснення нормального результату тесту на абсорбцію L-тироксину:
- збільшення екскреції T4 ШКТ унаслідок стимуляції кишково-печінкового циклу (наприклад, холестираміном);
- підвищення активності дейодинази типу 3;
- вплив ліків (таких як фенітоїн, фенобарбітал, рифампін і нікардипін).
Можливі наслідки впливу на роботу ендокринної системи хімічних сполук (бісфенол А і пер/поліфторалкільні сполуки) [153]. До того ж хімічні сполуки, що негативно впливають на ендокринну систему, такі як бісфенол А та інші біосфеноли (наприклад, бісфенол В), схожі за структурою із Т4 і Т3 та призводять до серйозних наслідків у роботі ендокринної залози [154, 155]. На додачу до антагонізму ядерних рецепторів ЩЗ, а отже, і втручання в стимульовану гормонами транскрипційну активність, бісфеноли безпосередньо впливають на експресію генів у ЩЗ та гіпофізі [156].
Більше того, da Silva та співавт. з’ясували, що бісфенол А інгібує активність у лабораторних умовах дейодинази типу 1 і типу 2 і (призначався перорально дорослим щурам Wistar чоловічої статті) це пов’язано з вираженим зниженням активності печінкової дейодинази типу 1 (але не активності дейодинази типу 2 коричневої жирової тканини) [157]. Рівні Т4 в сироватці крові щурів, яким призначали бісфенол А, були аномально високими, тоді як рівні Т3 залишалися незмінними [157].
Хоча гідроксильовані і галогенізовані бісфеноли конкурентно зв’язуються з білками-переносниками ТГ, такими як ТЗГ і транстиретин, слабкі контакти (подібні до Т3 і Т4) і низькі концентрації бісфенолу в живому організмі не чинять значного впливу на транспорт у пацієнтів, що лікуються L-тироксином [158, 159].
Аномально повільне або недостатнє підвищення рівнів Т4 у тесті на абсорбцію є приводом для консультації в гастроентеролога, який у зазначених випадках зазвичай проводить скринінг на гастрит, спричинений H. pylori (за допомогою дихального тесту з 13С-сечовиною), автоімунний гастрит (тест на антитіла проти парієтальних клітин і гастроскопію для виявлення атрофії слизової оболонки шлунка), целіакію, непереносимість лактози (за допомогою водневого дихального тесту), паразитарні інфекції (лямбліоз) і стеаторею (підвищення виведення L-тироксину з калом).
Виключаючи справжню мальабсорбцію L-тироксину, лікар має припустити наявність псевдомальабсорбції. Її першопричиною вважають радше недотримання режиму прийому препарату або фізіологічні причини, аніж неналежне зберігання L-тироксину або неправильний вибір дозування.
Проте низький комплаєнс може не одразу визнаватися пацієнтом. Lips та співавт. запропонували чіткий і неконфронтаційний підхід до усунення такої проблеми, як псевдомальабсорбція [160]. Лікар має пояснити пацієнтові процес лікування гіпотиреозу, підкреслити переваги хорошого комплаєнсу і, навпаки, висвітлити несприятливі наслідки хронічного гіпотиреозу за низького комплаєнсу. Якщо такий підхід не вирішує проблему, варто вдатися до інших, зокрема до зміни лікарської форми для перорального прийому препарату, щотижневого прийому L-тироксину під наглядом медичного персоналу або, у виняткових випадках (бажано в спеціальному центрі), – до парентерального введення L-тироксину.
Літературний пошук не виявив публікацій щодо зв’язку між бактеріальними або вірусними інфекціями й ефективністю L-тироксину.
Початкові дані, зібрані впродовж пандемії коронавірусної хвороби 2019 року, свідчать, що вилікований гіпотиреоз не є чинником ризику розвитку чи тяжчого перебігу інфекції, спричиненої коронавірусом‑2 тяжкого гострого респіраторного синдрому (SARS-CoV‑2) [161].
Проте потрібно брати до уваги той факт, що тиреоїдний статус необхідно оцінювати повторно в першому триместрі вагітності у вагітних жінок з еутиреозом, інфікованих SARSCoV‑2, особливо якщо вони мають високий ризик розвитку дисфункції ЩЗ або автоімунні захворювання в анамнезі [162, 163].
Реферативний огляд статті Caron Ph. et al. Factors influencing the levothyroxine dose in the hormone replacement therapy of primary hypothyroidism in adults. Endocrine and Metabolic Disorders, 2022:23.
Підготувала Дарина Павленко
Повну версію дивіться: https://link.springer.com/article/10.1007/s11154-021-09691-9
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 4 (60) 2022 р.