5 лютого, 2023
Сучасні аспекти терапії генітоуринарного менопаузального синдрому
В останнє століття тривалість життя людей збільшилася майже вдвічі. З огляду на зниження народжуваності неминучим є процес старіння населення, що веде до збільшення кількості асоційованих із віком захворювань, одним із яких є генітоуринарний менопаузальний синдром, що розвивається у жінок на фоні естрогенного дефіциту у період згасання гормональної функції яєчників.
Ключові слова: генітоуринарний менопаузальний синдром, менопауза, гіпоестрогенія, вагінальна сухість, негормональні вагінальні зволожувачі, лубриканти, гіалуронова кислота, вагінальний гель.
Успіхи сучасної медицини призвели до того, що сьогодні одним із найскладніших викликів для системи охорони здоров’я є неухильне збільшення тривалості життя у всьому світі, що асоціюється зі зростанням кількості людей похилого та старечого віку. З огляду на зниження народжуваності неминучим є процес старіння населення. Згідно з даними за 2018 рік, вперше в історії людства кількість осіб старшої вікової групи (>65 років) перевищила кількість дітей віком <5 років у світовій популяції [1]. За прогнозами Всесвітньої організації охорони здоров’я, це співвідношення із часом буде лише збільшуватися: до 2025 року на планеті буде понад мільярд людей старше 60 років, а до 2050‑го – люди старшої вікової групи становитимуть 22% [2]. Разом зі старінням населення збільшується і кількість асоційованих із віком захворювань. Одним із них є генітоуринарний менопаузальний синдром (ГУМС) – комплекс вагінальних і сечових симптомів, пов’язаних із розвитком атрофічних і дистрофічних процесів у тканинах піхви та вульви, м’язах тазового дна, зв’язковому апараті матки, а також в уретрі та сечовому міхурі, які розвиваються на фоні естрогенного дефіциту у період згасання гормональної функції яєчників. Уперше термін «генітоуринарний менопаузальний синдром» був запропонований 2012 року консенсусом Міжнародного товариства з вивчення жіночого сексуального здоров’я (International Society for the Study of Women’s Sexual Health) та Північноамериканського товариства з питань менопаузи (North American Menopause Society – NAMS) і замінив застарілий термін «вульвовагінальна (урогенітальна) атрофія» [3].
Менопауза: від естрогенного дефіциту до ГУМС
Менопауза — один із фізіологічних етапів розвитку жіночого організму, який визначається як завершення менструального періоду внаслідок згасання функції яєчників і супроводжується припиненням репродуктивної функції та менструації [4]. Етапи репродуктивного старіння жінки є клініко-гормональною характеристикою, яка визначає етапи старіння репродуктивної системи. Вони включають пременопаузу, перименопаузу, менопаузу та постменопаузу. Період менопаузального переходу характеризується варіабельністю циклів із різними рівнями фолікулостимулюючого гормона, естрадіолу, симптомами естрогенного дефіциту, що починається у віці 40-45 років і завершується настанням менопаузи. Перименопауза включає період менопаузального переходу й +12 міс після останньої самостійної менструації. Менопауза (оцінюється ретроспективно через 12 міс) – остання самостійна менструація, зумовлена віковим зниженням і «вимиканням» гормональної та репродуктивної функцій, яку прийнято класифікувати залежно від віку настання на передчасну (<40 років), ранню (40-45 років), своєчасну (46-54 роки) і пізню (>55 років). Постменопауза є періодом після настання менопаузи [5].
Клінічно менопауза визначається як відсутність менструацій протягом 12 міс, що пов’язано з припиненням функції яєчників, супроводжуваним зниженням вмісту естрогенів та інших статевих гормонів. Перехід організму до стану менопаузи (стійкого припинення менструації) – складний процес, який інколи може тривати понад 10 років. Згідно зі статистикою, у європейських країнах середній вік настання менопаузи становить від 46 до 50 років. Враховуючи збільшення загальної тривалості життя населення, постменопаузальний період триває приблизно 40% життя жінки [6]. ГУМС та вазомоторні симптоми (припливи, нічна пітливість, відчуття серцебиття) є основними у цей період і спостерігаються у ≥80% жінок. Інші, менш поширені симптоми також включають: психопатологічні – емоційна лабільність, депресивні стани, тривога, дратівливість, порушення сну (майже у 40% жінок); загальнофізичні – астенізація, головний біль, біль у м’язах та суглобах, неприємні відчуття на шкірі; а також сексуальні – зниження лібідо (відмічають близько 10% жінок) [7]. Хоча не у всіх осіб з урогенітальними атрофічними змінами при обстеженні мають місце менопаузальні симптоми, за оцінками, у США більше половини жінок у постменопаузі відчувають симптоми, пов’язані з ГУМС [8]. Увесь цей симптомокомплекс спричиняє значний дискомфорт і, як наслідок, відчутне зниження якості життя жінки. На відміну від вазомоторних симптомів, пов’язаних із менопаузою (наприклад, припливи, нічна пітливість, відчуття серцебиття та зміни артеріального тиску), які мають тенденцію до зменшення із часом, прояви ГУМС не вщухають спонтанно, а погіршуються з віком [9, 10].
Важливо також зазначити, що ГУМС може виникати на будь-якому етапі життєвого циклу жінки, хоча частіше зустрічається саме у фазі постменопаузи, внаслідок гіпоестрогенії [11]. У випадках, коли причиною гіпоестрогенії є не менопауза (лактація, різні види лікування раку молочної залози, використання деяких лікарських засобів), клінічні симптоми ГУМС можуть зникати спонтанно, після відновлення нормального рівня естрогенів, натомість як зміни внаслідок менопаузи є необоротними.
Патофізіологія ГУМС
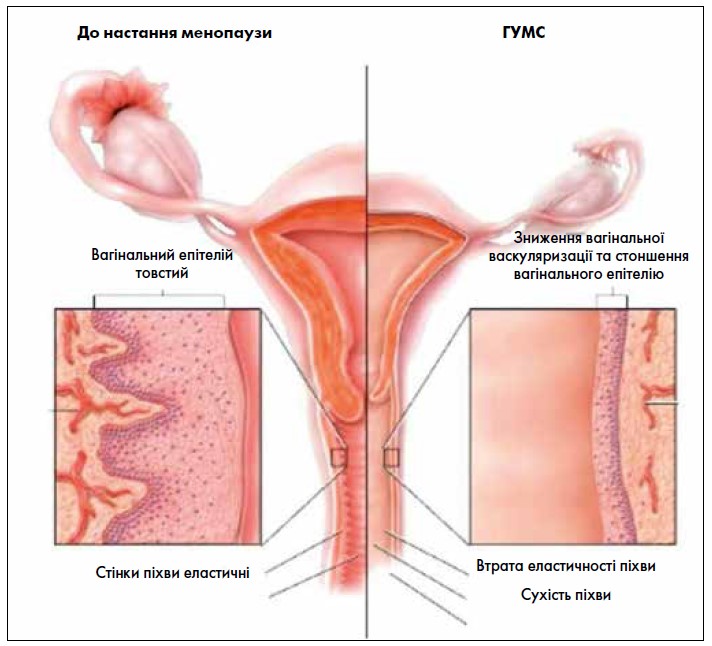
Патофізіологія впливу естрогенів та їх дефіциту на певні системи організму, такі як кісткова або серцево-судинна, добре задокументовано в медичній літературі. Однак даних, які б ілюстрували зв’язок між гіпоестрогенією та ураженням урогенітального тракту, на початку 2000‑х років було недостатньо [12]. Тому останні два десятиліття ознаменувалися проведенням численних досліджень у цій галузі, результати яких дозволили здійснити значний прорив у розумінні патофізіології впливу гіпоестрогенії на сечостатеву систему. Наразі відомо, що внаслідок дефіциту естрогенів спостерігаються анатомічні й фізіологічні зміни у сечостатевому тракті, які включають зниження вагінальної васкуляризації, зменшення вагінального змащування та стоншення вагінального епітелію разом із проліферацією сполучної тканини, фрагментацією еластину та гіалінізацією колагену (рисунок) [13, 14].
Рис. Вплив гіпоестрогенії на сечостатеву систему
Загальний патогенез розвитку атрофії у тканинах піхви й уретри жінок на фоні дефіциту естрогенів у перименопаузі пов’язаний із тим, що поступово припиняється мітотична активність клітин слизової не лише піхви, а й уретри. По мірі зростання прогресуючих атрофічних змін із боку піхви спостерігаються зниження об’ємного кровотоку і кровопостачання, фрагментація еластичних і гіаліноз колагенових волокон, зниження вмісту глікогену у клітинах епітелію піхви [15]. Останній фактор також зумовлений тим, що внаслідок зниження вмісту глікогену менша кількість останнього доступна для гідролізу до глюкози та подальшого перетворення на молочну кислоту лактобактеріями. Ці процеси призводять до підвищення рН піхви до 6,5-8,0. Залежно від ступеня естрогенного дефіциту й вікових метаболічних порушень елімінується основний компонент піхвового біотопу – лактобацили.
Клініко-морфологічна характеристика ГУМС
Стоншення вагінального епітелію, як наслідок гіпоестрогенії, збільшує сприйнятливість до травмування, що призводить до кровотечі, петехій і виразок при тиску будь-якого характеру, включаючи сексуальну активність чи простий гінекологічний огляд. Внаслідок патологічного процесу також оголюється підлягаюча сполучна тканина, яка є більш вразливою щодо розвитку запального процесу. Внаслідок зміни мікробіому піхви відбувається колонізація вагінального біотопу як екзогенними, так і ендогенними мікроорганізмами з подальшим ризиком розвитку висхідної інфекції, що, відповідно, асоціюється з ризиком вагінальних і сечових інфекцій, виразок або тріщин, частого й болісного сечовипускання, ургентних позивів до сечовипускання. За таких умов в організмі жінки простежуються зміни мікробіоценозу піхви й ослаблення механізмів локального захисту, що полегшує його інфікування [15].
Гіпоестрогенний стан включає зміни й у самому складі сполучної тканини зі зменшенням співвідношення колагену І/ІІІ типу, що призводить до зниження міцності тканини [3]. Внаслідок цих гістологічних змін клінічно на вагінальному рівні виникає низка симптомів: від сухості та недостатнього зволоження, почервоніння, втрати еластичності, петехій, виразок, запалення, атипових виділень до фіброзу й облітерації піхви. На рівні вульви ключовими клінічними ознаками гіпоестрогенії є зменшення підшкірно-жирової клітковини зовнішніх статевих органів, дистрофія статевих губ, випадіння волосся на лобку та ушкодження шкірного покриву через свербіж. Прояви ГУМС багатогранні: вони полягають у змінах не лише нижніх відділів статевої, а й сечової системи, що клінічно проявляється різними видами нетримання сечі й відчуттям дискомфорту при сечовипусканні.
З огляду на те що ГУМС є хронічним станом, він негативно впливає на якість життя жінки не лише із фізичної точки зору, а й із психологічної. ГУМС не загрожує летальним кінцем або серйозними порушеннями загального стану, проте призводить до соціальної ізольованості й суттєво знижує якість життя. Дійсно, ГУМС чинить значний негативний вплив на інтимне та сексуальне здоров’я жінок, а також на їхню самооцінку. Окрім того, цей стан також може позначатися на якості сну, темпераменті, працездатності, а також зменшувати жагу до життя.
Таким чином, зміни у сечостатевому тракті, пов’язані зі зниженням рівня естрогенів, які включають зменшення вагінальної васкуляризації й зволоження, а також стоншення вагінального епітелію, негативно впливають як на сексуальну функцію, так і на загальну якість життя. У середньому віці на симптоми, пов’язані із ГУМС, часто не зважають, приділяючи більше уваги довгостроковим наслідкам гормональних менопаузальних змін для кісткової тканини та серцево-судинної системи. Крім того, припливи та нічна пітливість вважаються типовими симптомами менопаузи, натомість як симптоми ГУМС часто пов’язують із самим старінням. Таким чином, ведення пацієнток менопаузального періоду є актуальною медичною та соціальною проблемою, яка потребує корекції не лише типових вазомоторних симптомів, а й симптомів ГУМС для забезпечення нормального життя жінки.
Сучасні аспекти терапії, націлені на полегшення симптомів ГУМС
Відповідно до заяви NAMS, основною метою лікування ГУМС є покращення або полегшення суб’єктивних симптомів захворювання [16]. Наразі у доробку клініцистів наявна значна кількість різноманітних методик лікування ГУМС, які спрямовані на купірування його клінічних проявів: від класичних заходів (застосування лубрикантів) до менопаузальної гормональної терапії (МГТ) [17]. При цьому терапевтичну стратегію необхідно обирати послідовно, враховуючи вік жінки, симптоми, загальний стан здоров’я, а також з урахуванням можливих переваг/ризиків [6]. Найбільш ефективними сучасними опціями є лубриканти, зволожувачі, вагінальні естрогени (естрадіол, естріол, проместрієн, кон’юговані естрогени), андрогени й застосування лазера.
Негормональні вагінальні зволожувачі й лубриканти рекомендовані як терапія першої лінії при симптомах ГУМС, пов’язаних з атрофією піхви [6, 18-20]. У рекомендаціях Американського товариства клінічної онкології (American Society of Clinical Oncology – ASCO)/Американського онкологічного товариства (American Cancer Society – ACS) та NAMS зазначено, що негормональні засоби, такі як індивідуальні зволожуючі та змащувальні речовини, є найкращим варіантом терапії першої лінії ГУМС [21-23].
Тяжкі ознаки ГУМС, резистентні до терапії негормональними засобами, потребують фармакологічного лікування із застосуванням МГТ. Дана рекомендація набирає сили протягом останніх 10 років, незважаючи на відсутність клінічних даних, які б порівнювали ефективність використання негормональних та гормональних вагінальних засобів. Також при призначенні МГТ слід враховувати протипоказання цього методу при естроген-чутливих пухлинах, печінковій недостатності та тромбоемболізації, пов’язаній з дією естрогенного компоненту. Так, відповідно до гайдлайну NAMS 2020 року та огляду експертів S.S. Faubion et al. (2018), пацієнткам із раком молочної залози або гормон-залежними пухлинами рекомендована саме негормональна терапія ГУМС [24-27]. Також важливо звернути увагу на побічні ефекти МГТ, які включають чутливість молочних залоз, нудоту і блювання, вагінальну кровотечу, ризик прогресування пухлин, залежних від естрогенів, і в меншій мірі – біль у промежині.
У 2022 році були оприлюднені результати проспективного відкритого багатоцентрового багатонаціонального рандомізованого дослідження S. Garcia de Arriba et al., у якому оцінювалась ефективність лікування вагінальним негормональним зволожуючим кремом порівняно з вагінальним кремом з естріолом (0,1%) у групі жінок у постменопаузі із симптомами ГУМС [28]. Результати дослідження надали клінічні докази того, що негормональний вагінальний зволожуючий крем не поступається за своєю ефективністю крему з 0,1% естріолу. Ефективність негормональних кремів також була продемонстрована в інших численних дослідження [29, 30].
Гіалуронова кислота: ефективний терапевтичний варіант раннього лікування ГУМС
Гіалуронова кислота (ГК) – важливий компонент сполучної, епітеліальної та нервової тканин [31]. За рахунок виражених гідродинамічних властивостей ГК забезпечує сильний зволожуючий ефект, що сприяє підтриманню належного рівня гідратації у сечостатевій системі [32]. ГК бере участь у кількох фізіологічних процесах, включаючи гомеостаз і регенерацію тканин, загоєння ран, запалення, міграцію та проліферацію клітин, а також ембріональний розвиток. ГК також відіграє важливу роль у роботі сечостатевої системи, оскільки за фізіологічних умов вона допомагає підтримувати водний баланс і цілісність тканин.
Як відомо, менопауза спричиняє ендокринні зміни у сечостатевій системі, зокрема призводить до зниження синтезу ГК і мукополісахаридів у позаклітинному матриксі. Результати сучасних досліджень свідчать, що реологічні та структурні властивості ГК залежать безпосередньо від її молекулярної маси. Так, молекули ГК із високою молекулярною масою (>500 кДa) забезпечують миттєве інтенсивне зволоження слизової оболонки та шкіри, створюючи на її поверхні захисну плівку [33]. Високий рівень в’язкості ГК сприяє накопиченню молекул води на поверхні слизової піхви й запобігає втраті ліпідів. Таким чином, високомолекулярна ГК за своїми хімічними й біологічними властивостями є більш ефективною при лікуванні синдрому вагінального дискомфорту, ніж низькомолекулярна ГК [6].
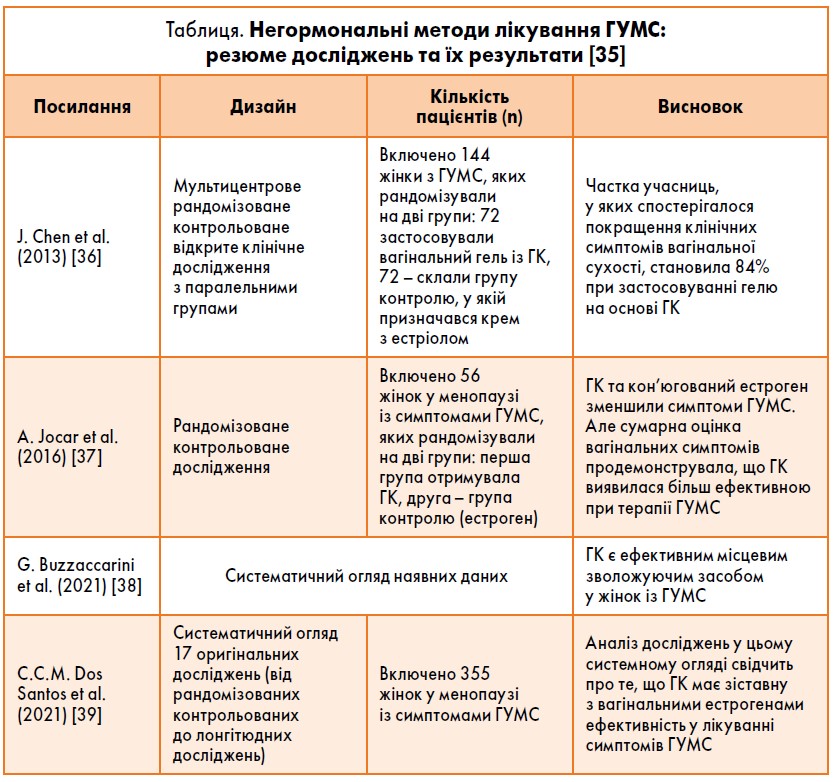
Враховуючи, що ГК у нормі задіяна у кількох фізіологічних процесах, які відбуваються, зокрема, і в органах сечостатевої системи (підтримання належного рівня гідратації для еластичності тканин і зменшення сухості піхви), її можна розглядати як перспективний зволожуючий засіб для лікування ГУМС. Наразі наявна значна кількість даних, які демонструють, що застосування негормональних вагінальних зволожувачів на основі ГК є ефективною стратегією боротьби із клінічними симптомами ГУМС. Такі зволожувачі та полімери, отримані із ГК, показали хороші клінічні результати в лікуванні симптомів, пов’язаних із ГУМС, – як із точки зору ефективності, так і безпечності/переносимості [34]. Препарати цієї групи мають високий профіль ефективності й безпеки, а їх використання не асоціюється з виникненням жодного відомого побічного ефекту, властивого МГТ (таблиця).
Отже, дані сучасних досліджень свідчать про те, що зволожуючі засоби на основі ГК є ефективними, безпечними та добре переносяться, а також можуть представляти ефективний варіант лікування ГУМС у пацієнток, які мають протипоказання або відмовляються від гормональної терапії. Враховуючи ефективність і безпечність застосування, стратегії впровадження засобів на основі ГК можуть бути інтегровані у терапію одразу після появи клінічних симптомів ГУМС.
Сьогодні на фармацевтичному ринку України наявний ефективний препарат ГК – Гідрофемін Плюс (виробництво фармацевтичної компанії «Егіс») у формі вагінального гелю, призначений для полегшення симптомів вагінальної сухості (подразнення, печіння, свербежу, ураження слизової оболонки, болю) та відновлення кислотного рівня рН піхви. Гідрофемін Плюс має добрий профіль безпеки й може бути рекомендований усім жінкам із симптомами ГУМС, у тому числі пацієнткам онкологічного профілю.
Список літератури знаходиться в редакції.
Підготувала Анна Хиць
Тематичний номер «Акушерство. Гінекологія. Репродуктологія» № 5 (51) 2022 р.