Ефективність препарату Азибіот® у лікуванні пацієнтів з негоспітальною пневмонією
Аналіз клінічних випадків
Відомо, що історія застосування макролідів у клінічній практиці розпочалася зі створення еритроміцину, який на той час відіграв значну роль у лікуванні пацієнтів з інфекціями верхніх та нижніх дихальних шляхів. Згодом період масових призначень лікарями еритроміцину змінився роками дискусій про зростання резистентності бактерій до його впливу, незручність використання препарату для пацієнтів, високий ризик його побічної дії.
На сьогодні макроліди залишаються одними з найбільш часто уживаних у клінічній практиці антибіотиків, оскільки при правильному застосуванні вони демонструють хорошу ефективність при достатньо високому рівні безпеки. Основою хімічної структури сучасних макролідів залишається макроциклічне лактонне кільце, зв’язане з одним або декількома вуглеводними залишками. Залежно від числа атомів вуглеводу в гетероциклічній структурі макроліди традиційно поділяють на 14-членні (природні – еритроміцин, олеандоміцин; напівсинтетичні – кларитроміцин, рокситроміцин та ін.), 15-членні (азаліди), представником яких є азитроміцин, і 16-членні (спіраміцин, джозаміцин). У світі нині існує близько 20 різних макролідних антибіотиків, але найчастіше використовуються азитроміцин і кларитроміцин. Для всіх представників класу характерний схожий механізм дії, який полягає в інгібуванні РНК-залежного синтезу білків у чутливих до них мікроорганізмів.
У клінічній практиці макроліди застосовують в основному при інфекціях дихальної системи. Дослідження останніх років демонструють, що найбільш частими збудниками гострих інфекцій верхніх дихальних шляхів залишаються Streptococcus pneumoniae (42%), Haemophilus influenzae (29-38%), Moraxella catarrhalis (17-20%), Streptococcus pyogenes (15-23%). Однак при рецидивуючих і хронічних інфекціях респіраторної системи зростає роль таких патогенів, як стафілококи, анаероби, внутрішньоклітинні збудники, зокрема Chlamydophila pneumoniae, Legionella, Mycoplasma pneumoniae. Крім того, нерідко в розвитку інфекцій верхніх дихальних шляхів беруть активну участь мікробні асоціації, до складу яких входять не тільки патогенні, а й умовно-патогенні мікроорганізми. При цьому відсутність у цілій низці випадків ефекту при використанні стандартної антибактеріальної терапії за наявності інфекцій дихальних шляхів все частіше змушує лікарів звертати увагу на можливу етіологічну роль внутрішньоклітинних мікроорганізмів. Так, за даними Всесвітньої організації охорони здоров’я, у світі спостерігається висока поширеність інфекцій, викликаних атиповими збудниками. Рівень інфікованості населення хламідіями і мікоплазмами становить близько 59%. Для хламідіозу властиве тривале персистування інфекції з подальшим розвитком хронічного носійства, при цьому хламідії здатні викликати патологію респіраторного тракту в асоціації з іншими мікроорганізмами; мікоплазми проникають всередину епітеліальних клітин респіраторного тракту, де вони, перебуваючи у відносній недосяжності від імунної системи, здатні розмножуватися і тривало персистувати в організмі. Слід підкреслити, що для хламідій і мікоплазм притаманна участь у мікробних асоціаціях, що спочатку створює клінічну видимість типової інфекції респіраторної системи і стає підставою для застосування стандартної антибіотикотерапії. При цьому призначення пацієнтам бета-лактамів пригнічує лише типову мікрофлору, а внутрішньоклітинні мікроорганізми продовжують персистувати на слизових оболонках, що супроводжується хронізацією інфекційного процесу.
Варто звернути увагу, що т. зв. атипова мікрофлора є частим збудником не тільки інфекцій верхніх дихальних шляхів: атипові патогени виявляються в 40-60% хворих з негоспітальною пневмонією (НП), а змішані інфекції спостерігаються в 48% пацієнтів. Частота виділення C. pneumoniae становить 17%, Legionella – 0,7-13%, M. pneumoniae – 13-37%. Крім того, C. pneumoniae відповідальна за 4-16% випадків загострень хронічного обструктивного захворювання легень, а серед курців і пацієнтів, що приймають системні глюкокортикоїди, ця цифра може досягати 34%. Також доведено, що інфікування C. pneumoniae асоціюється з виникненням бронхіальної астми в дорослих, а також з її загостреннями і рецидивуючими захворюваннями дихальних шляхів у дітей.
Діагноз НП – абсолютне показання до призначення антибіотиків, які є основою лікування таких хворих. Здебільшого пацієнтам з НП антибактеріальна терапія призначається емпірично, оскільки на сьогодні не існує достатньо ефективних методів її етіологічної експрес-діагностики. Вибір антибіотика для етіотропної терапії пацієнтів з НП здійснюється з урахуванням природної активності препаратів щодо основних патогенів. Однак у кожній конкретній ситуації слід обов’язково враховувати розповсюдженість і характер вторинної резистентності вірогідних збудників НП. Препаратами вибору для лікування хворих на пневмококову НП або НП, викликану гемофільною паличкою, є бета-лактами (частіше амоксицилін), у тому числі інгібіторзахищені (амоксицилін/клавуланат та ін.) і цефалоспорини ІІ-ІІІ покоління. Макроліди (переважно азитроміцин або кларитроміцин) є альтернативними препаратами при алергії до бета-лактамів, їх прийомі пацієнтами за останні 3 місяці або неефективності бета-лактамів протягом 48-72 годин лікування. Але якщо НП викликана M. pneumoniae, C. pneumoniae або Legionella spp., препаратами вибору є саме макроліди, рідше – доксициклін та респіраторні фторхінолони.
Останніми роками в пульмонології серед макролідів частіше використовується азитроміцин, що пов’язано з низкою його переваг:
- широкий спектр впливу, який охоплює типові і атипові респіраторні патогени;
- більш висока активність порівняно з іншими макролідами щодо H. influenzae;
- низька резистентність збудників до азитроміцину (у 10% штамів пневмококів в Україні у 2008-2009 рр.);
- створення високих концентрацій препарату в клітинах і тканинах;
- унікальний механізм доставки (фагоцити) антибіотика у вогнище запалення;
- зручний режим прийому (1 раз на добу);
- висока ефективність і безпечність;
- можливість терапії короткими (3-5 днів) курсами, що обумовлено його тривалим постантибіотичним (до 50 годин) ефектом;
- імуномодулюючі та протизапальні властивості.
Традиційно для проведення емпіричної антибактеріальної терапії слід використовувати антибіотики, що ефективні щодо основних імовірних збудників НП, мають оптимальний профіль безпеки (низьку частоту розвитку побічних ефектів), створюють високі концентрації в тканинах і біологічних рідинах органів дихання, характеризуються оптимальним співвідношенням вартість/ефективність, зручні в застосуванні. З метою дотримання хворим відповідного режиму лікування (комплаєнс), що значною мірою залежить від частоти прийому препарату протягом доби, а також від тривалості курсу лікування, перевагу надають лікарським засобам, які призначають 1 раз на добу та короткими курсами (3-5 днів). Усім зазначеним вимогам відповідає азитроміцин, представлений на фармацевтичному ринку України препаратом Азибіот® виробництва компанії КRКА (Словенія).
Азибіот® є представником групи азалідів, що мають широкий спектр антимікробної дії. Механізм дії азитроміцину полягає в інгібуванні синтезу бактеріями білків за рахунок зв’язування з 50S-субодиницею рибосом і пригнічення транслокації пептидів.
Спектр антимікробної дії азитроміцину включає:
- аеробні грампозитивні бактерії (метицилінчутливі штами Staphylococcus aureus, пеніцилінчутливі штами S. pneumoniae, S. pyogenes;
- аеробні грамнегативні бактерії (H. influenzae, Haemophilus parainfluenzae, Legionella pneumophila, M. catarrhalis, Pasteurella multocida);
- анаеробні бактерії (Clostridium perfringens, Fusobacterium spp., Prevotella spp., Porphyromonas spp.);
- інші мікроорганізми (C. trachomatis, C. pneumoniae, M. pneumoniae).
Біодоступність препарату після перорального застосування становить приблизно 37%. Максимальна концентрація в сироватці крові досягається через 2-3 години після його вживання. При пероральному прийомі азитроміцин розподіляється у всьому організмі. У фармакокінетичних дослідженнях було продемонстровано, що його концентрація в тканинах значно вища (у 50 разів), ніж у плазмі крові, а період напіввиведення з тканин триває 2-4 дні. Азитроміцин також має протизапальні, імуномодулюючі та мукорегулюючі властивості, які проявляються незалежно від його антибактеріальної активності. Профіль безпеки азитроміцину, у тому числі в педіатричній практиці, добре вивчений у численних клінічних дослідженнях.
Отже, на сьогодні азитроміцин є одним з антибіотиків, які найбільш часто призначаються лікарями загальної практики – сімейної медицини, пульмонологами, оториноларингологами, терапевтами, педіатрами. Нижченаведені клінічні випадки підтверджують високу ефективність та безпечність використання препарату Азибіот®.
Клінічний випадок 1
Пацієнт К., 1989 року народження, водій муніципального транспорту, захворів гостро 16.08.2017, коли після переохолодження відчув підвищення температури тіла до 37,7 °C, озноб, періодичний непродуктивний кашель. Лікувався самостійно симптоматичними препаратами (парацетамол, екстракт листя плюща). Протягом наступної доби симптоми захворювання наростали, температура тіла підвищилась до 38,5 °C, кашель набув надсадного характеру, з’явилися задишка при помірному фізичному навантаженні, пітливість, виражена загальна слабкість, відсутність апетиту. Із вказаними вище скаргами 18.08.2017 звернувся за медичною допомогою до пульмонолога.
Анамнез життя: наявність туберкульозу, вірусних гепатитів, цукрового діабету, виразкової хвороби шлунка і дванадцятипалої кишки, травм, оперативних втручань та шкідливих звичок заперечує. У пацієнта часто виникають захворювання верхніх дихальних шляхів. З приводу гострого бактеріального риносинуситу 2 місяці тому приймав амоксицилін.
Дані фізикального обстеження: загальний стан середнього ступеня тяжкості, свідомість ясна; шкірні покриви бліді, без висипань, видимі слизові оболонки рожевого кольору, чисті. При аускультації над правою легенею вислуховується везикулярне дихання, над нижніми відділами лівої легені – ослаблене дихання, вологі дрібнопухирчасті хрипи в невеликій кількості. Тони серця ритмічні, звучні, частота серцевих скорочень – 96 уд/хв, артеріальний тиск – 100/70 мм рт. ст., частота дихання – 24/хв. Живіт при пальпації м’який, безболісний, печінка не виступає з-під краю правої реберної дуги. Набряки відсутні. Фізіологічні випорожнення в межах норми.
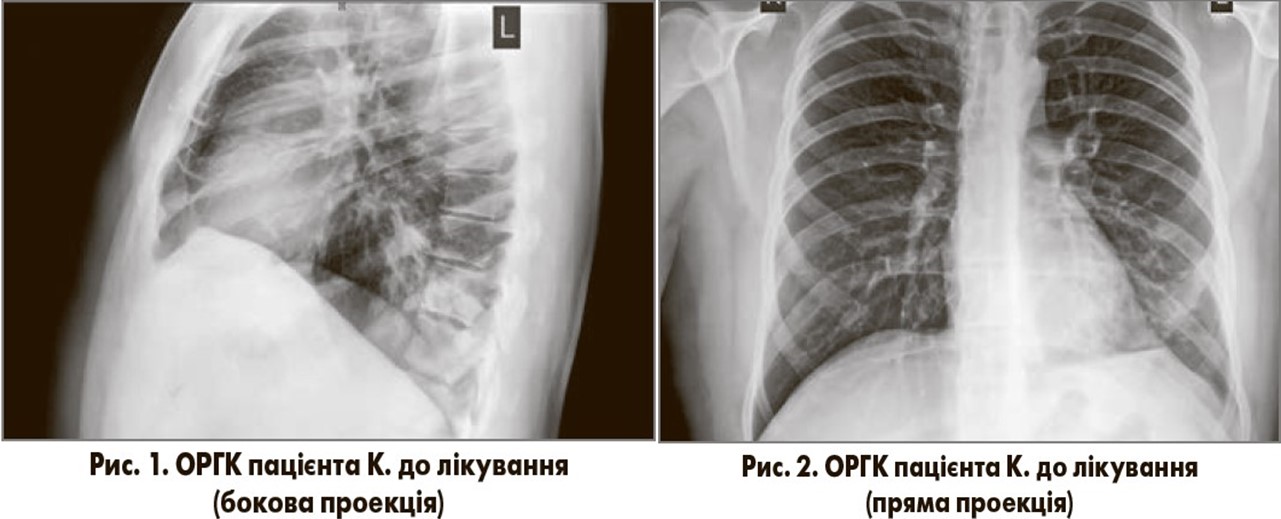
Дані лабораторних та інструментальних досліджень. Загальний аналіз крові (18.08.2017): рівень гемоглобіну – 126 г/л, еритроцитів – 4,1×1012/л; лейкоцитів – 10,6×109/л; лейкоцитарна формула: еозинофіли – 1%, паличкоядерні нейтрофіли – 8%, сегментоядерні нейтрофіли – 70%, моноцити – 3%; лімфоцити – 18%; швидкість осідання еритроцитів (ШОЕ) – 24 мм/год. На оглядовій рентгенограмі органів грудної клітки (ОРГК) у двох проекціях (18.08.2017; рис. 1, 2) спостерігаються вогнищево-інфільтративні зміни в нижній долі лівої легені, контури купола діафрагми чіткі, плевральні синуси вільні, тінь серця в межах норми.
На підставі скарг, анамнезу хвороби, фізикальних, лабораторних та рентгенологічних даних пацієнту було встановлено такий клінічний діагноз: негоспітальна лівобічна нижньодольова пневмонія, легкий перебіг, 1 клінічна група, легенева недостатність 0-І ст.
Лікування. Оскільки пацієнт 2 місяці тому приймав амоксицилін, йому був призначений азитроміцин (Азибіот®) 500 мг 1 раз на добу протягом 3 днів, амброксол 30 мг 3 рази на добу.
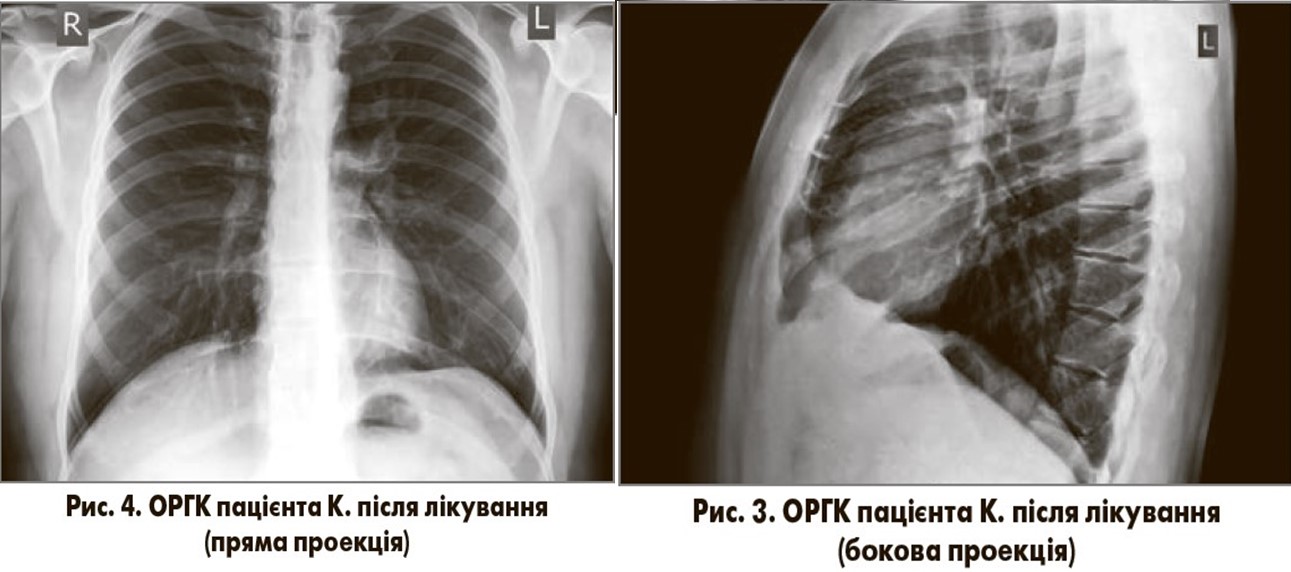
Динаміка. Температура тіла пацієнта нормалізувалась на 2-й день антибактеріальної терапії, зменшились ознаки інтоксикаційного синдрому, інтенсивність кашлю та задишки. На 5-й день лікування скарги у хворого були відсутні. Загальний аналіз крові (28.08.2017): рівень гемоглобіну – 128 г/л, еритроцитів – 4,2×1012/л, лейкоцитів – 6,8×109/л; лейкоцитарна формула: еозинофіли – 1%, паличкоядерні нейтрофіли – 3%, сегментоядерні нейтрофіли – 71%, моноцити – 4%; лімфоцити – 21%; ШОЕ – 10 мм/год. Контрольне рентгенологічне обстеження органів грудної клітки (28.08.2017; рис. 3, 4): легеневі поля прозорі, без вогнищевих та інфільтративних змін, синуси вільні, тінь серця в межах норми.
Отже, лікування пацієнта К. із застосуванням Азибіоту сприяло зникненню клінічних, лабораторних та рентгенологічних ознак НП. Препарати, які були використані під час лікування, не зумовили виникнення побічних ефектів. Цей клінічний випадок підтверджує високу ефективність та безпечність застосування Азибіоту в пацієнта з НП, яка, ймовірно, викликана типовим респіраторним патогеном.
Клінічний випадок 2
Пацієнтка В., 1995 року народження, студентка, мешкає в гуртожитку, скаржиться на поступову (протягом 2-3 тижнів) появу патологічних симптомів, таких як виражена слабкість, пітливість, осиплість голосу, біль у м’язах та суглобах, підвищення температури тіла до 37,3-37,5 °C, надсадний сухий кашель. Лікувалася самостійно симптоматичними засобами (парацетамол, льодяники для розсмоктування в порожнині рота, грудний збір, аскорбінова кислота). Упродовж останніх днів самопочуття погіршилось, оскільки зросла інтенсивність загальної слабкості, пітливості, осиплості голосу, болю в м’язах та суглобах, температура тіла підвищилася до 38,0 °C, кашель став продуктивним, з виділенням невеликої кількості мокроти жовтого кольору, з’явилася задишка при помірному фізичному навантаженні. 08.09.2017 звернулася за медичною допомогою до пульмонолога.
Анамнез життя: наявність туберкульозу, вірусних гепатитів, цукрового діабету, виразкової хвороби шлунка і дванадцятипалої кишки, травм, оперативних втручань та шкідливих звичок пацієнтка заперечує.
Дані фізикального обстеження: загальний стан середнього ступеня тяжкості, свідомість ясна; шкірні покриви бліді, без висипань, видимі слизові оболонки рожевого кольору, чисті. При аускультації над легенями вислуховувались жорстке дихання, поодинокі сухі хрипи, крепітація над верхніми відділами правої легені. Тони серця ритмічні, звучні, частота серцевих скорочень – 78 уд/хв, артеріальний тиск – 115/75 мм рт. ст., частота дихання – 25/хв. Живіт при пальпації м’який, безболісний, печінка не виступає з-під краю правої реберної дуги. Набряки відсутні. Фізіологічні випорожнення в межах норми.
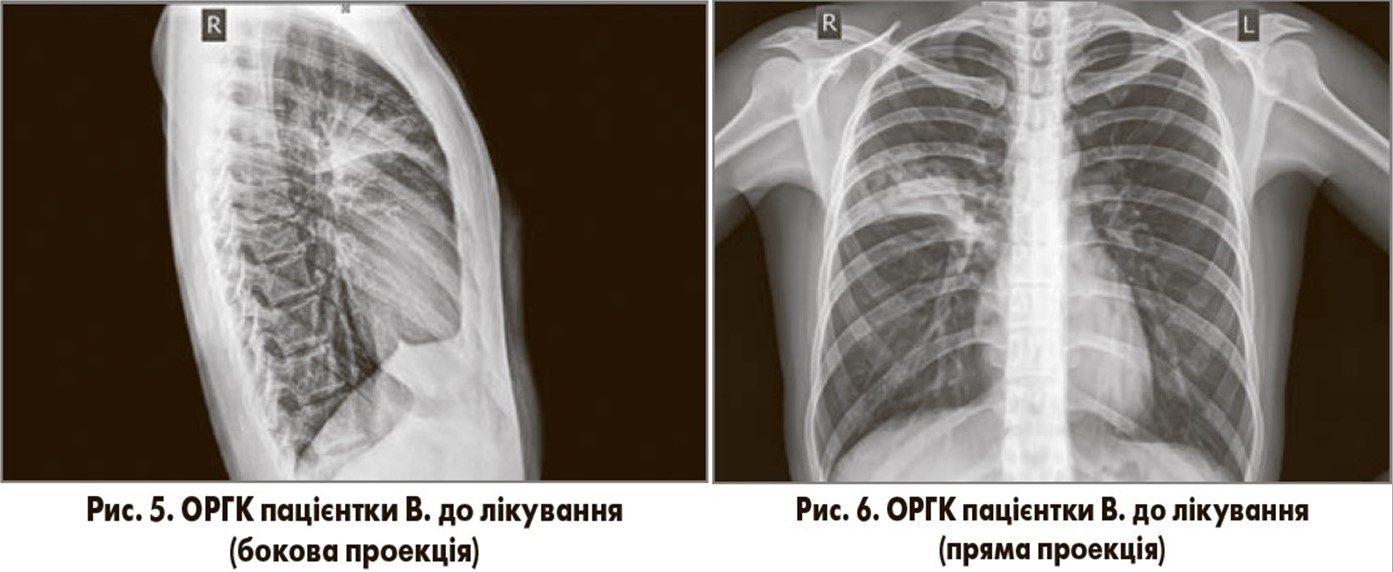
Дані лабораторних та інструментальних досліджень. Загальний аналіз крові (08.09.2017): рівень гемоглобіну – 116 г/л, еритроцитів – 3,6×1012/л, лейкоцитів – 9,1×109/л; лейкоцитарна формула: еозинофіли – 1%, паличкоядерні нейтрофіли – 7%, сегментоядерні нейтрофіли – 70%, моноцити – 5%; лімфоцити – 17%; ШОЕ – 28 мм/год. На ОРГК у двох проекціях (08.09.2017; рис. 5, 6) спостерігаються вогнищево-інфільтративні зміни у верхніх відділах правої легені, контури купола діафрагми чіткі, плевральні синуси вільні, тінь серця в межах норми.
На підставі скарг, анамнезу хвороби, фізикальних, лабораторних та рентгенологічних даних пацієнтці було встановлено такий клінічний діагноз: негоспітальна правобічна верхньодольова пневмонія, легкий перебіг, 1 клінічна група, легенева недостатність 0-І ст.
Лікування. Оскільки особливості скарг і анамнезу хворої дозволили припустити мікоплазменну етіологію НП, їй був призначений азитроміцин (Азибіот®) 500 мг 1 раз на добу протягом 3 днів, ацетилцистеїн 200 мг 3 рази на добу.
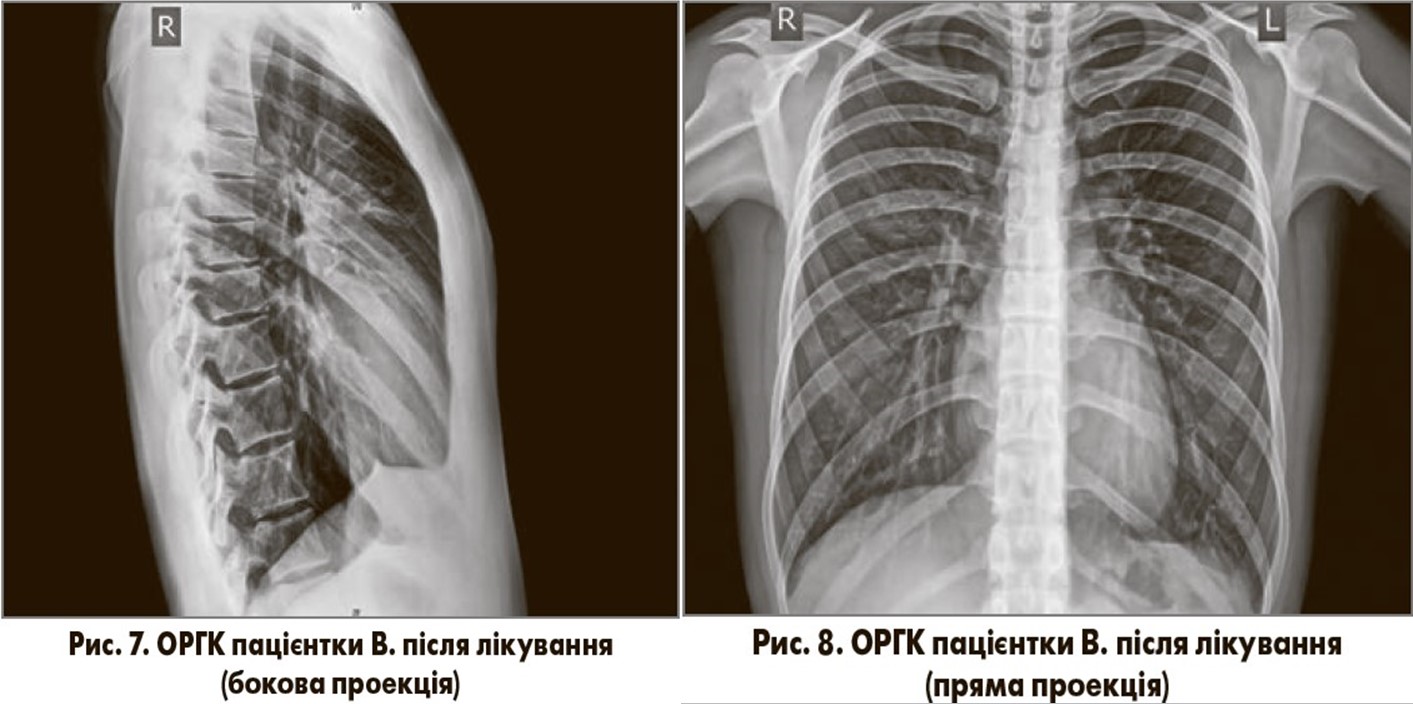
Динаміка. На фоні лікування в пацієнтки вже на 3-й день зменшилися вираженість загальної слабкості, пітливості, осиплості голосу, болю в м’язах та суглобах, кашлю та задишки. На 4-й день терапії нормалізувалася температура тіла, зникли вищенаведені скарги, спостерігався лише періодичний кашель без виділення мокроти. Загальний аналіз крові (22.09.2017): рівень гемоглобіну – 120 г/л, еритроцитів – 4,0×1012/л, лейкоцитів – 6,6×109/л; лейкоцитарна формула: еозинофіли – 0%, паличкоядерні нейтрофіли – 2%, сегментоядерні нейтрофіли – 71%, моноцити – 4%; лімфоцити – 23%; ШОЕ – 12 мм/год. Контрольне рентгенологічне обстеження органів грудної клітки (22.09.2017; рис. 7, 8): легеневі поля прозорі, без вогнищевих та інфільтративних змін, синуси вільні, тінь серця в межах норми.
Отже, антибактеріальна терапія пацієнтки В. із застосуванням Азибіоту сприяла зникненню клінічних, лабораторних та рентгенологічних ознак НП. Препарати, які були використані під час лікування, не зумовили виникнення побічних ефектів. Зазначений клінічний випадок демонструє високу ефективність та безпечність використання Азибіоту в пацієнтки з НП, що, ймовірно, була викликана атиповим респіраторним патогеном.
Азитроміцин (Азибіот®) поєднує повний спектр переваг сучасних макролідів, включаючи високу ефективність щодо інфекцій органів дихання, викликаних атиповою мікрофлорою. При цьому препарат зручний у використанні, має високий профіль безпеки і характеризується низькою частотою розвитку медикаментозної алергії та інших побічних ефектів.
Медична газета «Здоров’я України 21 сторіччя» № 23 (420), грудень 2017 р.
СТАТТІ ЗА ТЕМОЮ Пульмонологія та оториноларингологія
Риносинусит (РС) є одним із найчастіших захворювань у первинній медичній практиці. Трьома найбільш чутливими й специфічними симптомами гострого РС є виділення з носа, закладеність носа, лицевий і головний біль. Неконтрольований гострий біль значно погіршує якість життя пацієнтів із РС: спричиняє психоемоційні розлади, знижує працездатність і соціальну активність, сприяє хронізації больового синдрому і збільшує вартість лікування. Отже, полегшення болю при РС є найпершим завданням лікаря....
У всьому світі біль у горлі, зумовлений запальними захворюваннями горла (ЗЗГ), є найчастішою причиною звернень до лікарів загальної практики та оториноларингологів; із ним пов’язано ≈25% відвідувань лікаря. За даними Всесвітньої організації охорони здоров’я, >100 соматичних захворювань із провідним інфекційно-залежним і токсико-алергічним механізмом пов’язані саме із ЗЗГ. Здебільшого причина болю в горлі – гостре запалення інфекційного ґенезу: ГТ, ГФ і ГРВІ....
Антибіотикорезистентність (АБР) визнано загрозою для глобального здоров’я, яка щороку спричиняє мільйони смертей в усьому світі. Невідповідне та надмірне використання антибіотиків (АБ) зумовлює підвищення стійкості мікробних збудників і негативно впливає на ефективність цих дуже важливих лікарських засобів. Завдяки Глобальному плану дій щодо АБР Всесвітня організація охорони здоров’я (ВООЗ) працює над поліпшенням нагляду за резистентністю до протимікробних препаратів і скороченням нераціонального використання АБ. ...
Медичні інформаційні кампанії спрямовані на поширення важливих знань про охорону здоров’я серед населення. З урахуванням потреб і інтересів понад семи мільярдів людей у світі міжнародні організації шукають способи етичного обміну важливими відомостями, без упередженості та несправедливості. Обізнаність у сфері охорони здоров’я має вирішальне значення для кожного, оскільки хвороби та інфекції можуть вразити будь-кого в будь-який час. Таким чином, важливо поширювати відомості про охорону здоров’я за допомогою зрозумілих кожному усних, письмових і візуальних засобів. Ця інформація має сприяти соціальному здоров’ю і не містити дискримінаційного контенту. Заходи з підвищення обізнаності про здоров’я допомагають пацієнтам ліпше розуміти стан свого здоров’я, а також можливі варіанти та методи лікування. Кампанія з підвищення обізнаності відрізняється від маркетингу товарів для здоров’я, оскільки не спонукає купувати той чи інший продукт, а намагається сприяти свідомішому ставленню до свого здоров’я. Глобальні дні громадського здоров’я пропонують великі можливості для підвищення обізнаності та розуміння проблем здоров’я і мобілізації підтримки дій від місцевої громади до міжнародної спільноти. ...