Острый бронхит в пожилом возрасте: вопросы диагностики и лечения
Согласно статистическим данным, одной из самых распространенных причин обращения за амбулаторной медицинской помощью является остро возникший кашель. В подобных случаях наиболее часто диагностируется острый бронхит (ОБ).
ОБ – острое или подострое заболевание, основным клиническим признаком которого выступает продуктивный или непродуктивный кашель, продолжающийся не более 2-3 нед и сопровождающийся симптомами инфекции верхних дыхательных путей (ИВДП). Ежегодная заболеваемость ОБ составляет 20-40%. Статистика свидетельствует, что ОБ поражает около 5% взрослого населения ежегодно, причем 82% случаев фиксируется в осенне-зимний период [1]. В ходе многочисленных культуральных, серологических и молекулярно-генетических исследований было установлено, что основными возбудителями ОБ являются различные респираторные вирусы, а именно аденовирусы, коронавирусы, коксакивирусы, энтеровирусы, вирусы гриппа, парагриппа, респираторно-синцитиальный (РС)-вирус, риновирус. Доля специфических патогенов варьирует и зависит от многих факторов, в т. ч. от наличия эпидемии, времени года, уровня охвата населения соответствующей вакцинацией. Инфекции, вызванные парагриппом, энтеровирусом и риновирусом, наиболее часто развиваются осенью; грипп, РС-вирусная и коронавирусная инфекции – в зимний и весенний периоды. Чаще всего с ОБ ассоциируется вирус гриппа [4, 5].
Термин «острый бактериальный бронхит» в наше время считается некорректным, поскольку существовавшая долгое время гипотеза о том, что ОБ способны вызывать пневмококк, гемофильная палочка, золотистый стафилококк, моракселла и грамотрицательные бактерии, не нашла должного подтверждения. Исключение составляют больные, перенесшие хирургические манипуляции (трахеотомия) либо эндотрахеальную интубацию, во время которых возможна контаминация ВДП этими микроорганизмами [11].
Так называемого золотого стандарта диагностики инфекций нижних дыхательных путей (ИНДП), в т. ч. ОБ, на данный момент не существует. Согласно рекомендациям Американской коллегии специалистов по заболеваниям органов грудной клетки (American College of Chest Physicians, ACCP), диагноз ОБ устанавливается только при отсутствии клинических или рентгенологических признаков пневмонии, а также при исключении ИВДП (в англоязычной литературе common cold), бронхиальной астмы или обострений хронического бронхита как причины кашля [3].
Поскольку причиной ОБ в абсолютном большинстве случаев является вирусная инфекция, обычно требуется только симптоматическое лечение (противокашлевые или муколитические средства, бронходилататоры, противовоспалительная терапия). Однако при лечении ОБ очень часто назначаются и антибактериальные препараты (АП), а именно в 50-79% случаев [2]. Больше чем в половине случаев это антибиотики широкого спектра. Кокрановский обзор 14 рандомизированных контролируемых исследований (2004) с участием >1,5 тыс. больных выявил умеренный позитивный эффект антибиотикотерапии (АБТ) у пациентов с ОБ или острым продуктивным кашлем без других очевидных причин [7].
Следует отметить, что гнойная мокрота как единственный признак не является показанием к АБТ у ранее здоровых пациентов при отсутствии физикальных признаков пневмонии [6]. Однако Американское общество по инфекционным болезням рекомендует применение АП при тяжелом или длительном (>14 дней) течении ОБ, а также при обоснованной вероятности наличия коклюша [12]. В рекомендациях Национального института здоровья и качества медицины (NICE) Соединенного Королевства Великобритании и Северной Ирландии указывается, что ОБ не следует лечить АП, за исключением случаев высокого риска тяжелых осложнений вследствие коморбидных состояний. Прием АП рекомендован пациентам с острым кашлем в возрасте старше 65 лет с наличием ≥2 таких критериев: случаи госпитализации за последний год; сахарный диабет (СД); застойная хроническая сердечная недостаточность (ХСН); терапия глюкокортикоидами. Кроме того, АП рекомендованы всем пациентам в возрасте старше 80 лет с наличием ≥1 из вышеперечисленных признаков [9].
Критериями выбора АП являются его эффективность, безопасность, удобство применения и оптимальные фармакоэкономические параметры. При выборе АП для лечения ОБ в большинстве случаев основываются на статистических данных о наиболее частых возбудителях респираторных инфекций. Следует также учесть доказательную базу этих препаратов, т. е. подтвержденную в контролируемых клинических исследованиях эффективность при инфекциях известной этиологии. Не менее важным аспектом АБТ является ее безопасность. К наименее токсичным АП, в частности, относится азитромицин, эффективность которого при ИНДП изучалась в 29 крупных рандомизированных контролируемых исследованиях у 5901 больного, в т. ч. у 762 детей [8]. В сравнительных исследованиях макролидов была продемонстрирована сходная клиническая и бактериологическая эффективность азитромицина, кларитромицина, диритромицина, мидекамицина, мидекамицина ацетата, рокситромицина, джозамицина и эритромицина у взрослых и детей с ИНДП, в т. ч. ОБ, обострениями хронического бронхита, внебольничной пневмонией, включая микоплазменную. Отсутствие клинической эффективности азитромицина было обнаружено у 56 из 928 (6%) пациентов по сравнению с 72 из 746 (10%) больных, получавших АП сравнения.
Эффективность муколитических средств при ОБ продолжает активно изучаться многими исследователями, однако обоснованных рекомендаций по их использованию на данный момент не существует [13]. Именно это и явилось основанием для авторского исследования эффективности муколитика эрдостеина у больных с ОБ.
Эрдостеин представляет собой пролекарство, содержащее две блокированные тиоловые группы. Этот препарат начинает действовать после прохождения через печень, метаболизируясь до трех активных соединений. Свободная SH-группа в главном активном метаболите эрдостеина обусловливает многонаправленный механизм его действия: муколитический эффект (снижение вязкости мокроты, улучшение мукоцилиарного транспорта и клиренса); антибактериальное влияние (угнетение бактериальной адгезии к слизистой оболочке дыхательных путей, увеличение концентрации антибиотиков в мокроте); антиоксидантные и противовоспалительные свойства (увеличение содержания глутатиона в промывных водах бронхов, уменьшение продукции активных форм кислорода и перекисного окисления липидов, снижение уровня провоспалительных цитокинов в бронхиальном секрете) [10].
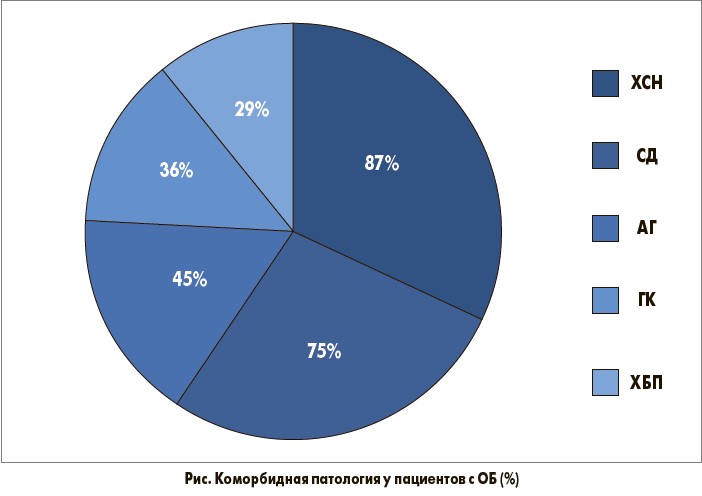 Целью авторского исследования стала оценка клинической эффективности и безопасности эрдостеина и азитромицина в комплексном лечении пожилых больных с ОБ и коморбидной патологией. В исследование было включено 36 пациентов в возрасте 65-75 лет (средний возраст – 69,4±1,5 года), у которых имелись признаки ОБ на фоне острых респираторных вирусных инфекций (ОРВИ). Больные были госпитализированы на 3-5-е сутки от начала ОРВИ в связи с ухудшением общего состояния и прогрессированием нарушений дыхания. Коморбидная патология у пациентов была представлена СД 2 типа (75%), ХСН III-IV функционального класса по NYHA (87%), артериальной гипертензией (АГ, 45%), хронической болезнью почек (ХБП, 29%). 36% участников исследования постоянно принимали глюкокортикоиды (ГК) для лечения сопутствующих заболеваний (бронхиальная астма, ревматоидный артрит и др.) (рис. 1). Стационарному лечению в течение последнего года подлежали 57% больных.
Целью авторского исследования стала оценка клинической эффективности и безопасности эрдостеина и азитромицина в комплексном лечении пожилых больных с ОБ и коморбидной патологией. В исследование было включено 36 пациентов в возрасте 65-75 лет (средний возраст – 69,4±1,5 года), у которых имелись признаки ОБ на фоне острых респираторных вирусных инфекций (ОРВИ). Больные были госпитализированы на 3-5-е сутки от начала ОРВИ в связи с ухудшением общего состояния и прогрессированием нарушений дыхания. Коморбидная патология у пациентов была представлена СД 2 типа (75%), ХСН III-IV функционального класса по NYHA (87%), артериальной гипертензией (АГ, 45%), хронической болезнью почек (ХБП, 29%). 36% участников исследования постоянно принимали глюкокортикоиды (ГК) для лечения сопутствующих заболеваний (бронхиальная астма, ревматоидный артрит и др.) (рис. 1). Стационарному лечению в течение последнего года подлежали 57% больных.
Для лечения ОБ пациентам назначался эрдостеин (Муцитус, Маклеодс Фармасьютикалс Лтд, Индия) в дозе 300 мг 2 р/сут и азитромицин (Зитрокс, Маклеодс Фармасьютикалс Лтд, Индия) по 500 мг в первый день, далее по 250 мг со 2-го по 5-й день. Клиническое наблюдение за динамикой состояния продолжалось в течение 2 нед.
Комплексное обследование участников исследования включало оценку клинических симптомов, цитологическое исследование выделяемой мокроты, компьютерную спирографию, рентгенологическое исследование органов грудной клетки, электрокардиографию (ЭКГ). Для оценки эффективности терапии использовалась индивидуальная карта больного, которая включала ежедневную оценку главных симптомов. Одышка оценивалась по шкале Modified Medical Research Council (MMRC) Dyspnea Scale. Для других симптомов были использованы 5-балльные шкалы: кашель (0 – отсутствует, 1 – редкий, 2 – умеренно выраженный, 3 – выраженный, 4 – сильный); характер и количество мокроты (0 – отсутствует, 1 – слизистая в небольшом количестве, 2 – слизистая в большом количестве, 3 – слизисто-гнойная, 4 – гнойная); консистенция мокроты (0 – отсутствует, 1 – легко откашливается, 2 – откашливается после незначительных усилий, 3 – вязкая, откашливается с трудом, 4 – вязкая, не откашливается); характер и количество хрипов (сухие хрипы: 0 – отсутствуют, 1 – единичные, 2 – умеренное количество, 3 – рассеянные). Для изучения влияния заболевания на повседневную активность и качество жизни больных использовали тест САТ (COPD Assessement Test). Эффективность терапии оценивалась через 14 дней лечащим врачом и пациентами также по 5-балльной шкале (0 – отсутствие эффекта, 1 – незначительный, 2 – удовлетворительный, 3 – хороший, 4 – отличный).
На момент госпитализации у всех пациентов наблюдалась экспираторная одышка при физической нагрузке или в покое, что соответствовало легочной недостаточности I (65,5%) или II (35,5%) степени. Умеренно выраженные явления интоксикации, присутствующие у 89% больных, постепенно исчезли к 3-му дню пребывания в стационаре. Хотя повышение температуры до субфебрильных показателей фиксировалось у всех пациентов, через 3 дня комплексного лечения у всех больных отмечалась нормализация температуры тела. Выделения из носа и гиперемия слизистой оболочки ротоглотки были ликвидированы у всех пациентов на 4-е сутки лечения.
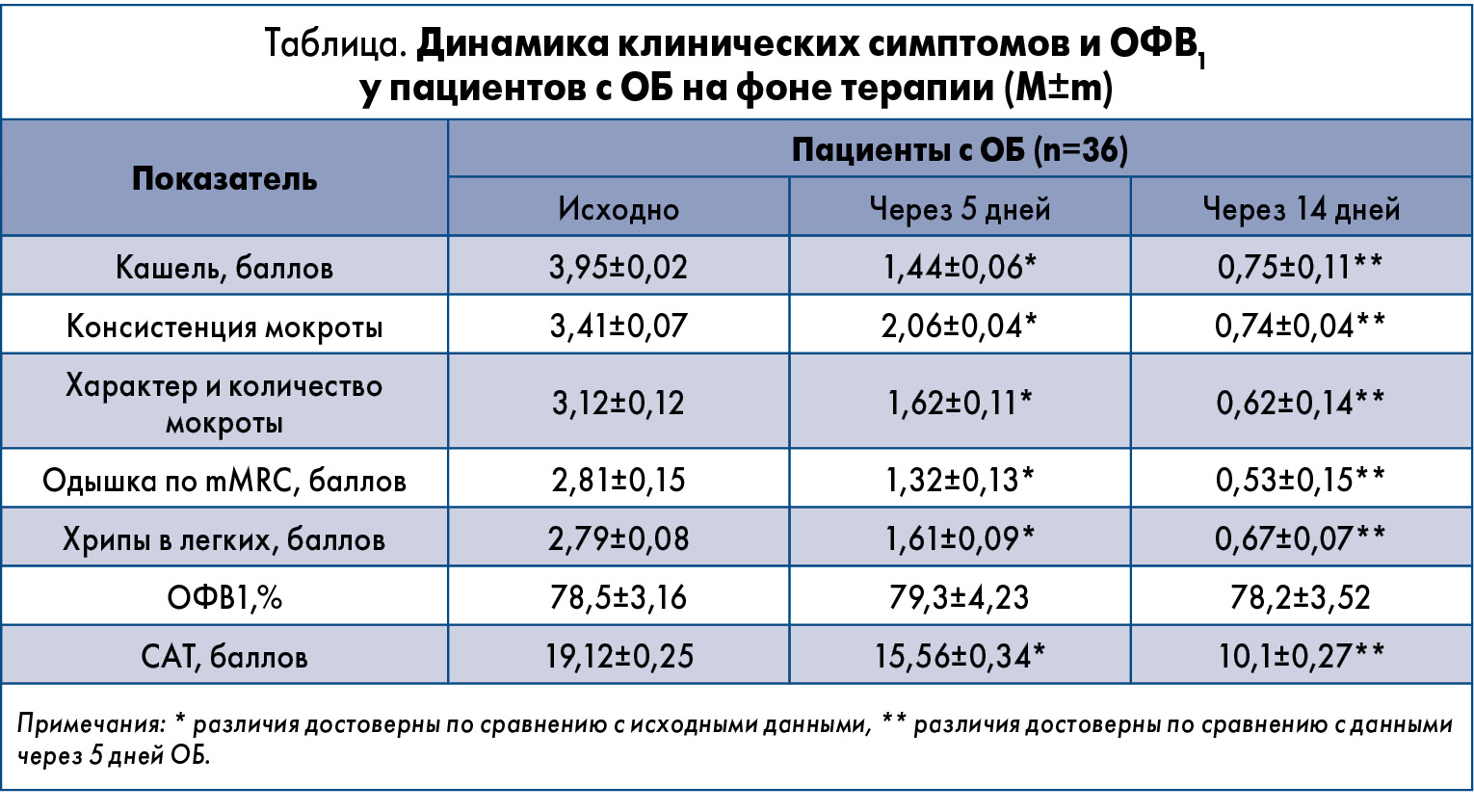 Результаты анализа динамики клинических симптомов и объема форсированного выдоха за 1-ю секунду (ОФВ1) у больных с ОБ на фоне лечения представлены в таблице.
Результаты анализа динамики клинических симптомов и объема форсированного выдоха за 1-ю секунду (ОФВ1) у больных с ОБ на фоне лечения представлены в таблице.
Согласно полученным результатам, у пациентов с ОБ на фоне терапии имела место достоверная регрессия характера кашля по сравнению с исходным состоянием. Согласно оценке по шкале mMRC, в процессе лечения одышка у больных с ОБ уменьшилась на 46,8%. Достоверно значимые различия этого клинического симптома на фоне терапии были зарегистрированы уже на 5-е сутки терапии. Также значительно улучшилась аускультативная картина – умеренное количество хрипов сохранялось у 12 (45%) пациентов.
На 14-й день лечения наблюдалось значимое улучшение консистенции мокроты (уменьшение вязкости, облегчение откашливания), снижение одышки. Единичные хрипы сохранились лишь у 6 пациентов (13%). При оценке влияния ОБ на повседневную активность и качество жизни пациентов по тесту САТ отмечена положительная динамика (снижение показателя на 54,7% от исходного).
По наблюдениям лечащего врача, у 29 из 36 пациентов (85%) фиксировалась положительная динамика клинического состояния. Согласно оценке терапии самими пациентами, большинство (95,4%) также отметили в своем состоянии значительное улучшение. Таким образом, положительное влияние двухнедельной комплексной терапии эрдостеином и азитромицином отмечалось как исследователями, так и участниками.
Авторы также провели оценку переносимости и влияния проводимой терапии ОБ на коморбидную патологию. Каких-либо значимых показаний к ограничению применения препаратов выявлено не было. Данный анализ позволяет сделать вывод о хорошем профиле безопасности эрдостеина и азитромицина при лечении пациентов пожилого возраста с коморбидной патологией.
Выводы исследования свидетельствуют, что:
- Включение эрдостеина и азитромицина в схему терапии пожилых больных с ОБ на фоне коморбидной патологии улучшает клиническую эффективность лечения, что проявляется в сокращении сроков редукции основных симптомов болезни (кашель, одышка), а также в значительном уменьшении их выраженности.
- На фоне терапии с использованием эрдостеина и азитромицина достоверно улучшалось самочувствие и качество жизни пациентов.
- Добавление эрдостеина и азитромицина к терапии ОБ у пожилых больных с коморбидной патологией не приводило к какому-либо увеличению частоты нежелательных явлений и ухудшений клинического состояния, связанных с сопутствующими заболеваниями.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 4 (425), лютий 2018 р.
СТАТТІ ЗА ТЕМОЮ
Основою лікування осіб з явним гіпотиреозом і деяких пацієнтів із субклінічним гіпотиреозом є довічна замісна гормональна терапія (ЗГТ) левотироксином (LT4) в адекватних дозах [1, 2]. Звичайна добова доза LT4 залежно від індивідуальних обставин варіює від 12,5 до 150 мг. Більшості пацієнтів літнього віку, із супутніми захворюваннями щитоподібної залози (ЩЗ) та інших органів і систем (особливо серцево-судинної), а також особам із низькою масою тіла необхідно стартувати з низьких доз LT4, наприклад 25-50 мг. В огляді проаналізовано практичні аспекти терапії LT4 залежно від рівня тиреотропного гормону (ТТГ) у пацієнтів із гіпотиреозом, особливо в разі необхідності застосування нижчих доз. Акцент зроблено на важливості точного і ретельного підбору початкової дози, подальшого титрування та врахування різних перешкод на шляху до побудови відповідної схеми лікування. ...
21-22 березня 2024 року на базі ДУ «Інституту проблем ендокринної патології ім. В.Я. Данилевського НАМН України» в режимі онлайн відбулася конференція «Досягнення та перспективи експериментальної і клінічної ендокринології» (ХХІІІ Данилевські читання). Слухачі мали можливість ознайомитися із сучасними досягненнями в ендокринології і новими тенденціями в лікуванні найпоширеніших ендокринних захворювань. Професор кафедри сімейної медицини з курсом дерматовенерології Сумського державного університету МОН України, кандидат медичних наук Оксана Костянтинівна Меліховець розповіла про нові можливості в стратегії зниження ризику прогресування атеросклерозу (АС) у хворих на цукровий діабет (ЦД). ...
Тиреоїдит Хашимото (ТХ), який ще називають хронічним аутоімунним, або лімфоцитарним, тиреоїдитом, є найчастішою причиною гіпотиреозу в регіонах із достатнім умістом йоду [1]. На цю патологію страждають приблизно 160 млн людей в усьому світі, причому жінки у 4-10 разів уразливіші за чоловіків [1, 2]. ТХ характеризується хронічним запаленням щитоподібної залози (ЩЗ), підвищенням рівнів антитіл до антигенів ЩЗ і типовою ультразвуковою картиною [1]. З моменту виникнення гіпотиреозу та пожиттєво пацієнтам рекомендована замісна терапія гормонами (ЗТГЩЗ) [3]. Метою цього дослідження було проведення оновленого систематичного огляду та метааналізу рандомізованих контрольованих досліджень ефективності добавок селену при ТХ, з акцентом на функції ЩЗ, рівнях антитіл проти ЩЗ, імунних маркерів та безпеці застосування. ...
Цукровий діабет (ЦД) – це група розладів метаболізму вуглеводів, коли глюкоза недостатньо використовується як джерело енергії та утворюється у надлишковому рівні через невідповідний глюконеогенез і глікогеноліз, що призводить до виникнення гіперглікемії [1]. Діагноз ЦД встановлюють у разі підвищення рівня глюкози в плазмі венозної крові або рівня глікованого гемоглобіну (HbA1c). Діабет умовно поділяють на декілька клінічних груп, наприклад ЦД 1 чи 2 типу, гестаційний ЦД (ГЦД) та інші специфічні типи, які виникають від інших причин (наприклад, при генетичних розладах, розладах екзокринної функції підшлункової залози чи внаслідок впливу медикаментів) [2]. ...





