Рекомбінантний штам Bacillus subtilis як засіб профілактики антибіотикасоційованої діареї у дітей
 Однією з найбільш глобальних проблем не лише педіатрії, а й усієї світової медицини є раціональне використання антибіотиків. Серед лікарських призначень близько 1/4 припадає на антибактеріальні засоби. За даними Всесвітньої організації охорони здоров’я, лише у 25-50% випадків проведення антибактеріальної терапії є обґрунтованим та раціональним. У решті клінічних ситуацій таке лікування пов’язане з багатьма негативними наслідками: ростом резистентності мікроорганізмів до наявних лікарських засобів, побічними ефектами з боку шлунково-кишкового тракту, імунної системи та мікробіому кишечнику. Одним із таких ускладнень є антибіотикасоційована діарея (ААД), яка потребує негайного проведення медикаментозної корекції.
Однією з найбільш глобальних проблем не лише педіатрії, а й усієї світової медицини є раціональне використання антибіотиків. Серед лікарських призначень близько 1/4 припадає на антибактеріальні засоби. За даними Всесвітньої організації охорони здоров’я, лише у 25-50% випадків проведення антибактеріальної терапії є обґрунтованим та раціональним. У решті клінічних ситуацій таке лікування пов’язане з багатьма негативними наслідками: ростом резистентності мікроорганізмів до наявних лікарських засобів, побічними ефектами з боку шлунково-кишкового тракту, імунної системи та мікробіому кишечнику. Одним із таких ускладнень є антибіотикасоційована діарея (ААД), яка потребує негайного проведення медикаментозної корекції.
Співіснування організму людини з мікробіомом є унікальною формою життя, що стала об’єктом багатьох наукових досліджень. Саме тому вчення про людський мікробіом, зокрема його значення у підтриманні здоров’я людини, визнано науковим проривом ХХІ століття. Так, у 2007 р. стартував масштабний проект Human Microbiome Project. Він продемонстрував, що людський макроорганізм та мікроби співіснують у межах єдиної унікальної, стабільної та водночас динамічної системи. Тому підтримання оптимальних кількісних і якісних показників мікробіому є стратегічним напрямом збереження здоров’я усього організму.
Неконтрольоване застосування антибіотиків є найчастішою причиною розвитку ятрогенної діареї. Згідно з офіційними висновками Управління з контролю якості харчових продуктів і лікарських препаратiв США (FDA), усі антибіотики широкого спектра дії певною мірою пригнічують нормальну мікрофлору кишечнику та можуть спровокувати надмірний ріст Clostridium difficile. Із цією бактерією пов’язане виникнення тяжкої діареї, яка становить реальну загрозу для життя пацієнта.
Відповідно до дефініції Всесвітньої організації охорони здоров’я, під ААД слід вважати наявність ≥3 епізодів виділення неоформленого калу протягом 2 діб, які виникли на тлі антибіотикотерапії. За різними даними, ААД реєструють у 5-35% хворих, які приймають антибіотики. В Україні при пероральному застосуванні антибіотиків широкого спектра дії ААД розвивається у 5-15,5% дітей. Деякі клініки повідомляють про збільшення цього показника до 62% у разі носійства токсигенних штамів Clostridium difficile (Л.В. Закордонец и соавт., 2013).
ААД може виникнути на тлі використання будь-якого антибіотика широкого спектра дії, незалежно від способу введення лікарського засобу. Найчастіше ААД розвивається при застосуванні кліндаміцину і лінкоміцину (20-30%), амоксициліну/клавуланату (10-25%), цефіксиму (10-20%), рідше – інших цефалоспоринів (2-5%), амоксициліну (5‑10%), макролідів (2-5%) і фторхінолонів (2-5%; Л.В. Закордонец и соавт., 2013).
За етіопатогенезом виділяють два види ААД: інфекційну (20-25%) та неінфекційну (75-80%). Інфекційна ААД виникає внаслідок протимікробної дії антибіотика та проявляється пригніченням цільової патогенної флори та кишкового мікробіому. У ролі етіологічних факторів інфекційної ААД виступають Clostridium difficile, Staphylococcus aureus, Salmonella spp., Clostridium perfringens, Klebsiella oxytoca, гриби роду Candida. Неінфекційна ААД є наслідком побічної дії антибіотиків на шлунково-кишковий тракт. Наприклад, амоксицилін/клавуланат активізує перистальтику тонкої кишки, макроліди чинять мотиліноподібний ефект внаслідок впливу на рецептори на рецептори товстої кишки, тому прийом цих препаратів може супроводжуватися виникненням діареї гіпермоторного характеру. Осмотичний тип діареї як прояв порушення всмоктування у кишечнику може виникати на тлі застосування цефалоспоринів. Найбільш схильними до розвитку ААД є новонароджені та діти до 5 років, у яких кишковий мікробіом ще не повністю сформований (В.В. Черников, А.Н. Сурков, 2012).
Між часом появи симптомів і механізмом розвитку ААД існує певна залежність. Розвиток діареї безпосередньо на тлі прийому антибіотиків зазвичай є наслідком побічної дії засобу (гіпермоторна чи осмотична діарея). Імовірність впливу інфекційного чинника на виникнення ААД зростає, якщо симптоми з’явилися уже після антибіотикотерапії.
Звичайно, повністю утриматися від застосування антибактеріальних засобів у педіатричній практиці неможливо, адже існує велика кількість захворювань, які є показанням до негайного призначення антибіотикотерапії. Оскільки негативна дія антибактеріальних препаратів на кишковий мікробіом є прогнозованою, педіатри мають інструмент, який може захистити кишкову мікрофлору, а саме пробіотики.
Під терміном «пробітики» слід розуміти живі мікроорганізми, які приносять користь організму людини за умови їх застосування в адекватній кількості. Сьогодні як пробіотики використовують різні види молочнокислих бактерій (Lactobacillus), біфідобактерій (Bifidobacterium), сахароміцетів (Saccharomyces cerevisiae), кишкової палички (Escherichia coli), а також деякі види бацил (Bacillus subtilis, Bacillus clausi, Bacillus cereus). Оптимальний пробіотик повинен задовольняти такі критерії: основним компонентом засобу має бути непатогенний мікроорганізм, який наявний у складі нормальної мікрофлори та стійкий до шкідливого впливу антибіотиків, шлункового соку; інгібуюча активність відносно патогенних бактерій, а також імуномоделювальна та метаболічна дія.
Основною метою призначення пробіотичного засобу є нормалізація кількісного та якісного складу мікробіому кишечнику.
Bacillus subtilis синтезують літичні ферменти, ензими, еластазу (проявляють протимікробну активність щодо грампозитивних і грамнегативних бактерій), а також амілазу, пектинолітичні, літолітичні, целюлозолітичні, протеолітичні ферменти (стимулюють репарацію, покращують процеси травлення). Крім того, Bacillus subtilis продукують незамінні амінокислоти, вітаміни групи В і К. Доведено, що застосування пробіотика сприяє підвищенню імунітету, зокрема за рахунок зростання активності секреторних IgA, індукції синтезу ендогенного інтерферону.
У разі призначення дитині пробіотичного штаму на тлі застосування антибіотикотерапії необхідно звернути увагу на таку характеристику засобу, як безпечність. У цьому аспекті штам B. subtilis має низку переваг:
- за рахунок того, що бактерія не утворює біоплівок у кишечнику, виключається можливість її тривалої та безконтрольної персистенції в організмі;
- FDA присвоїло B. subtilis статус GRAS (generally recognized as safe), що є найвищим показником безпечності штаму.
Bacillus subtilis виділяють також дипіколінову кислоту. Ця речовина є додатковим фактором ерадикації патогенних та умовно-патогенних мікроорганізмів і водночас сприяє росту представників нормальної мікрофлори кишечнику (И.Б. Псахис, Т.Е. Маковская, 2014).
Пропонуємо звернути увагу на сучасний засіб Субалін®, до складу якого входить пробіотичний рекомбінантний штам Bacillus subtilis 2335/105 – спороутворююча аеробна бактерія з унікальними властивостями.
 Мінімізація негативної дії антибіотика за допомогою пробіотика Субалін® продемонстрована результатами клінічного дослідження за участю 60 дітей, яким з певних причин було призначено курс антибіотика із групи цефалоспоринів тривалістю 7-10 днів. Пацієнти були розділені на дві групи. Терапія для пацієнтів 2-ї (основної) групи (n=30) була доповнена пробіотиком Субалін®, пацієнти 1-ї (контрольної) групи (n=30) не отримували пробіотик. У 3 дітей із контрольної групи на 3‑6‑й день антибіотикотерапії виникла діарея, у той час як у пацієнтів 2-ї групи на тлі використання пробіотика жодних ознак діареї не виявлено. За результатами бактеріологічного дослідження випорожнень дисбіотичні зміни кишечнику (зменшення загальної кількості кишкової палички та лактобактерій, збільшення E. coli з гемолітичними властивостями) були встановлені ще до початку антибактеріальної терапії, яка згодом спричиняла їх прогресування. Проте застосування пробіотика Субалін® зменшувало негативний вплив антибіотика на стан кишкового мікробіому (С.О. Крамарьов, Л.В. Закордонець, 2016).
Мінімізація негативної дії антибіотика за допомогою пробіотика Субалін® продемонстрована результатами клінічного дослідження за участю 60 дітей, яким з певних причин було призначено курс антибіотика із групи цефалоспоринів тривалістю 7-10 днів. Пацієнти були розділені на дві групи. Терапія для пацієнтів 2-ї (основної) групи (n=30) була доповнена пробіотиком Субалін®, пацієнти 1-ї (контрольної) групи (n=30) не отримували пробіотик. У 3 дітей із контрольної групи на 3‑6‑й день антибіотикотерапії виникла діарея, у той час як у пацієнтів 2-ї групи на тлі використання пробіотика жодних ознак діареї не виявлено. За результатами бактеріологічного дослідження випорожнень дисбіотичні зміни кишечнику (зменшення загальної кількості кишкової палички та лактобактерій, збільшення E. coli з гемолітичними властивостями) були встановлені ще до початку антибактеріальної терапії, яка згодом спричиняла їх прогресування. Проте застосування пробіотика Субалін® зменшувало негативний вплив антибіотика на стан кишкового мікробіому (С.О. Крамарьов, Л.В. Закордонець, 2016).
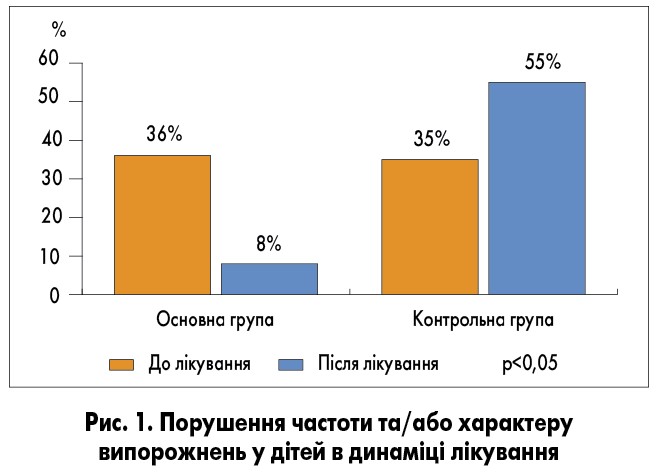
Висока ефективність Bacillus subtilis як засобу профілактики ААД у дітей раннього віку була продемонстрована ще в одному клінічному дослідженні за участю 45 дітей віком від 1 міс до 3 років, яким проводили антибактеріальну терапію. Дітей розділили на дві групи: 1-ша – основна (антибіотик + пробіотик Субалін®), 2-га – контрольна (лише антибіотик). Після лікування лише у 8% пацієнтів 1-ї групи зафіксовано порушення частоти та/або характеру випорожнень, тоді як ці симптоми виникли у 55% дітей 2-ї групи (рис. 1).
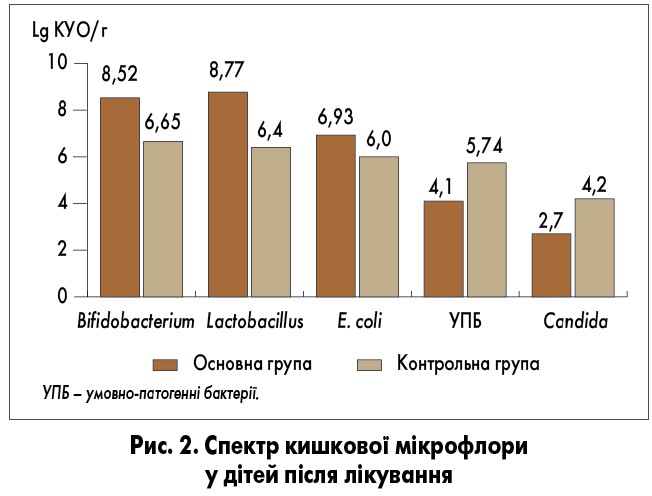 Варто зазначити, що перед стартом антибіотикотерапії за результатами бактеріологічного дослідження випорожнень у 28,9% дітей було виявлено дисбіоз кишечнику різного ступеня (в основному за рахунок зменшення загальної кількості кишкової палички, лактобактерій та збільшення кількості представників умовно-патогенної флори, зокрема стафілококів, протея, клебсієл, ентеробактерій, грибів роду Candida), що також обґрунтовувало потребу призначення пробіотика. За допомогою бактеріологічного дослідження випорожнень у динаміці на тлі застосування пробіотика Субалін® виявлено достовірне збільшення кількості основних представників індигенної мікрофлори порівняно з такою у контрольній групі, де спостерігався негативний вплив антибіотика у вигляді дисбіозу кишечнику (рис. 2; О.Г. Шадрін та співавт., 2018).
Варто зазначити, що перед стартом антибіотикотерапії за результатами бактеріологічного дослідження випорожнень у 28,9% дітей було виявлено дисбіоз кишечнику різного ступеня (в основному за рахунок зменшення загальної кількості кишкової палички, лактобактерій та збільшення кількості представників умовно-патогенної флори, зокрема стафілококів, протея, клебсієл, ентеробактерій, грибів роду Candida), що також обґрунтовувало потребу призначення пробіотика. За допомогою бактеріологічного дослідження випорожнень у динаміці на тлі застосування пробіотика Субалін® виявлено достовірне збільшення кількості основних представників індигенної мікрофлори порівняно з такою у контрольній групі, де спостерігався негативний вплив антибіотика у вигляді дисбіозу кишечнику (рис. 2; О.Г. Шадрін та співавт., 2018).
Таким чином, при виборі оптимального пробіотика для профілактики розвитку ААД у дітей пропонуємо звернути увагу на такі переваги штаму B. subtilis 2335/105 (Субалін®):
- висока антагоністична активність відносно великої кількості патогенних та умовно-патогенних мікроорганізмів;
- підвищення загальної резистентності організму, підсилення гуморального та клітинного імунітету, активація синтезу ендогенного інтерферону альфа-2;
- клінічна ефективність: сприяє усуненню та профілактиці виникнення основних симптомів, пов’язаних із прийомом антибіотиків (діареї, нудоти, здуття живота, дискомфорту і болю в животі);
- у ході експериментальних досліджень при прийомі засобу Субалін® у дозі вищій за рекомендовану не виявлено жодних патологічних змін з боку внутрішніх органів і центральної нервової системи;
- доведена безпечність (навіть у високих дозах);
- стійкість рекомбінантного штаму B. subtilis 2335/105 до дії антибіотиків і літичних ферментів, що дає можливість застосовувати пробіотик з 1-го дня антибіотикотерапії та ефективно запобігати розвитку ААД.
Субалін® – це пробіотик, який розроблений спеціально для застосування у дітей та представлений у зручних лікарських формах: для дітей від народження – порошок для приготування суспензії у флаконах, з 1 року зручніше використовувати саше, від 12 років – капсули Субалін®-Форте. Рекомендований режим прийому – вміст 1 флакона/саше або 1 капсула 2 рази на добу протягом 20 днів.
Підготувала Ілона Цюпа
Тематичний номер «Педіатрія» №1 (48), березень 2019 р.
СТАТТІ ЗА ТЕМОЮ Педіатрія
Вроджена дисфункція кори надниркових залоз (ВДКНЗ) – це захворювання з автосомно-рецесивним типом успадкування, в основі якого лежить дефект чи дефіцит ферментів або транспортних білків, що беруть участь у біосинтезі кортизолу. Рання діагностика і початок лікування пацієнтів з ВДКНЗ сприяє покращенню показників виживаності та якості життя пацієнтів....
Алергічний риніт (АР) є поширеним запальним захворюванням верхніх дихальних шляхів (ВДШ), особливо серед педіатричних пацієнтів. Ця патологія може знижувати якість життя, погіршувати сон та щоденну продуктивність. Метою наведеного огляду є надання оновленої інформації щодо епідеміології АР та його діагностики, з урахуванням зв’язку з бронхіальною астмою (БА). ...
Американська академія педіатрії (AAP) оновила рекомендації щодо контролю грипу серед дитячого населення під час сезону 2023-2024 рр. Згідно з оновленим керівництвом, для профілактики та лікування грипу в дітей необхідно проводити планову вакцинацію з 6-місячного віку, а також своєчасно застосовувати противірусні препарати за наявності показань. ...
Поширеність і вплив алергічних захворювань часто недооцінюють [1]. Ключовим фактором алергічної відповіді є імуноглобулін (Ig) Е, присутній на поверхні тучних клітин і базофілів. Взаємодія алергену з IgЕ та його рецепторним комплексом призводить до активації цих клітин і вивільнення речовин, у тому числі гістаміну, які викликають симптоми алергії [2]. Враховуючи ключову роль гістаміну в розвитку алергічних реакцій, при багатьох алергічних станах, включаючи алергічний риніт і кропив’янку, пацієнту призначають антигістамінні препарати [3, 4]....




