Пертузумаб в ад’ювантній терапії HER2-позитивного раку грудної залози ранніх стадій
Надлишкова експресія рецептора людського епідермального фактора росту 2 (HER2) виявляється приблизно у 20% пацієнток з раком грудної залози (РГЗ) та асоціюється з агресивністю пухлини, зниженою відповіддю на стандартну терапію та низькою виживаністю. Це зумовлено тим, що активація HER2‑рецепторів призводить до утворення гомо- та гетеродимерів (HER2/HER2, HER2/HER3), які активують низку молекулярних шляхів з подальшим підвищенням проліферації та виживання пухлинних клітин.
Впровадження у клінічну практику трастузумабу, препарату моноклональних антитіл проти HER2, здійснило революцію у веденні пацієнток з HER2-позитивним РГЗ. У перших дослідженнях додавання трастузумабу до хіміотерапії (ХТ) значно збільшувало виживаність без прогресування і загальну виживаність у пацієнток з РГЗ пізніх стадій. Сьогодні трастузумаб застосовується як стандартний препарат також в ад’ювантній і неоад’ювантній терапії.
Попри високу ефективність трастузумабу при HER-позитивному РГЗ, у деяких пацієнток не досягалася відповідь на лікування або в них розвивався рецидив, що потребувало розробки нових методів терапії, спрямованих проти HER2. Пертузумаб – препарат моноклональних антитіл, перший представник класу інгібіторів димеризації рецепторів HER2, який порушує здатність HER2 зв’язуватися з іншими рецепторами родини HER. Цей унікальний механізм дає змогу доповнити дію трастузумабу, забезпечуючи більш повну блокаду сигнального шляху HER. У разі призначення в комбінації з доцетакселом і трастузумабом у 1-й лінії терапії при метастатичному HER2-позитивному РГЗ пертузумаб покращував загальну виживаність, на підставі чого був схвалений Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) і сьогодні застосовується як стандартна терапія за цим показанням. Пертузумаб також став першим онкологічним препаратом, який отримав прискорене схвалення FDA для застосування з метою неоад’ювантної терапії.
За результатами рандомізованих досліджень було встановлено, що додавання пертузумабу до терапії трастузумабом підвищує частоту повної патологічної відповіді при HER2-позитивному РГЗ ранніх стадій. Нещодавно було завершено рандомізоване клінічне дослідження III фази APHINITY, у якому оцінювали ефективність і безпеку пертузумабу як ад’ювантної терапії в комбінації з ХТ при РГЗ ранніх стадій (von Minckwitz G. et al. APHINITY Steering Committee and Investigators. Adjuvant Pertuzumab and Trastuzumab in Early HER2-Positive Breast Cancer. N Engl J Med. 2017 Jul 13; 377(2): 122-131).
Рак грудної залози ранніх стадій – це пухлини, обмежені грудною залозою та регіонарними лімфатичними вузлами за відсутності віддалених метастазів (протокова карцинома in situ – DCIS, а також РГЗ I, IIA, IIB та IIIA стадій). РГЗ ранніх стадій виділяють тому, що за належного лікування він може бути повністю виліковним.
Для участі у дослідженні APHINITY у 549 клінічних центрах 43 країн (зокрема 7 центрах України) відбирали пацієнток з гістологічно верифікованим інвазивним HER2-позитивним РГЗ з метастазами у регіонарних лімфатичних вузлах (або з неураженими лімфатичними вузлами при розмірі пухлини >1,0 см). Позитивність за HER2 визначали як імуногістохімічну оцінку 3+ у >10% імунореактивних клітин або ампліфікацію ERBB2 (гена, який кодує HER2) у тесті з гібридизацією in situ. Пацієнток із синхронним двобічним інвазивним захворюванням включали у дослідження за умови HER2-позитивності обох вогнищ. Пацієнтки з N0 і пухлинами 0,5-1,0 см повинні були мати принаймні одну ознаку високого ризику з таких: гістологічний або ядерний ступінь 3, негативний статус за рецепторами естрогенів і прогестерону (ER/PR), вік молодше 35 років. Інтервал між радикальним хірургічним втручанням і введенням першої дози хіміопрепарату мав становити не більше 8 тижнів. Критерії виключення з дослідження: фракція викиду лівого шлуночка <55%; рак іншої локалізації протягом останніх 5 років (крім карциноми in situ шийки матки або товстої кишки, меланоми in situ, базально- або плоскоклітинного раку шкіри); будь-яка ХТ, променева, анти-HER2-, біологічна або імунотерапія раку в анамнезі; супутні хвороби, наявність яких може вплинути на досліджуване лікування, зокрема тяжкі кардіоваскулярні або легеневі захворювання.
Пацієнток рандомізували 1:1 для лікування пертузумабом або плацебо (навантажувальна доза 840 мг внутрішньовенно – в/в, потім 420 мг в/в через кожні 3 тижні) в комбінації з трастузумабом (навантажувальна доза 8 мг/кг маси тіла в/в, потім 6 мг/кг в/в через кожні 3 тижні). Пертузумаб і трастузумаб призначали з першого циклу таксанвмісної ХТ і продовжували максимум 18 циклів протягом 1 року. Анти-HER2-терапію застосовували у комбінації з ХТ за однією з таких схем:
- 3 або 4 цикли (через кожні 3 тижні) 5-фторурацилу + епірубіцин або доксорубіцин + циклофосфамід, потім 3 або 4 цикли (через кожні 3 тижні) доцетакселу або 12 однотижневих циклів паклітакселу;
- 4 цикли (через кожні 2 або 3 тижні) циклофосфаміду + доксорубіцин або епірубіцин, потім 4 цикли доцетакселу або 12 циклів паклітакселу;
- 6 циклів (через кожні 3 тижні) доцетакселу + карбоплатин.
Пацієнтки з ER/PR-позитивними пухлинами після завершення ХТ отримували стандартну гормонотерапію з плановою тривалістю 5 років. Променеву терапію призначали за клінічними показаннями наприкінці ХТ одночасно з анти-HER2-терапією.
Первинною кінцевою точкою була виживаність без інвазивної хвороби (ВБХ), яку визначали як час від рандомізації до фіксування першої події з зазначених: рецидив іпсилатеральної інвазивної пухлини грудної залози, рецидив іпсилатеральної локорегіонарної інвазивної хвороби, віддалений рецидив, контралатеральний інвазивний РГЗ, смерть від будь-якої причини. Як вторинні кінцеві точки оцінювали загальну виживаність, час до розвитку віддаленого рецидиву, безпеку, якість життя та ін.
Загалом 4805 пацієнток рандомізували для отримання ХТ і трастузумабу в комбінації з пертузумабом (n=2400) або плацебо (n=2405). За початковими клініко-демографічними характеристиками групи були добре збалансованими. Метастази в регіонарних лімфатичних вузлах мали 63% пацієнток, ER/PR-негативний статус пухлини – 36%. Медіана спостереження становила 45,4 міс.
Один рік терапії завершили 84,5% пацієнток групи пертузумабу та 87,4% хворих групи плацебо. З міркувань безпеки лікування припинили 7,8 та 6,4% пацієнток відповідно.
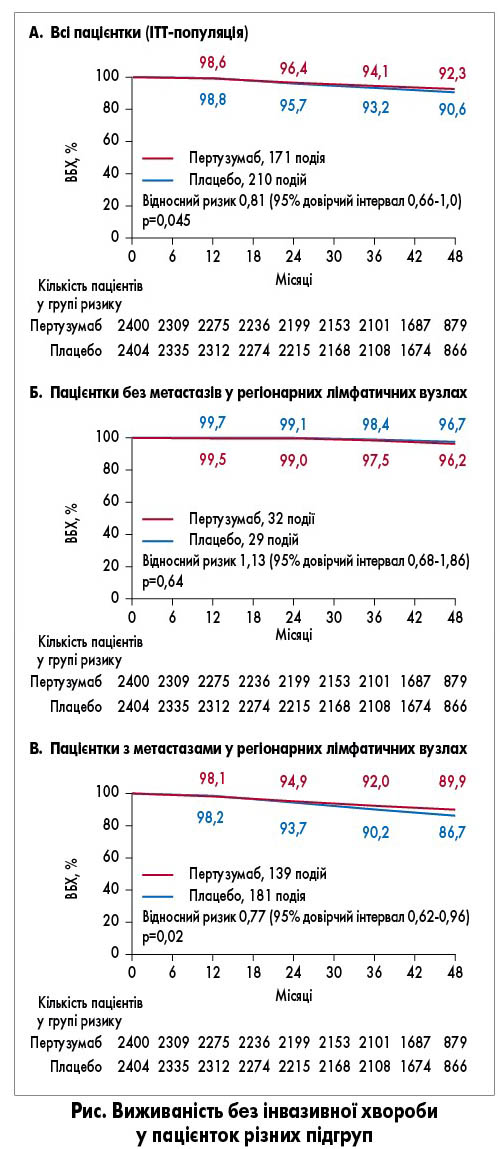 Аналіз первинної точки показав, що додавання пертузумабу асоціювалося зі значно вищим показником ВБХ порівняно з плацебо (рис. А). Трирічна ВБХ становила 94,1% у групі пертузумабу та 93,2% у групі плацебо (зниження ризику розвитку інвазивного рецидиву або смерті на 19% на користь пертузумабу; р=0,045). Віддалені метастази розвинулись у 112 (4,7%) пацієнток групи пертузумабу та 139 (5,8%) хворих групи плацебо, локорегіонарний рецидив – у 26 (1,1%) та 34 (1,4%) відповідно.
Аналіз первинної точки показав, що додавання пертузумабу асоціювалося зі значно вищим показником ВБХ порівняно з плацебо (рис. А). Трирічна ВБХ становила 94,1% у групі пертузумабу та 93,2% у групі плацебо (зниження ризику розвитку інвазивного рецидиву або смерті на 19% на користь пертузумабу; р=0,045). Віддалені метастази розвинулись у 112 (4,7%) пацієнток групи пертузумабу та 139 (5,8%) хворих групи плацебо, локорегіонарний рецидив – у 26 (1,1%) та 34 (1,4%) відповідно.
Позитивний вплив пертузумабу на ВБХ був подібним в усіх підгрупах пацієнток. У підгрупі із РГЗ N0 кількість подій була надто малою, щоб продемонструвати статистично значимий ефект терапії (рис. Б). Натомість у підгрупі з метастазами у регіонарних лімфатичних вузлах перевага пертузумабу була ще помітнішою (зниження ризику інвазивного рецидиву або смерті на 23%; р=0,02; рис. В). Загальну виживаність поки оцінювати рано, проте вже спостерігається тенденція до збільшення цього показника у групі пертузумабу.
Частота небажаних подій ≥3 ступеня становила 64,2% у групі пертузумабу та 57,3% у групі плацебо. Найбільша абсолютна різниця між групами терапії спостерігалась щодо частоти діареї будь-якого ступеня (71,2 vs 45% відповідно). Показники якості життя у пацієнток різних груп не відрізнялися й залишалися стабільними протягом лікування, окрім тимчасового клінічно значимого зниження в кінці терапії таксанами.
Отже, у дослідженні APHINITY додавання до ХТ і трастузумабу пертузумабу як ад’ювантної терапії значно покращило результати лікування. Терапевтичний ефект помітніше проявлявся у пацієнток з вищим ризиком рецидиву (з ураженням регіонарних лімфатичних вузлів або ER/PR-негативними пухлинами), проте статистично був подібним у пацієнток усіх підгруп. Лікування з включенням пертузумабу характеризувалося хорошою переносимістю, жодних нових повідомлень стосовно безпеки не зафіксовано.
На підставі результатів дослідження APHINITY у грудні 2017 р. FDA схвалило пертузумаб як ад’ювантну терапію у комбінації з трастузумабом і ХТ у пацієнток з HER2-позитивним РГЗ ранніх стадій з високим ризиком рецидиву. У квітні 2018 р. Комітет з медичних продуктів для застосування людиною (CHMP) Європейського агентства з лікарських засобів (ЕМА) також рекомендував розширити показання до застосування пертузумабу.
Відповідно до рекомендацій Американського товариства клінічної онкології (ASCO, 2018), клініцисти можуть призначати ад’ювантну терапію пертузумабом протягом 1 року додатково до трастузумабу та ХТ у пацієнток з HER2-позитивним РГЗ ранніх стадій з високим ризиком рецидиву. У настановах Національної онкологічної мережі США (NCCN; версія за 8 лютого 2019 р.) ад’ювантна терапія пертузумабом із трастузумабом і ХТ рекомендована пацієнткам з HER2-позитивним РГЗ ранніх стадій у разі позитивного статусу лімфатичних вузлів (≥1 іпсилатерального метастазу діаметром >2 мм).
Таким чином, подвійна анти-HER2-блокада із застосуванням пертузумабу й трастузумабу в комбінації з ХТ стала стандартною опцією ад’ювантної терапії при РГЗ ранніх стадій з позитивним HER2-статусом. Крім усунення високого ризику (метастази в регіонарних лімфатичних вузлах, негативний статус гормональних рецепторів), предиктором користі від додавання пертузумабу може бути інфільтрація пухлини лімфоцитами. У дослідженні TRYPHAENA за участю пацієнток з РГЗ ранніх стадій, які отримували пертузумаб/трастузумаб + ХТ, було встановлено, що з кожним збільшенням на 10% початкової кількості лімфоцитів, які інфільтрують пухлину, ризик прогресування або смерті зменшувався на 25% протягом 5 років спостереження (M. Ignatiadis et al., 2019).
Підготував Олексій Терещенко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (57), лютий 2019
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
Гостра лімфобластна лейкемія (ГЛЛ) є найпоширенішим онкогематологічним захворюванням у дітей і складає значну частку серед лейкемій у дорослих. Незважаючи на значні успіхи в лікуванні ГЛЛ у дітей, де рівень виліковності сягає 90%, результати терапії у дорослих залишаються незадовільними. У рамках науково-практичної конференції з міжнародною участю «Діагностика та лікування гематологічних захворювань: підведення підсумків 2023 року» (15-16 грудня 2023 року) проведено секцію, присвячену ГЛЛ....
Хронічна лімфоцитарна лейкемія (ХЛЛ) залишається актуальною проблемою сучасної онкогематології. Незважаючи на певні досягнення в терапії, ХЛЛ є невиліковним захворюванням. Стандартна хіміотерапія не забезпечує стійкої відповіді, а трансплантація гемопоетичних стовбурових клітин можлива лише для окремої когорти пацієнтів. Тому пошук нових підходів до терапії ХЛЛ, зокрема таргетної, є нагальним завданням. ...
Гепатоцелюлярна карцинома (ГЦК) – злоякісне новоутворення в печінці, що розвивається з гепатоцитів. Рання діагностика і початок лікування пацієнтів із ГЦК запобігає виникненню тяжких ускладнень і покращує якість життя пацієнтів. Медична допомога пацієнтам із ГЦК потребує міждисциплінарної співпраці та інтегрованого ведення хворих мультидисциплінарною командою фахівців, яка займається або спеціалізується на злоякісних новоутвореннях печінки. Саме цьому сприятимуть положення Стандарту медичної допомоги «Гепатоцелюлярна карцинома»....
Традиційно січень є місяцем обізнаності про рак шийки матки (РШМ) – однієї з найпоширеніших патологій у структурі онкогінекологічних захворювань. Протягом цього місяця світ забарвлюється в палітру бірюзового та білого з метою привернення уваги громадськості до проблеми РШМ. ...




